Aufgabe 4 – Von-Willebrand-Faktor – ein Schlüsselprotein der Blutgerinnung
Der Von-Willebrand-Faktor (VWF) ist ein Protein, das eine wichtige Rolle bei der Funktion und Regulation der Blutgerinnung spielt. Durch Mutation eines der Gene der an der Blutgerinnung beteiligten Proteine kann es zu einer Störung der Blutgerinnung kommen. Die am häufigsten auftretende Form einer erblichen Blutgerinnungsstörung ist das Von-Willebrand-Syndrom.
Vergleiche tabellarisch den Aufbau von DNA und RNA anhand von drei selbst gewählten Kriterien.
Erläutere anhand der Abbildung 1 (A-C) die Rolle des Von-Willebrand-Faktors in der frühen Phase der Blutgerinnung bei gesunden Menschen (M 1).
Leite die Art des Erbgangs des Von-Willebrand-Syndroms ab (M 2).
Ermittle die Wahrscheinlichkeit, mit der die möglichen Phänotypen und Genotypen bei weiteren Geschwistern auftreten (M 2).
Gib die resultierenden Aminosäuresequenzen für die in Abbildung 3 gezeigten Genausschnitte an (M 3).
Leite den vorliegenden Mutationstyp sowie die Folge für das Genprodukt ab (M 3).
Erkläre die Auswirkung der Mutation im VWF-Gen auf die Blutgerinnung der Patientin (M 1, M 3, M 4).
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?M 1: Die Rolle des Von-Willebrand-Faktors bei der Blutgerinnung
An der Blutgerinnung sind Proteinbestandteile des Blutes beteiligt, die in fein abgestimmter Weise aktiviert werden müssen, um für einen eng begrenzten Zeitraum das Blut gerinnungsfähig zu machen. Dieses fein abgestimmte System sorgt dafür, dass Verletzungen von Blutgefäßen zuverlässig verschlossen werden (Abb. 1).
Einer dieser Bestandteile ist der Von-Willebrand-Faktor (VWF). Der Von-Willebrand-Faktor spielt eine wichtige Rolle in der frühen Phase der Blutgerinnung, die durch Thrombozyten (Blutplättchen) vermittelt wird. Im Blutplasma zirkulieren die VWF-Polypeptide in Form von großen Proteinkomplexen (Multimere). Einen weiteren wichtigen Bestandteil des Blutgerinnungssystems stellen Kollagen-Fasern dar, welche die Blutgefäße umgeben und diese stabilisieren.
A: Intaktes Blutgefäß (Längsschnitt)
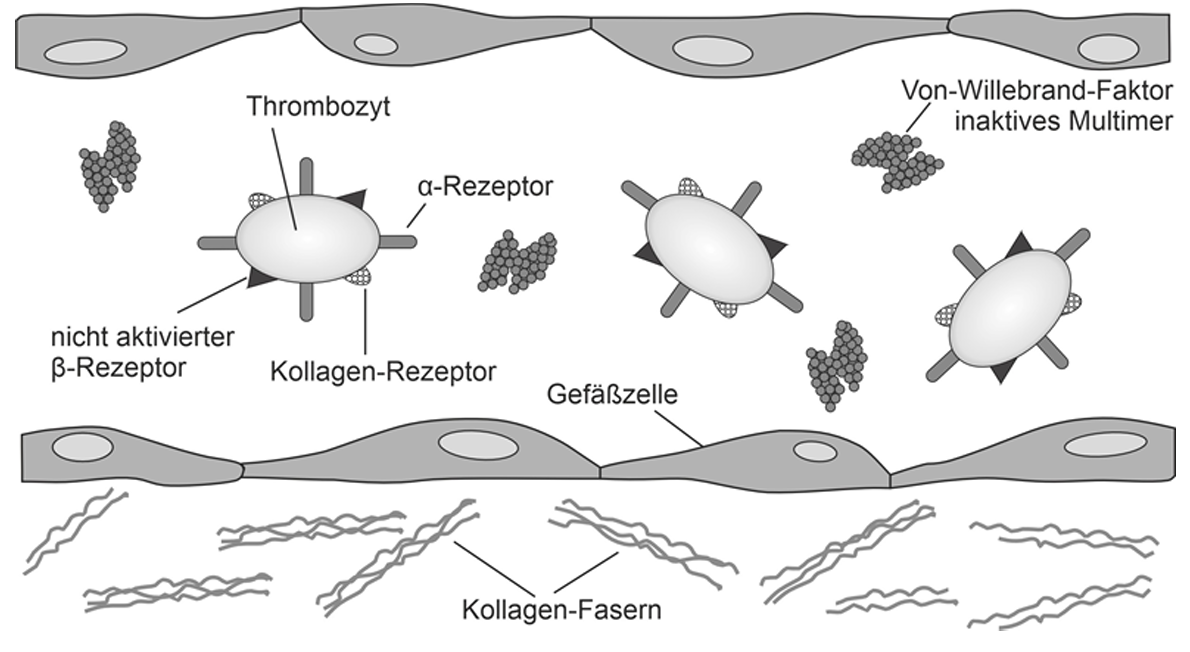
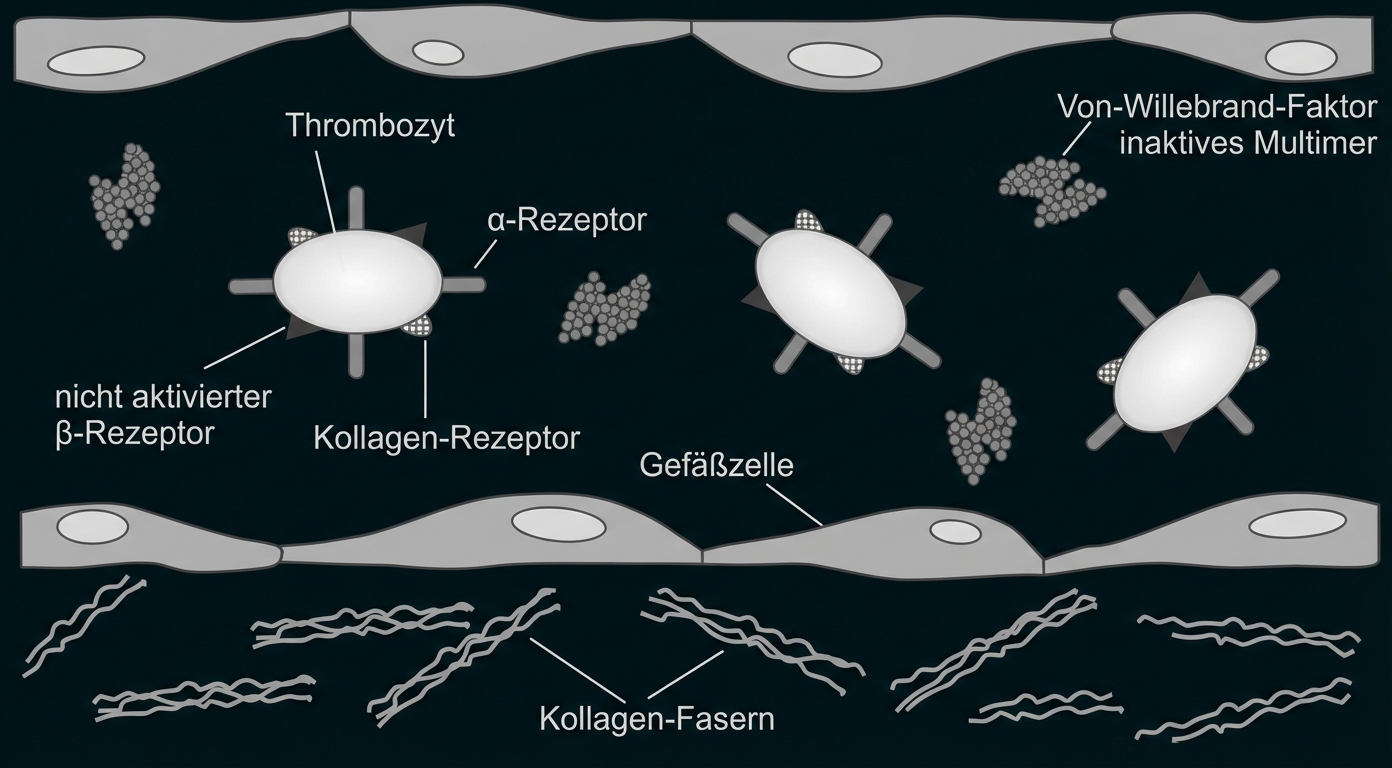
B: Verletztes Blutgefäß (Längsschnitt)
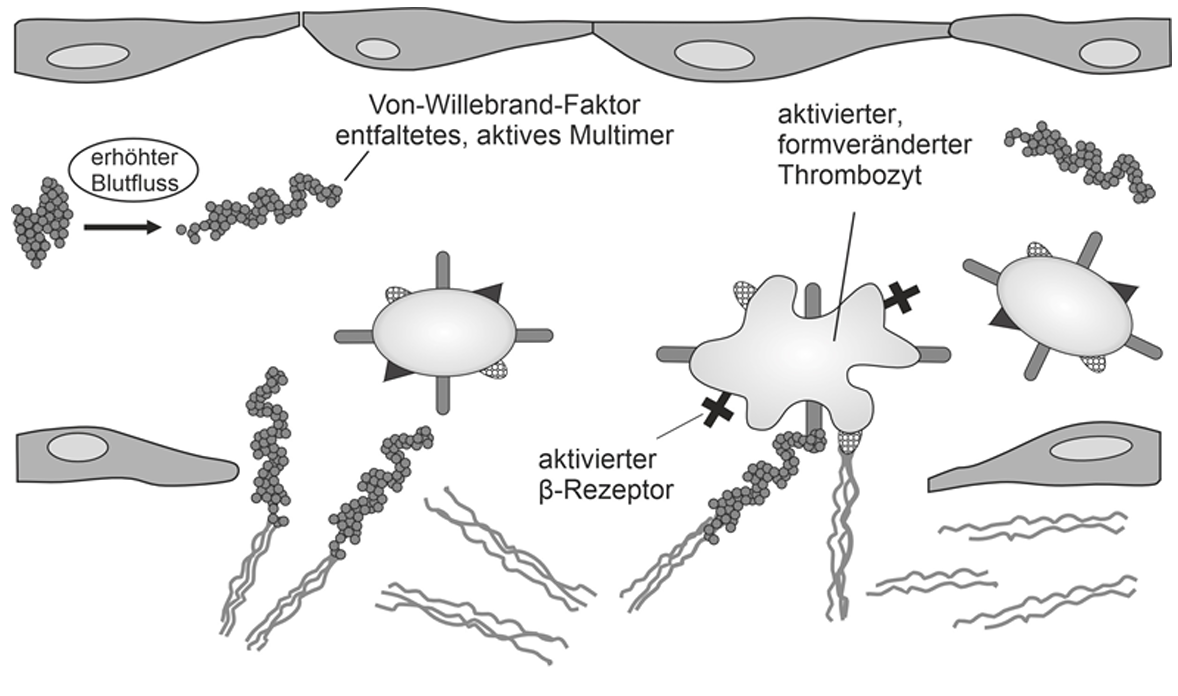
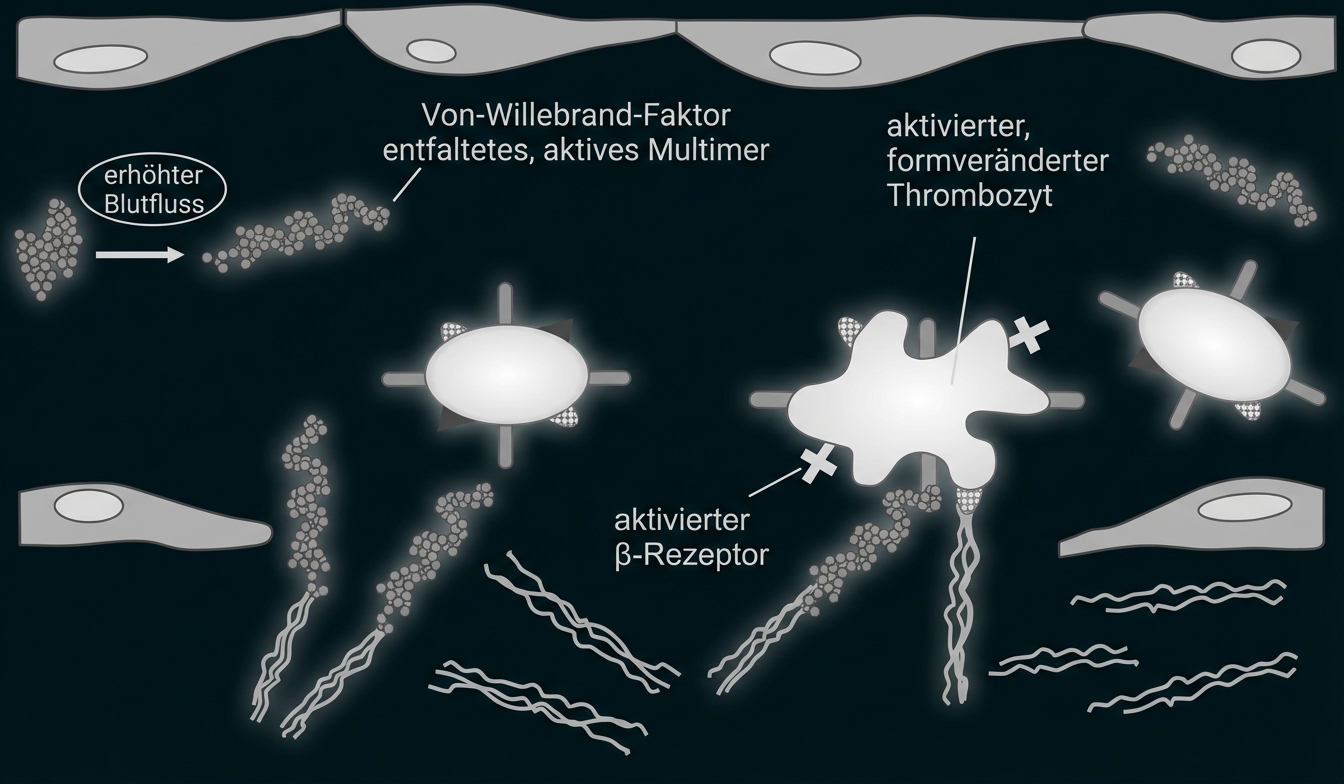
C: Bildung eines Blutpfropfes
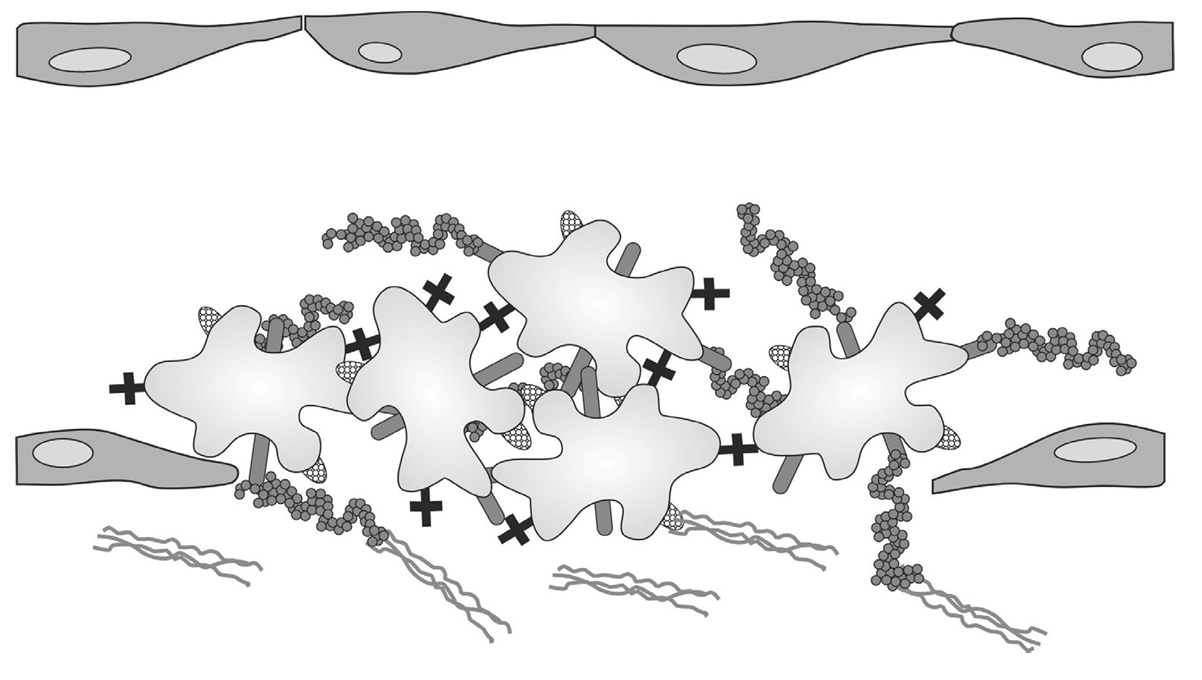
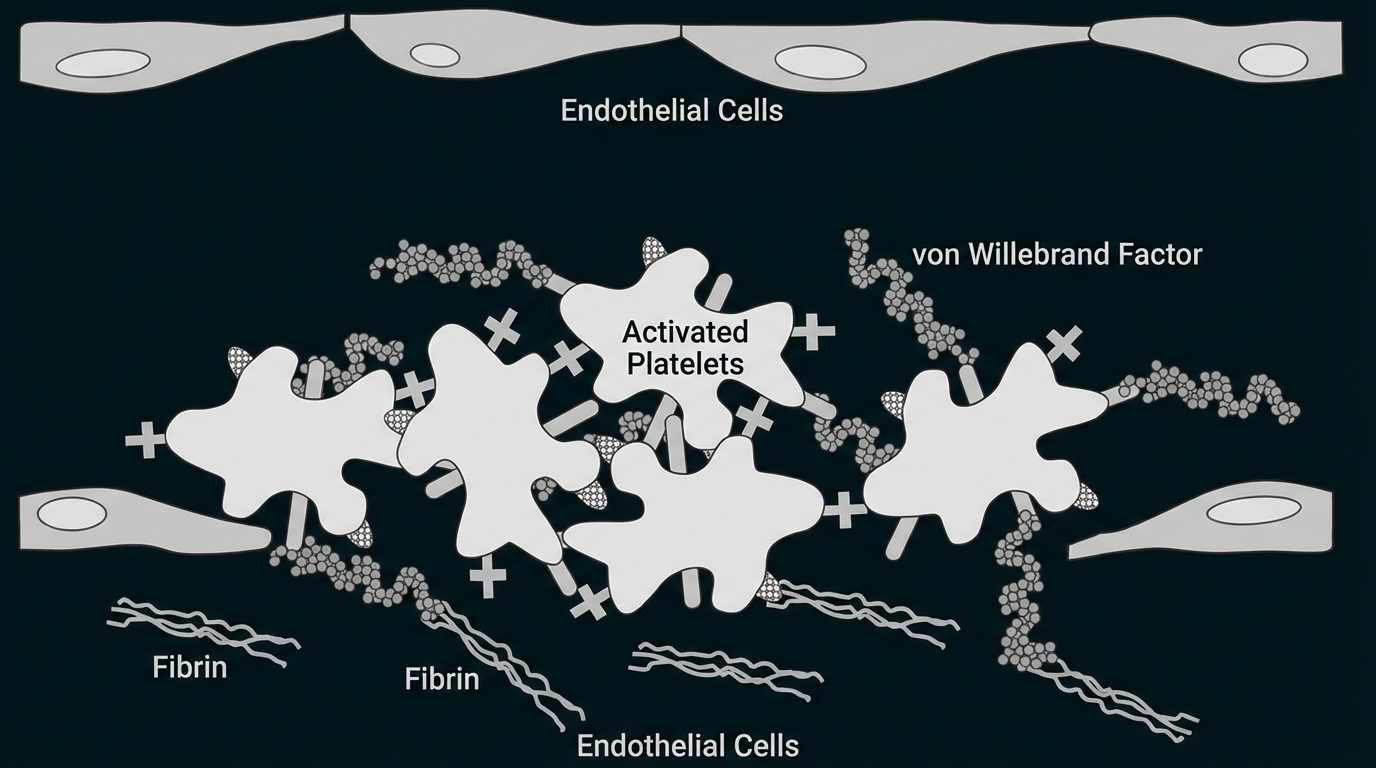
Abb. 1 (A-C): Ablauf der frühen Phase der Blutgerinnung bei gesunden Menschen
verändert nach: Alastair, J. J., Wood, M. D. (2004). Treatment of von Willebrand’s Disease. The New England Journal of Medicine, p. 684. DOI: 10.1056/NEJMra040403
M 2: Das Von-Willebrand-Syndrom
Das Von-Willebrand-Syndrom ist weltweit die häufigste angeborene Blutgerinnungsstörung. Etwa 1% der Bevölkerung ist davon betroffen. Wie bei jedem Syndrom treten auch hier gleichzeitig verschiedene Symptome unterschiedlich starker Ausprägung auf, beispielsweise Nasenbluten, eine auffällig starke Regelblutung, blaue Flecken an der Haut oder eine längere Nachblutung nach kleinen Verletzungen.
Der Familienstammbaum einer Patientin mit Von-Willebrand-Syndrom ist in Abbildung 2 dargestellt.
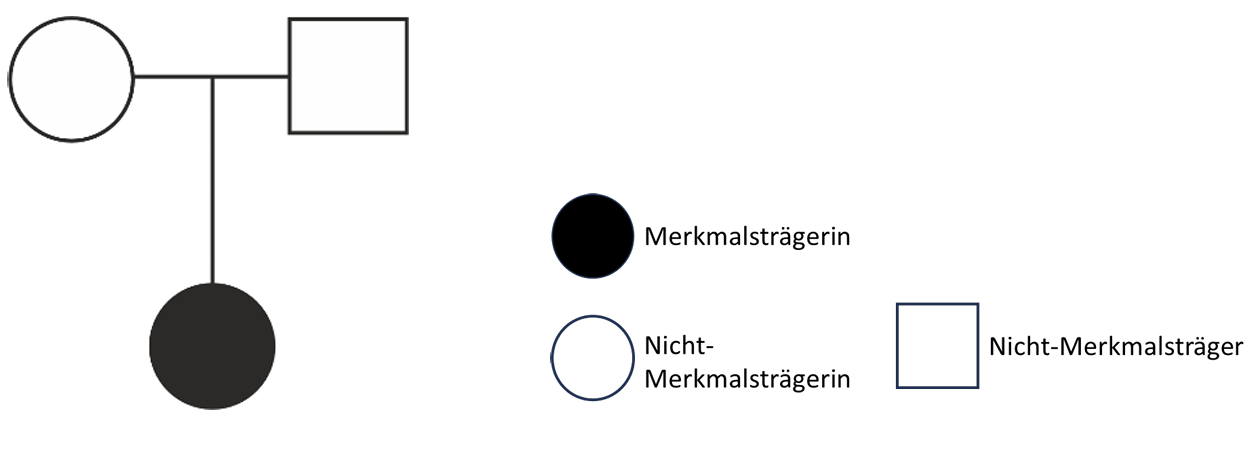

Abb. 2: Familienstammbaum einer Patientin mit Von-Willebrand-Syndrom
angelehnt an: Schneppenheim R. et al. (2001). Expression and characterization of von Willebrand factor dimerization defects in different types of von Willebrand disease. Blood, 97, p. 2059-2066. doi.org/10.1182/blood.V97.7.2059
M 3: Mutation im VWF-Gen und Von-Willebrand-Syndrom
Die Bildung der großen VWF-Proteinkomplexe erfolgt über Monomere. Diese bestehen aus Proteinketten mit jeweils 2813 Aminosäuren. Monomere bilden zunächst Dimere aus zwei Proteinketten, welche über Disulfidbrücken zwischen den Resten der Aminosäure Cystein miteinander verbunden sind. Im Anschluss werden die Dimere zu Multimeren, dem VWF-Proteinkomplex, zusammengesetzt.
Es sind zahlreiche Mutationen im Gen des Von-Willebrand-Faktors (VWF-Gen) beschrieben, welche die Funktion des exprimierten Proteins in unterschiedlicher Weise verändern. Sie führen zu unterschiedlichen Formen des so genannten Von-Willebrand-Syndroms. Bei der in Material 2 gezeigten Patientin mit Von-Willebrand-Syndrom wurde die Mutation im VWF-Gen näher untersucht. In Abbildung 3 ist ein Ausschnitt der Nukleotidsequenzen des nicht-codogenen DNA-Strangs des VWF-Gens dargestellt. Der nicht-codogene Strang ist der Strang, der nicht transkribiert wird.
Person ohne VWF-Syndrom: 5’… GGG CAA TGT GCA GCA … 3’
Patientin mit VWF-Syndrom: 5’… GGG CAA TGG GCA GCA … 3’
Abb. 3: Ausschnitt aus der Nukleotidsequenz des nicht-codogenen DNA-Strangs des VWF-Gens
angelehnt an: ebenda.
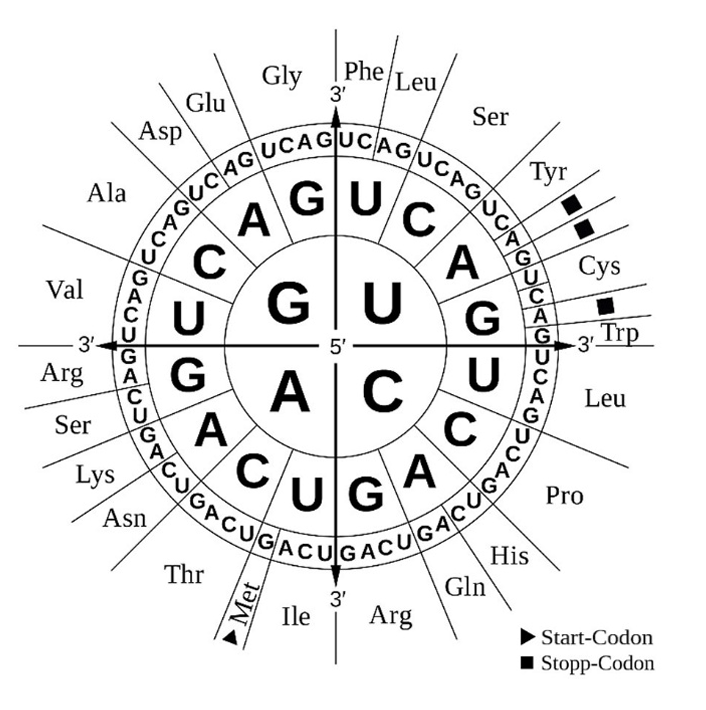
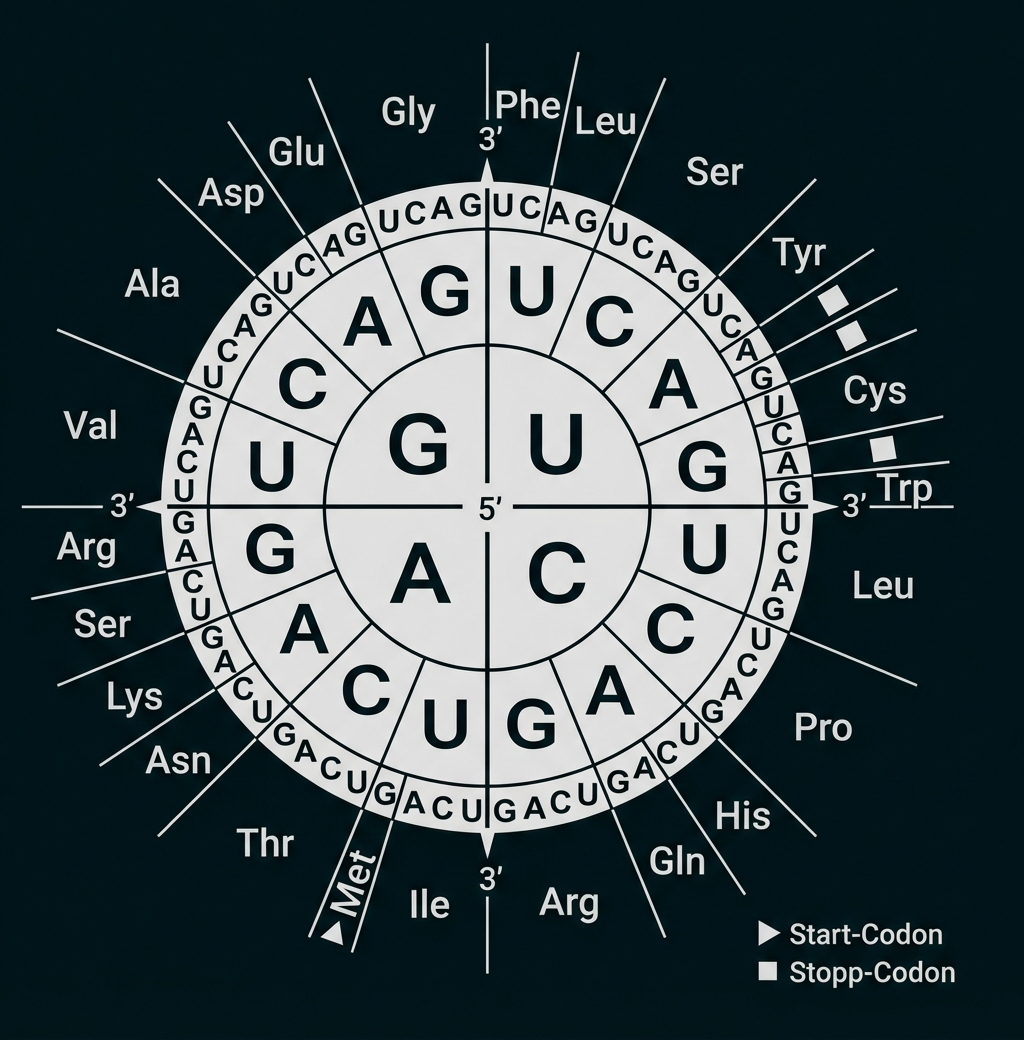
Abb. 4: Codesonne
M 4: Analyse des VWF-Proteins
Die Bedeutung der in Material M 3 dargestellten Mutation für den molekularen Aufbau des VWF-Proteins der Patientin wurde in weiteren Experimenten untersucht. Hierfür wurde das mutierte VWF-Gen in einer Zellkultur exprimiert und die entstehenden Proteine wurden hinsichtlich ihres Aufbaus analysiert. Dabei zeigte sich, dass zwar VWF-Monomere gebildet wurden, jedoch keine Di- oder Multimere nachweisbar waren.
angelehnt an: ebenda.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Aufbau von DNA und RNA:
|
DNA |
RNA |
|
Organische Basen Adenin, Guanin, Cytosin Thymin |
Organische Basen Adenin, Guanin, Cytosin Uracil |
|
Zucker Desoxyribose |
Zucker Ribose |
|
Struktur Doppelhelix |
Struktur meist einsträngig |
Rolle des Von-Willebrand-Faktors:
Der Von-Willebrand-Faktor zirkuliert als Multimer zusammen mit inaktiven Blutplättchen (Thrombozyten) im Blut. Die Verletzung der Gefäßwand mit einhergehendem erhöhten Blutfluss führt zur Veränderung des Von-Willebrand-Faktors: Das Multimer entfaltet sich. Im entfalteten Zustand bindet der VWF das Kollagen, das aufgrund der Gefäßwand-Verletzung in das Blut übergetreten ist. Ebenso ist er jetzt in der Lage, inaktive Thrombozyten über deren α-Rezeptor zu binden. Kollagen bindet an Kollagenrezeptoren des Thrombozyten. Diese Bindungen bewirken eine Formänderung der Thrombozyten. Des Weiteren führen diese Bindungen zu einer Aktivierung der β-Rezeptoren. Über die aktivierten β-Rezeptoren erfolgt eine Bindung zu weiteren aktivierten Thrombozyten. Es kommt zu einer starken Vernetzung der Thrombozyten, was letztlich zur Bildung eines Blutpfropfes führt, welcher das Blutgefäß verschließt, und die Blutung stillt.
Erbgangs des Von-Willebrand-Syndroms:
Das an die Tochter vererbte Allel kann nicht dominant sein, da beide Elternteile phänotypisch gesund sind. Möglich ist ein autosomal rezessiver Vererbungsmodus, bei dem der Vater und die Mutter jeweils heterozygote Überträger eines mutierten Allels sind. Ein X-chromosomal rezessiver Erbgang ist auszuschließen, da in diesem Fall der Vater ein mutiertes Allel tragen müsste, welches bei ihm zu einer phänotypischen Manifestation der Erkrankung führen würde.
Wahrscheinlichkeit:
Da es sich um einen rezessiven Vererbungsmodus handelt, müssen beide Eltern heterozygot bezüglich des mutierten Allels sein. Daher ist ein weiteres Kind mit einer Wahrscheinlichkeit von 75 % phänotypisch gesund. In 50 % der Fälle liegt jedoch ein heterozygoter Genotyp mit einem mutierten Allel vor. Die Wahrscheinlichkeit, mit der ein weiteres Geschwister der Patientin homozygot zwei nicht mutierte Allele trägt, beträgt demzufolge nur 25 %.
Aminosäuresequenzen für die in Abbildung 3 gezeigten Genausschnitte:
-
Gesunde Person: Gly – Gln – Cys – Ala – Ala
-
Patientin: Gly – Gln – Trp – Ala – Ala
Mutationstyp sowie die Folge für das Genprodukt:
Es liegt eine Punktmutation mit Austausch von Thymin gegen Guanin vor. Dies führt im VWF-Protein zu einem Austausch der Aminosäure Cystein gegen Tryptophan.
Auswirkung der Mutation im VWF-Gen auf die Blutgerinnung:
Da die Mutation im VWF-Gen zum Austausch der Aminosäure Cystein gegen Tryptophan führt, ist bei der untersuchten Patientin die Bildung von Dimeren des Von-Willebrand-Faktors über Disulfidbrücken zwischen Cysteinresten bei der Patientin nicht möglich. Dies bestätigt die Analyse der exprimierten Polypeptide, welche bei der Patientin ausschließlich aus Monomeren des Von-Willebrand-Faktors bestehen. Folglich werden auch Dimere sowie die größeren Multimere nicht gebildet, die bei einer Gefäßverletzung zur Bildung eines Blutpfropfes und damit zur Blutstillung beitragen. Daher hat die Patientin eine verlängerte Blutgerinnungszeit bei Verletzungen und damit ein erhöhtes Risiko schwerer Blutungen.