Teil I – Pflichtaufgaben
Hinweis: Die Pflichtaufgabe 1 ist von allen Prüflingen zu lösen.
Aufgabe 1 Stoffe – Teilchen – Chemische Reaktionen
Dir werden folgende Demonstrationsexperimente vorgeführt:
In drei mit A, B und C gekennzeichneten Gefäßen befanden sich Essigsäurelösung, Ethanol und Natriumhydroxidlösung. Die Stoffproben werden nacheinander
a) auf elektrische Leitfähigkeit und
b) mit Universalindikator geprüft.
-
Übernimm die Tabelle in Ihre Arbeit.
Notiere deine Beobachtungen zu den Experimenten a) und b).
|
Beobachtungen |
a) Prüfen auf elektrische Leitfähigkeit |
b) Prüfen mit Universalindikator |
|
Reagenzglas A |
||
|
Reagenzglas B |
||
|
Reagenzglas C |
-
Ordne die Stoffproben den Gefäßen A, B und C zu.
-
Begründe für eine Stoffprobe die Zuordnung anhand deiner Beobachtungen.
Natriumhydroxidlösung und Schwefelsäurelösung reagieren unter Wärmeentwicklung
miteinander.
-
Begründe an einem Merkmal chemischer Reaktionen, dass dabei eine
chemische Reaktion abläuft.
-
Entwickle für die chemische Reaktion von Natriumhydroxid und Schwefelsäure
die Reaktionsgleichung.
-
Ordne diese chemische Reaktion einer Reaktionsart zu.
Essigsäure, Ethanol und Natriumhydroxid enthalten das Element Sauerstoff.
-
Leite für Sauerstoff drei Aussagen zum Atombau aus dem Periodensystem der
Elemente ab.
-
Skizziere ein Modell des Ions von Sauerstoff und beschrifte dein Modell mit
vier Angaben.
-
Begründe die elektrische Ladung dieses Ions.
Ethanol gehört zur Stoffklasse der Molekülsubstanzen.
-
Notiere eine Formel für Ethanol.
-
Kennzeichne und benenne an der Formel das Strukturmerkmal.
-
Gib die Art der chemischen Bindung im Ethanolmolekül an.
-
Leite aus einer Eigenschaft des Ethanols eine Verwendungsmöglichkeit ab.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Tabellarische Darstellung der Beobachtungen
|
Reagenzglas |
Stoffprobe |
a) Elektrische Leitfähigkeit |
b) Universalindikator (Farbe/pH-Wert) |
|
A |
Essigsäurelösung |
leitet (schwach) |
Rot / Orange (sauer) |
|
B |
Ethanol |
leitet nicht |
Grün (neutral) |
|
C |
Natriumhydroxidlösung |
leitet (gut) |
Blau / Violett (alkalisch) |
Zuordnung der Stoffproben
Die Zuordnung erfolgt basierend auf dem chemischen Charakter der Stoffe.
Hinweis: Die Zuordnung muss in der Prüfung von dir abgeleitet werden und ist hier ohne Experiment pauschal gewählt worden.
Begründung der Zuordnung (Beispiel Natriumhydroxidlösung)
Die Stoffprobe in Gefäß C färbt den Universalindikator blau/violett, was auf eine alkalische Lösung hinweist. Zudem zeigt die Probe eine hohe elektrische Leitfähigkeit, da Natriumhydroxid als Ionenverbindung in Wasser vollständig in frei bewegliche Ionen und
dissoziiert. Diese Kombination aus alkalischem pH-Wert und Leitfähigkeit ist charakteristisch für eine Lauge wie Natriumhydroxidlösung.
Hinweis: Zur Erreichung der vollen Punktzahl kann auch eine der anderen beiden Zuordnungen begründet werden.
Begründung des Ablaufs einer chemischen Reaktion
Ein Merkmal chemischer Reaktionen ist die Energieänderung. Da im Text explizit eine Wärmeentwicklung (Exothermie) beschrieben wird, findet eine Stoffumwandlung unter Energieabgabe statt.
Reaktionsgleichung
Zuordnung der Reaktionsart
Diese Reaktion wird als Neutralisation bezeichnet. (Säure-Base-Reaktion)
Drei Aussagen zum Atombau von Sauerstoff aus dem Periodensystem
-
Sauerstoff steht in der 2. Periode, woraus folgt, dass die Atome zwei besetzte Elektronenschalen besitzen.
-
Sauerstoff steht in der VI. Hauptgruppe, woraus folgt, dass die Atome sechs Außenelektronen (Valenzelektronen) besitzen.
-
Sauerstoff hat die Ordnungszahl 8, woraus folgt, dass sich im Atomkern acht Protonen befinden und in der Elektronenhülle acht Elektronen verteilt sind.
Skizze des Sauerstoff-Ions (Oxid-Ion)
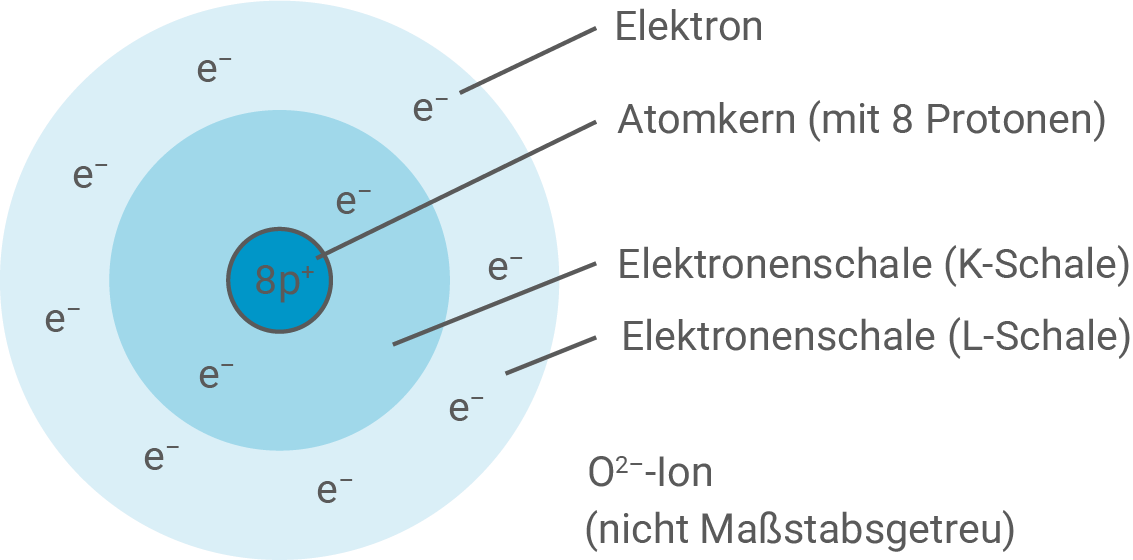
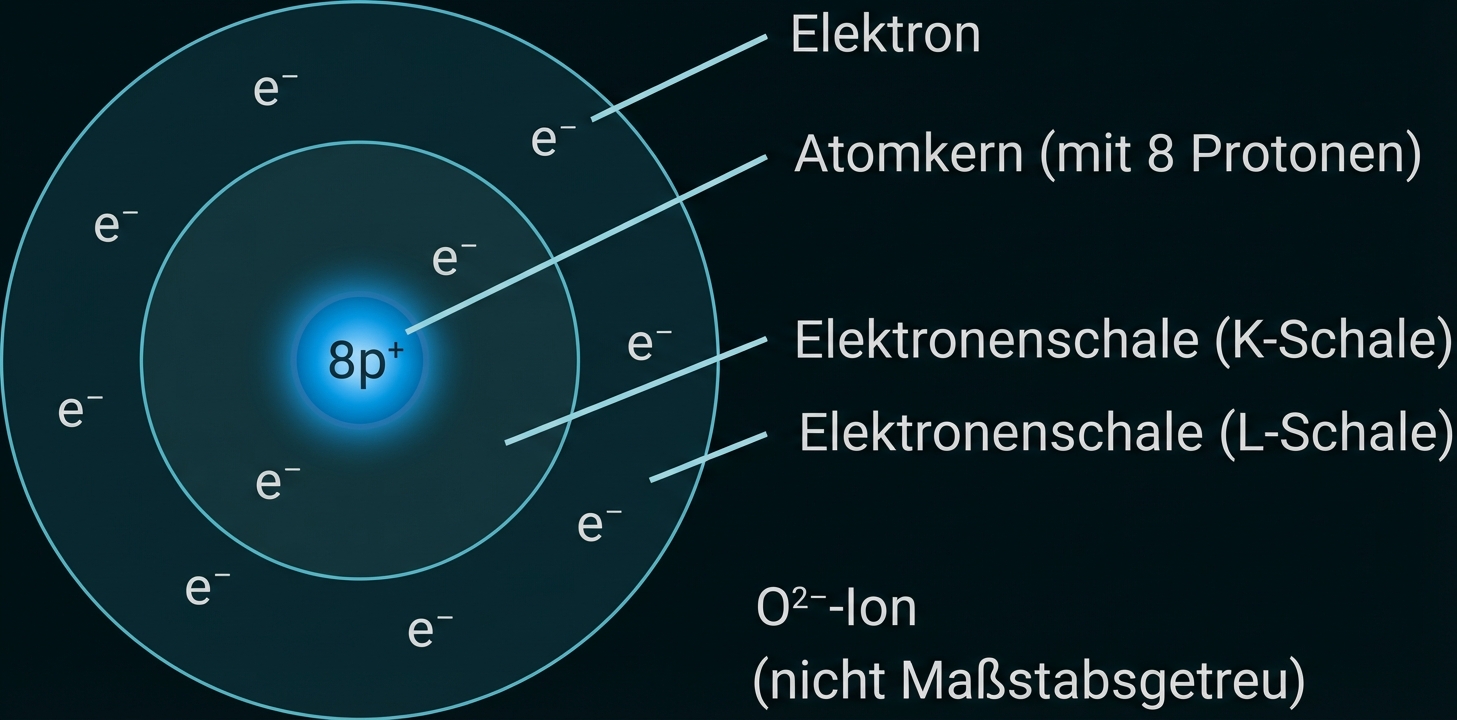
Begründung der elektrischen Ladung
Sauerstoffatome nehmen zwei Elektronen auf, um den stabilen Edelgaszustand (Oktettregel) zu erreichen. Da das Ion nun weiterhin 8 positiv geladene Protonen im Kern, aber 10 negativ geladene Elektronen in der Hülle besitzt, überwiegt die negative Ladung um zwei Einheiten, woraus die zweifach negative Ladung () resultiert.
Formel für Ethanol
Hinweis: Alternativ kann Ethanol auch in Skelettschreibweise notiert werden.
Strukturmerkmal (Kennzeichnung und Benennung)
In der Formel ist die
-Gruppe das entscheidende Merkmal.
Bezeichnung: Hydroxylgruppe (oder Hydroxygruppe).
Art der chemischen Bindung im Ethanolmolekül
Im Ethanolmolekül liegen Atombindungen (Elektronenpaarbindungen / kovalente Bindungen) vor. Da zwischen Sauerstoff und Wasserstoff sowie Sauerstoff und Kohlenstoff eine Elektronegativitätsdifferenz besteht, handelt es sich teilweise um polare Atombindungen.
Verwendungsmöglichkeit abgeleitet aus einer Eigenschaft
-
Eigenschaft: Ethanol ist leicht brennbar/entzündlich.
-
Verwendung: Einsatz als Brennstoff (z. B. in Spirituskochern) oder als Biokraftstoff (E10).