Teil II – Wahlaufgaben
Hinweis: Von den Wahlaufgaben 2, 3 und 4 ist nur eine Aufgabe zu bearbeiten.
Aufgabe 2 Stoffgemische
Die uns umgebenden Stoffe auf der Erde, im Wasser und in der Luft sind vielfältig.
Als sinnvolle Einteilung der Stoffe hat sich eine Einteilung in Stoffgemische und
Reinstoffe erwiesen.
-
Ordne die aufgeführten Stoffe den Stoffgemischen bzw. Reinstoffen zu.
Erdöl – Aluminium – Müsliriegel – Stahl – Sauerstoff – Cola – Kohlenstoffdioxid –
Kochsalz
-
Gib für zwei Stoffgemische je zwei enthaltene Bestandteile an.
Stoffgemische können als Ausgangsstoff für die Herstellung wirtschaftlich wichtiger
Stoffe dienen.
-
Erläutere diese Aussage am Beispiel von Eisenerz.
Lies den Text „Das Linde-Verfahren“ und bearbeite die nachstehenden
Aufgaben.
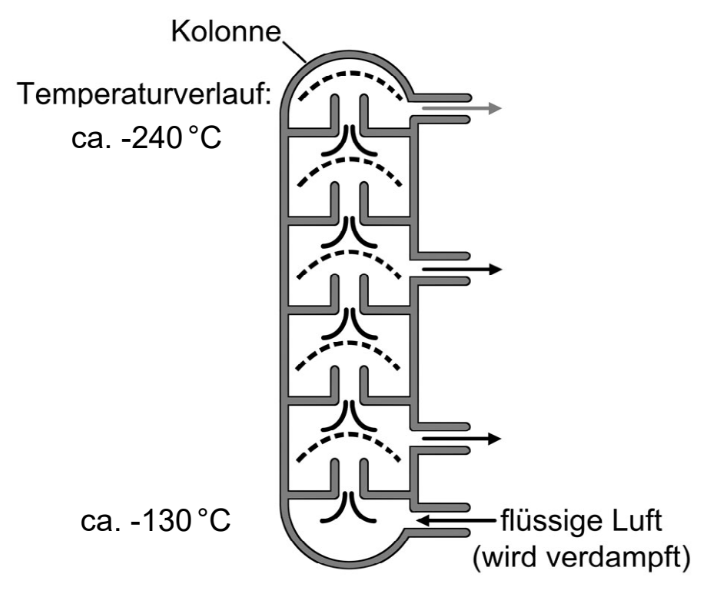
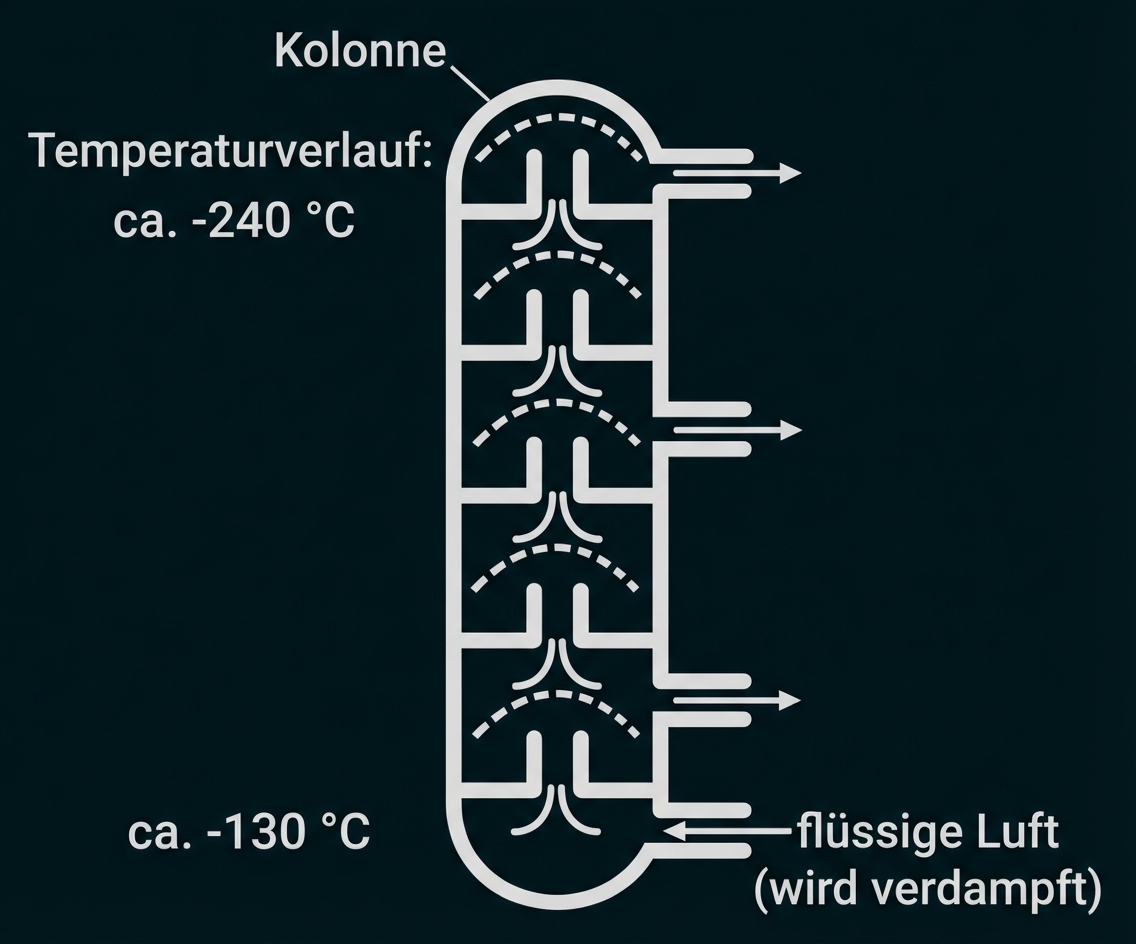
Das Linde-Verfahren
Das Linde-Verfahren ist eine technische Methode, die die Verflüssigung von
Gasgemischen und deren anschließende Zerlegung durch Destillation in ihre
Bestandteile ermöglicht. Die Luftverflüssigung wurde 1895 von Carl von Linde
entwickelt und patentiert. Das Linde-Verfahren beruht auf einem ständigen Wechsel
zwischen Verdichtung (Kompression) und Entspannung (Dekompression) der Luft.
Dadurch sinkt die Temperatur der Luft sehr stark ab (Joule-Thompson-Effekt). Dies
wird so lange wiederholt, bis alle Bestandteile der Luft im flüssigen Aggregatzustand
vorliegen.
Da die Stoffe Sauerstoff, Stickstoff sowie Argon und andere Edelgase verschiedene
Siedetemperaturen besitzen, können die Gase anschließend durch fraktionierte
Destillation als Reinstoffe gewonnen werden. Die flüssige Luft lässt man dazu in eine
Bodenkolonne fließen und erhitzt sie am Boden der Kolonne. In den jeweiligen Böden
kondensieren die Gase, sie setzen sich ab und können zur weiteren Verwendung
abgetrennt werden.
-
Notiere das Trennverfahren, welches bei der Gewinnung der Reinstoffe aus der
flüssigen Luft angewendet wird.
-
Gib die Eigenschaft an, die es ermöglicht, die Reinstoffe aus der flüssigen Luft
zu gewinnen.
-
Entscheide, in welcher
Reihenfolge (Destillationskolonne
von unten nach oben) die Reinstoffe
gewonnen werden.
A Sauerstoff – Argon – Stickstoff
B Argon – Stickstoff – Sauerstoff
C Stickstoff – Sauerstoff – Argon
-
Begründe deine Entscheidung.
-
Notiere für Sauerstoff sechs Angaben
zu Bau, Eigenschaften und
Verwendungsmöglichkeiten.
Das Wissenschaftsprojekt „The Ocean Cleanup“ macht es sich zur Aufgabe, die ständig
steigende Gefahr von Plastikmüll aus den Meeren zu beseitigen. Das Meerwasser ist ein
wichtiger Lebensraum und dient als Grundlage zur Salzgewinnung.
Experiment: Trennung eines Stoffgemisches
Du erhältst eine mit Plastikmüll (Kunststoffe) verunreinigte Salzwasserprobe.
Trenne dieses Stoffgemisch, so dass der Kunststoff und das Salz getrennt
vorliegen.
-
Entwickle einen Plan zur Trennung des Stoffgemisches.
Begründe deine Arbeitsschritte mit den Eigenschaften der Stoffe.
Lege deinen Plan der Lehrkraft vor.
-
Führe das Experiment durch.
-
Beurteile das Ergebnis deiner Stofftrennung hinsichtlich der Aufgabenstellung.
Kraftstoff ist ein Stoffgemisch. In ihm sind flüssige Kohlenwasserstoffe enthalten,
z. B. Hexan.
-
Berechne das Volumen an Kohlenstoffdioxid, das bei der Verbrennung von
640 g Hexan entsteht.
Aufgabe 3 Metalle – eine glänzende Stoffgruppe
Lies den Text „Metalle in Formel-1-Rennwagen“ und bearbeite die nachstehenden Aufgaben.
Metalle in Formel-1-Rennwagen
Formel-1-Rennwagen sind die Spitzenprodukte des Automobilbaus. Alle bestehen aus
nahezu gleichen Werkstoffen. Diese gehören vor allem zur Gruppe der Metalle wie die
Leichtmetalle Aluminium und Magnesium und das hochfeste Titan.
Titan bzw. Titanlegierungen werden für Motorteile und für Radaufhängungen
verwendet. Um Gewicht zu sparen, sind weniger stark belastete Teile, wie der
Zylinderkopf, aus Aluminium gefertigt. Die Kurbelwelle und die Nockenwelle werden
aus einem einzigen Stahlwerkstück hergestellt. Die elektrischen Anlagen und die
Steuerelektronik arbeiten mit Kupferkabeln.
-
Notiere drei im Text genannte Metalle, die in einem Rennwagen verbaut werden.
-
Gib zwei Eigenschaften aller Metalle an.
-
Stelle für zwei Metalle den Zusammenhang von Eigenschaft und Verwendung
her.
-
Notiere den Unterschied zwischen Titan und Titanlegierungen.
Metalle als Stoffgruppe.
-
Übertrage die folgenden Sätze in Ihre Arbeit und vervollständigen Sie diese
chemisch korrekt.
a) Ag, Pt und ... sind Edelmetalle.
b) Unedle Metalle wie ... und ... reagieren mit sauren Lösungen, dabei entstehen
ein Salz und ... .
c) Metalle leiten den elektrischen Strom, weil ... ... vorhanden sind.
Experiment: Die Reaktion von Oxiden mit Wasser
Du erhältst einen Magnesiumspan.
a) Stelle aus dem Magnesiumspan das Oxid her.
b) Gib das Oxid in Wasser und prüfe die Lösung anschließend mit
Universalindikator.
-
Plane dein experimentelles Vorgehen für a).
Lege dein Plan der Lehrkraft vor.
-
Formuliere zwei notwendige Arbeitsschutzmaßnahmen für a).
-
Führe die Experimente durch.
-
Notiere zu a) und b) drei Beobachtungen.
-
Entwickle die Reaktionsgleichung zu Experiment a).
-
Gib das im Experiment b) nachgewiesene Teilchen an.
In einem Kraftfahrzeug haben Stahl- und Eisenwerkstoffe einen hohen Anteil.
Die Herstellung von Eisen kann durch folgende Reaktionsgleichung beschrieben
werden.
-
Berechne das Volumen von Kohlenstoffmonooxid, das bei der Herstellung von
3,5 kg Eisen verbraucht wird.
Aufgabe 4 Bioplastik
Lies den Text „Bioplastik“ und bearbeite die nachstehenden Aufgaben.
Bioplastik
Mit dem Zusatz „Bio“ darf sich Plastik nennen, das entweder abbaubar ist oder anteilig aus pflanzlichen Rohstoffen hergestellt wurde. Häufig sind diese Rohstoffe Mais, Zuckerrohr, Raps oder Palmöl. Hierfür werden zum Teil riesige Wälder in Monokulturen verwandelt. Im chemischen Aufbau unterscheidet sich Bioplastik nicht von gewöhnlichem Plastik. Der einzige Unterschied besteht darin, dass seine Polymere nicht aus fossilen, sondern erneuerbaren Quellen stammen.
Oft werden bei der Herstellung jedoch beide Plastiksorten gemischt, um bessere Eigenschaften zu erzielen. Dies wiederum führt zu Problemen bei der Kompostierbarkeit. Zersetzt sich Bioplastik, entstehen Kohlenstoffdioxid und Wasser, jedoch keine Mineralsalze für den Boden. Wurde herkömmliches Plastik zugesetzt, entsteht außerdem Mikroplastik. Bioplastik dient vorwiegend zur Herstellung von Einwegprodukten wie Mülltüten, Besteck und Teller.
-
Notiere drei erneuerbare Rohstoffe für die Herstellung von Bioplastik.
-
Erläutere den Begriff Polymer.
-
Gib einen Vorteil von Bioplastik an.
-
Positioniere dich dazu, ob Bioplastik langfristig eine Lösung des Müllproblems
sein kann.
Kunststoffe aus fossilen Rohstoffen sind aus unserem Alltag derzeit noch nicht
wegzudenken.
-
Gib einen fossilen Rohstoff an, aus dem Kunststoffe hergestellt werden
können.
-
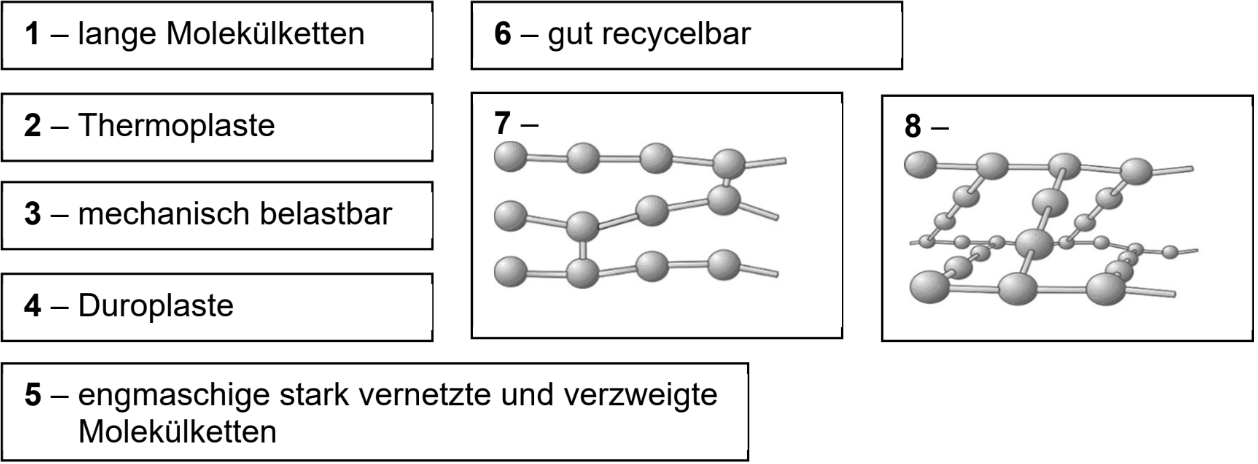
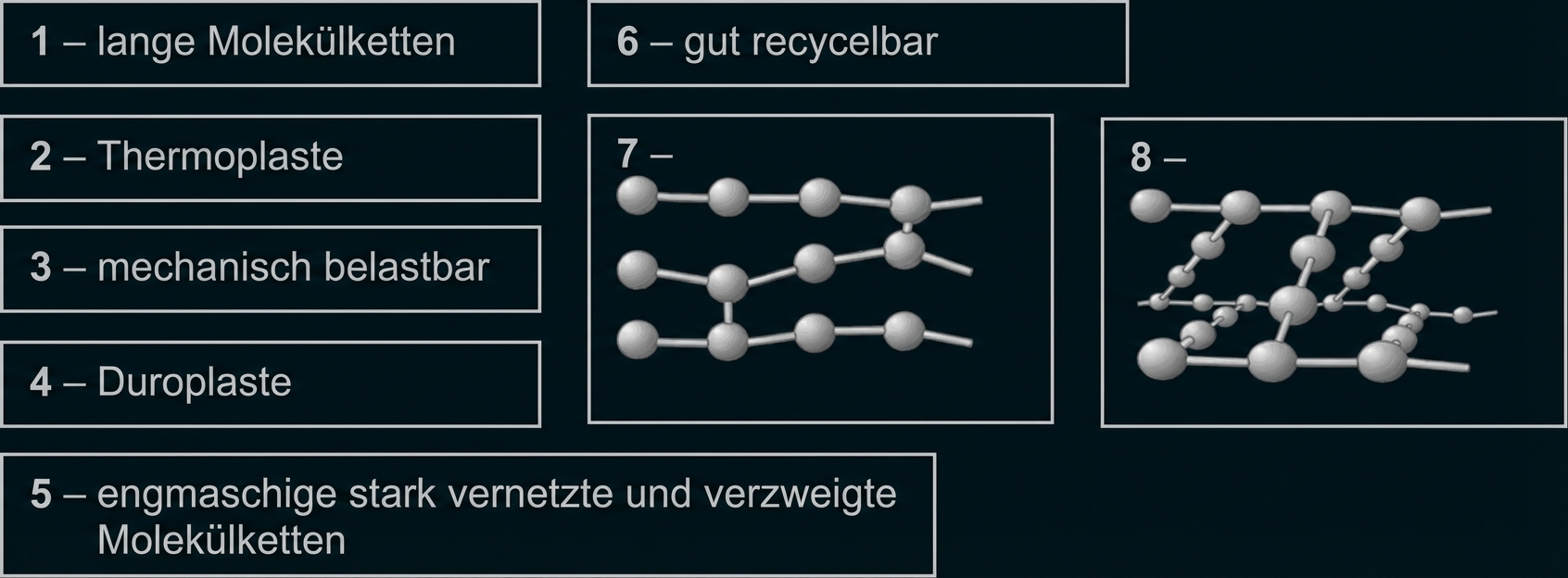
Ordne den Buchstaben aus der Tabelle die entsprechende Nummer der
vorgegebenen Textfelder zu.
|
Kunststoff |
Strukturbild |
Bau |
Eigenschaften |
Verwendung |
|
A |
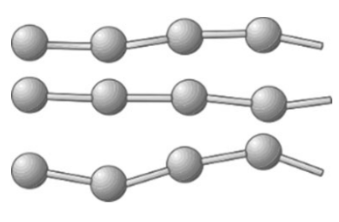 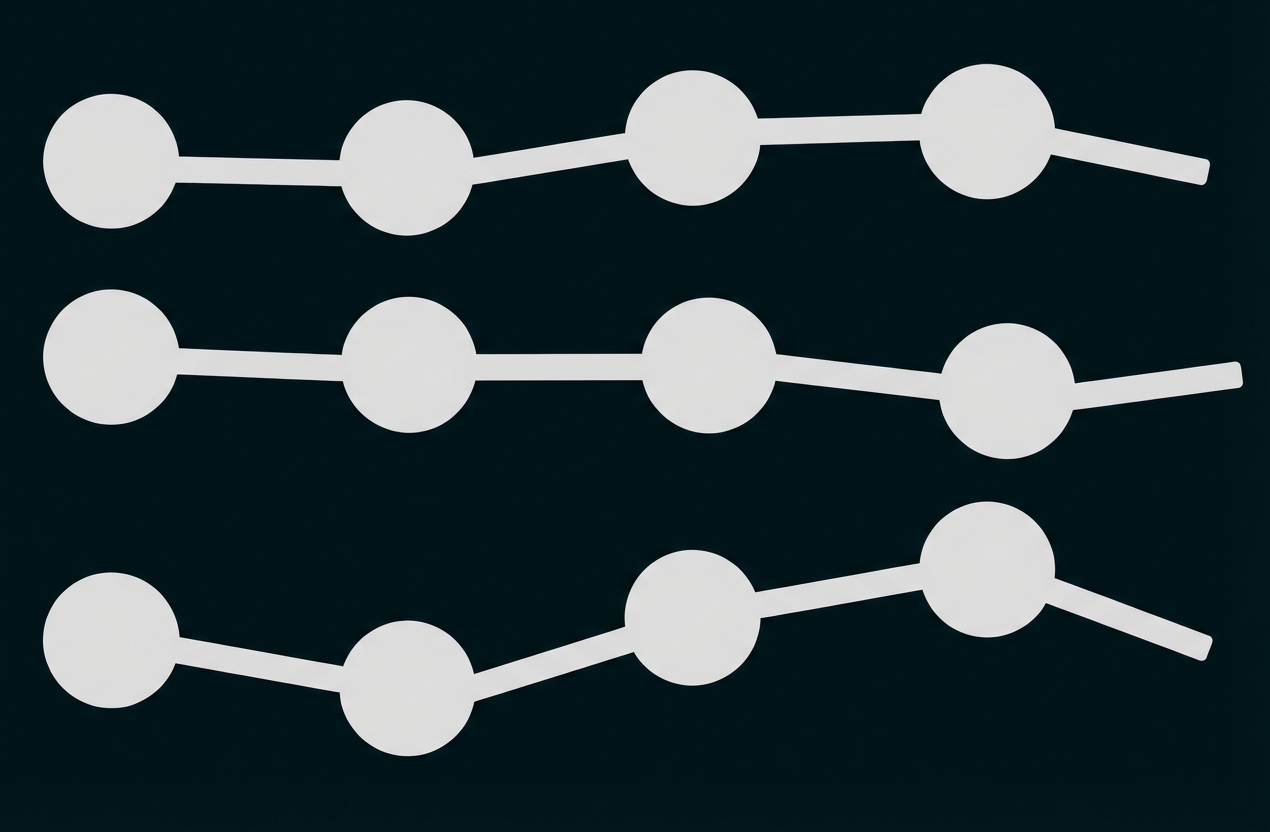
|
B |
C |
PE-Flaschen |
|
D |
E |
F |
stabil und hitzebeständig |
Gehäuse eines Wasserkochers |
|
Elastomere |
G |
weitmaschig und wenig vernetzte Molekülketten |
H |
Turnmatten |
Experiment: Nachweis von sauren Lösungen
Kunststoffe, darunter auch Bioplastik, sind säurebeständig.
Du erhältst in mit A, B und C gekennzeichneten Gefäßen farblose Lösungen.
Identifiziere die Salzsäure und die Schwefelsäurelösung und ordne beide
Lösungen den entsprechenden Gefäßen zu.
-
Plane dazu dein experimentelles Vorgehen.
Lege deinen Plan der Lehrkraft vor.
-
Führe das Experiment durch.
-
Notiere deine Beobachtungen.
-
Werte deine Beobachtungen entsprechend der Aufgabenstellung aus.
-
Entwickle für einen Ionennachweis die Reaktionsgleichung in verkürzter
Ionenschreibweise.
Für die Bildung von Maisstärke zur Herstellung von Bioplastik benötigt die Pflanze
Sonnenenergie, Kohlenstoffdioxid und Wasser. Hierbei entstehen zunächst Sauerstoff
und Glucose.
-
Berechne die Masse an Glucose, die aus 1000 Litern Kohlenstoffdioxid entsteht.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Zuordnung der Stoffe
|
Stoffgemische |
Reinstoffe |
|
Erdöl, Müsliriegel, Stahl, Cola |
Aluminium, Sauerstoff, Kohlenstoffdioxid, Kochsalz |
Bestandteile von zwei Stoffgemischen (Beispiele)
-
Stahl: Eisen und Kohlenstoff.
-
Cola: Wasser und Zucker (oder Kohlenstoffdioxid/Phosphorsäure).
Erläuterung am Beispiel Eisenerz
Eisenerz ist ein Stoffgemisch (Gestein), das metallhaltige Mineralien (wie Eisenoxide) und wertloses Nebengestein (Gangart) enthält. Durch chemische Verfahren, wie die Reduktion im Hochofen, wird aus diesem Gemisch der wirtschaftlich wichtige Reinstoff Eisen gewonnen.
Trennverfahren zur Gewinnung der Reinstoffe
Das angewendete Verfahren ist die fraktionierte Destillation.
Maßgebliche Eigenschaft
Die Trennung ist möglich, da die Bestandteile der Luft (Sauerstoff, Stickstoff, Argon) unterschiedliche Siedetemperaturen (Siedepunkte) besitzen.
Entscheidung zur Reihenfolge (von unten nach oben)
Die korrekte Antwort ist A (Sauerstoff – Argon – Stickstoff)
Begründung
In der Destillationskolonne nimmt die Temperatur von unten nach oben ab. Stoffe mit einer höheren Siedetemperatur kondensieren bereits im unteren, wärmeren Bereich der Kolonne, während Stoffe mit niedrigeren Siedetemperaturen weiter nach oben steigen, bis sie dort kondensieren. Da Sauerstoff den höchsten Siedepunkt der drei Gase hat (ca. °C), setzt er sich unten ab, gefolgt von Argon (ca.
°C) und schließlich Stickstoff (ca.
°C) an der Spitze.
Sechs Angaben zu Sauerstoff (Bau, Eigenschaften, Verwendung)
-
Bau: Besteht aus zweiatomigen Molekülen (
).
-
Bau: Die Atome sind über eine Doppelbindung (Atombindung) verknüpft.
-
Eigenschaft: Farbloses, geruchloses und geschmackloses Gas.
-
Eigenschaft: Fördert die Verbrennung (brandfördernd), ist aber selbst nicht brennbar.
-
Verwendung: Einsatz in der Medizin zur Beatmung.
-
Verwendung: Nutzung als Oxidationsmittel in der Metallindustrie (z. B. beim Schweißen oder in Hochöfen).
Versuchsplan zur Trennung des Stoffgemisches (Plastikmüll, Salz, Wasser)
-
Mechanische Trennung (Dekantieren/Abschöpfen): Der oben schwimmende Kunststoff wird mechanisch von der Salzwasserlösung getrennt.
-
Begründung: Kunststoffe besitzen meist eine geringere Dichte als Salzwasser und schwimmen an der Oberfläche.
-
-
Filtration: Die verbleibende Lösung wird filtriert, um kleinere, nicht schwimmfähige Kunststoffpartikel (Mikroplastik) abzutrennen.
-
Begründung: Der Kunststoff ist im Gegensatz zum Salz nicht wasserlöslich (heterogenes Gemisch) und bleibt als Rückstand im Filterpapier hängen.
-
-
Eindampfen: Das Filtrat (die Salzlösung) wird in einer Abdampfschale über dem Brenner erhitzt, bis das Wasser vollständig verdampft ist.
-
Begründung: Wasser hat eine deutlich niedrigere Siedetemperatur als Kochsalz. Während das Wasser gasförmig entweicht, bleibt das Salz als Feststoff zurück.
-
Beurteilung des Ergebnisses
Das Ziel der Aufgabe wurde erreicht, da beide Feststoffe (Kunststoff und Salz) getrennt und in fester Form wiedergewonnen wurden. Die Reinheit des Salzes hängt dabei von der Sorgfalt bei der Filtration ab.
Gegeben
-
Masse Hexan:
-
Reaktionsgleichung:
-
Molare Masse Hexan:
-
Molares Volumen (unter Normalbedingungen):
Gesucht
-
Volumen Kohlenstoffdioxid:
Rechnung
-
Berechnung der Stoffmenge von Hexan:
-
Bestimmung der Stoffmenge von Kohlenstoffdioxid über das Stoffmengenverhältnis: Laut Gleichung gilt:
(bzw.
).
-
Berechnung des Volumens von Kohlenstoffdioxid:
Ergebnis
Bei der Verbrennung von Hexan entstehen ca.
(bzw.
) Kohlenstoffdioxid.
Drei im Text genannte Metalle
-
Aluminium
-
Magnesium
-
Titan (Alternativ: Kupfer oder Eisen/Stahl)
Zwei Eigenschaften aller Metalle
-
Gute elektrische Leitfähigkeit
-
Gute Wärmeleitfähigkeit (Alternativ: Metallischer Glanz, Verformbarkeit (Duktilität))
Zusammenhang von Eigenschaft und Verwendung (zwei Beispiele)
-
Kupfer: Aufgrund seiner sehr guten elektrischen Leitfähigkeit wird es für die Kupferkabel in der Steuerelektronik verwendet.
-
Aluminium: Aufgrund seiner geringen Dichte (Leichtmetall) wird es für den Zylinderkopf verwendet, um das Gesamtgewicht des Rennwagens zu reduzieren. (Alternativ: Stahl/Titan aufgrund der hohen Festigkeit für mechanisch belastete Teile)
Unterschied zwischen Titan und Titanlegierungen
Titan ist ein Reinstoff (Element), der nur aus Titanatomen besteht. Eine Titanlegierung hingegen ist ein Stoffgemisch (fest in fest), bei dem Titan mit mindestens einem anderen Metall oder Nichtmetall verschmolzen wurde, um die Eigenschaften (z. B. Härte oder Korrosionsbeständigkeit) zu optimieren.
Vervollständigung der Sätze
a) ,
und
(oder
) sind Edelmetalle.
b) Unedle Metalle wie Magnesium und Zink reagieren mit sauren Lösungen, dabei entstehen ein Salz und Wasserstoff.
c) Metalle leiten den elektrischen Strom, weil frei bewegliche Elektronen (im Elektronengasmodell) vorhanden sind.
Versuchsplan zu a) (Herstellung des Oxids)
-
Ein Stück Magnesiumspan wird mit einer Tiegelzange festgehalten.
-
Der Span wird in die nicht leuchtende Brennerflamme gehalten, bis er sich entzündet.
-
Das entstehende Reaktionsprodukt (Magnesiumoxid) wird in einer Abdampfschale aufgefangen.
Arbeitsschutzmaßnahmen
-
Schutzbrille tragen: Zum Schutz vor Funkenflug und dem hellen Licht.
-
Nicht direkt in die Flamme schauen: Die starke UV-Strahlung beim Verbrennen von Magnesium kann die Augen schädigen.
Beobachtungen
-
Zu a): Das Magnesium verbrennt mit einer gleißend hellen Flamme.
-
Zu a): Es entsteht ein weißer, spröder Feststoff (Asche).
-
Zu b): Der Universalindikator färbt sich in der Lösung blau bzw. violett.
Reaktionsgleichung zu a)
Nachgewiesenes Teilchen in b)
In der entstandenen alkalischen Lösung (Magnesiumhydroxidlösung) wurden Hydroxid-Ionen nachgewiesen.
Gegeben
-
Masse Eisen:
-
Reaktionsgleichung:
-
Molare Masse Eisen:
-
Molares Volumen:
Gesucht
Volumen Kohlenstoffmonooxid:
Rechnung
-
Berechnung der Stoffmenge von Eisen:
-
Bestimmung der Stoffmenge von Kohlenstoffmonooxid über das Verhältnis: Laut Gleichung reagieren
zu
. Das Verhältnis
ist also
(bzw.
-
Berechnung des Volumens von Kohlenstoffmonooxid:
Ergebnis
Für die Herstellung von Eisen werden ca.
Kohlenstoffmonooxid verbraucht.
Drei erneuerbare Rohstoffe für die Herstellung von Bioplastik
-
Mais
-
Zuckerrohr
-
Raps (alternativ: Palmöl)
Erläuterung des Begriffs Polymer
Ein Polymer ist ein Riesenmolekül (Makromolekül), das aus einer Vielzahl von miteinander verknüpften, sich ständig wiederholenden kleineren Bausteinen, den Monomeren, besteht.
Vorteil von Bioplastik
Ein wesentlicher Vorteil ist, dass die verwendeten Polymere aus erneuerbaren (nachwachsenden) Quellen stammen und nicht aus fossilen Rohstoffen wie Erdöl gewonnen werden. (Alternativ: Es ist unter bestimmten Bedingungen biologisch abbaubar ).
Positionierung zum Müllproblem
Bioplastik ist langfristig keine alleinige Lösung für das Müllproblem.
-
Begründung: Bei der Zersetzung entstehen zwar
und Wasser, aber keine wertvollen Mineralsalze für den Boden. Zudem entstehen bei Mischungen mit herkömmlichem Plastik Probleme bei der Kompostierbarkeit und es bildet sich schädliches Mikroplastik. Auch der Anbau der Rohstoffe in Monokulturen stellt eine ökologische Belastung dar.
Fossiler Rohstoff
Erdöl
Zuordnung der Tabellenelemente
|
Buchstabe |
Nummer des Textfeldes |
Erläuterung / Inhalt |
|
A |
2 |
Thermoplaste |
|
B |
1 |
lange Molekülketten |
|
C |
6 |
gut recycelbar |
|
D |
4 |
Duroplaste |
|
E |
8 |
(Strukturbild der engmaschigen Vernetzung) |
|
F |
5 |
engmaschige stark vernetzte und verzweigte Molekülketten |
|
G |
7 |
(Strukturbild der weitmaschigen Vernetzung) |
|
H |
3 |
mechanisch belastbar |
Versuchsplan
-
Identifikation der sauren Lösungen: Alle drei Proben (A, B, C) werden mit Universalindikator geprüft. Die beiden Proben, die eine Rotfärbung zeigen, sind die Salzsäure und die Schwefelsäurelösung.
-
Unterscheidung der Säuren (Sulfatnachweis): Zu den beiden sauren Lösungen wird eine Bariumchloridlösung (
) gegeben.
-
Beobachtung: Die Lösung, in der ein weißer, feinkörniger Niederschlag entsteht, ist die Schwefelsäure (
). Die Lösung ohne Niederschlag ist die Salzsäure (
).
Beobachtungen
-
Bei Zugabe von Universalindikator färben sich zwei Lösungen rot.
-
Nach Zugabe von Bariumchloridlösung entsteht in einer der sauren Proben ein weißer Niederschlag.
Auswertung und Reaktionsgleichung (verkürzte Ionenschreibweise)
Der weiße Niederschlag beweist die Anwesenheit von Sulfat-Ionen (), was die Lösung als Schwefelsäure identifiziert.
Gegeben
-
Volumen Kohlenstoffdioxid:
-
Reaktionsgleichung:
-
Molares Volumen:
-
Molare Masse Glucose (
):
Gesucht
-
Masse Glucose:
Rechnung
-
Berechnung der Stoffmenge von Kohlenstoffdioxid:
-
Bestimmung der Stoffmenge von Glucose über das Stoffmengenverhältnis: Laut Gleichung reagieren
zu
. Das Verhältnis
ist also
.
-
Berechnung der Masse von Glucose:
Ergebnis
Aus Kohlenstoffdioxid entstehen ca.
(bzw.
) Glucose.