C1 Brom
Brom kommt in der Natur nicht elementar vor. Jedoch finden sich im Meerwasser gelöste Bromide.
1
Einige Algenarten besitzen das Enzym Bromidperoxidase, mit dessen Hilfe sie Kohlenwasserstoffe bromieren und dadurch z. B. Brommethan bilden können.
1.1
Bei dieser katalysierten Reaktion reagieren zunächst Bromid-Ionen mit Wasserstoffperoxid-Molekülen zu Molekülen der Hypobromigen Säure  und Hydroxid-lonen.
und Hydroxid-lonen.
Formuliere die Redoxgleichung mit Teilgleichungen.
Formuliere die Redoxgleichung mit Teilgleichungen.
(5 BE)
1.2
Mehrere Bromidperoxidase-Proben einer Rotalge aus der Gattung Gracilaria werden in einer Versuchsreihe zunächst auf unterschiedliche Temperaturen (Inkubationstemperaturen) erwärmt. Nach dem Abkühlen wird bei Raumtemperatur jeweils die relative Aktivität der Bromidperoxidase gemessen (Abb. 1):
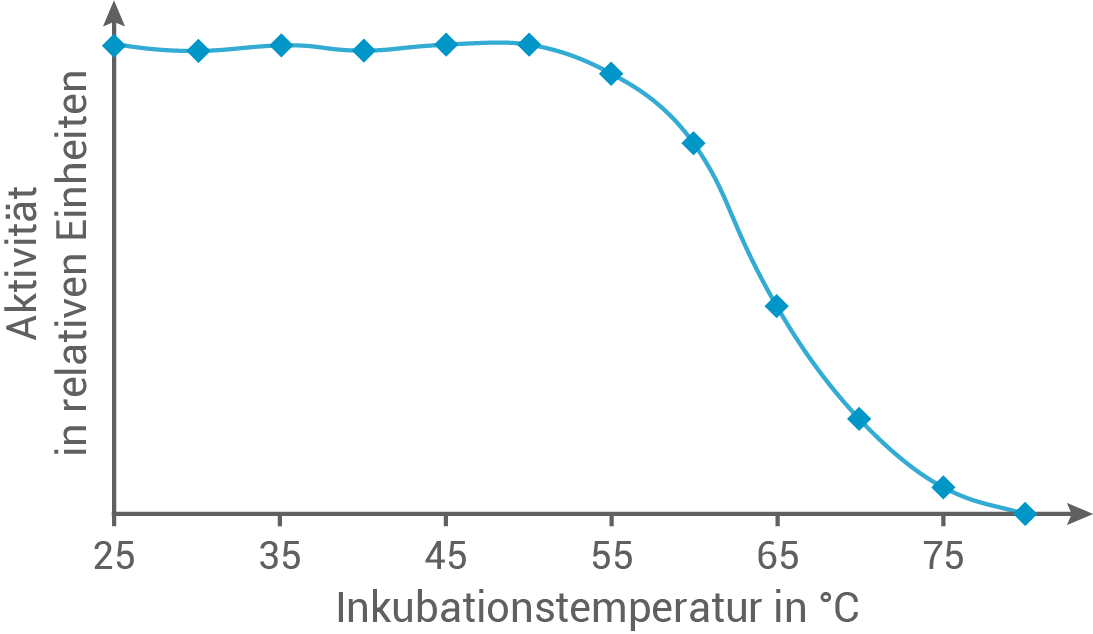

Abb. 1: Temperaturstabilität der Bromidperoxidase aus Algen der Gattung Gracilaria
verändert nach: Jirasak Kongkiattikajorn: Characterization of Non-Heme Haloperoxidase from Marine Red Algae, Gracilaria sp, (Nat. Sci.) 40(5)
1.2.1
Erkläre den in Abbildung 1 angegebenen Kurvenverlauf anhand des räumlichen Baus von Protein-Molekülen.
(6 BE)
1.2.2
Zeichne auf Grundlage der in Abbildung 1 dargestellten Daten ein Diagramm, das die Reaktionsgeschwindigkeit der Bildung von Hypobromiger Säure durch die Bromidperoxidase von Algen der Gattung Gracilaria bei Temperaturen zwischen  und
und  darstellt. Begründe den Kurvenverlauf Ihres Diagramms.
darstellt. Begründe den Kurvenverlauf Ihres Diagramms.
(6 BE)
2
Andere Meeresorganismen besitzen eine Halogenase. Dieses Enzym katalysiert folgende Reaktion (Abb. 2):


Abb. 2: Reaktionsschema der Bromierung von Indol zu 3-Bromindol
2.1
Tabelle 1 zeigt den zeitlichen Verlauf der enzymatisch katalysierten Bromierung von Indol:
Zeichne anhand der Daten in der Tabelle 1 ein Konzentrations-Zeit-Diagramm und bestimme daraus die momentane Reaktionsgeschwindigkeit bei  Minuten sowie die mittlere Reaktionsgeschwindigkeit über den Zeitraum zwischen
Minuten sowie die mittlere Reaktionsgeschwindigkeit über den Zeitraum zwischen  und
und  Minuten.
Minuten.
| Zeit in min | Konzentration von 3-Bromindol in |
|---|---|
Tab. 1: Konzentration von 3-Bromindol in Abhängigkeit von der Zeit
eigene Zusanmenstellung nach: Pia R. Neubauer et al.: A flavin-dependent halogenase from metagenomic analysis prefers bromination over chlorination, PLOS ONE, May 2018
(8 BE)
2.2
Die Halogenase dieser Meeresorganismen katalysiert nicht nur Bromierungs-, sondern auch Chlorierungsreaktionen.
Tabelle 2 zeigt die Konzentrationen von Chlorid- und Bromid-Ionen in Meerwasser:
Bei den durch diese Halogenase katalysierten Reaktionen entstehen mehr Bromverbindungen als Chlorverbindungen.
Stelle anhand einer Modellvorstellung zur Wirkungsweise von Enzymen eine Hypothese zur Erklärung dieses Sachverhalts auf.
Tabelle 2 zeigt die Konzentrationen von Chlorid- und Bromid-Ionen in Meerwasser:
| Ion | Massenkonzentration in Meerwasser in Promille |
|---|---|
| Chlorid | |
| Bromid |
Tab. 2: Massenkonzentrationen von Chlorid und Bromid in Meerwasser
eigene Zusammenstellung nach: Pia R. Neubauer et al.: A flavin-dependent halogenase from metagenomic analysis prefers bromination over chlorination, PLOS ONE, May 2018
Stelle anhand einer Modellvorstellung zur Wirkungsweise von Enzymen eine Hypothese zur Erklärung dieses Sachverhalts auf.
(6 BE)
2.3
Mithilfe eines Experiments soll der Proteincharakter der Halogenase gezeigt werden. Nenne eine geeignete Nachweisreaktion und beschreibe deren Durchführung und die Beobachtung bei positivem Verlauf.
(4 BE)
3
Die synthetische Herstellung der Aminosäure Alanin kann nach dem in Abbildung 3 gezeigten Schema erfolgen:
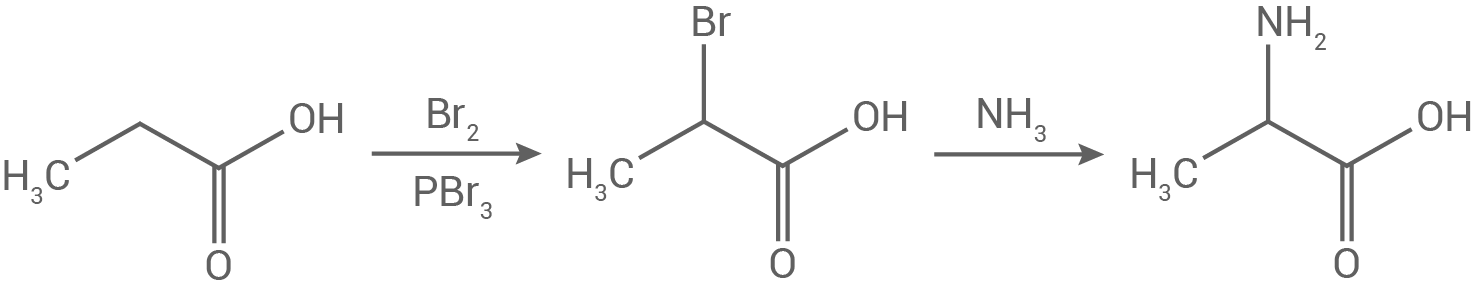 Leite die Anzahl der möglichen Stereoisomere von synthetisch hergestelltem Alanin ab und begründe, weshalb eine wässrige Lösung der bei dieser Synthese entstehenden Produkte keine optische Aktivität zeigt.
Leite die Anzahl der möglichen Stereoisomere von synthetisch hergestelltem Alanin ab und begründe, weshalb eine wässrige Lösung der bei dieser Synthese entstehenden Produkte keine optische Aktivität zeigt.

Abb. 3: Reaktionsschema zur Synthese von Alanin
(5 BE)
(40 BE)
1.1
Redoxgleichung mit Teilgleichungen
In dieser Redoxreaktion wird das Bromatom oxidiert (-I  +I) und der Sauerstoff aus dem Wasserstoffperoxid reduziert (-I
+I) und der Sauerstoff aus dem Wasserstoffperoxid reduziert (-I  -II).
-II).
1.2.1
Erklärung des räumlichen Baus von Protein-Molekülen
Sobald die Inkubationstemperatur etwa  erreicht, nimmt die Aktivität der Bromidperoxidase rasch ab. Bei ungefähr
erreicht, nimmt die Aktivität der Bromidperoxidase rasch ab. Bei ungefähr  lässt sich keine Aktivität mehr feststellen, da die Enzym-Moleküle nicht mehr intakt sind. Temperaturen über
lässt sich keine Aktivität mehr feststellen, da die Enzym-Moleküle nicht mehr intakt sind. Temperaturen über  verursachen eine thermische Denaturierung des Eiweißanteils der Enzyme, da die Wechselwirkungen zwischen den Aminosäureresten verloren gehen. Daraus folgt eine irreversible Veränderung der Sekundär- und Tertiärstruktur der Proteine, wodurch das Substrat nach dem Schlüssel-Schloss-Prinzip nicht mehr in das aktive Zentrum passt. Folglich kann kein Substrat mehr umgesetzt werden.
verursachen eine thermische Denaturierung des Eiweißanteils der Enzyme, da die Wechselwirkungen zwischen den Aminosäureresten verloren gehen. Daraus folgt eine irreversible Veränderung der Sekundär- und Tertiärstruktur der Proteine, wodurch das Substrat nach dem Schlüssel-Schloss-Prinzip nicht mehr in das aktive Zentrum passt. Folglich kann kein Substrat mehr umgesetzt werden.
1.2.2
Diagramm und Begründung der Reaktionsgeschwindigkeit
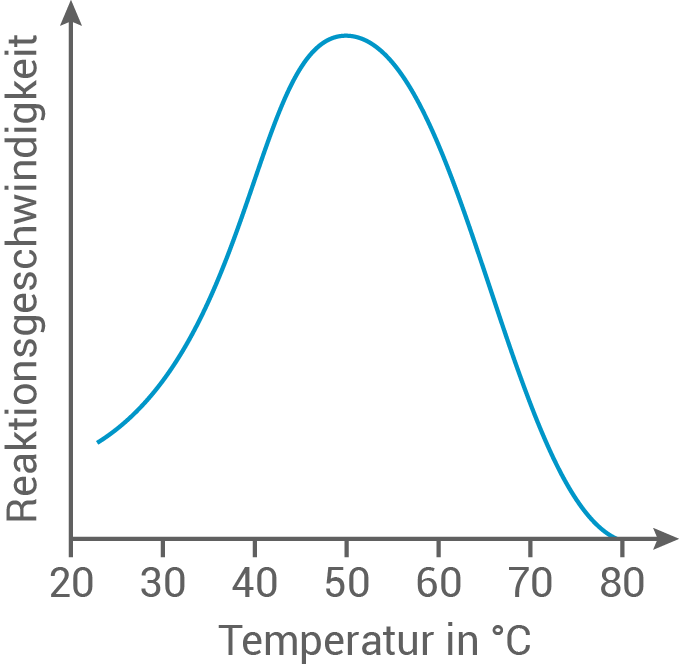 Für enzymatische Reaktionen gilt bei niedrigen Temperaturen die RGT-Regel, die besagt, dass sich die Reaktionsgeschwindigkeit bei einer Temperaturerhöhung von
Für enzymatische Reaktionen gilt bei niedrigen Temperaturen die RGT-Regel, die besagt, dass sich die Reaktionsgeschwindigkeit bei einer Temperaturerhöhung von  jeweils verdoppelt. Mit steigender Temperatur denaturieren jedoch immer mehr Eiweiß-Moleküle, wodurch die Enzyme ihre Wirkung verlieren. Dies führt dazu, dass die Reaktionsgeschwindigkeit wieder abnimmt, da immer weniger Enzyme aktiv sind. Dadurch entsteht eine „Optimumskurve“. Das Temperaturoptimum dieses Enzyms liegt bei etwa
jeweils verdoppelt. Mit steigender Temperatur denaturieren jedoch immer mehr Eiweiß-Moleküle, wodurch die Enzyme ihre Wirkung verlieren. Dies führt dazu, dass die Reaktionsgeschwindigkeit wieder abnimmt, da immer weniger Enzyme aktiv sind. Dadurch entsteht eine „Optimumskurve“. Das Temperaturoptimum dieses Enzyms liegt bei etwa 

2.1
Konzentrations-Zeit-Diagramm
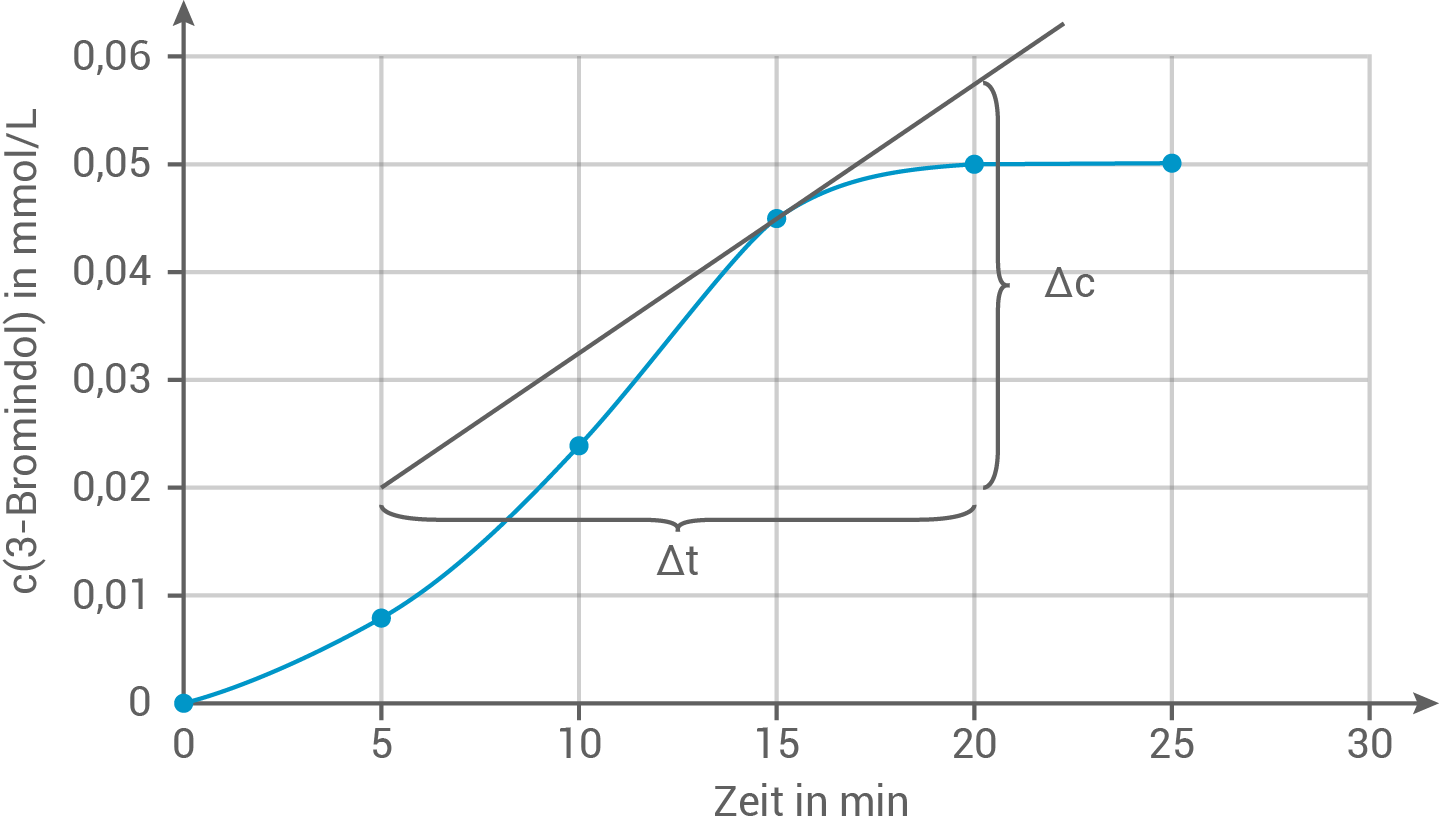 Bestimmung der momentanen Reaktionsgeschwindigkeit
Die momentane Reaktionsgeschwindigkeit ergibt sich aus der Tangentensteigung, bei
Bestimmung der momentanen Reaktionsgeschwindigkeit
Die momentane Reaktionsgeschwindigkeit ergibt sich aus der Tangentensteigung, bei  welche sich mithilfe des Steigungsdreiecks berechnen lässt:
welche sich mithilfe des Steigungsdreiecks berechnen lässt:
![\(\begin{array}[t]{rll}
v\,_{t=15}&=& \dfrac{\Delta c}{\Delta t} & \\[5pt]
&=& \dfrac{0,036\,\text{mmol} \cdot \text{L}^{-1}}{15\,\text{min}} & \\[5pt]
&=& 0,0024\,\text{mmol} \cdot \text{L}^{-1} \cdot \text{min}^{-1}
\end{array}\)](https://www.schullv.de/resources/formulas/f0f4330ba4d07518042b129e4aa43ef7708f97a6e0ca1587f4ba8886ac941e0a_light.svg) Bestimmung der mittleren Reaktionsgeschwindigkeit
Für die Berechnung der mittleren Reaktionsgeschwindigkeit zwischen
Bestimmung der mittleren Reaktionsgeschwindigkeit
Für die Berechnung der mittleren Reaktionsgeschwindigkeit zwischen  und
und  Minuten folgt:
Minuten folgt:
![\(\begin{array}[t]{rll}
\bar{v} &=& \dfrac{c_{15}- c_5}{t_{15}-t_5} & \\[5pt]
&=& \dfrac{(0,045 - 0,008)\,\text{mmol} \cdot \text{L}^{-1}}{15\,\text{min} - 5\,\text{min}} & \\[5pt]
&=& 0,0037\,\text{mmol} \cdot \text{L}^{-1} \text{min}^{-1}
\end{array}\)](https://www.schullv.de/resources/formulas/b688010b70cafe281d0db0341399e5915fe40df919a1193a41a3b9f300417b68_light.svg)

2.2
Hypothese zur Wirkungsweise von Enzymen
Substrate binden an das aktive Zentrum von Enzymen. Dabei gilt das Schlüssel-Schloss-Prinzip:
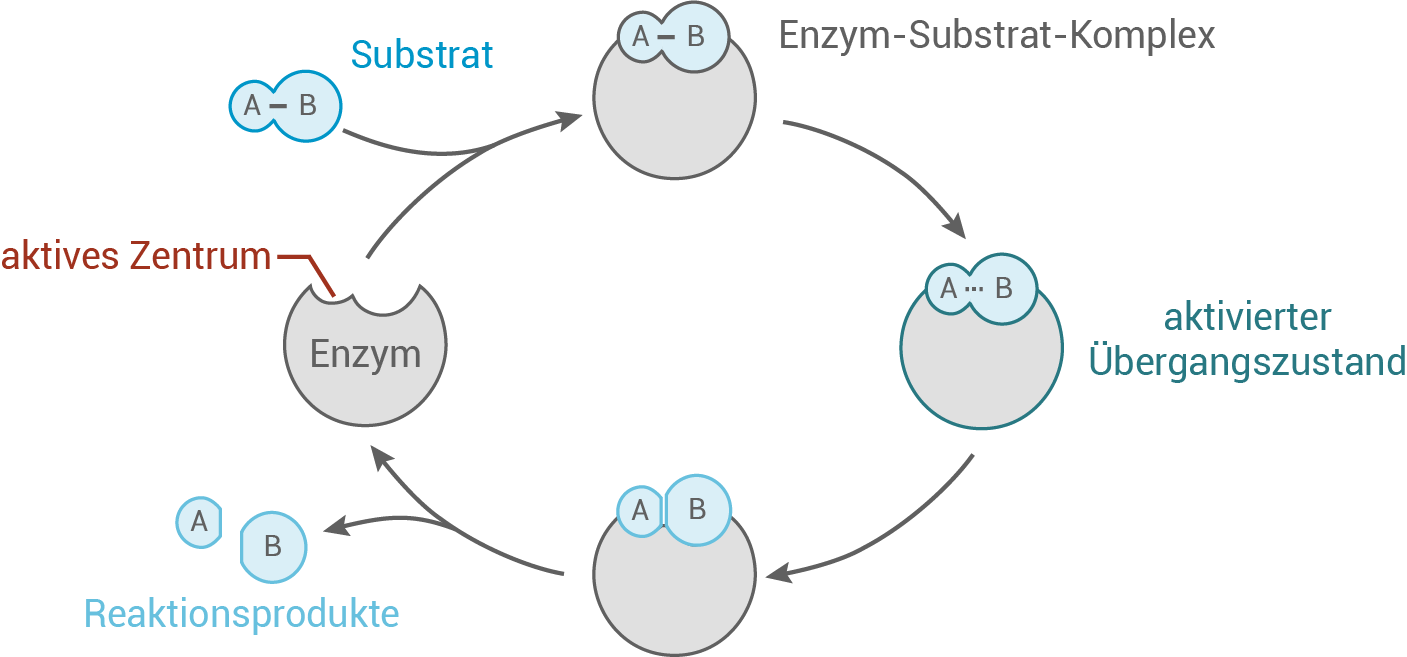 In Meerwasser ist die Konzentration der Chlorid-Ionen viel höher als die von Bromid-Ionen, jedoch produziert die Halogenase trotzdem mehr Brom- als Chlorverbindungen. Dies liegt an der Substratspezifität der Enzyme: Bromid-Ionen passen besser in das aktive Zentrum des Enzyms als Chlorid-Ionen, wodurch die Halogenase mehr Bromid- als Chlorid-Ionen umsetzt.
In Meerwasser ist die Konzentration der Chlorid-Ionen viel höher als die von Bromid-Ionen, jedoch produziert die Halogenase trotzdem mehr Brom- als Chlorverbindungen. Dies liegt an der Substratspezifität der Enzyme: Bromid-Ionen passen besser in das aktive Zentrum des Enzyms als Chlorid-Ionen, wodurch die Halogenase mehr Bromid- als Chlorid-Ionen umsetzt.

2.3
Durchführung und Beobachtung einer geeigneten Nachweisreaktion
Der Proteincharakter kann mithilfe der Biuret-Reaktion nachgewiesen werden.
Hierbei wird die zu untersuchende Halogenase-Lösung zunächst mit Natronlauge  versetzt. Anschließend wird die Biuret-Reagenz, eine Kupfer(II)-sulfat-Lösung, zur Probe gegeben. Der Proteincharakter zeigt sich durch eine Komplexbildung, die die Lösung blau-violett färbt. Bei einem negativen Test würde sich hingegen ein blauer Feststoff am Boden absetzen.
Eine weitere geeignete Nachweisreaktion ist die Xanthoprotein-Reaktion.
versetzt. Anschließend wird die Biuret-Reagenz, eine Kupfer(II)-sulfat-Lösung, zur Probe gegeben. Der Proteincharakter zeigt sich durch eine Komplexbildung, die die Lösung blau-violett färbt. Bei einem negativen Test würde sich hingegen ein blauer Feststoff am Boden absetzen.
Eine weitere geeignete Nachweisreaktion ist die Xanthoprotein-Reaktion.
3
Ableitung der Anzahl an möglichen Stereoisomeren
Ein Molekül mit  Stereozentren besitzt
Stereozentren besitzt  Stereoisomere.
Alanin besitzt ein chirales Zentrum an
Stereoisomere.
Alanin besitzt ein chirales Zentrum an  also ist
also ist 
Es existieren demnach Stereoisomere.
Begründung der optischen Inaktivität
Die entstandenen Produkte bilden ein Racemat, wobei die beiden Enantiomere im Verhältnis 1:1 entstehen. Sie zeigen denselben Drehwinkel für linear polarisiertes Licht, jedoch in entgegengesetzten Richtungen. Aufgrund dieser entgegengesetzten Drehungen heben sich die Effekte gegenseitig auf, was bedeutet, dass im Polarimeter keine Änderung des Drehwinkels beobachtet wird.
Stereoisomere.
Begründung der optischen Inaktivität
Die entstandenen Produkte bilden ein Racemat, wobei die beiden Enantiomere im Verhältnis 1:1 entstehen. Sie zeigen denselben Drehwinkel für linear polarisiertes Licht, jedoch in entgegengesetzten Richtungen. Aufgrund dieser entgegengesetzten Drehungen heben sich die Effekte gegenseitig auf, was bedeutet, dass im Polarimeter keine Änderung des Drehwinkels beobachtet wird.
Es existieren demnach