A1 – Wasserstoff zur Energiespeicherung
Hinweis: Wähle drei der vier vorliegenden Aufgaben in der Prüfung zur Bearbeitung aus.
Der Einsatz von Wasserstoff als Energiespeicher wird intensiv erforscht. Elektrische Energie lässt sich durch Elektrolyse von Wasser in chemische Energie umwandeln. Die Energie kann auf diese Weise zur späteren Verwendung gespeichert werden.
Skizziere den Aufbau einer PEM-Elektrolysezelle. Erkläre die Bedeutung der Protonenaustauschmembran für die Funktion der Zelle. (M 1)
Erkläre anhand von Abbildung 1 die photokatalytische Wasserspaltung. Beurteile auf Basis des jeweiligen Stoff- und Energiebedarfs der elektrochemischen und der photokatalytischen Wasserstoffgewinnung deren technische Einsetzbarkeit. (M 1)
Berechne für den Modellreaktor die bei der RWGS-Reaktion im Gleichgewicht vorliegende Konzentration an Kohlenstoffmonoxid. Erkläre anhand des Prinzips von Le Chatelier sowie Tabelle 1 zwei Möglichkeiten, um die Ausbeute von Kohlenstoffmonoxid zu erhöhen. (M 2)
Bewerte die drei in Tabelle 2 dargestellten Methoden der Wasserstoffspeicherung hinsichtlich der Kriterien Wirtschaftlichkeit, Sicherheit und Energieeffizienz. (M 3)
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Material 1: Wasserstofferzeugung
Wasserstoff für den Betrieb von Brennstoffzellen kann durch Elektrolyse von Wasser erzeugt werden. Ein Beispiel dafür ist die sogenannte PEM-Elektrolyse, deren Besonderheit die Verwendung einer Protonenaustauschmembran (proton exchange membrane = PEM) ist. Bei diesem Verfahren wird Wasser an einer Iridiumelektrode vorbeigeleitet. Die Wasser-Moleküle geben hier ihre Protonen ab und es bilden sich Sauerstoff-Moleküle. Die abgegebenen Protonen wandern erst durch die Iridiumelektrode, danach durch die PEM und dann durch eine Kohlenstoffelektrode und reagieren an der Platinbeschichtung dieser Kohlenstoffelektrode mit Elektronen zu Wasserstoff.
Eine weitere Möglichkeit zur Gewinnung von Wasserstoff stellt die photokatalytische Spaltung von Wasser dar, bei der Wasserstoff direkt mithilfe von Licht erzeugt wird.
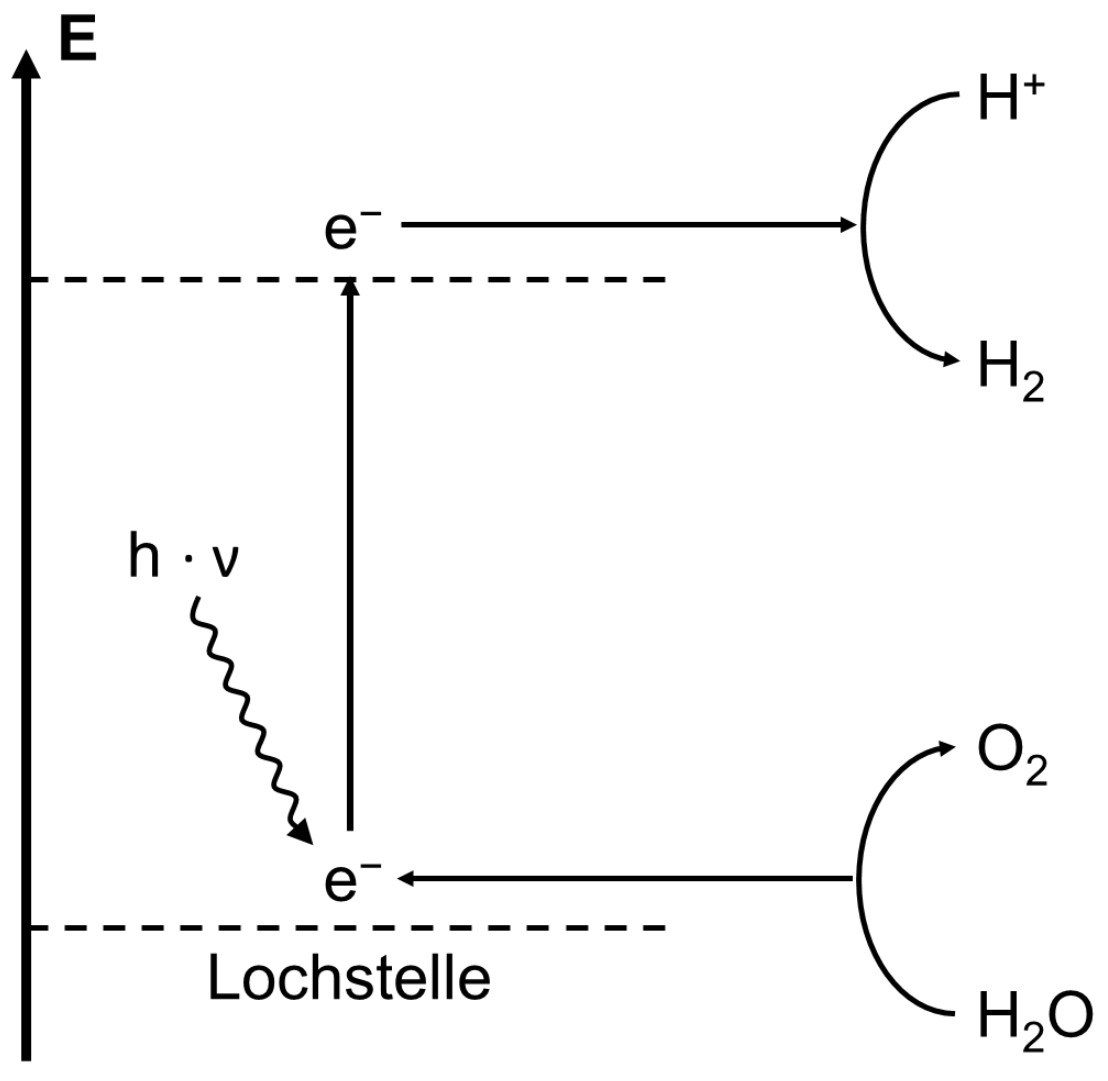
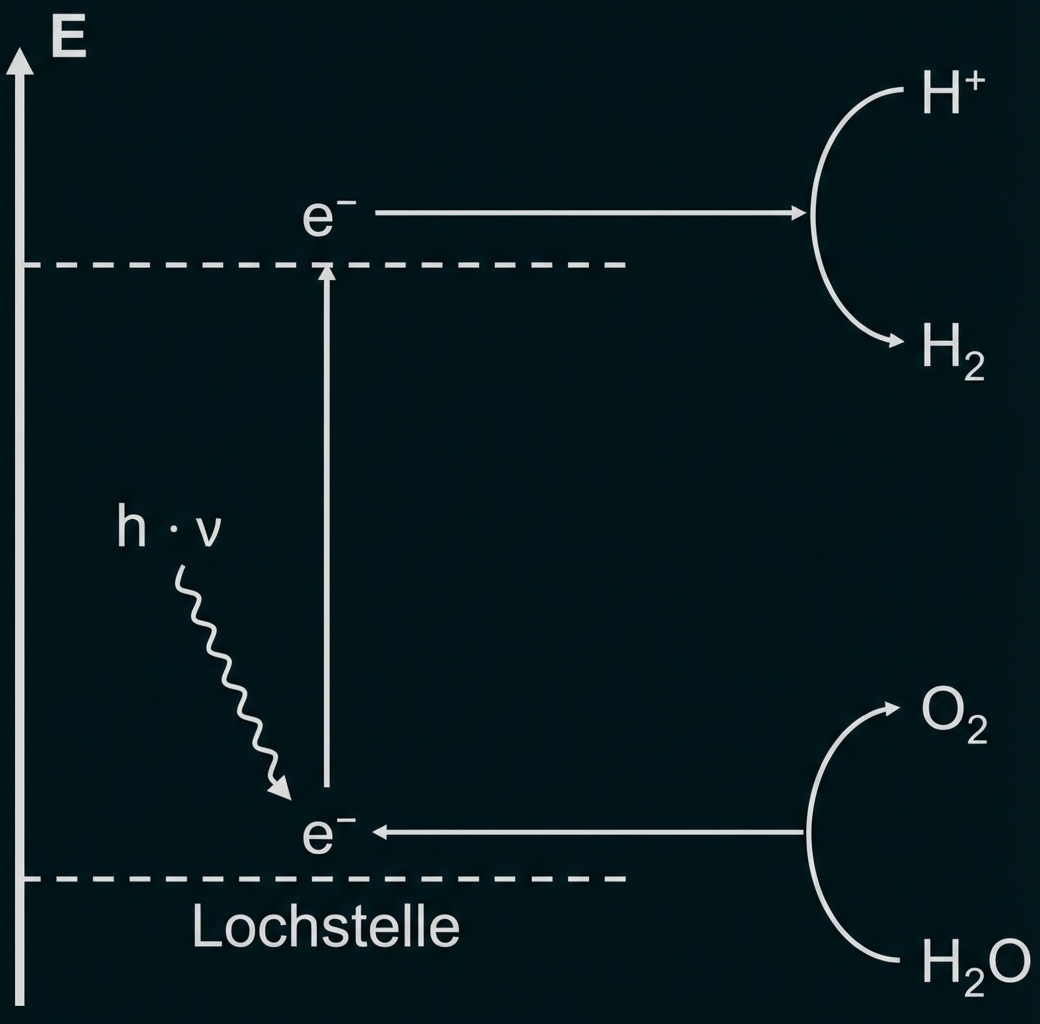
Abb. 1: Schema zur photokatalytischen Wasserspaltung
Material 2: Power-to-gas
Der erzeugte Wasserstoff kann zur weiteren Verwendung mit einer Kohlenstoffverbindung zu Methan umgesetzt werden. Eine Möglichkeit ist die Methanisierung von Kohlenstoffdioxid, die in zwei Reaktionsschritten abläuft (Tab. 1).
Tab. 1: Methanisierung von Kohlenstoffdioxid1
|
Reaktionsgleichung |
Reaktionsenthalpie in kJ/mol |
|
|---|---|---|
|
Reverse Wassergas- Shift-Reaktion (RWGS) |
|
|
|
Sabatier-Prozess |
|
|
|
Gesamtreaktion |
|
|
In einem kleinen Modellreaktor wird die RWGS-Reaktion bei durchgeführt. Eingeleitet wird ein Eduktgemisch aus Wasserstoff und Kohlenstoffdioxid. Im Gleichgewicht beträgt die Wasserstoffkonzentration
und die Kohlenstoffdioxidkonzentration
Zu Beginn liegen weder Kohlenstoffmonoxid noch Wasser vor. Die Gleichgewichtskonstante der Reaktion beträgt
Material 3: Wasserstoffspeicher
Wasserstoff weist eine relativ geringe Dichte auf. Zur technischen Nutzung ist es nötig, ihn platzsparend speichern zu können. Tabelle 2 stellt verschiedene Möglichkeiten gegenüber.
Tab. 2: Möglichkeiten der Wasserstoffspeicherung2,3
|
Verflüssigung |
Kompression |
Methanisierung (Power-to-gas) |
|
|
volumetrische Lagerungskapazität in
|
ca. |
ca. |
ca. |
|
Betriebstemperatur des Systems |
|
Raum- temperatur |
Lagerung:
|
|
Lagerdruck in |
|
|
|
|
Nutzung vorhandener Infrastruktur |
nein |
nein |
ja |
|
Energieverlust durch Lagerung und Freisetzung |
|
|
|
Quellen:
1 https://elib.dlr.de/114888/1/Adelung_WCCE10_Experimental%20investigation%20of%20the%20reverse%20water-gas%20shift%20reaction%20at%20high%20temperature%20and%20elevated%20pressure.pdf
2 https://www.researchgate.net/figure/Overview-of-selected-materials-and-their-volumetric-and-gravimetric-hydrogen-density-The_fig2_312870399
3 Aakko-Saksa, P., Cook, C., Kiviaho, J., & Repo, T. (2018). Liquid organic hydrogen carriers for transportation and storing of renewable energy – Review and discussion. Journal of Power Sources, 396, 803–823. https://doi.org/10.1016/j.jpowsour.2018.04.011
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Skizze der beschriebenen PEM-Elektrolysezelle:
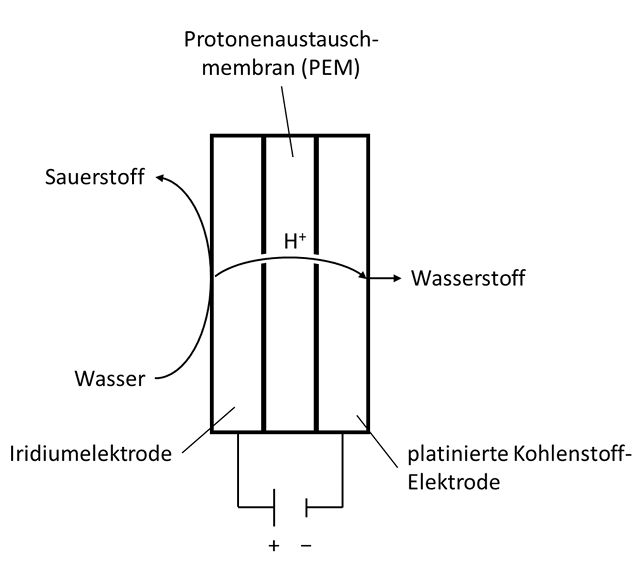
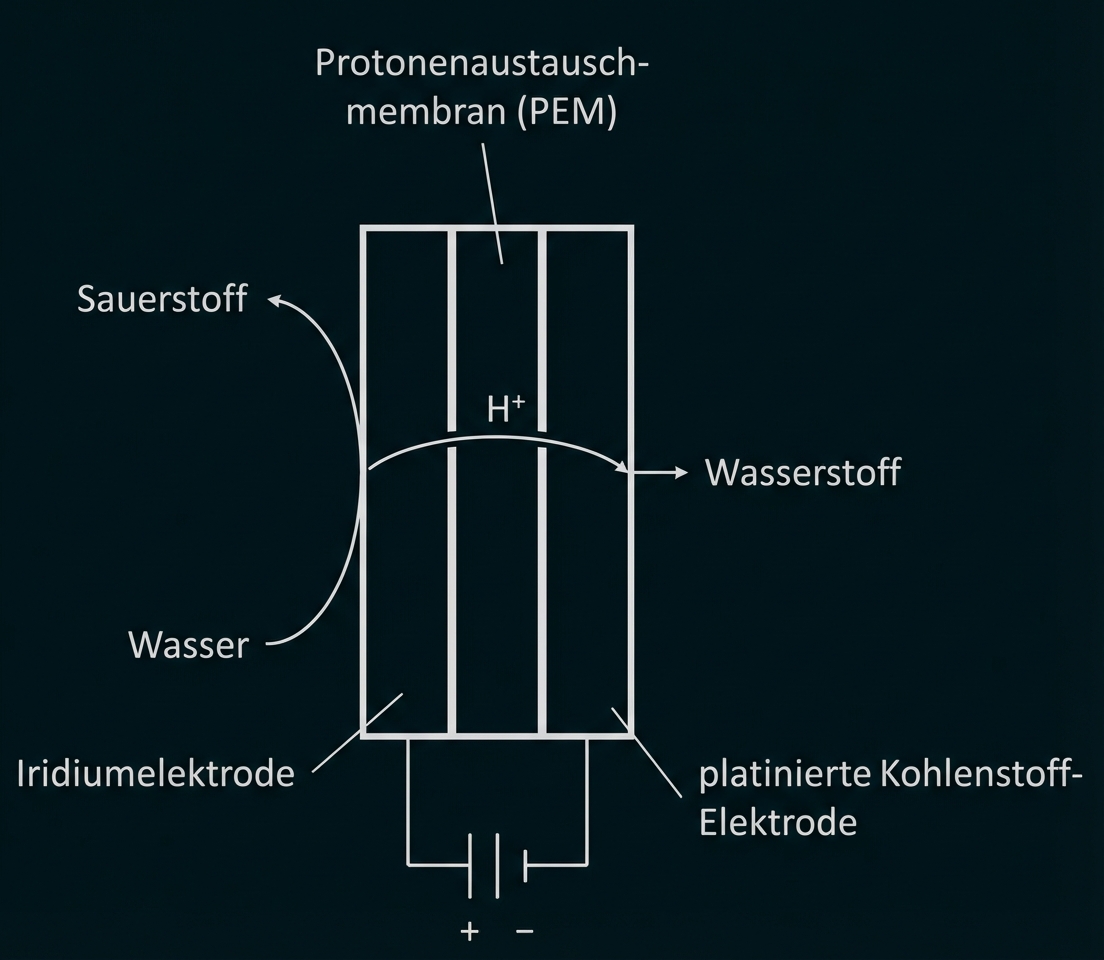
Die Protonenaustauschmembran ermöglicht den Ionenfluss und schließt damit den Stromkreis. Außerdem würde sonst keine Möglichkeit bestehen, dass die Protonen zur Kathode gelangen.
Bei der photokatalytischen Wasserstoffgewinnung werden an einem geeigneten Trägermaterial, das gleichzeitig Lichtenergie absorbiert und die Wasserspaltung katalysiert, angeregte Elektronen auf Protonen übertragen und so elementarer Wasserstoff erzeugt. Die Elektronenlücke im Material wird durch die Spaltung von Wasser in Protonen und elementaren Sauerstoff gefüllt.
Vergleich zwischen Elektrolyse und photokatalytischer Spaltung, z. B.: Der Wirkungsgrad bei der Elektrolyse liegt wesentlich höher als bei der photokatalytischen Spaltung. Sonnenlicht ist im Gegensatz zu elektrischer Energie nicht durchgehend verfügbar. Für den Aufbau einer elektrochemischen Zelle zur Photokatalyse sind deutlich weniger Rohstoffe als für die Elektrolyse nötig.
Aufgrund der beiden ersten Nachteile der photokatalytischen Spaltung ist deren Einsetzbarkeit derzeit noch nicht großtechnisch möglich.
Gegeben: ca.
Gesucht:
Aufstellen des Massenwirkungsgesetzes:
Ersetzen der Wasser- durch die Kohlenstoffmonoxid-Konzentration:
Auflösen und Einsetzen:
Möglichkeit 1: Temperaturerhöhung
Die RWGS-Reaktion hat eine positive Reaktionsenthalpie, ist also endotherm. Nach dem Prinzip von Le Chatelier reagiert ein im Gleichgewicht befindliches System auf einen äußeren Zwang immer durch eine Neueinstellung des Gleichgewichts so, dass es dem Zwang ausweicht. Durch eine Temperaturerhöhung wird die endotherme Reaktionsrichtung bevorzugt, wodurch sich mehr Kohlenstoffmonoxid bildet.
Möglichkeit 2: z. B.: Erhöhen der Konzentration des eingeleiteten Kohlenstoffdioxids.
Nach dem Prinzip von Le Chatelier folgt hier, dass einer Erhöhung der Kohlenstoffdioxid-Konzentration entgegengewirkt wird, indem die Eduktkonzentrationen ab- und die Produktkonzentrationen zunehmen.
Kriterium 1: Wirtschaftlichkeit
Die volumetrische Lagerkapazität sollte möglichst groß sein, da andernfalls größere Tanks zur Speicherung gebaut werden müssen und die Materialkosten für den Bau somit höher werden. Eine Nutzung bestehender Infrastruktur spart Kosten.
Kriterium 2: Energieeffizienz
Bei der Lagerung und Freisetzung des gespeicherten Wasserstoffs sollte möglichst wenig Energie benötigt werden. Damit sind alle Verfahren, bei denen eine Kühlung oder Erhitzen notwendig sind, eher als ungünstig einzuschätzen.
Kriterium 3: Sicherheit
Eine Lagerung unter hohem Druck birgt das Risiko, dass Behälter bei Beschädigung platzen können und die entstehende Druckwelle für große Schäden sorgt.
Schlussfolgerung
Eine Lagerung unter Kompression bietet sich nicht an, da ein Sicherheitsrisiko besteht. Die Lagerung als Flüssigwasserstoff verbraucht große Energiemengen, um die Kühlung aufrechtzuerhalten und ist deshalb weder nachhaltig noch wirtschaftlich. Bei der Methanisierung muss nicht so stark gekühlt werden und es kann die bereits bestehende Infrastruktur genutzt werden, womit diese Methode hier wahrscheinlich am besten geeignet ist.