Aufgabe A – Kältesofortkompressen
Hinweis: Die Aufgabe A beinhaltet einen fachpraktischen Anteil und muss in der Prüfung bearbeitet werden. Von den anderen drei Aufgaben B, C und D müssen zwei zur Bearbeitung ausgewählt werden.
Zur Kühlung von Verletzungen kann man in der Ersten Hilfe und im Rettungswesen sogenannte Kältesofortkompressen verwenden.
Fertige eine beschriftete Skizze für den Lösevorgang einer Ionensubstanz in Wasser auf der Teilchenebene an.
Erläutere den allgemeinen Zusammenhang zwischen Gitter-, Hydratations- und Lösungsenthalpie für den Lösevorgang.
Schülerexperiment
Ermittle experimentell auch unter Angabe der relevanten Beobachtungen mit den gegebenen Materialien die molare Lösungsenthalpie von Ammoniumnitrat (M 2).
Beurteile die Eignung des Experiments zur Bestimmung der molaren Lösungsenthalpie von Ammoniumnitrat unter Berücksichtigung des zu berechnenden theoretischen Wertes.
Hinweis: Solltest du keinen Wert für die theoretische Lösungsenthalpie ermitteln können, nutze den fiktiven Wert von
Erkläre die Funktionsweise einer Kältesofortkompresse (M 1).
Beweise rechnerisch, dass der Lösevorgang von Ammoniumnitrat unter Standardbedingungen exergonisch verläuft.
Der Lösevorgang eines Salzes wird häufig als chemische Reaktion bezeichnet.
Beurteile die Richtigkeit dieser Aussage am Beispiel des Lösevorgangs von Ammoniumnitrat anhand von zwei Kriterien.
Der Einsatz der beschriebenen Do-it-yourself Kompresse ist nicht zu empfehlen.
Begründe diese Aussage unter Zuhilfenahme einer Berechnung (M 3).
Formuliere die Reaktionsgleichung für die Herstellung
von Ammoniumnitrat (M 4).
eines Edukts für die Reaktion aus Aufgabe a.
Diskutiere anhand von vier Argumenten die Verwendung von Ammoniumnitrat in Kältesofortkompressen (M 1 bis M 4).
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Material 1: Kältesofortkompressen
In einer Kunststoffhülle befinden sich granuliertes Ammoniumnitrat und ein mit Wasser gefülltes Päckchen. Zur Anwendung wird die Kompresse bis zum Platzen dieses Päckchens zusammengedrückt. Die äußere Hülle muss dabei verschlossen bleiben.
Die Kompresse ist bis zu Minuten kalt und kann nur einmal verwendet werden. Zudem sollte diese bei Raumtemperatur, sowie außerhalb der Reichweite von Kindern, gelagert werden.
Bei Berührung des Inhalts einer Kompresse mit der Haut sollte diese Minuten lang mit Wasser gespült werden. Bei Einnahme sollte sofort ein Arzt aufgesucht werden.
[1], [2]
Material 2: Experiment zur kalorimetrischen Bestimmung der Lösungsenthalpie
Geräte
-
Waage
-
Kalorimetergefäß
-
Temperaturmessgerät
-
ggf. Glasstab oder Magnetrührwerk
-
Messzylinder
-
Filterpapier oder Uhrglas o. Ä.
-
Spatel
Chemikalien
-
Ammoniumnitrat
-
destilliertes Wasser
Anmerkung:
Material 3: Do-it-yourself-Bauanleitung für Kältesofortkompressen
Eine Do-it-yourself-Bauanleitung für Kältekompressen empfiehlt ein Mischungsverhältnis der Inhaltsstoffe von (Bsp.
Ammoniumnitrat und
Wasser).
In Wasser sind theoretisch bis zu
Ammoniumnitrat löslich.
[3]
Material 4: Herstellung und Verwendung von Ammoniumnitrat
Ammoniumnitrat findet weiterhin vielseitige Verwendung z. B. als anorganisches Düngermittel und Sprengstoff. Ammoniumnitrat kann sich explosionsartig zersetzen. In den letzten Jahrzehnten ereignete sich eine große Zahl von Unfällen.
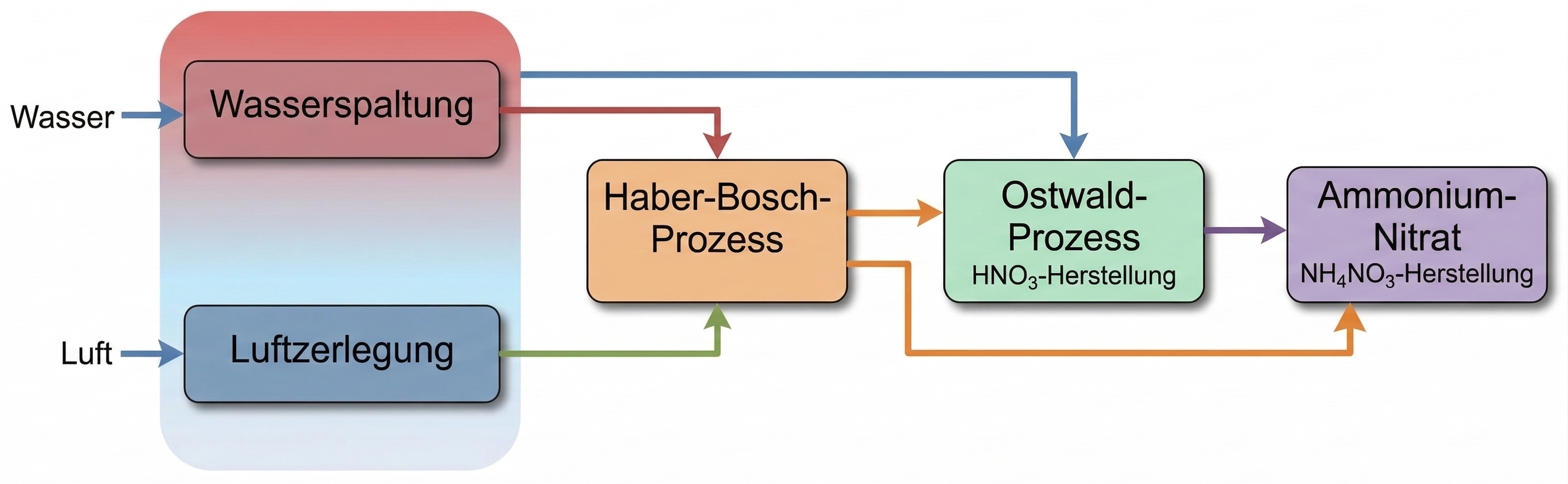
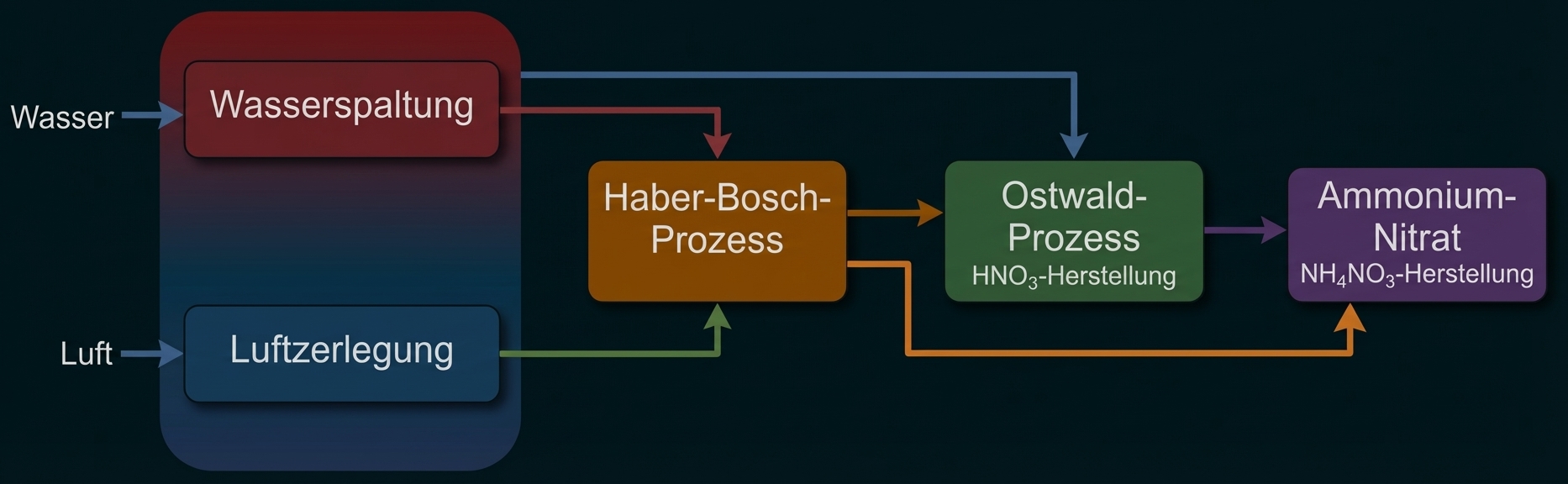
Abb. 1: Prozess zur Herstellung von Ammoniumnitrat (vereinfacht)
[4]
Anlage
Thermodynamische Werte
|
Ammoniumnitrat |
Ammonium-Ion |
Nitrat-Ion |
|
|
molare Gitter- enthalpie in |
|
/ |
|
|
molare Hydratations- enthalpie in |
|
|
|
|
molare Standard- bildungsenthalpie in |
|
|
|
|
molare Standardentropie in |
|
Quellen (ggf. verändert):
[1] Einsatz von Ammoniumnitrat (08.08.2013): http://anorganik.chemie.vias.org/ammoniumnitrat.html (letzter Zugriff am 03.02.2025)
[2] Aufbau und Untersuchung eines Kältesofortkompresse (05.01.2012): https://www.chemieunterricht.de/dc2/tip/08_05.htm (letzter Zugriff am 03.02.2025)
[3] Aufbau und Untersuchung eines Kältesofortkompresse (05.01.2012): https://www.chemieunterricht.de/dc2/tip/08_05.htm (letzter Zugriff am 03.02.2025)
[4] Üstun, Helin (2022): Synthese und Charakterisierung von sphärischen Perowskit-Granulaten für solare Anwendungen: https://elib.dlr.de/191766/1/Masterthesis_HelinU%CC%88stu%CC%88n.pdf (letzter Zugriff am 03.02.2025)
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Anfertigen einer Skizze
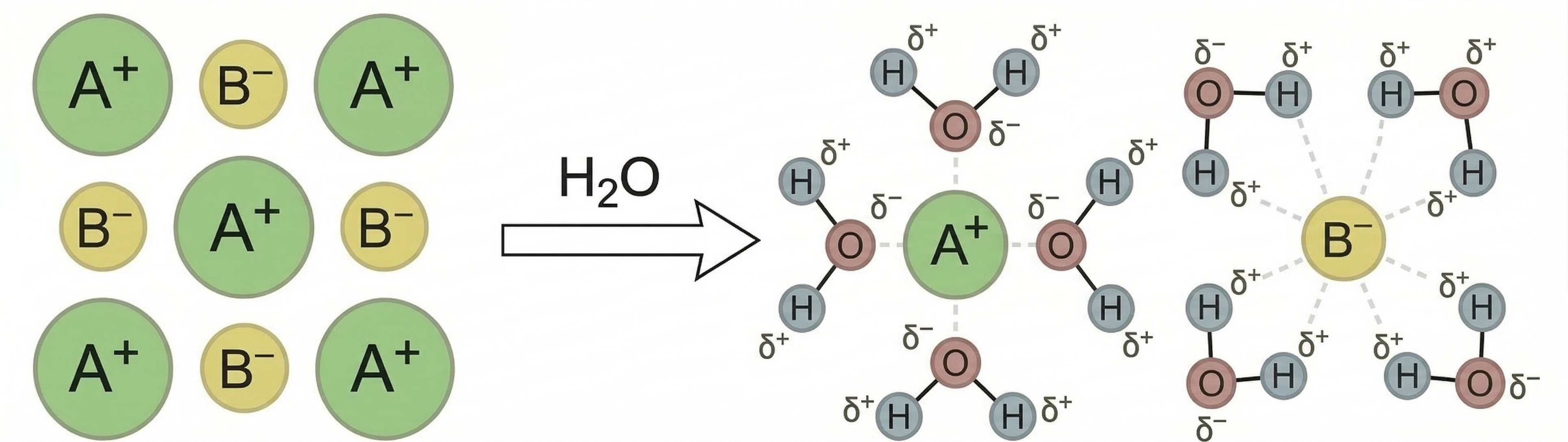
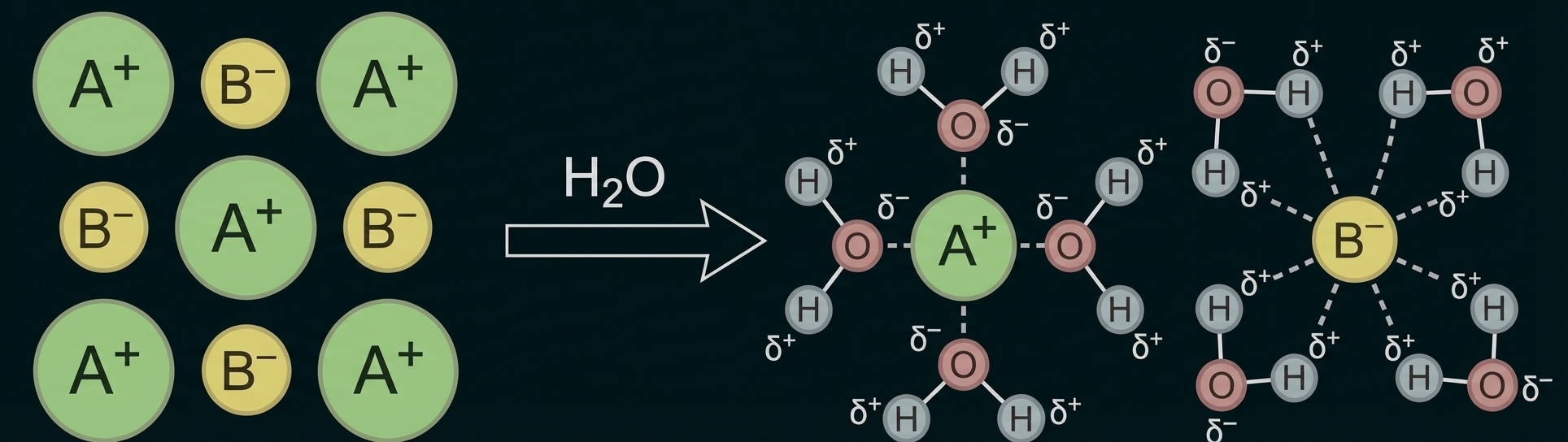
Erläuterung des Zusammenhangs
-
Gitterenthalpie: Energie, die zum Herauslösen von Ionen aus dem Ionengitter (Ionenbindung zu überwinden) aufgewendet werden muss
-
Hydratationsenthalpie: Energie, die freigesetzt wird, wenn sich Wasser-Moleküle an die Ionen anlagern
-
Lösungsenthalpie: Summe aus Gitterenthalpie und Hydratationsenthalpie, bei positiven Werten ist der Vorgang endotherm, im umgekehrten Fall exotherm
Hinweis: Bei dem Schülerexperiment werden außerdem der Arbeitsschutz und die Durchführung bewertet.
Angeben der Beobachtungen
-
vollständiges Auflösen des Salzes
-
Werte für Temperatur des Anfangs- und Endzustands
Berechnung der molaren Lösungsenthalpie mithilfe der Kalorimetergleichung
Berechnung des theoretischen Werts der molaren Lösungsenthalpie
Anhand der Abweichung zum theoretisch berechneten Wert soll das kalorimetrische Experiment auf seine Eignung zur Bestimmung der molaren Lösungsenthalpie beurteilt werden.
Erklärung der Funktionsweise
-
Durch Zusammendrücken des inneren Päckchens kommen Wasser und Ammoniumnitrat in Kontakt.
-
Ammoniumnitrat löst sich in einem endothermen Vorgang im Wasser.
-
Die Umgebung kühlt sich durch den Wärmeaustausch mit der Lösung ab.
Berechnung der freien molaren Standardbildungsenthalpie als Beweis für den spontanen Lösevorgang
Hinweis: Bei der Berechnung über den Satz von Hess ergeben sich je nach Werten deutlich abweichende, jedoch stets negative Ergebnisse.
Da die freie molare Standardlösungsenthalpie einen negativen Wert aufweist, handelt es sich somit um eine exergonische Reaktion.
Beurteilung der Aussage
-
Einerseits korrekt, da Energieumwandlung stattfindet
-
Andererseits nicht korrekt, denn es werden keine neuen Stoffe gebildet.
Umstellen der kalorimetrischen Grundgleichung:
Die Temperaturverringerung von Raumtemperatur um bedeutet Kühlung auf etwa
Solch eine Kompresse kann nicht eingesetzt werden, da Verletzungen der Haut auftreten können.
Formulieren der Reaktionsgleichungen
Diskussion der Verwendung von Ammoniumnitrat in Kältesofortkompressen
Pro-Argumente:
-
gut in Wasser löslich
-
bereits geringe Masse an Salz sorgt für effektive Abkühlung
Contra-Argumente:
-
Herstellung trotz hoher Verfügbarkeit des Stickstoffs sehr energieaufwendig, da Trennung von Sauerstoff, Gewinnung Wasserstoff, Salpetersäure usw.
-
Sprengstoff, hohes Gefährdungspotential
-
nur einmalige Verwendung möglich