Aufgabe B – Korrosion sinnvoll genutzt
Der Begriff Korrosion ist für Laien fast immer negativ besetzt, nicht allein, weil es durch diese pro Jahr zu Verlusten von etwa des Bruttoinlandsprodukts kommt. Es gibt aber auch Beispiele, bei denen diese elektrochemischen Vorgänge von Vorteil sind. Dazu gehört die Wärmekompresse.
Beschreibe die Reaktionen A bis E zur Bildung von Rost (M 1).
Erkläre die Beobachtungsergebnisse im Experiment zur Untersuchung der Einflussfaktoren auf Korrosion.
Benenne die verwendete Lösung in Ansatz C und formuliere die Reaktionsgleichung unter Angabe von Teilgleichungen (M 2).
Bestimme sowohl das Oxidations- und Reduktionsmittel als auch den Elektrolyten in einer Wärmekompresse.
Entwickle passend zur Fragestellung der Lernenden eine Versuchsdurchführung (M 3, M 4).
Beurteile die Handlungsempfehlungen beim Umgang mit Wärmekompressen (M 5).
Diskutiere die Verwendung von Wärmekompressen anhand von vier Argumenten.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Material 1: Die Bildung von Rost
Chemisch betrachtet ist Rost ein Stoffgemisch aus Eisen(II)-oxid und Eisen(III)-oxid, deren Teilchen von Wasser-Molekülen (Kristallwasser) umlagert sind. Da es sich nicht stöchiometrisch exakt in seiner Zusammensetzung beschreiben lässt, gilt für das rotbraune Stoffgemisch die folgende Formel:
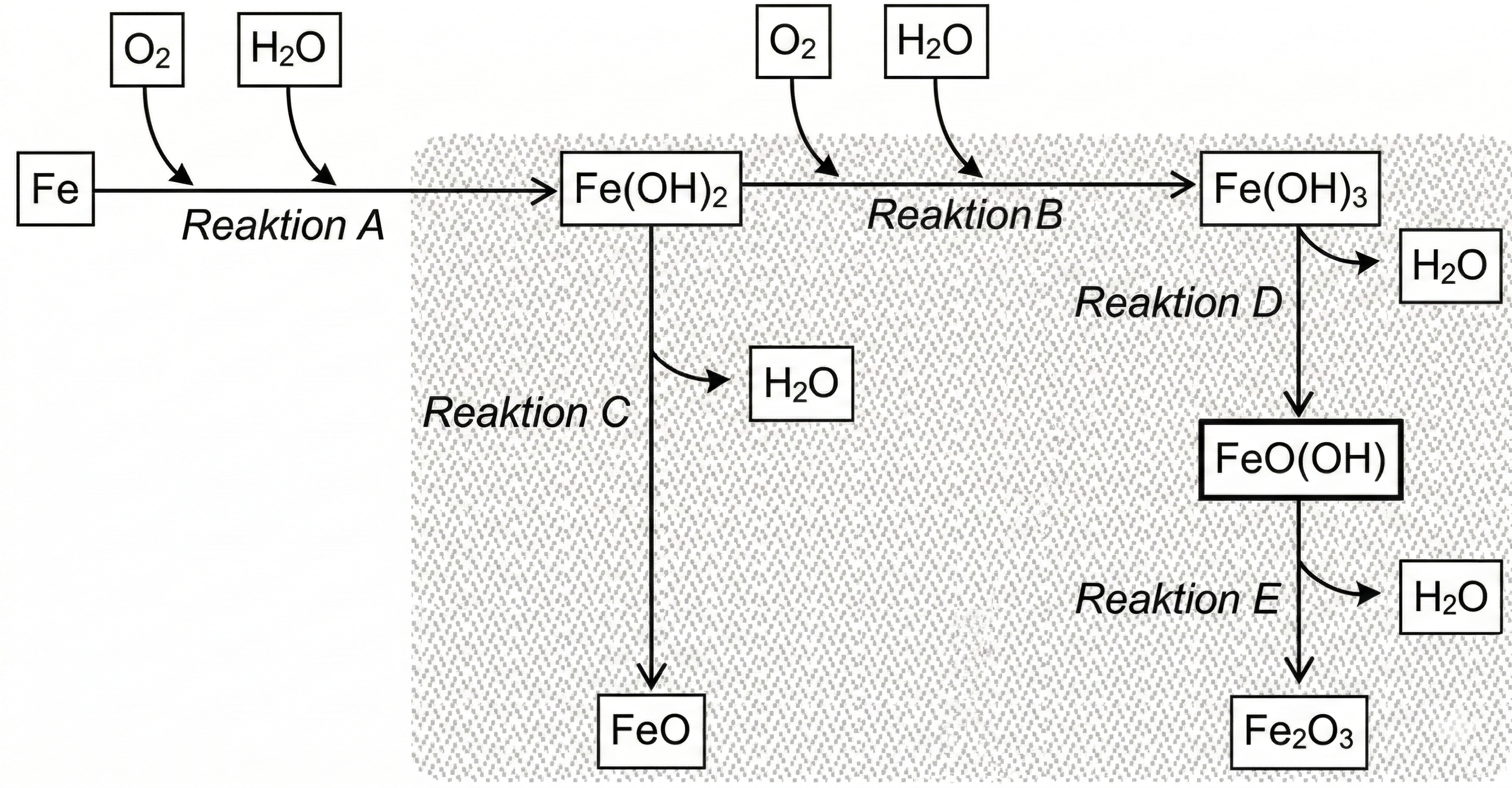
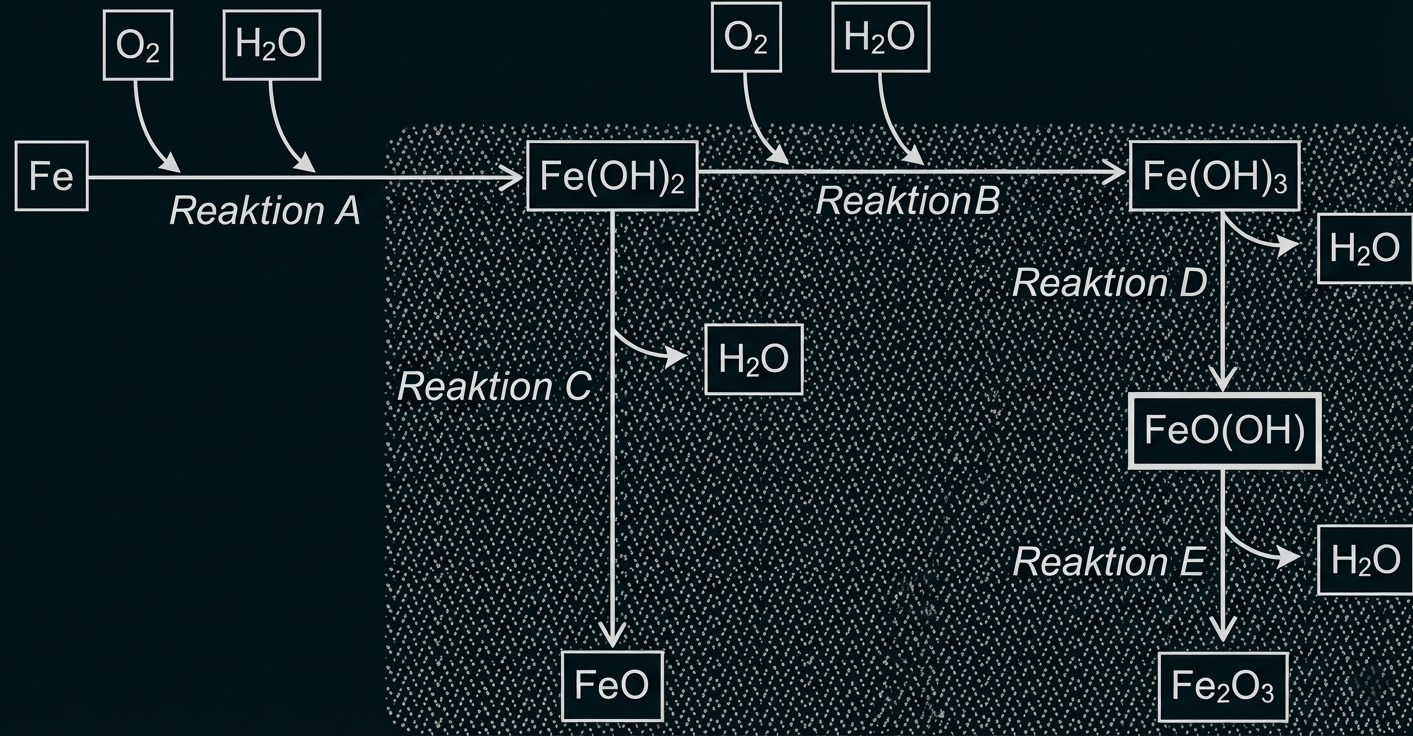
Abb. 1: ablaufende Reaktionen beim Vorgang des Rostens
[1]
Material 2: Einflussfaktoren auf die Korrosion
Jeweils ein gereinigter Eisennagel wird für die angegebene Zeit in verschiedene Lösungen getaucht.
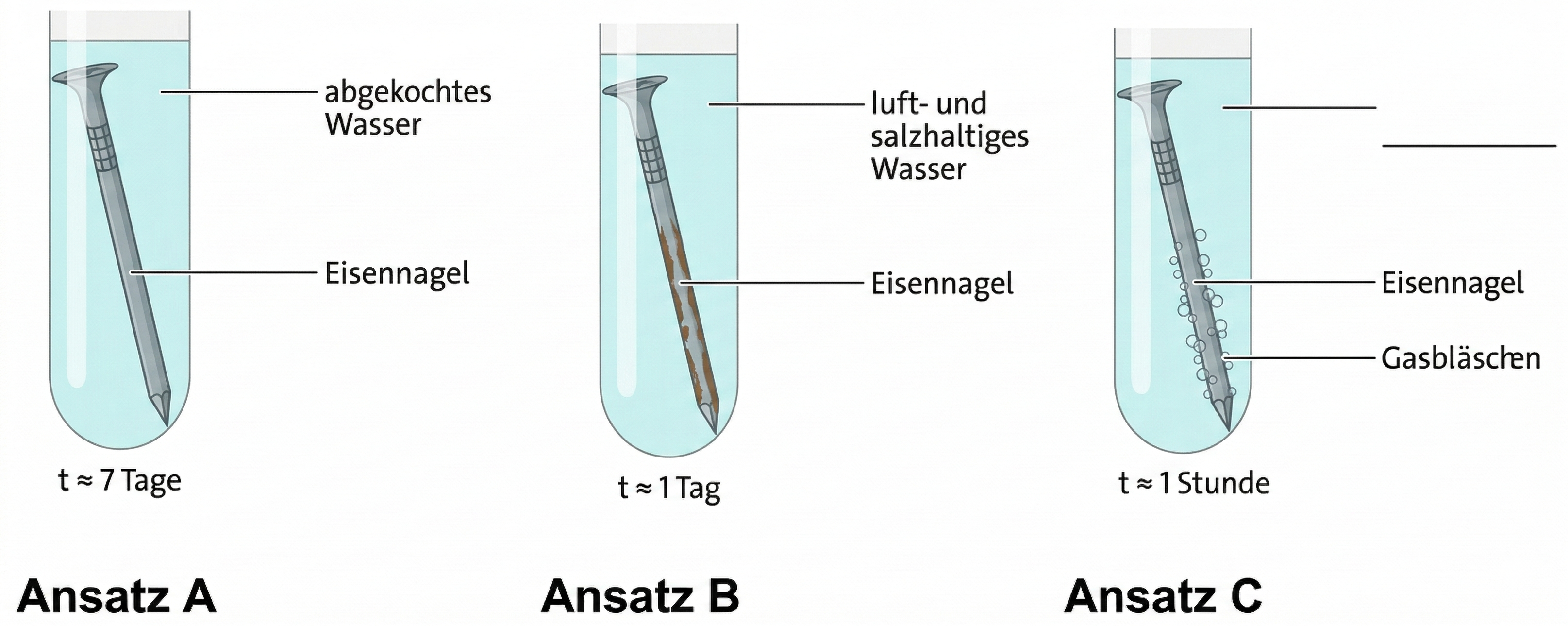
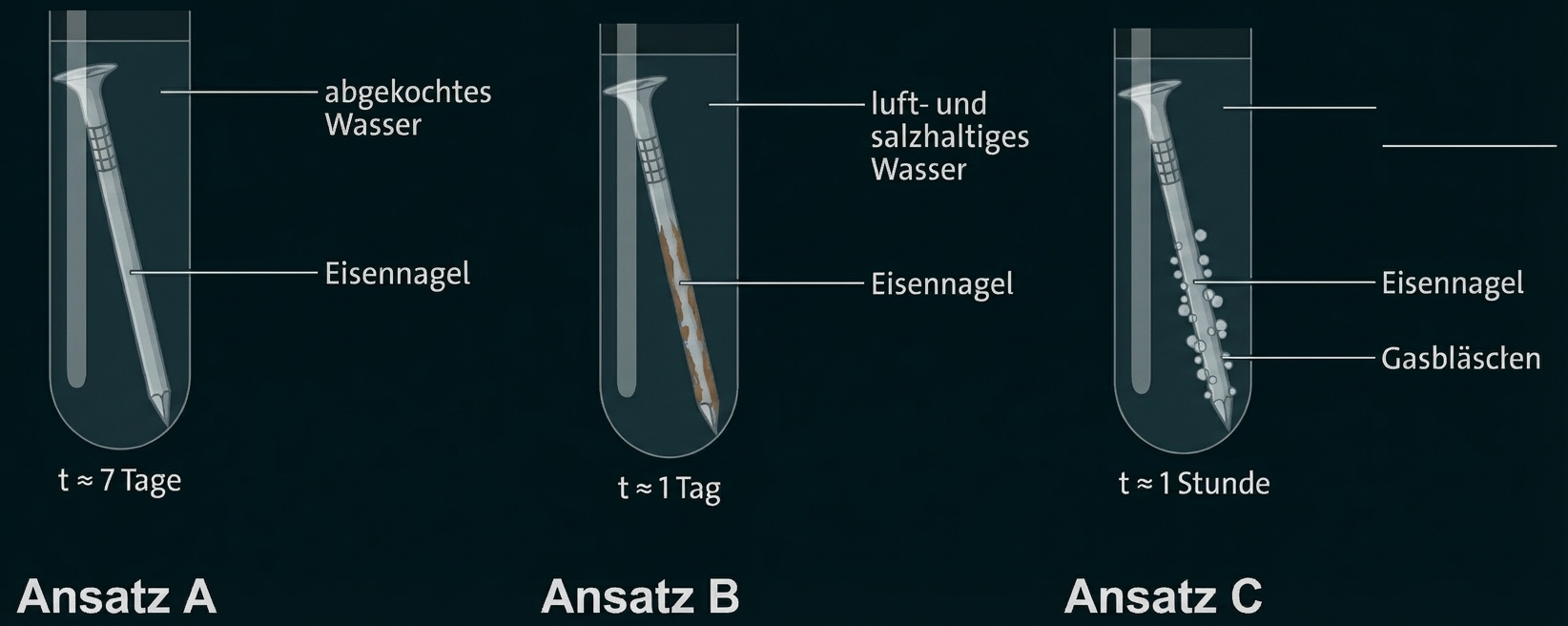
Abb. 2: Experimentierergebnisse (Ansatz A, Ansatz B, Ansatz C)
[2]
Material 3: Wärmekompressen
Wärmekompressen bestehen aus einem hautfreundlichen Vlies, welches einzelne Wärmezellen mit einer Mischung aus Eisengranulat, Aktivkohle, Natriumchlorid und Wasser umschließt. Kurz vor dem Gebrauch wird die Folienverpackung geöffnet, die Kompresse entnommen und an der schmerzenden Körperstelle angebracht. Die Wärmezellen erwärmen sich und erreichen innerhalb von 30 Minuten eine angenehme Temperatur, die über einen Zeitraum von 8 bis 12 Stunden (je nach Produkt) konstant beibehalten wird.
[3]
Material 4: Untersuchung der Funktionsweise einer Wärmekompresse im Schülerexperiment
Im Chemieunterricht möchten Schülerinnen und Schüler einer 8. Klasse folgende Frage zur Funktionsweise von Wärmekompressen experimentell untersuchen:
Durch welchen Luftbestandteil wird die Kompresse aktiviert?
In einer Experimentierbox stehen folgende Geräte zur Verfügung:
Waage, Thermometer, Spatel, Frischhaltefolie, drei Kunststoffspritzen mit Kanülen
[4]
Material 5: Handlungsempfehlungen beim Umgang mit Wärmekompressen
Der Hersteller von Wärmekompressen gibt u.a. folgende Hinweise zum Umgang:
|
a) |
Verpackung erst kurz vor der Anwendung öffnen. |
|
b) |
Die Haut muss an der zu behandelnden Stelle trocken sein. |
|
c) |
Vor der Entsorgung in den Hausmüll muss die Kompresse intensiv gewässert werden. |
[3]
Quellen (ggf. verändert):
[1] Duvinage et. al (2018): Wärmepflaster im Chemieunterricht nachgebaut: https://www.gdch.de/fileadmin/downloads/Publikationen/Nachrichten_aus_der_Chemie/PDFs/Downloads/waermepflaster.pdf (letzter Zugriff am 16.05.24)
[2] Arnold, Karin (Hrsg.) (2018): Korrosion von Eisennägeln Fokus Chemie, Sekundarstufe II, Unterrichtsmanager, Materialien, S.206
[3] Funktionsweise eines Wärmepflasters: https://www.thermacare.de/produkte/anwendung-funktionsweise (letzter Zugriff am 16.05.24)
[4] Aufbau einer Wärmekompresse: Lebensnaher Chemieunterricht, Unterricht Chemie 142/2014 S. 24-30
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?-
Reaktion A: Eisen(II)-hydroxid entsteht, wenn es zu einem direkten Kontakt von Eisen mit Sauerstoff und Wasser kommt.
-
Reaktion B: Dieses reagiert mit Wasser und Sauerstoff zu Eisen(III)-hydroxid.
-
Reaktion C: Eisen(II)-hydroxid reagiert unter Abspaltung von Wasser zu Eisen(II)- oxid weiter.
-
Reaktion D: Unter Abspaltung von Wasser bildet sich aus Eisen(III)-hydroxid unter anderem Eisen(III)-oxidhydroxid.
-
Reaktion E: Umwandlung von Eisen(III)-oxidhydroxid unter Abgabe von Wasser zu Eisen(III)-oxid
Hinweis: Die Beschreibung der Reaktionen ist auch auf Teilchenebene möglich.
Erklärung der Experimentbeobachtungen
-
Ansatz A: nach sieben Tagen keine Veränderungen → abgekochtes Wasser enthält keinen Sauerstoff → keine Korrosion
-
Ansatz B: nach einem Tag rotbraune Färbung → Sauerstoff/Wasser vorhanden, Ionen erhöhen die elektrische Leitfähigkeit → Korrosion läuft schnell ab
-
Ansatz C: Gasblasenaufstieg → sofortige Entstehung von Wasserstoff → Säurekorrosion
Es handelt sich bei der verwendeten Lösung im Ansatz C um eine Säurelösung.
Formulierung der Reaktionsgleichungen
|
Oxidation: |
|
|
Reduktion: |
|
|
Gesamtgleichung: |
|
|
|
|
Zuordnung der Fachbegriffe zu den Teilen der Wärmekompresse
-
Reduktionsmittel – Eisen
-
Oxidationsmittel – Sauerstoff
-
Elektrolyt – Wasser/Natriumchlorid
Planung eines Experiments
-
drei gleiche Ansätze bezüglich Masse von Eisen, Aktivkohle, Wasser und Natriumchlorid
-
jeweils gut zu einer Paste vermischen
-
in Haushaltsfolie einpacken/verschließen
-
über Kanüle und Spritze werden gleiche Volumen von Luft/reinem Sauerstoff/reinem Stickstoff durch Beimpfung zugegeben und somit die Reaktion gestartet
-
Luft als Referenzprobe
-
Messung der Temperaturänderung in einem Zeitintervall von je 30 Sekunden
-
Vergleich der Werte
|
a) |
Mit dem Entfernen der Folie beginnt die Reaktion durch Sauerstoffzufuhr (Oxidationsmittel), daher sollte erst unmittelbar vor der Anwendung die Folie entfernt werden. |
|
b) |
Die Haut muss trocken sein, da ansonsten zusätzlich Wasser eindringt und die Reaktion schneller oder langsamer ablaufen lässt und somit die Anwendungszeit beeinflusst. |
|
c) |
Bei Austrocknung des Gemisches kann es aufgrund der Wärmeentwicklung bei einer noch aktiven Kompresse zur Entzündung des Hausmülls kommen. |
Pro-Argumente
-
leicht zu handhaben, an nahezu allen Körperstellen einsetzbar
-
lokalisierte Wärmeentwicklung über einen längeren Zeitraum
-
führt ohne medikamentösen Eingriff zur Schmerzlinderung
-
ohne Verwendung von Gefahrstoffen → unproblematisch zu entsorgen
Contra-Argumente
-
einmalige Anwendung (relativ kostenintensiv)