Aufgabe C – Phosphorsäure und Phosphate – vielfach verwendete Lebensmittelzusatzstoffe
Phosphorsäure wird in einigen Nahrungsmitteln als Zusatzstoff mit der Nummer E 338 verwendet. Sie ist z. B. für den typischen Geschmack von Cola mitverantwortlich und ist in einigen Lebensmitteln als Säuerungs- und Konservierungsmittel enthalten. Doch seit einigen Jahren kommen Zweifel hinsichtlich der Unbedenklichkeit des ungebremsten Konsums an Phosphorsäure und ihren Salzen auf.
Formuliere eine Reaktionsgleichung für die zweite Stufe der Protolyse von Phosphorsäure-Molekülen in wässriger Lösung.
Erläutere anhand dieser Reaktionsgleichung das Säure-Base-Konzept nach Brønsted und am Beispiel des Dihydrogenphosphat-Ions den Begriff Ampholyt (M 1).
Begründe, dass für den pH-Wert einer wässrigen Phosphorsäure-Lösung hauptsächlich die erste Protolysestufe ausschlaggebend ist (M 1).
Begründe die Notwendigkeit, die Cola-Probe vorzubereiten (M 2).
Beurteile die genannten Möglichkeiten der Probenvorbereitung anhand von zwei Aspekten (M 2).
Beschreibe das Prinzip einer Säure-Base-Titration (M 2).
Erläutere die pH-Werte in den beiden markierten Punkten A und B in der aufgenommenen Titrationskurve (M 2).
Begründe, weshalb sich zur Bestimmung der Phosphorsäure-Konzentration in Cola eine Titration mit Indikator nicht eignet.
Ermittle die Stoffmengenkonzentration der Phosphorsäure in der untersuchten Cola unter der Annahme, dass keine weiteren Säuren in der Probe enthalten sind (M 2).
Überprüfe die Herstellerangabe bezüglich der Masse an zugesetzter Phosphorsäure (M 2).
Beurteile gesundheitliche Gefahren durch Aufnahme von Phosphor in Verbindungen, sollte ein Jugendlicher mit einem Körpergewicht von täglich einen Liter der in Aufgabe 4 untersuchten Cola zu sich nehmen (M 2, M 3).
Hinweis: Sollte die Berechnung in Aufgabe 4 keine Ergebnisse liefern, gehe von Phosphorsäure in einem Liter Cola aus.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Material 1: Phosphorsäure
Phosphorsäure ist in einigen Nahrungsmitteln als Lebensmittelzusatzstoff enthalten. Phosphorsäure-Moleküle können stufenweise bis zu drei Protonen in Säure-Base-Reaktionen abgeben. Bei den einzelnen Deprotonierungsstufen bilden sich ausgehend vom Phosphorsäure-Molekül nacheinander das Dihydrogenphosphat-Ion, das Hydrogenphosphat-Ion und das Phosphat-Ion.
[1]
Material 2: Bestimmung des Gehaltes an Phosphorsäure in Cola
Cola ist ein kohlensäure- und phosphorsäurehaltiges Erfrischungsgetränk. In Cola sind bis zu Phosphorsäure pro Liter zulässig. Ein Hersteller gibt an, dass einem Liter Cola bei der Herstellung
Phosphorsäure zugesetzt werde und der
-Wert
betrage. Im Labor soll die Cola dieses Herstellers auf ihren Phosphorsäure-Gehalt überprüft werden.
Zur Vorbehandlung der Cola werden zwei verschiedene Möglichkeiten vorgeschlagen:
|
a) |
eine Probe von |
|
b) |
Cola längere Zeit am Sieden halten, abkühlen lassen und danach eine Probe von |
Eine Cola-Probe wird vorbehandelt und danach mit einer Natronlauge-Maßlösung der Stoffmengenkonzentration titriert. Dabei erhält man folgende Titrationskurve (Abb. 1):
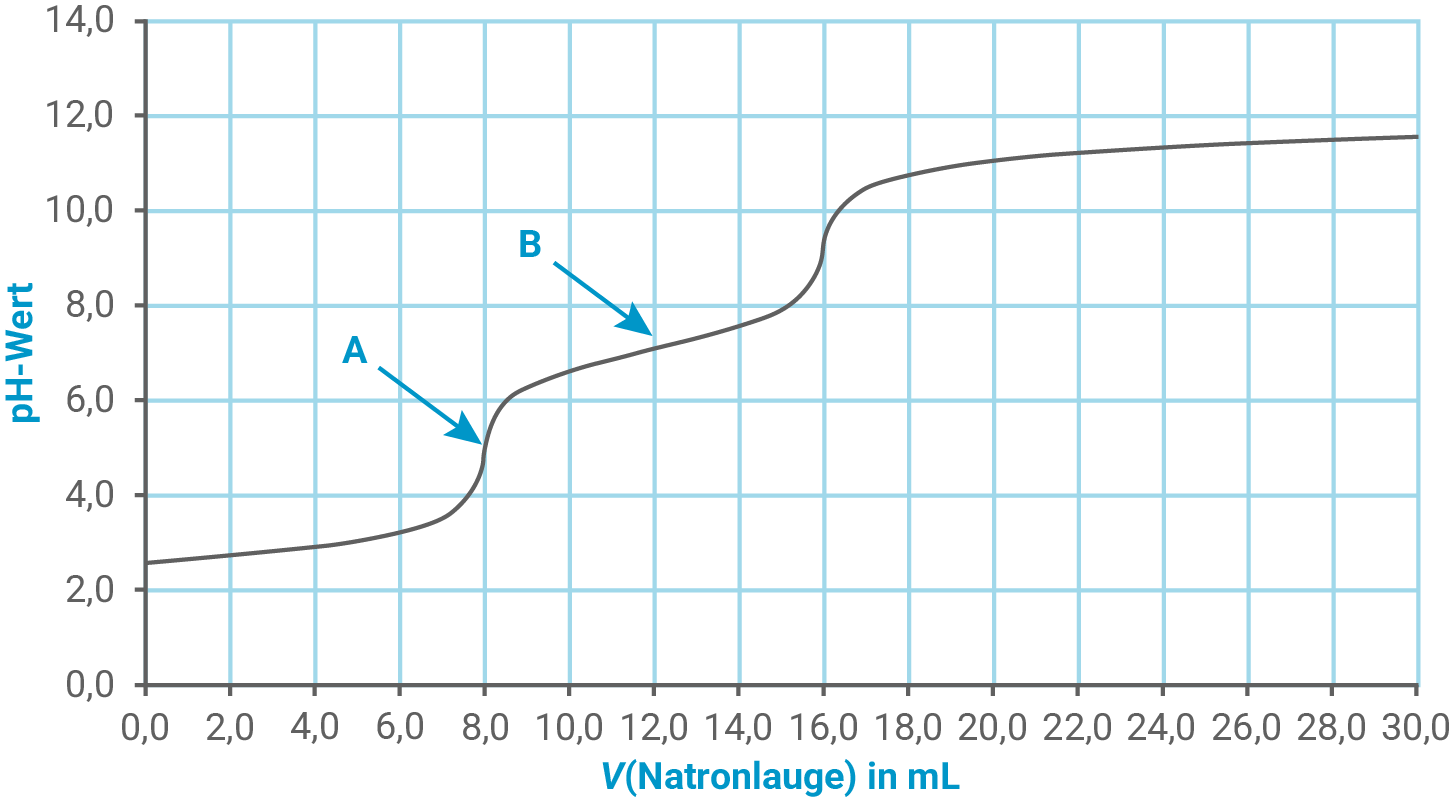
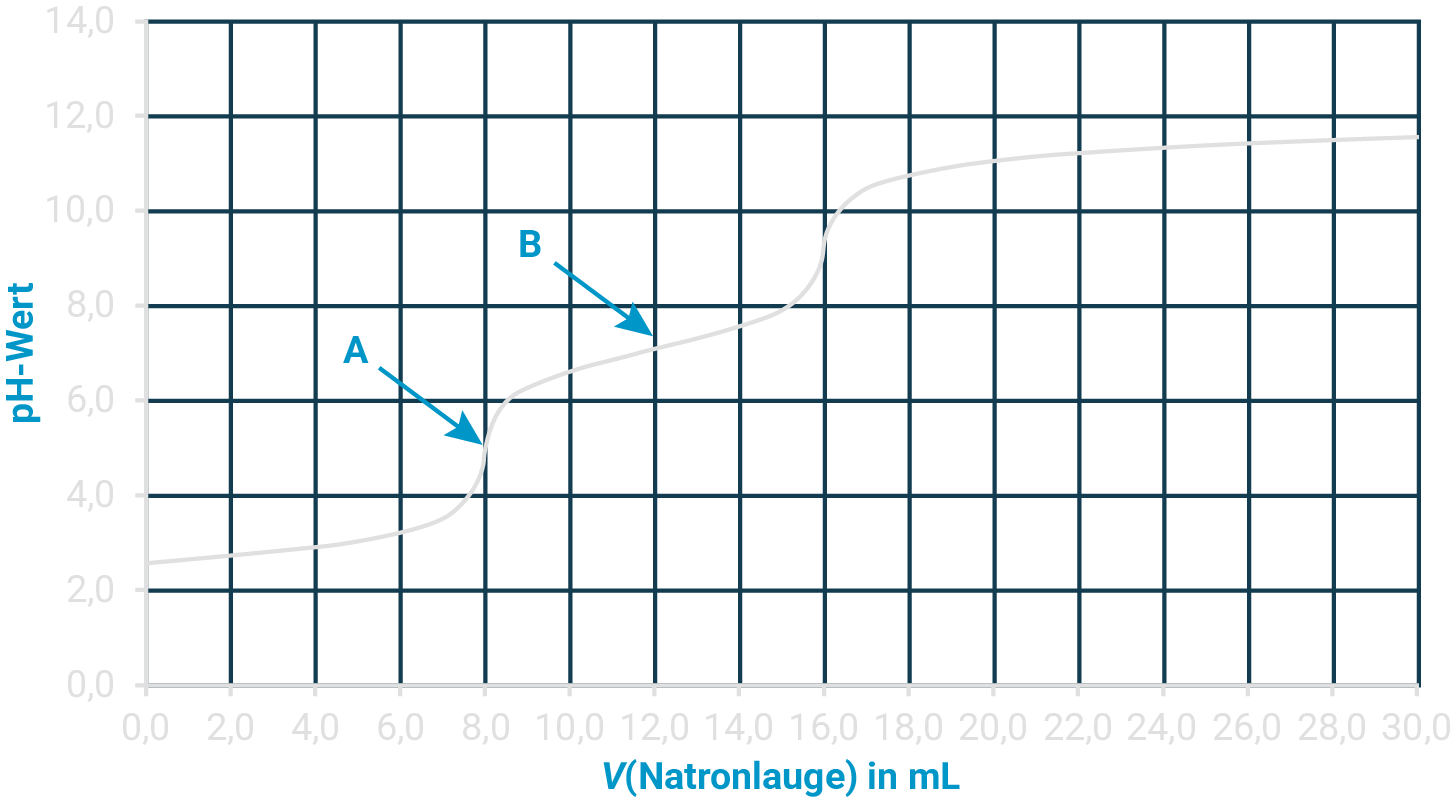
Abb. 1: Titrationskurve der Phosphorsäure (Cola-Probe), markierte Punkte A und B
[2]
Material 3: Phosphorsäure, Phosphate und unsere Gesundheit
Ein vermeidbares Gesundheitsproblem verbirgt sich hinter der verbreiteten Verwendung von Phosphorsäure und deren Salzen als Zusatzstoffe in Nahrungsmitteln. Dieses „freie“ Phosphat wird sehr effektiv vom Körper aufgenommen. Neben der Verwendung der Phosphorsäure in Cola werden in fast allen verarbeiteten Fleischprodukten (wie z. B. Brühwürste und Kochschinken), aber auch in Schmelzkäse und anderen Käsezubereitungen sowie in vielen Fertiggerichten Phosphate eingesetzt, um Wasser zu binden.
Im Jahr 2019 wurde deshalb ein ADI-Wert, bezogen auf die Aufnahme von Phosphor in Verbindungen (z. B. Phosphorsäure, Phosphate, Polyphosphate oder ähnliches), festgelegt. Der ADI-Wert (acceptable daily intake) ist die geschätzte Menge eines Stoffes in Lebensmitteln pro Kilogramm Körpergewicht, die täglich im Laufe eines Lebens konsumiert werden kann, ohne dass sie ein merkliches Risiko für die Gesundheit birgt. Der ADI-Wert für Phosphor in Verbindungen beträgt Körpergewicht.
[3], [4]
Quellen (ggf. verändert):
[1] Holleman, A. F., Wiberg, E., Wiberg, N. (2007). Phosphorsäure. In N. Wiberg (Hrsg.), Anorganische Chemie (102. Aufl., S.795−804). De Gruyter
[2] Bestimmung des Gehalts von Phosphorsäure in einem Cola-Getränk (o. D.). Leybold. https://www.ld-didactic.de/documents/en-US/EXP/C/C3/C3642_d.pdf (letzter Zugriff am 28.03.2024)
[3] Ritz, E., Hahn, K., Ketteler, M., Kuhlmann, M. & Mann, J. (2012, 27. Januar). Gesundheitsrisiko durch Phosphatzusätze in Nahrungsmitteln. Deutsches Ärzteblatt. https://www.aerzteblatt.de/archiv/119315/Gesundheitsrisiko-durch-Phosphatzusaetze-in-Nahrungsmitteln (letzter Zugriff am 28.03.2024)
[4] EFSA veröffentlicht neue Empfehlungen zu Phosphaten (2019, 12. Juni). Europäische Behörde für Lebensmittelsicherheit. https://www.efsa.europa.eu/de/press/news/190612 (letzter Zugriff am 21.11.2023)
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Formulierung der Reaktionsgleichung für die zweite Protolysestufe
Erläuterung des Säure-Base-Konzepts nach Brønsted
-
Das Dihydrogenphosphat-Ion ist eine Brønsted-Säure, weil es ein Proton abgibt (Protonendonator).
-
Das Wasser-Molekül ist eine Brønsted-Base, weil es ein Proton aufnimmt (Protonenakzeptor).
-
Insgesamt handelt es sich um eine Protonenübertragungsreaktion.
Erläuterung des Begriffs „Ampholyt“
-
Das Dihydrogenphosphat-Ion kann je nach Reaktionspartner sowohl ein Proton abgeben und dabei zum Hydrogenphosphat-Ion reagieren oder es kann ein Proton aufnehmen und zum Phosphorsäure-Molekül reagieren.
-
Teilchen, die je nach Reaktionspartner sowohl als Protonendonatoren als auch als Protonenakzeptoren wirken können, sind Ampholyte. Daher ist das Dihydrogenphosphat-Ion ein Ampholyt.
Begründung des Zusammenhangs zwischen pH-Wert und Protolysestufen
-
Der
-Wert der Phosphorsäure ist um ca.
kleiner als der
-Wert des Dihydrogenphophats.
-
Bei der ersten Protolysestufe wird im Vergleich zu den folgenden Protolysestufen ein Vielfaches an Oxonium-Ionen gebildet.
-
Die bei der zweiten und dritten Protolysestufe gebildeten Oxonium-Ionen ändern den pH-Wert daher kaum.
Begründung der Notwendigkeit der Vorbereitung
-
Kohlensäure würde als zusätzliche Säure das Titrationsergebnis verfälschen.
-
Die Kohlensäure muss daher vollständig aus der Probe entfernt werden.
Beurteilung der Möglichkeiten der Probenvorbereitung
-
In Möglichkeit a) wird die Probe über Nacht stehen gelassen. Da schon zu Beginn das Volumen bestimmt wurde, spielt eventuelles Verdunsten von Wasser keine Rolle. Es könnte noch Kohlensäure in der Probe vorhanden sein, sie sollte länger stehen gelassen werden.
-
In Möglichkeit b) wird die Probe längere Zeit am Sieden gehalten. Es muss sichergestellt werden, dass Wasser nicht verdampft, weil andernfalls die Konzentration der Phosphorsäure erhöht werden würde. Durch das Erhitzen wird Kohlensäure nahezu vollständig aus der Probe entfernt.
Gesamturteil: Wenn dafür gesorgt wird, dass kein Wasser verdampft, ist Variante b) vorzuziehen.
Beschreibung des Prinzips einer Säure-Base-Titration
-
Bei einer Säure-Base-Titration wird die Stoffmengenkonzentration einer Säure in einer Probelösung durch Zugabe einer Lauge bekannter Stoffmengenkonzentration (Maßlösung) bestimmt.
-
Der Titration zugrunde liegt die Neutralisationsreaktion. Im Äquivalenzpunkt haben Säure und Base entsprechend der Reaktionsgleichung im stöchiometrischen Verhältnis reagiert.
-
Der Äquivalenzpunkt wird zum Beispiel durch den Farbumschlag eines geeigneten pH-Indikators bestimmt.
Erläuterung der pH-Werte der markierten Punkte
-
Punkt A: Zugabe von
Natronlauge,
-Wert bei ca.
Die aus der ersten Protolysestufe gebildeten Oxonium-Ionen sind neutralisiert, es liegen hauptsächlich Dihydrogenphosphat-Ionen vor. Das Dihydrogenphosphat-Ion ist eine schwache Säure
die entsprechende Lösung ist sauer.
-
Punkt B: Zugabe von
Natronlauge,
-Wert bei ca.
Die Hälfte der Dihydrogenphosphat-Ionen hat zu Hydrogenphosphat-Ionen reagiert. Dihydrogenphosphat-Ionen und Hydrogenphosphat-Ionen liegen im Verhältnis
vor, der
-Wert entspricht dem
-Wert von Dihydrogenphosphat.
Begründung der Nichteignung eines Indikators
-
Cola hat eine dunkle Eigenfarbe, sodass ein Farbumschlag bei der Verwendung eines Säure-Base-Indikators nicht gut zu erkennen ist. Daher bietet sich die Verwendung eines pH-Meters bei der Titration an.
Ermittlung der Stoffmengenkonzentration
Der Verbrauch an Natronlauge (abgelesen am ersten Äquivalenzpunkt) beträgt
Für den ersten Äquivalenzpunkt gilt:
Mit dem Volumen der Probelösung bedeutet das final für die Konzentration:
Überprüfung der Herstellerangabe
Mithilfe der berechneten Konzentration lässt sich über die molare Masse die enthaltene Masse an Phosphorsäure in Cola bestimmen:
In einem Liter der untersuchten Cola sind Phosphorsäure. Es wurde mehr Phosphorsäure zugesetzt als angegeben. Die Menge liegt aber unter dem erlaubten Grenzwert.
Beurteilung der gesundheitlichen Gefahren durch Trinken von Cola
Ein Jugendlicher mit einem Körpergewicht von kann laut ADI-Wert täglich
Phosphor aufnehmen. Mit
pro Liter Cola liegt man bei einem Konsum von einem Liter pro Tag darunter und hat damit nicht mit gesundheitlichen Gefahren aufgrund der Aufnahme von Phosphor durch Cola zu rechnen.