Aufgabe 3 – Chlorung von Wasser
Eine Möglichkeit der Chlorung von Wasser ist das direkte Einleiten von Chlor. Dieses wird heutzutage zum Großteil über die Chlor-Alkali-Elektrolyse hergestellt.
Gib die Elektronenkonfiguration und drei Aussagen zum Bau eines Chlor-Atoms an, die sich aus der Stellung des Elements im Periodensystem ableiten lassen.
Gib eine Valenzstrichformel (Lewis-Formel) eines Moleküls der hypochlorigen Säure an (M 1).
Formuliere die Reaktionsgleichung in Ionenschreibweise der Chlorung von Wasser (M 1, M 2).
Nenne den Reaktionstyp und erläutere an diesem Beispiel das Donator-Akzeptor-Prinzip (M 2).
Begründe die Freiwilligkeit der Reaktion von Chlor mit Wasser mithilfe von Potenzialen (M 1, M 2, M 3).
Erkläre die Abhängigkeit der Chlorung von Wasser vom pH-Wert (M 2).
Nenne das Prinzip einer Elektrolyse und gib den allgemeinen Aufbau einer Elektrolysezelle an.
Ergänze die jeweiligen Teilchen in die Kästchen der Abbildung 1 in M 3.
Beurteile die Aussage mithilfe der Abbildung 2 in M 3:
Die angelegte Spannung bei der Chlor-Alkali-Elektrolyse muss größer als 1,8 V, aber kleiner als 2,1 V sein.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Material 1: Hypochlorige Säure
Die Moleküle der hypochlorigen Säure sind aufgrund der enthaltenen Hydroxygruppe schwache Säuren und zeigen eine oxidierende Wirkung (
bei
). Sie sind sehr unbeständig und nur in wässriger Lösung stabil.
Material 2: Chlorung von Wasser
Wasser in Schwimmbädern muss aus hygienischen Gründen desinfiziert werden. Dies kann durch Einleiten von Chlor in das Wasser geschehen. Dabei reagiert ein Anteil des Chlors mit Wasser. In einer Gleichgewichtsreaktion bilden sich Chlorwasserstoffsäure und hypochlorige Säure. Bei hohem pH-Wert reagiert ein höherer Anteil des Chlors mit Wasser.
Material 3: Chlor-Alkali-Elektrolyse
Die technische Herstellung von Chlor erfolgt durch Elektrolyse einer wässrigen Natriumchlorid-Lösung. Bei den entsprechenden Reaktionsbedingungen laufen folgende Reaktionen ab:
An der Kathode nehmen Wasserstoff-Ionen Elektronen auf und werden reduziert. Gleichzeitig geben Chlorid-Ionen an der Anode Elektronen ab und werden oxidiert.
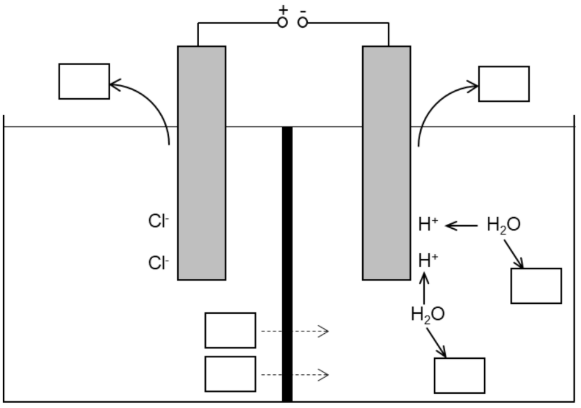
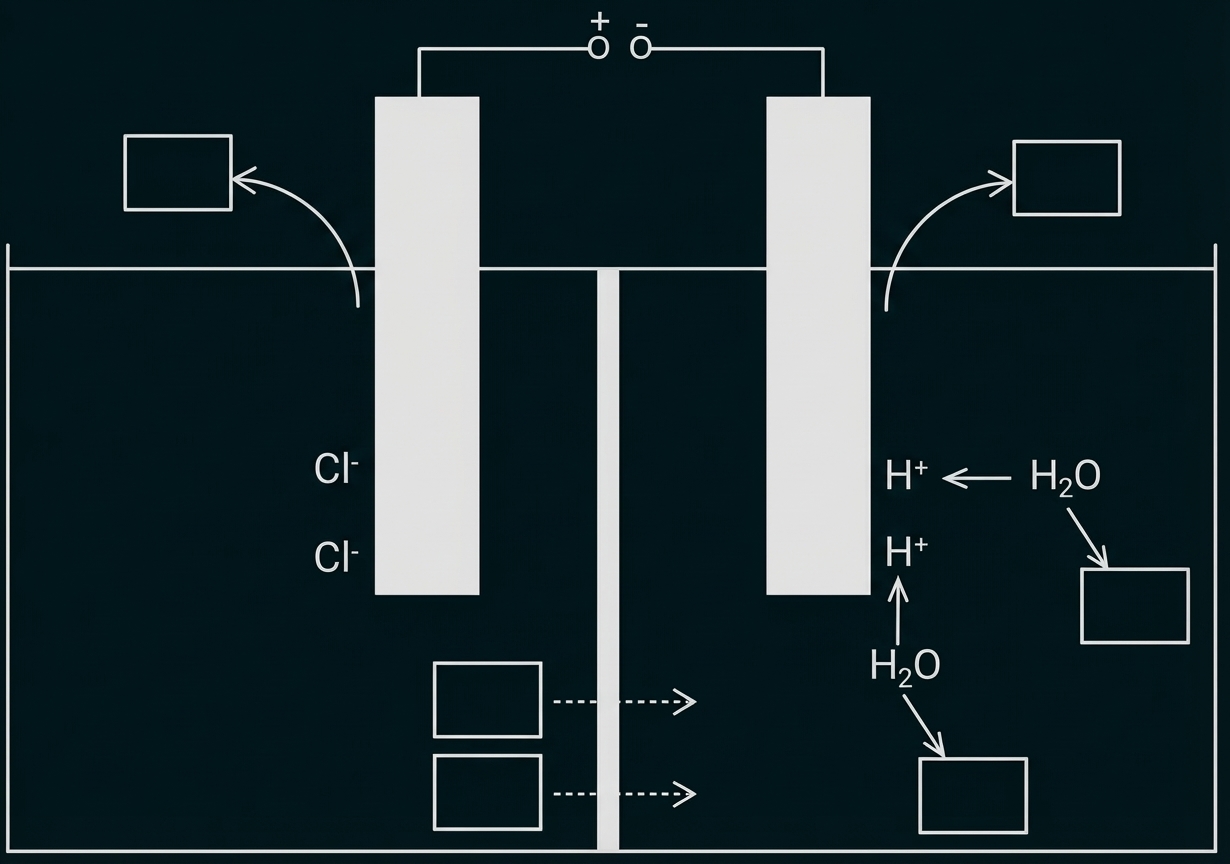
Abbildung 1: Modellhafte Darstellung des Aufbaus der Elektrolysezelle sowie die Veränderungen auf Teilchenebene im stöchiometrischen Verhältnis
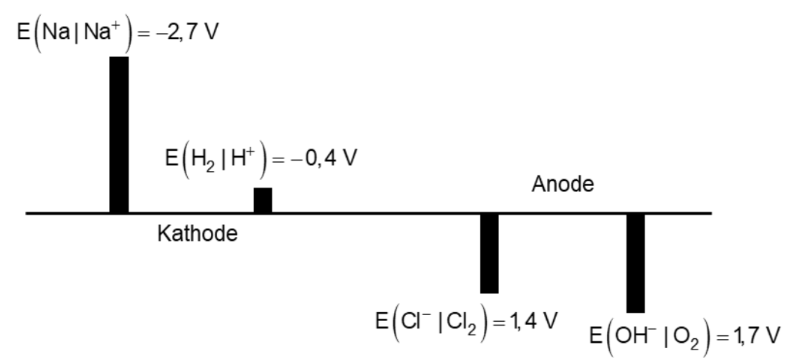
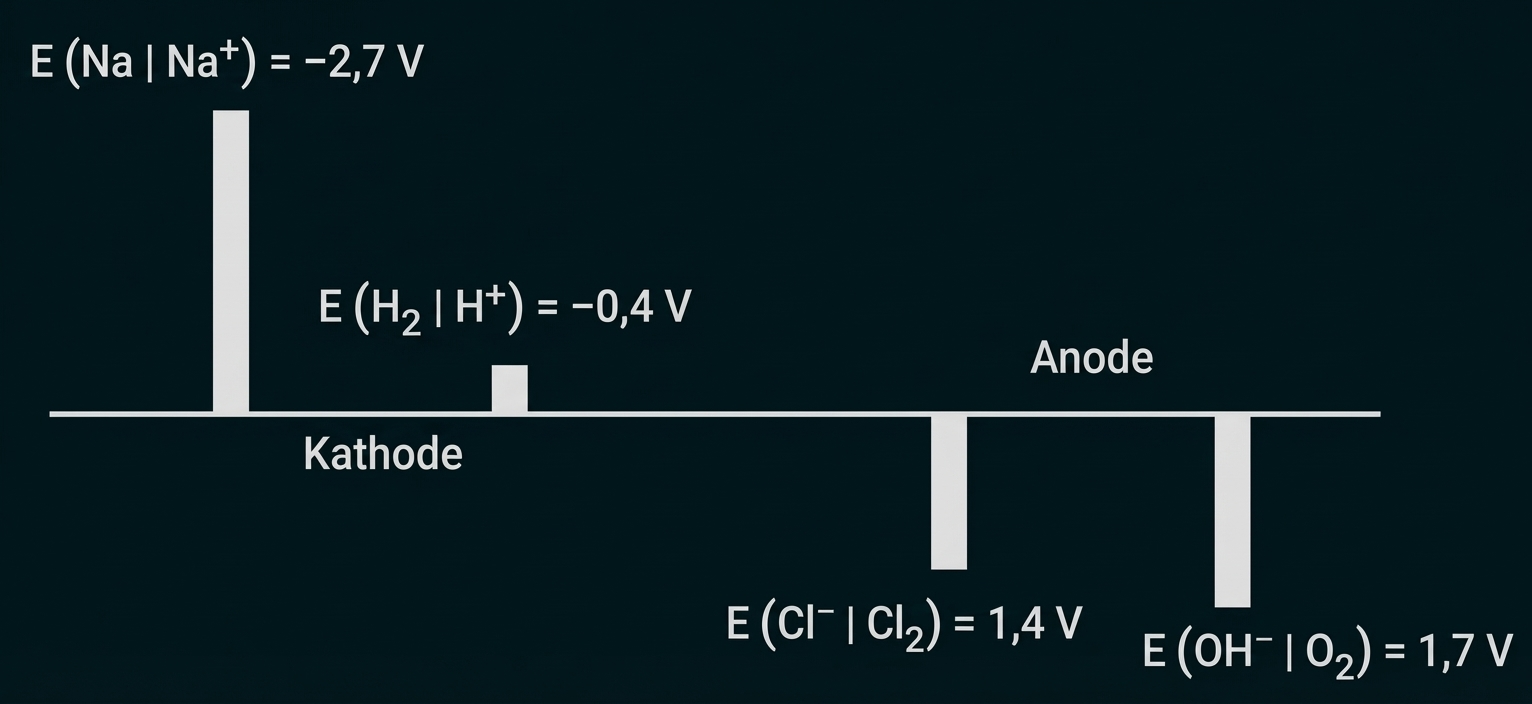
Abbildung 2: Potenziale bei den entsprechenden Reaktionsbedingungen (exemplarisch)
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Angeben der Elektronenkonfiguration
17Cl: 1s2 2s2 2p6 3s2 3p5
Angeben der drei Aussagen
-
17 Protonen im Atomkern und 17 Elektronen in der Atomhülle
-
3 besetzte Energieniveaus
-
7 Valenzelektronen (3s2 3p5)
Angeben einer Valenzstrichformel
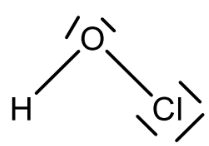
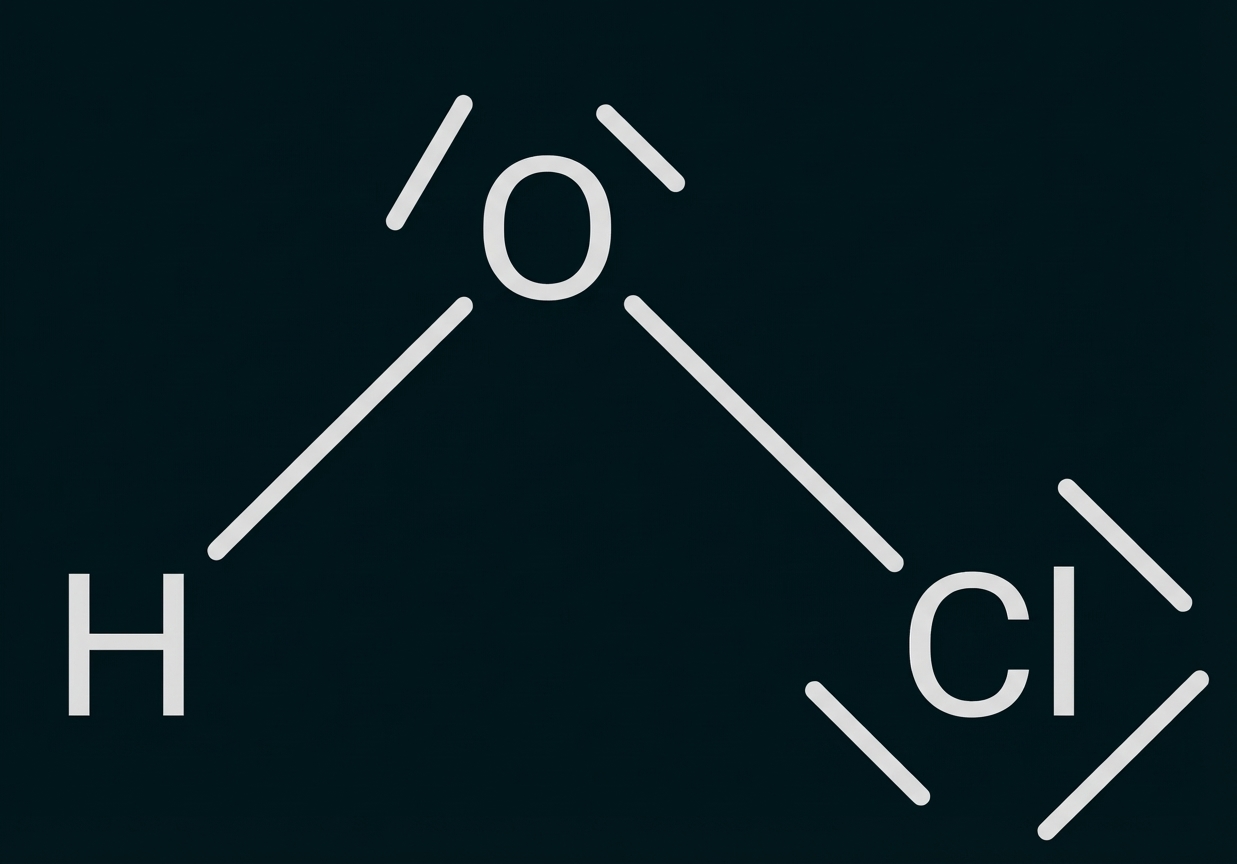
Formulieren der Reaktionsgleichung
Nennen des Reaktionstyps
-
Redoxreaktion
Erläutern des Donator-Akzeptor-Prinzips
-
Ein Chlor-Atom des Chlor-Moleküls, der Elektronendonator, gibt ein Elektron ab.
-
Ein Chlor-Atom des Chlor-Moleküls, der Elektronenakzeptor, nimmt ein Elektron auf.
-
Elektronenübergang vom Chlor-Atom auf das andere Chlor-Atom im Chlor-Molekül.
Begründen der Freiwilligkeit
-
-
Redoxpaar mit kleinerem Potenzial: Oxidation läuft ab.
Redoxpaar mit größerem Potenzial: Reduktion läuft ab.
-
Chlor-Atome im Chlor-Molekül werden jeweils reduziert bzw. oxidiert.
Erklären der Abhängigkeit vom pH-Wert
-
aufgrund des hohen pH-Werts ist die Hydroxid-Ionen-Stoffmengenkonzentration hoch
-
Hydroxid-Ionen reagieren mit den Wasserstoff-Ionen, Stoffmengenkonzentration an Wasserstoff-Ionen sinkt
-
Störung des Gleichgewichtszustands, Wiedereinstellung des Gleichgewichtszustands durch Reaktion von Chlor mit Wasser
Nennen des allgemeinen Prinzips einer Elektrolyse
-
erzwungene Redoxreaktion mithilfe von elektrischem Strom
Angeben des allgemeinen Aufbaus
-
zwei mit einer Gleichspannungsquelle verbundene Elektroden, die in einen Elektrolyten eintauchen
Ergänzen der Abbildung
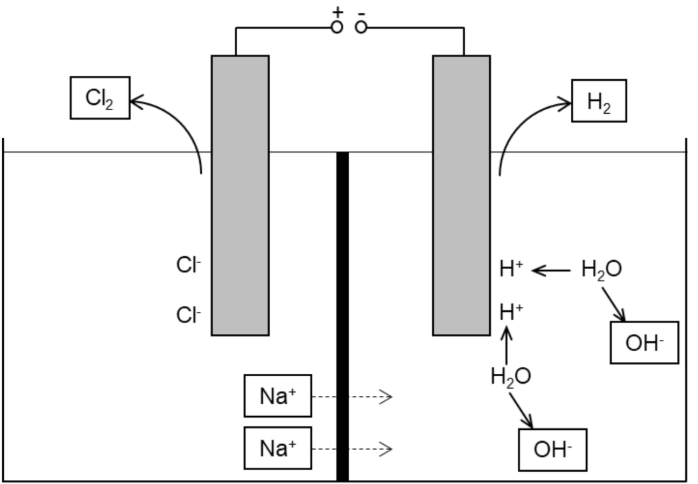
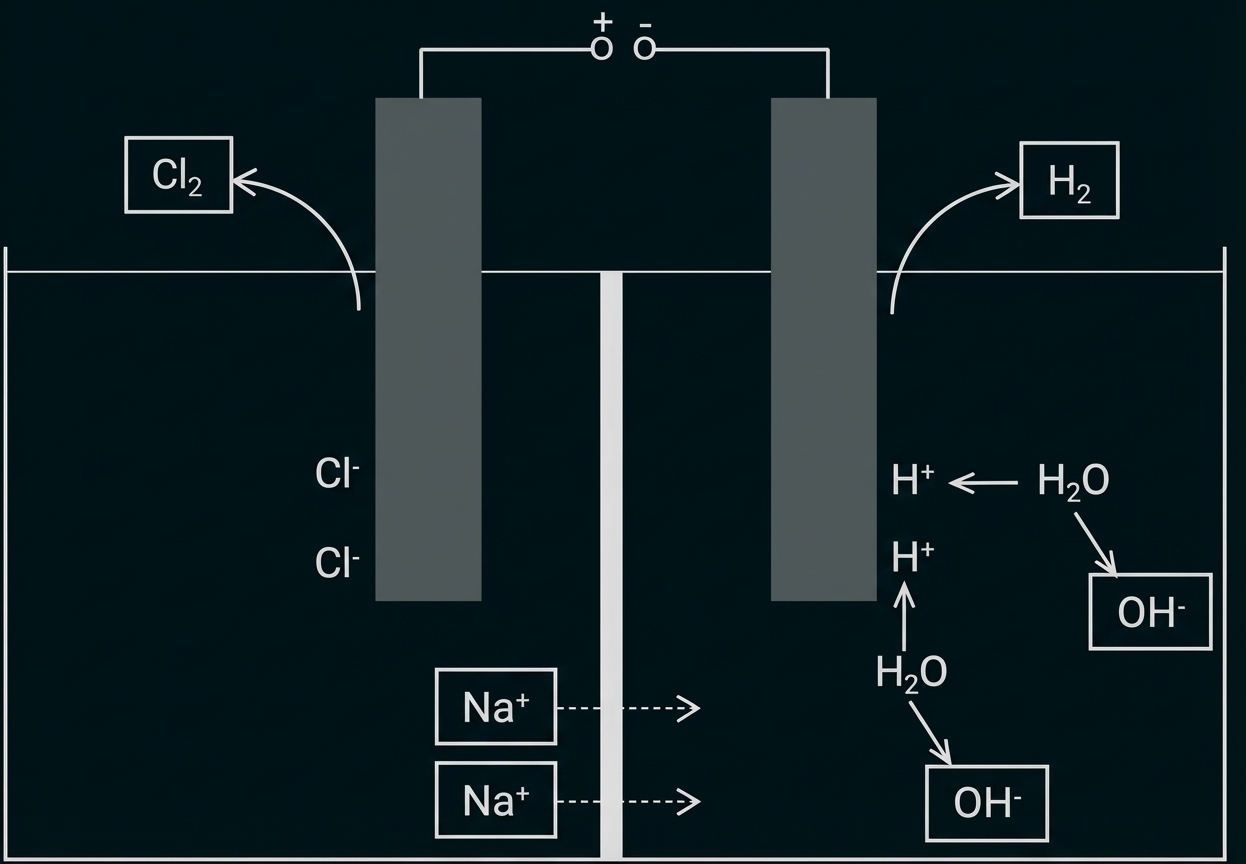
Beurteilen der Aussage
-
Bildung von Wasserstoff und Chlor:
-
Elektrolyse läuft erst nach Überschreiten der Potenzialdifferenz (Zersetzungsspannung) ab, somit muss sie größer als
sein.
-
Bildung von Wasserstoff und Sauerstoff:
-
Ist die angelegte Spannung größer
, würde Sauerstoff entstehen.
-
Sachurteil:
Die Aussage stimmt.