Aufgabe 4 – Schwefelsäure
Schwefelsäure ist einer der wichtigsten industriellen Grundstoffe. Ihre Weltjahresproduktion betrug 2015 etwa 200 Millionen Tonnen – das ist mehr als jedes andere synthetische Produkt. Aufgrund ihrer vielseitigen Eigenschaften ist Schwefelsäure als Reaktionspartner von großer Bedeutung.
Formuliere die Reaktionsgleichungen für die zwei Protolysestufen von Schwefelsäure-Molekülen in wässriger Lösung (M 1, M 2).
Erläutere an einer Protolysestufe das Säure-Base-Konzept nach Brönsted und gib die konjugierten Säure-Base-Paare an (M 1, M 2).
Leite eine Valenzstrichformel (Lewis-Formel) des Hydrogensulfat-Ions aus der Abbildung 1 oder der Abbildung 2 ab (M 1, M 2).
Erkläre anhand von Strukturbetrachtungen die Zuordnung des Schwefelsäure-Moleküls zu den Ampholyten (Abbildung 1, M 1, M 2).
Formuliere die Reaktionsgleichung der Autoprotolyse von Schwefelsäure-Molekülen (M 1, M 2).
Plane ein Experiment zum eindeutigen Nachweis von Sulfat-Ionen in einer Lösung, die auch Carbonat-Ionen enthält.
Werte die Beobachtungen des Experiments aus und formuliere die entsprechenden Reaktionsgleichungen (M 3).
Beurteile die in M 2 genannte These mithilfe des Experiments (M 3).
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Material 1: Schwefelsäure
Reine Schwefelsäure ist eine ölige, farblose Flüssigkeit.
Schwefelsäure-Moleküle reagieren in Abhängigkeit vom Reaktionspartner
-
als Säure, z. B. mit Wasser-Molekülen,
-
als Ampholyt, z. B. mit Schwefelsäure-Molekülen
oder
-
als Base, z. B. mit Iodwasserstoff-Molekülen.
Reine Schwefelsäure zeigt ein analoges Reaktionsverhalten wie reines Wasser. Die Schwefelsäure-Moleküle sind wie Wasser-Moleküle zur Autoprotolyse fähig.
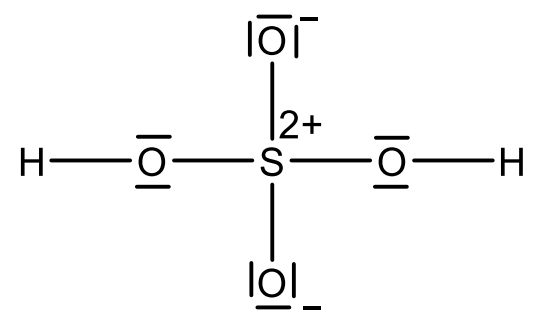
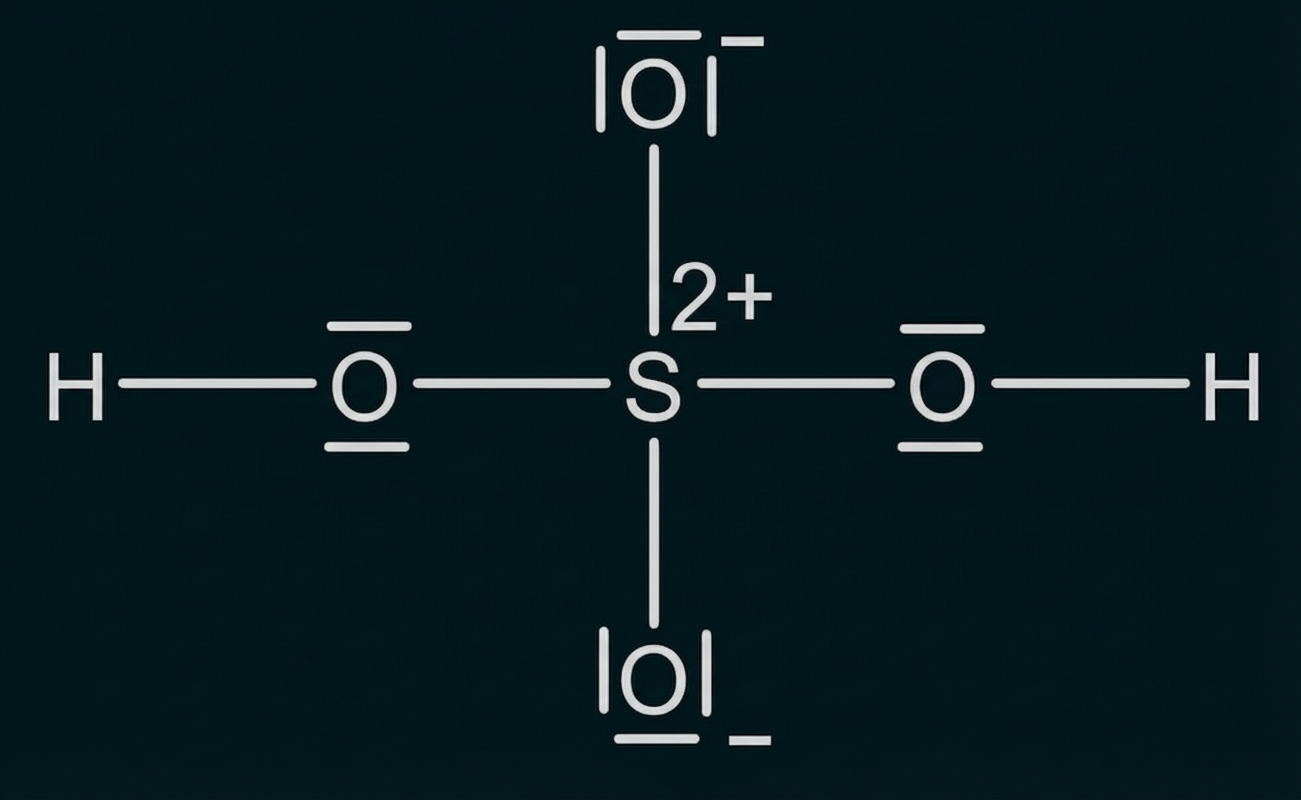
Abbildung 1: mögliche Valenzstrichformel eines Schwefelsäure-Moleküls
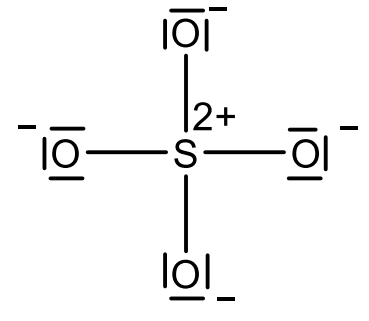
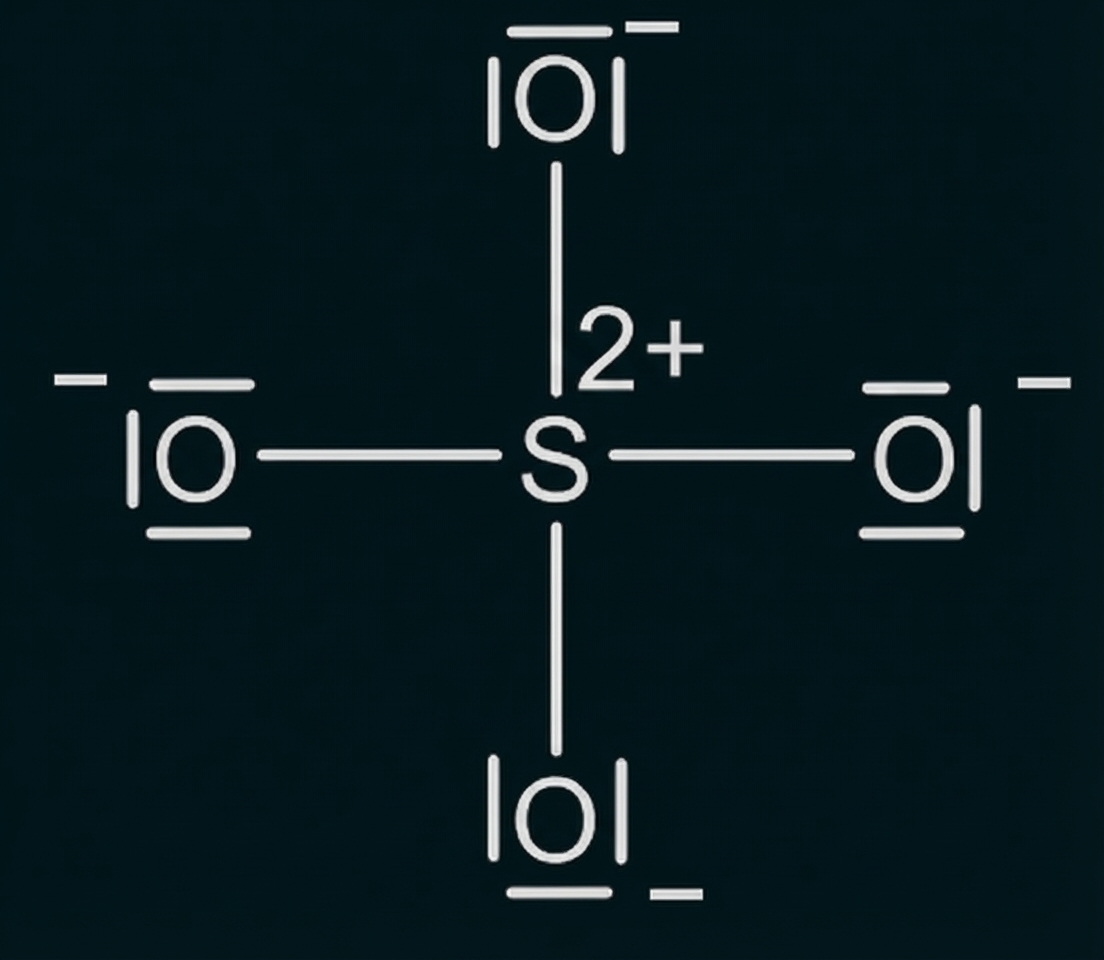
Abbildung 2: mögliche Valenzstrichformel eines Sulfat-Ions
Material 2: Hydrogensulfate
Hydrogensulfate zählen zu den Salzen, die aus Kationen und Hydrogensulfat-Ionen aufgebaut sind. Je nach Reaktionspartner können Hydrogensulfat-Ionen als Base oder als Säure reagieren.
Mit der These:
„Die schwächere Säure verdrängt die stärkere Säure aus ihrem Salz.“
soll das Reaktionsverhalten vorausgesagt werden.
Material 3: Dokumentiertes Experiment
Die Unterseite eines Uhrglases wird mit Calciumhydroxid-Lösung benetzt. Anschließend wird auf eine Probe Natriumcarbonat im Becherglas tropfenweise Natriumhydrogensulfat-Lösung gegeben und das Becherglas mit dem Uhrglas abgedeckt (siehe Abbildung 3).
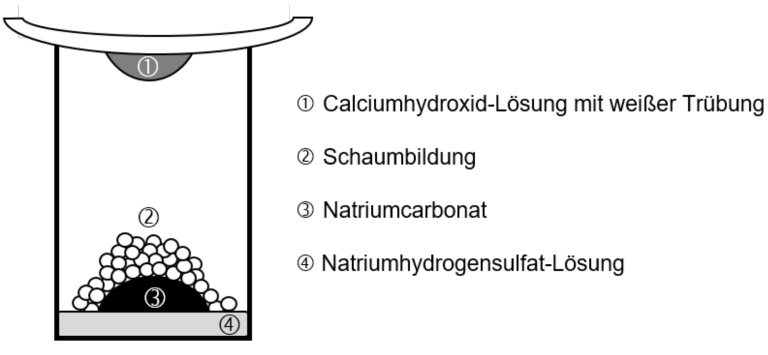
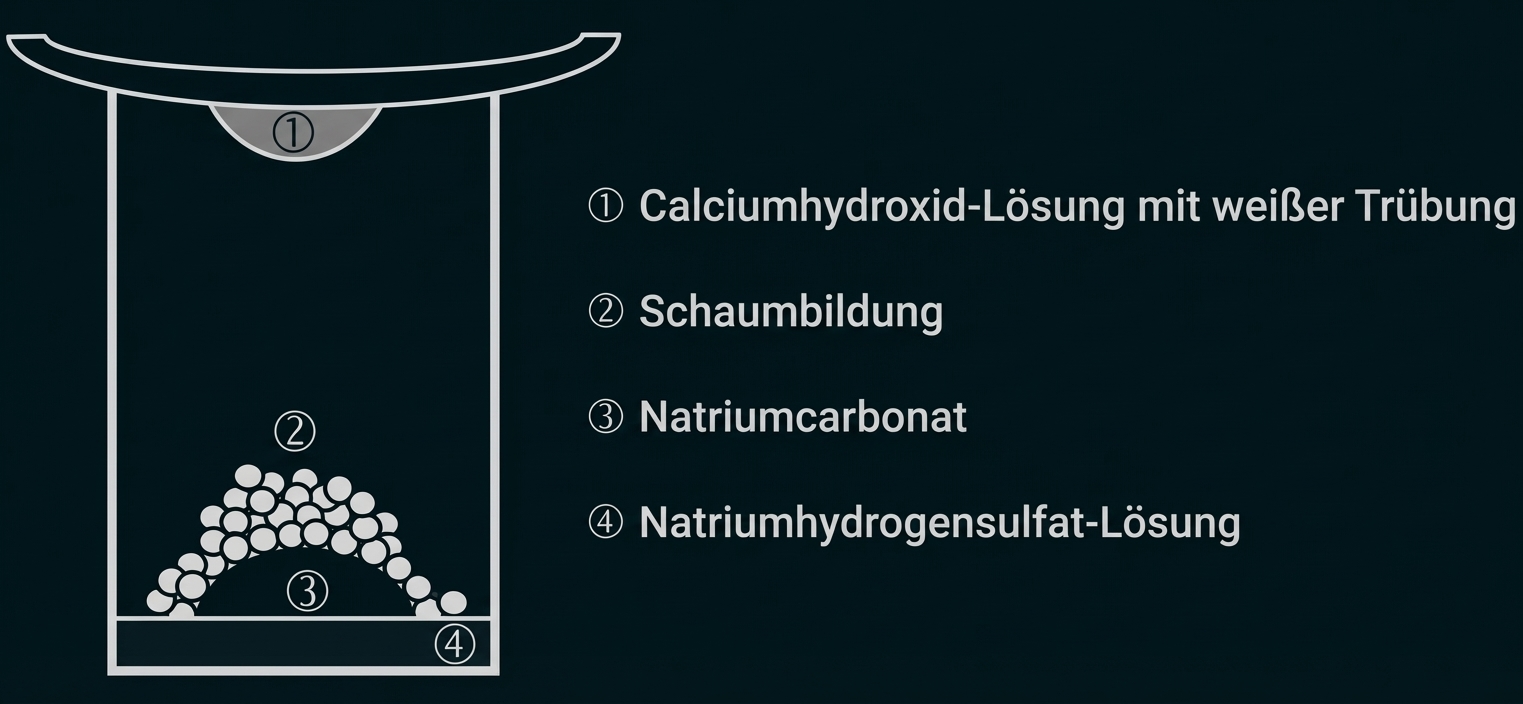
Abbildung 3: vereinfachte Darstellung des Experiments nach Zugabe der Natriumhydrogensulfat- Lösung
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Formulieren der Reaktionsgleichungen
Erläutern des Säure-Base-Konzepts nach Brönsted, z. B.
-
Das Hydrogensulfat-Ion ist eine Brönsted-Säure (Protonendonator), weil es ein Proton abgibt.
-
Das Wasser-Molekül ist eine Brönsted-Base (Protonenakzeptor), weil es ein Proton aufnimmt.
-
Protonenübergang von einem Hydrogensulfat-Ion auf ein Wasser-Molekül
Angeben der Säure-Base-Paare, z. B.
Ableiten einer Valenzstrichformel
-
Durch Abgabe eines Protons aus einer Hydroxygruppe entsteht eine negative Ladung am Sauerstoff-Atom.
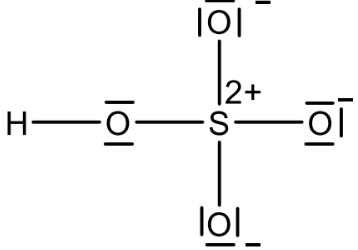
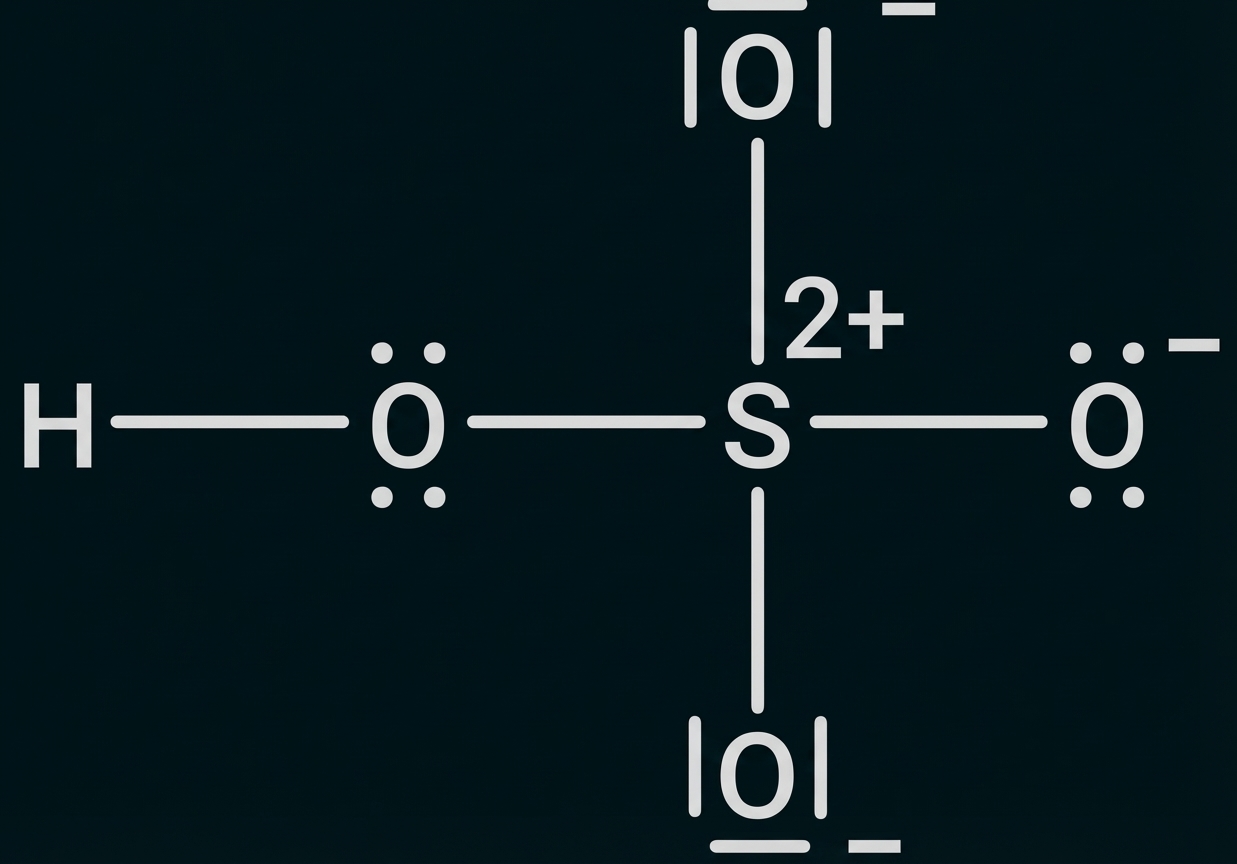
Erklären der Zuordnung
-
Schwefelsäure-Molekül enthält zwei polarisierte Wasserstoff-Atome (an den Hydroxygruppen)
-
Schwefelsäure-Moleküle können Protonen abgeben, dabei entstehen Hydrogensulfat-Ionen
-
Schwefelsäure-Moleküle enthalten zwei Sauerstoff-Atome, die negativ geladen sind und freie Elektronenpaare besitzen
-
Protonen können sich an ein freies Elektronenpaar anlagern, es bildet sich ein protoniertes Schwefelsäure-Molekül
-
Schwefelsäure-Molekül ist Ampholyt, da je nach Reaktionspartner Protonendonator oder Protonenakzeptor
Formulieren der Reaktionsgleichung
Planen des Nachweises
-
Zugabe einer Lösung mit Calcium- oder Barium-Ionen
-
Calciumsulfat bzw. Bariumsulfat sind schwer löslich und fallen aus
-
Zugabe einer Säure-Lösung
-
Ausschluss von Carbonat-Ionen, da Calcium- bzw. Bariumcarbonat sich in sauren Lösungen zersetzen würden
Auswerten der Beobachtungsergebnisse
-
Schaumbildung: Entstehen von Kohlenstoffdioxid (Gasentwicklung)
-
-
weiße Trübung: Entstehen von Calciumcarbonat
-
Beurteilen der These
-
-
Hydrogensulfat-Ion ist stärkere Säure als Kohlensäure-Molekül
-
Hydrogensulfat-Ionen geben Protonen an die Carbonat-Ionen ab und „verdrängen“ Kohlensäure-Moleküle, die in Kohlenstoffdioxid und Wasser zerfallen
-
Sachurteil: Die Aussage ist falsch.