Aufgabe 4 – Mit Benzoesäure konservierte Nordseekrabben
Benzoesäure ist ein häufig verwendeter Konservierungsstoff. Sie wird verwendet für die Haltbarmachung verschiedener Lebensmittel, wie z. B. Feinkostsalaten, Mayonnaisen und Nordseekrabben.
Erläutere anhand der Reaktionsgleichung in Strukturformeln für die Reaktion von Benzoesäure mit Wasser, weshalb die Nordseekrabben mit einem Gemisch aus Benzoesäure und Citronensäure behandelt werden (M1, M2).
Erläutere die Wasserlöslichkeit von Benzoesäure anhand von Struktur-Eigenschaftsbeziehungen (M1).
Berechne vier charakteristische Punkte der Titrationskurve von Benzoesäure mit Natronlauge (M1, M3).
Skizziere anhand der vier berechneten Werte die entsprechende Titrationskurve (M1, M3).
Erkläre den pH-Wert am Äquivalenzpunkt (M1, M3).
Berechne die Gesamtmasse der Benzoesäure in der in M4 genannten Portion Nordseekrabben (M1, M4).
Begründe, ob die Nordseekrabben aus der Probe für den Verzehr geeignet sind (M4).
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?M1: Benzoesäure und ihre Salze
Benzoesäure ist bei ein farbloser, kristalliner Feststoff. Der
-Wert von Benzoesäure beträgt
Die Salze der Benzoesäure heißen Benzoate. Der
-Wert von Benzoat-Ionen beträgt
Benzoesäure wird als Konservierungsstoff eingesetzt, um Lebensmittel vor dem Verderb durch Pilze und Hefen sowie in geringem Maße auch durch Bakterien zu schützen. Die antimikrobielle Wirkung geht von dem undissoziierten Benzoesäure-Molekül aus, da nur dieses in der Lage ist, die Zellmembran von Mikroorganismen zu durchdringen. Dem Benzoat-Ion wird keine wesentliche antimikrobielle Wirkung zugeschrieben.


Strukturformel eines Benzoesäure-Moleküls
verändert nach: H. D. Berlitz, W. Grosch, P. Schieberle, Lehrbuch der Lebensmittelchemie, 6. Auflage, Berlin: Springer-Verlag, 2008, S. 462
M2: Verarbeitung von Nordseekrabben nach dem Fang
Nordseekrabben werden häufig mit Benzoesäure konserviert. Die Nordseekrabben werden direkt nach dem Fang weiterverarbeitet. Bereits auf dem Kutter werden die Nordseekrabben in Meerwasser in einem Kessel gekocht, was ihnen auch zu ihrem speziellen Aroma und ihrer Farbe verhilft. Danach werden die Nordseekrabben nach Größe getrennt. Eine Maschine trägt dabei auf die feuchten Krabben ein Gemisch aus Kochsalz, Benzoesäure und Citronensäure für eine bessere Haltbarkeit auf. Kochsalz unterstützt dabei die konservierende Wirkung.
Citronensäure ist eine mehrprotonige Säure. Der -Wert für die erste Protolysestufe beträgt


verändert nach: https://lebensmittel-warenkunde.de/lebensmittel/fisch/fischdauerwaren/krabben-in-dosen.html
M3: Titration von Benzoesäure mit Natronlauge
Benzoesäure
werden mit
Natronlauge
titriert.
Der Äquivalenzpunkt liegt beim Verbrauch von Natronlauge. Die Stoffmengenkonzentration des gelösten Salzes am Äquivalenzpunkt entspricht vereinfacht der Ausgangskonzentration der Säure.
M4: Benzoesäure in Nordseekrabben
Die Zulassung von Zusatzstoffen in Lebensmitteln ist innerhalb der EU einheitlich geregelt. Es wird u. a. festgelegt, welche Lebensmittelzusatzstoffe in welchen Lebensmitteln und in welcher Menge zugelassen sind. Für gekochte Krebs- und Weichtiere wie Nordseekrabben beträgt die zulässige Höchstmenge Benzoesäure pro Kilogramm Lebensmittel. Für die tägliche Aufnahme von Benzoesäure gelten bis zu
Benzoesäure pro Kilogramm Körpergewicht als gesundheitlich unbedenklich.
Um zu überprüfen, wie hoch der Gehalt an Benzoesäure eines Lebensmittels ist, wird durch Titration die Stoffmengenkonzentration bestimmt. Bei festen Lebensmitteln muss vorher eine Extraktion der Benzoesäure durchgeführt werden. Vereinfacht wird dabei davon ausgegangen, dass Benzoesäure vollständig aus dem Lebensmittel extrahiert wird und keine weiteren Säuren in dem Extrakt vorhanden sind.
Experiment
Aus einer Portion von Nordseekrabben wurden
eines Gesamtextraktes gewonnen.
davon wurden mit einer Natronlauge der Stoffmengenkonzentration
titriert. Es wurden
Maßlösung bis zum Erreichen des Äquivalenzpunktes verbraucht.
zusammengestellt nach: https://www.icba-net.org/files/resources/benzene-german.pdf; https://www.bvl.bund.de/DE/Arbeitsbereiche/01_Lebensmittel/04_AntragstellerUnternehmen/04_Zusatzstoffe/lm_zusatzstoffe_Zulassung_node.html; https://doi.org/10.2903/j.efsa.2016.4433; letzter Zugriff: 17.07.2024
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Erläuterung:
-
-
Benzoesäure gehört mit einem
-Wert von
zu den schwachen Säuren: unvollständige Protolyse der Benzoesäure-Moleküle
-
Citronensäure ist mit einem
-Wert von
eine stärkere Säure als Benzoesäure: stärkere Protolyse von Citronensäure-Molekülen und damit Erhöhung der Konzentration an Hydronium/Oxonium-Ionen
-
Einfluss der erhöhten Konzentration an Hydronium/Oxonium-Ionen auf das Protolysegleichgewicht der Benzoesäure-Moleküle: verstärktes Ablaufen der Rückreaktion und damit Erhöhung der Konzentration an Benzoesäure-Molekülen
-
erhöhte Konzentration an Benzoesäure-Molekülen aufgrund ihrer guten antimikrobiellen Wirkung im Vergleich zu kaum wirksamen Benzoat-Ionen wünschenswert, da verbesserter Schutz der Nordseekrabben vor Verderb
Erläuterung:
-
Benzoesäure-Moleküle: unpolarer, aromatischer Benzyl-Rest und polare Carboxy-Gruppe mit positiv polarisierten Wasserstoff- und negativ polarisierten Sauerstoff-Atomen
-
Wasser-Moleküle: Dipole mit positiv polarisierten Wasserstoff- und negativ polarisierten Sauerstoff-Atomen
-
Ausbildung von Wasserstoffbrücken zwischen polaren Carboxy-Gruppen der Benzoesäure-Moleküle und Wasser-Molekülen jeweils über negativ polarisierte Sauerstoff-Atome und positiv polarisierte Wasserstoff-Atome der jeweiligen Moleküle
-
geringe Wasserlöslichkeit aufgrund des recht großen unpolaren Benzyl-Restes im Vergleich zur kleineren polaren Carboxy-Gruppe im Benzoesäure-Molekül
Anfangs-pH-Wert:
Äquivalenzpunkt:
Halbäquivalenzpunkt:
End-pH-Wert:
Titrationskurve
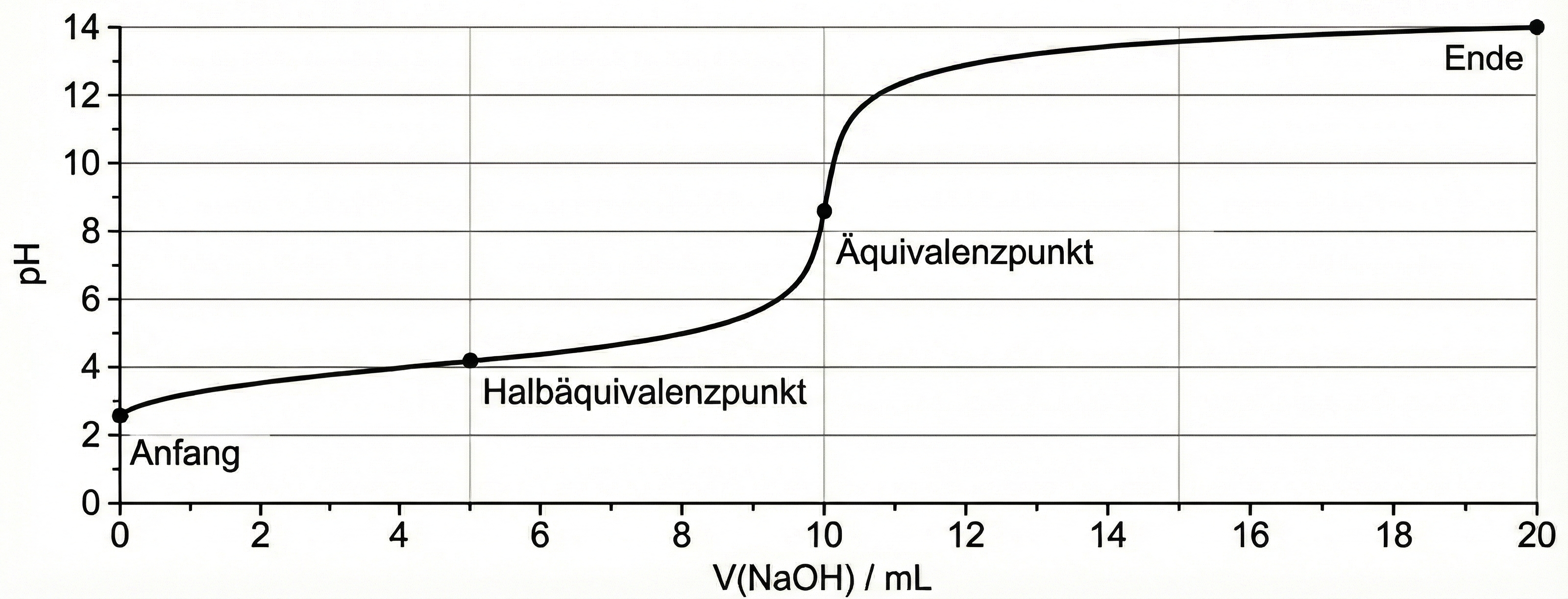
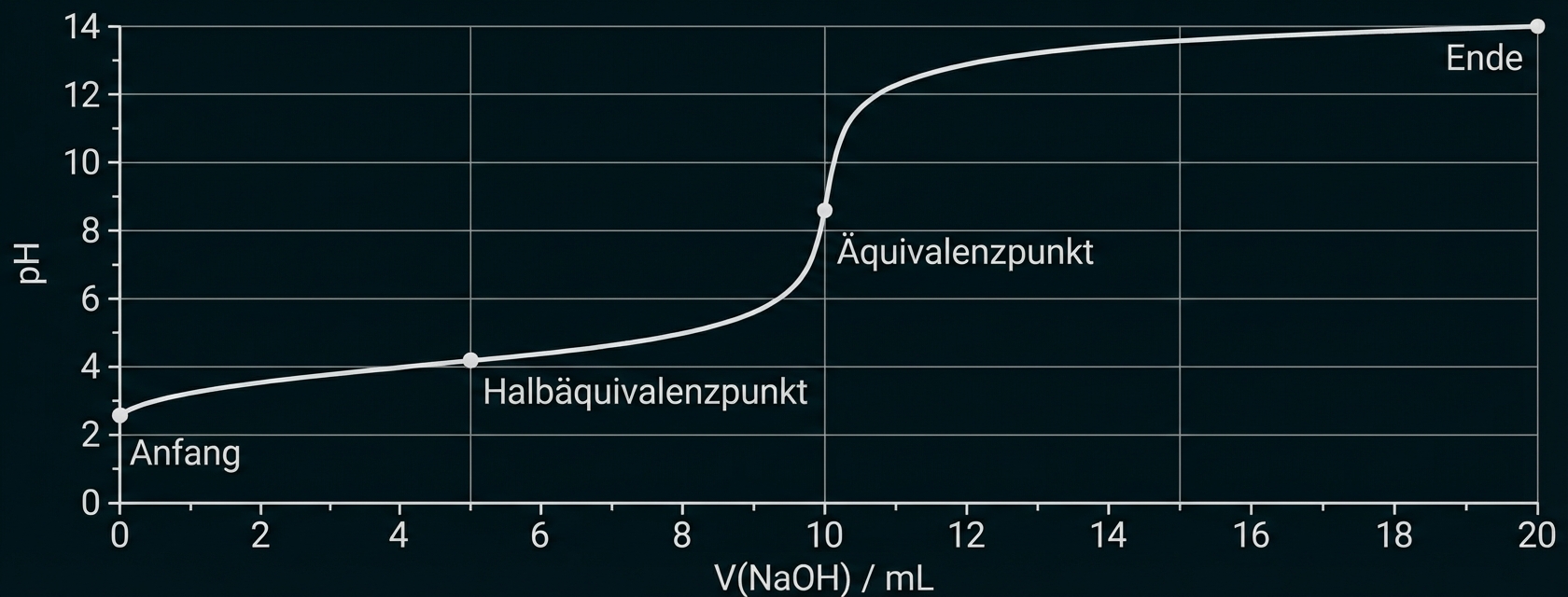
Erklärung:
-
Neutralisation aller aus der Protolyse von Benzoesäure-Molekülen stammenden Hydronium/Oxonium-Ionen durch die Hydroxid-Ionen; Vorliegen einer Natriumbenzoat-Lösung am Äquivalenzpunkt
-
pH-Wert am Äquivalenzpunkt durch Protolyse der als Brønsted-Base fungierenden Benzoat-Ionen bestimmt: Entstehung von Benzoesäure-Molekülen und Hydroxid-Ionen, daher Äquivalenzpunkt im alkalischen Bereich
Stoffmengenverhältnis:
Für gilt:
im Krabbenextrakt
Berechnung der Gesamtmasse an Benzoesäure:
Begründung:
-
zugelassene Höchstmenge an Benzoesäure:
pro Kilogramm Nordseekrabben, entsprechend
Benzoesäure in
Nordseekrabben
-
Überschreitung der zugelassenen Höchstmenge; keine Eignung zum Verzehr