Aufgabe 2 – Butanole
Isomere Alkanole mit vier Kohlenstoff-Atomen werden zur Gruppe der Butanole zusammengefasst. Die Butanole zeigen in Abhängigkeit von der Struktur der jeweiligen Moleküle unterschiedliches Reaktionsverhalten.
Gib die Valenzstrichformeln (Lewis-Formeln) der jeweiligen funktionellen Gruppe der Moleküle von Butan-1-ol, Butanal und Butansäure an und benenne diese (M 1).
Begründe anhand der Struktur der Moleküle die unterschiedlichen Siedetemperaturen von Butan-1-ol, Butanal und Butansäure (M 1).
Beschreibe den Mechanismus zur Bildung von Butan-2-ol-Molekülen (M 2).
Benenne den Mechanismus (M 2).
Formuliere einen Mechanismus zur Bildung von 2-Methylpropan-2-ol-Molekülen auf Grundlage von M 2.
Erkläre anhand des Zusammenhangs zwischen der Struktur und der Eigenschaft die Eignung von Ethanol als Lösungsmittel für Butansäure (M 1).
Leite den pKS-Wert von 2-Methylpropansäure aus dem dokumentierten Experiment ab (M 3, M 4).
Berechne den Heizwert von 2-Methylpropan-1-ol (M 5, M 6).
Diskutiere die Verwendung von Biobutanol als Kraftstoff unter dem Aspekt der Nachhaltigkeit anhand von drei Argumenten (M 5).
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Material 1: Siedetemperaturen ausgewählter organischer Verbindungen
Tabelle 1: Übersicht
|
Name der Verbindung |
mögliche Strukturformel |
Siedetemperatur in |
|
Butanal |
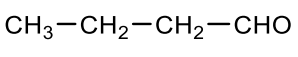 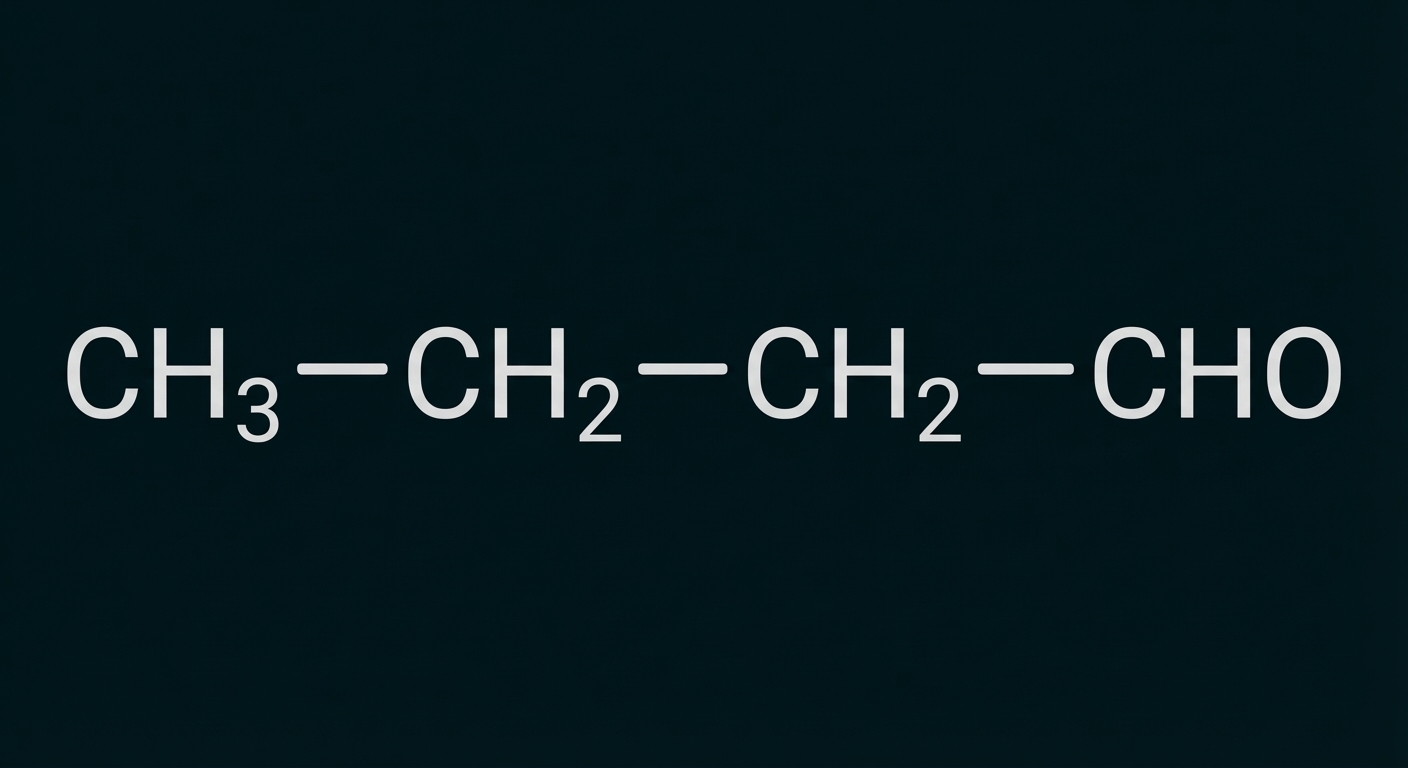
|
75 |
|
Butan-1-ol |
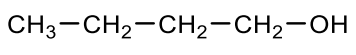 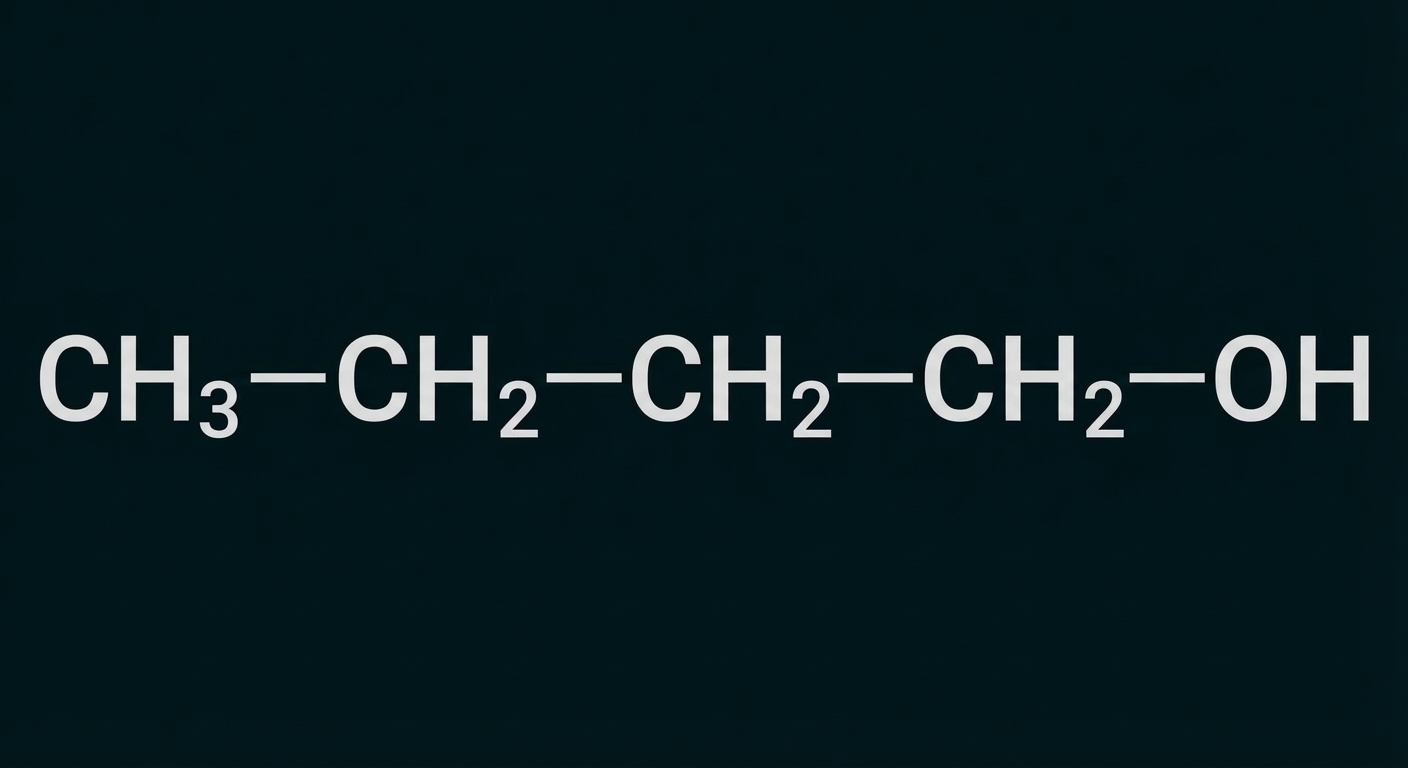
|
118 |
|
Butan-2-ol |
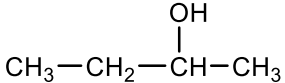 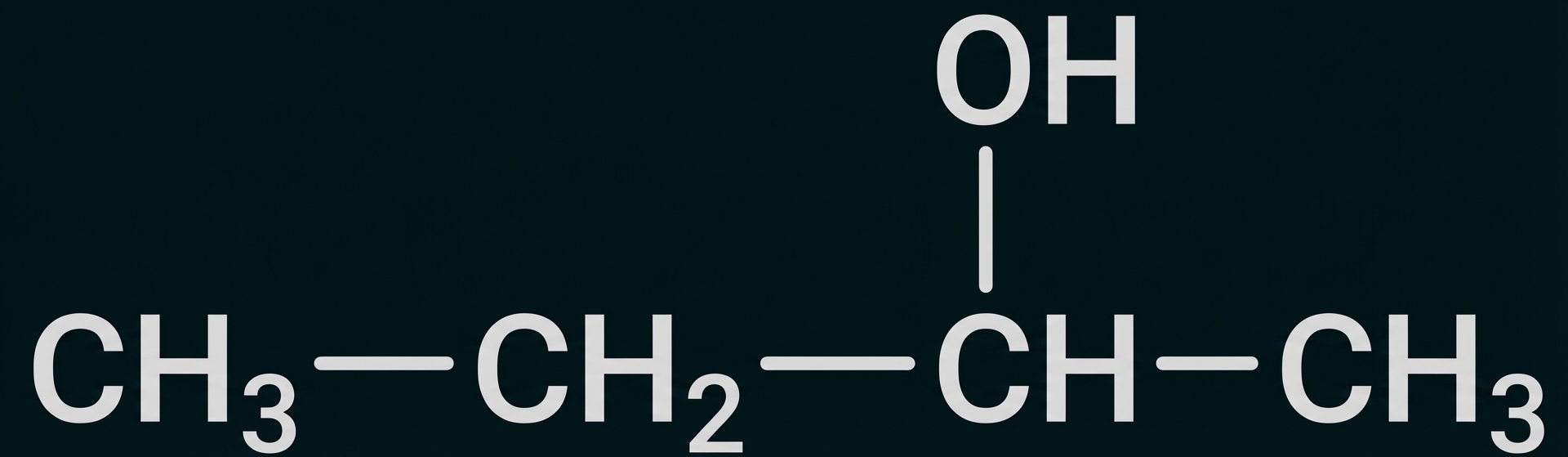
|
99 |
|
Butansäure |
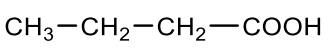 
|
163 |
|
2-Methylpropansäure |
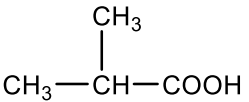 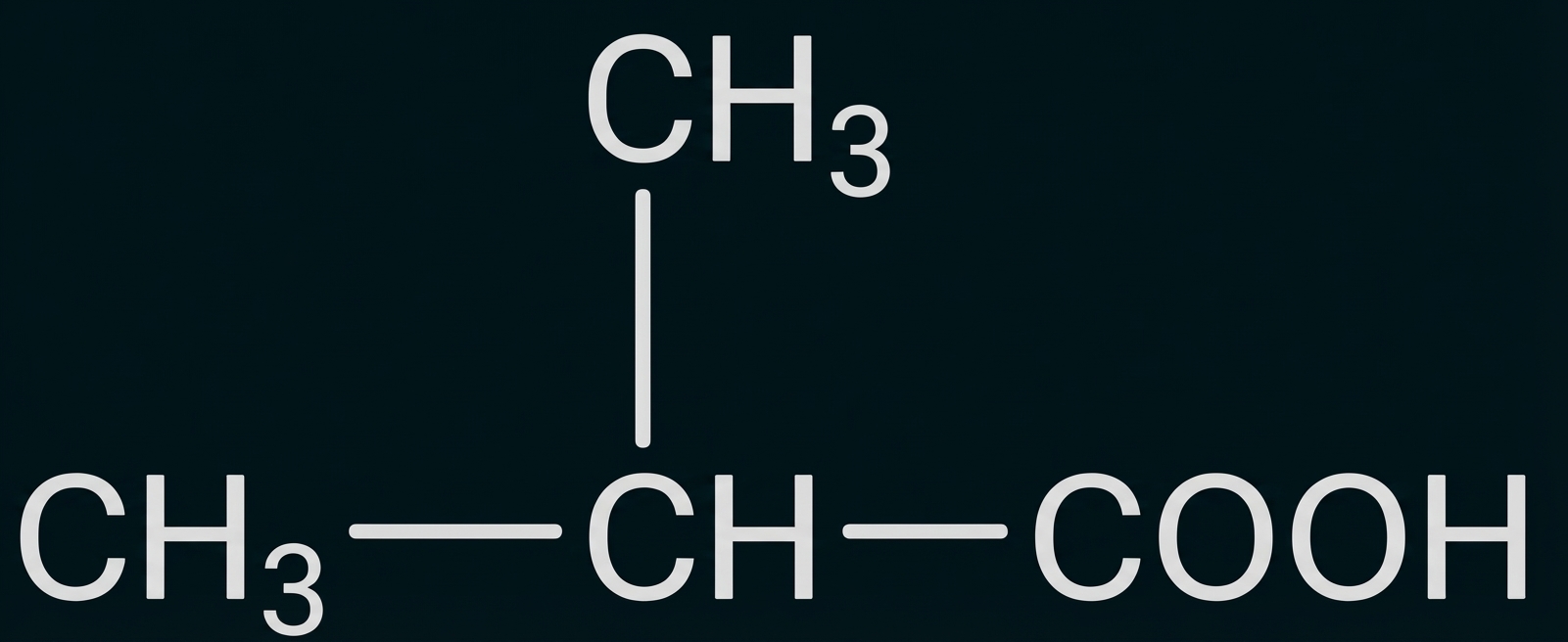
|
155 |
Material 2: Mechanismus der Bildung von Butan-2-ol-Molekülen
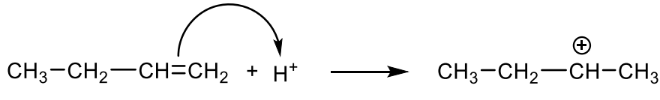
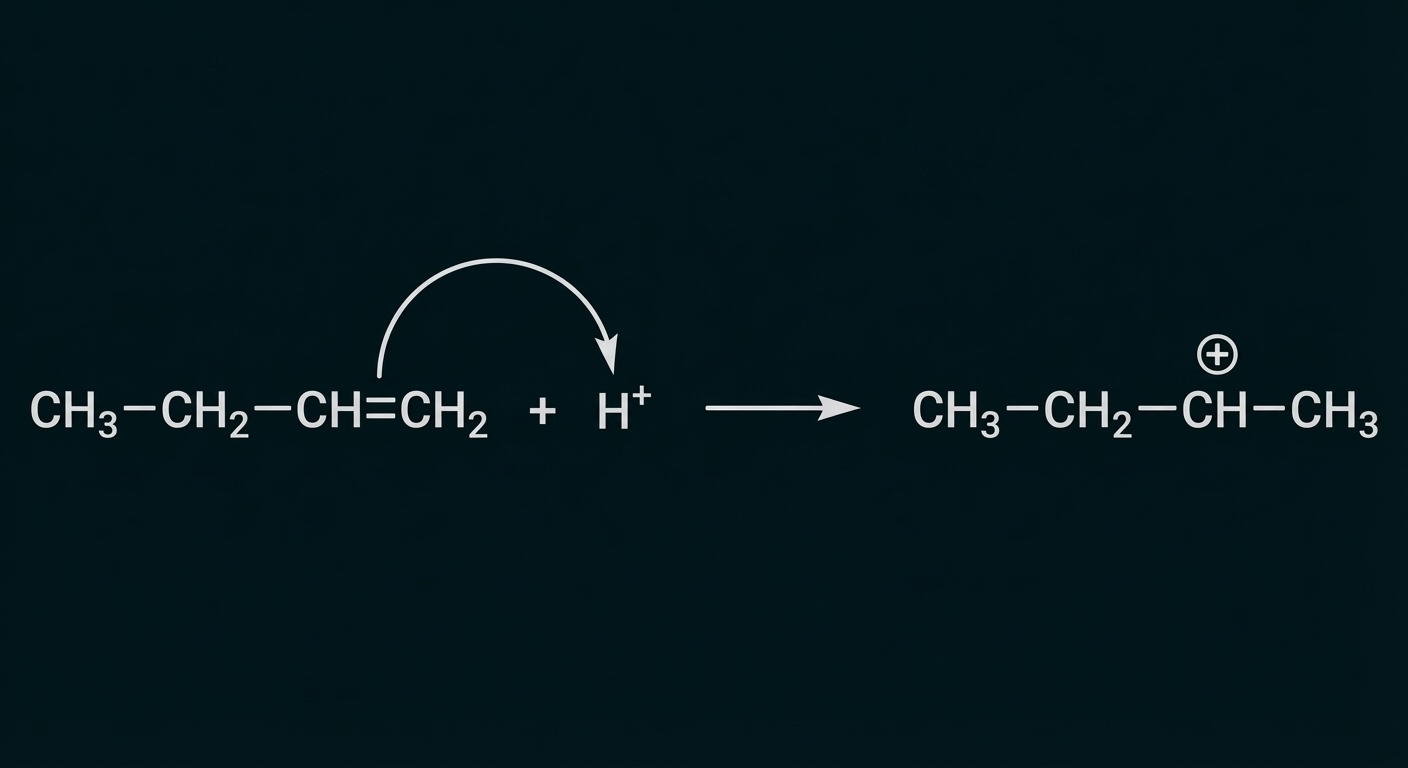
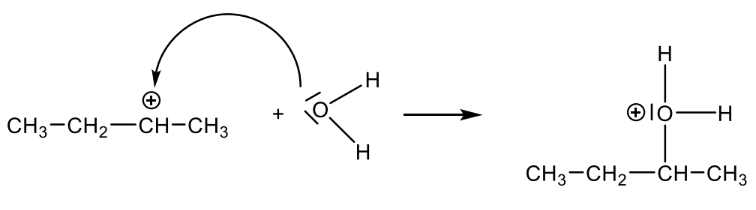
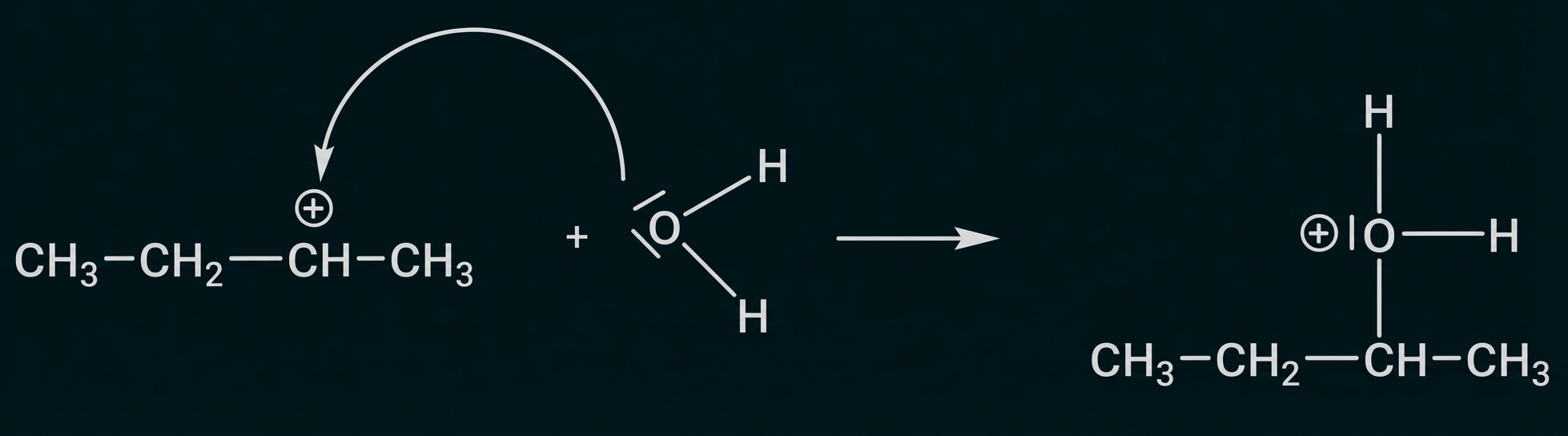
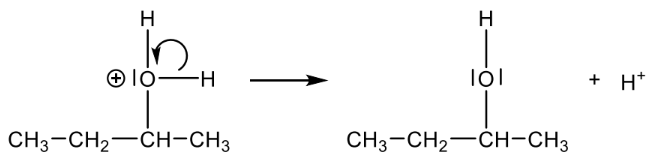
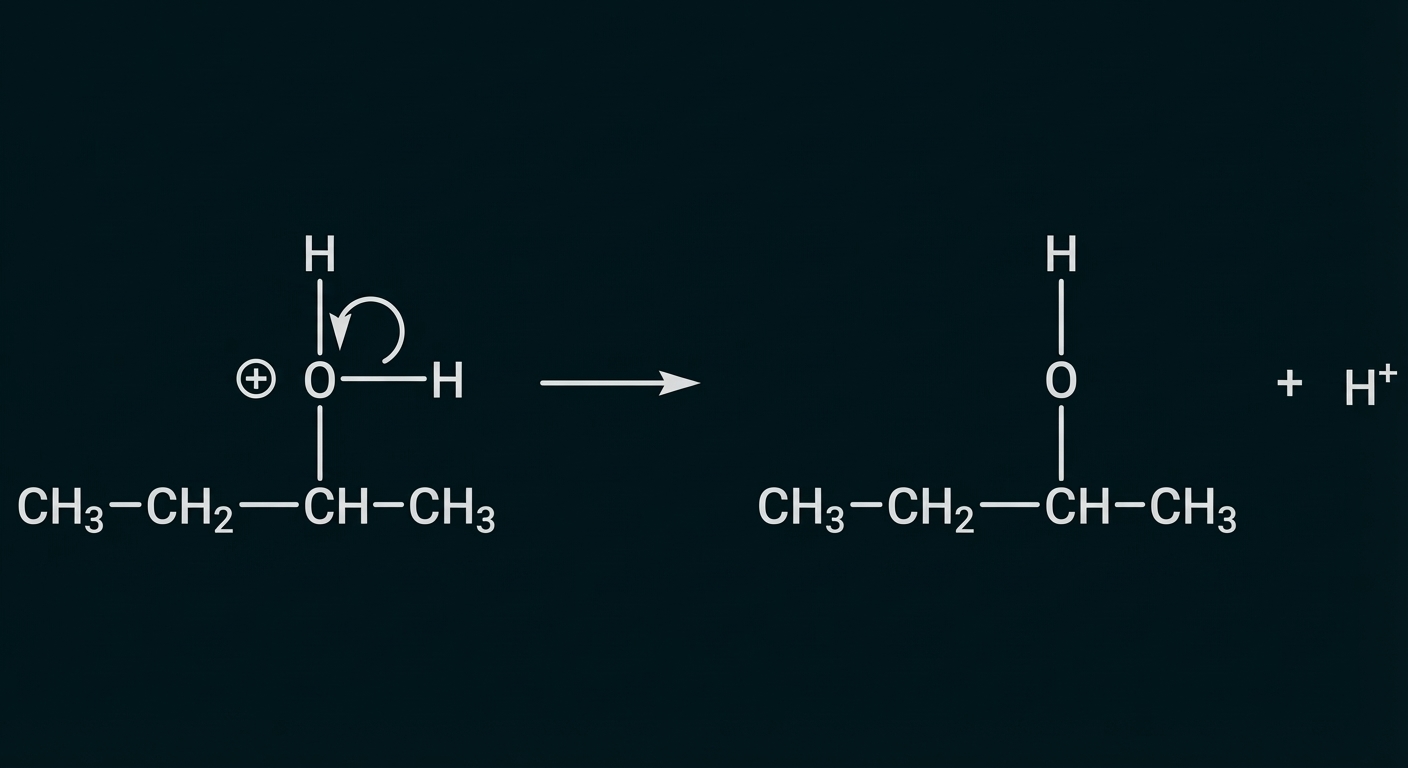
Material 3: Butansäure
Butansäure ist ein farbloser, nach ranziger Butter riechender Stoff, der sich gut in Wasser und in Ethanol löst. Die Salze der Butansäure sind geruchlos.
Material 4: dokumentiertes Experiment
Der pH-Wert gleichkonzentrierter Lösungen von Butansäure und 2-Methyl-propansäure wird untersucht.
Die Untersuchung ergibt den gleichen pH-Wert für beide Lösungen.
Material 5: Biobutanol
Biobutanol sind Butanole, insbesondere Butan-1-ol und 2-Methylpropan-1-ol, die aus Biomasse wie z. B. Ölpflanzen, Getreide, Holz oder tierischen Abfällen erzeugt werden. Biobutanol kann dem Kraftstoff für Otto-Motoren direkt beigemischt werden.
Um Brennstoffe miteinander vergleichen zu können, wird z. B. der Heizwert H angegeben. Der Heizwert eines Brennstoffs ist der positive Wert der Änderung der Enthalpie für die vollständige Verbrennung von 1 kg dieses Stoffes unter der Annahme, dass alle Reaktionsprodukte gasförmig vorliegen.
Dieser beträgt für Benzin ca. 41 MJ/kg, für Diesel ca. 43 MJ/kg.
Material 6: thermodynamische Daten
Tabelle 2: ausgewählte thermodynamische Größen
|
Name der Verbindung |
Summenformel |
|
|
Kohlenstoffdioxid |
|
|
|
2-Methylpropan-1-ol |
|
|
|
Wasser |
|
|
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Angeben und Benennen
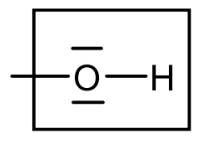
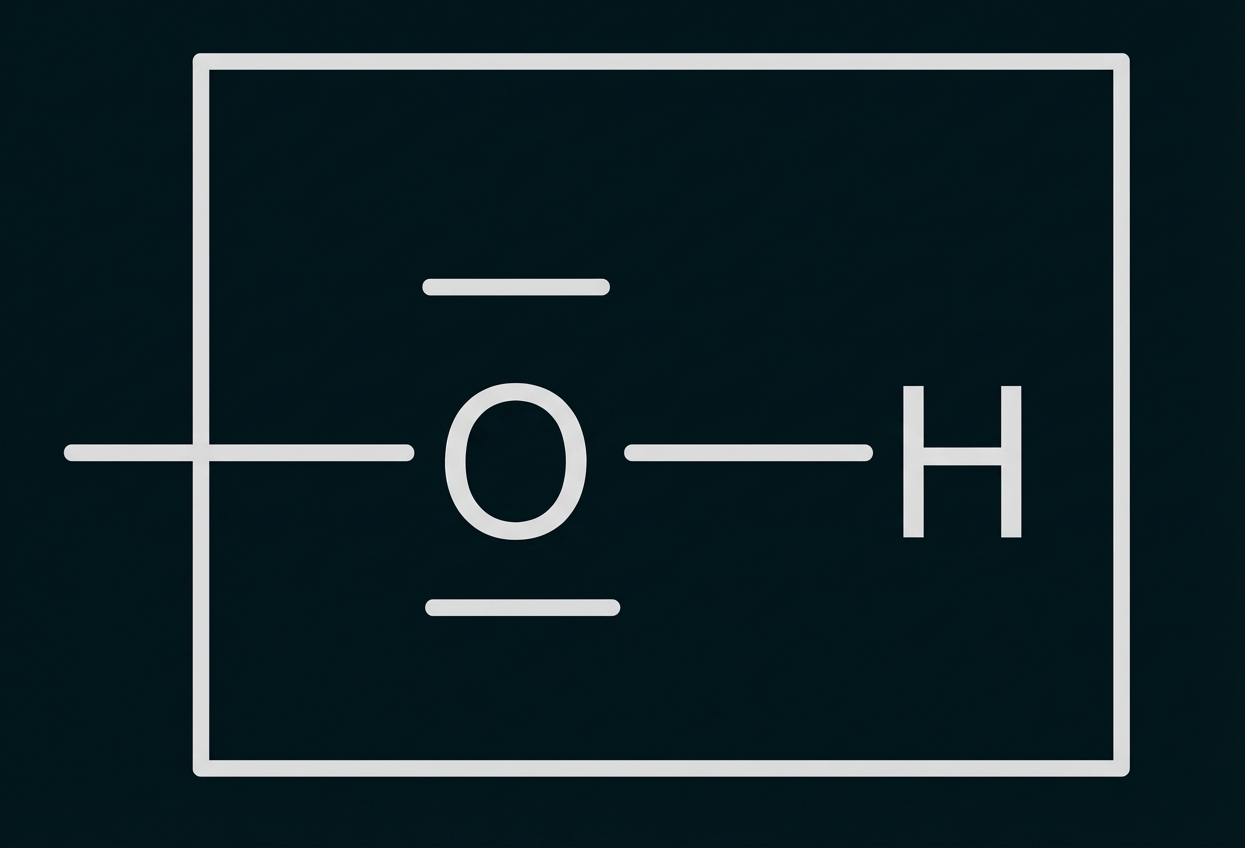
Hydroxygruppe
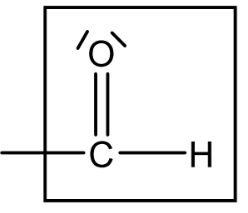
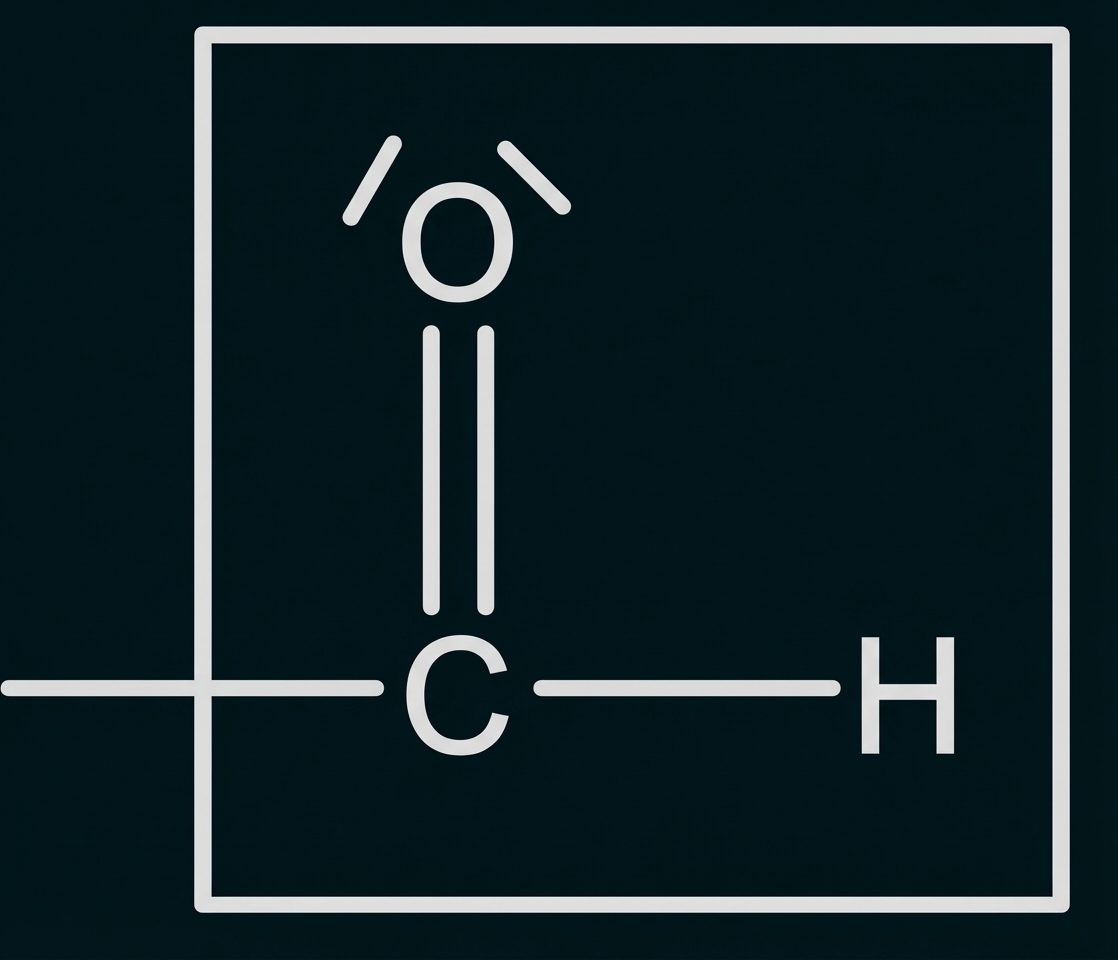
Aldehydgruppe
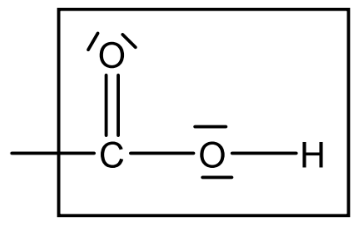
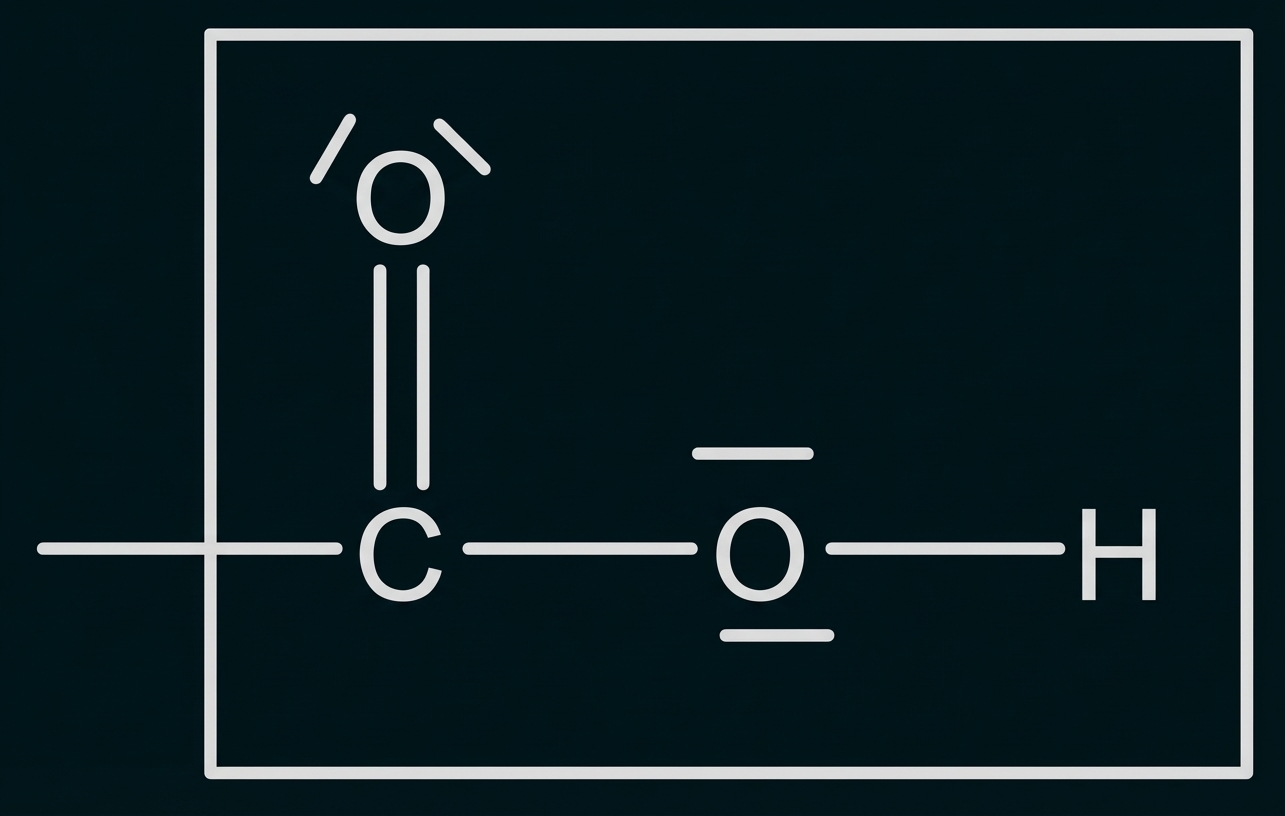
Carboxygruppe
Begründen der Siedetemperatur
-
je stärker die intermolekularen Wechselwirkungen zwischen den Molekülen einer Verbindung, desto mehr Energie ist notwendig, um den Molekülabstand zu erhöhen und desto höher ist die Siedetemperatur des Stoffes
-
Van-der-Waals-Wechselwirkungen sind schwächer als Dipol-Dipol- Wechselwirkungen, die schwächer als Wasserstoffbrücken sind
-
zwischen den Molekülen von Butanal wirken neben Van-der-Waals- Wechselwirkungen nur Dipol-Dipol-Wechselwirkungen
-
zwischen den Molekülen von Butan-1-ol wirken neben Van-der-Waals- Wechselwirkungen Dipol-Dipol-Wechselwirkungen und Wasserstoffbrücken
-
zwischen den Molekülen von Butansäure wirken neben Van-der-Waals- Wechselwirkungen stärkere Dipol-Dipol-Wechselwirkungen (Carbonylgruppe) und Wasserstoffbrücken
Beschreiben des Mechanismus
-
Wasserstoff-Ion greift elektrophil an der C-C-Doppelbindung an
-
Elektronenpaarbindung bildet sich zwischen einem Kohlenstoff-Atom der Doppelbindung und dem Wasserstoff-Ion aus
-
ein Carbo-Kation entsteht
-
Sauerstoff-Atom des Wasser-Moleküls greift nucleophil an das Kation an und bildet eine Elektronenpaarbindung zum Kohlenstoff-Atom aus
-
Elektronenpaarbindung zwischen Sauerstoff-Atom und Wasserstoff- Atom wird heterolytisch gespalten und ein Wasserstoff-Ion wird abgegeben
Benennen des Mechanismus
-
elektrophile Addition
Formulieren des Mechanismus
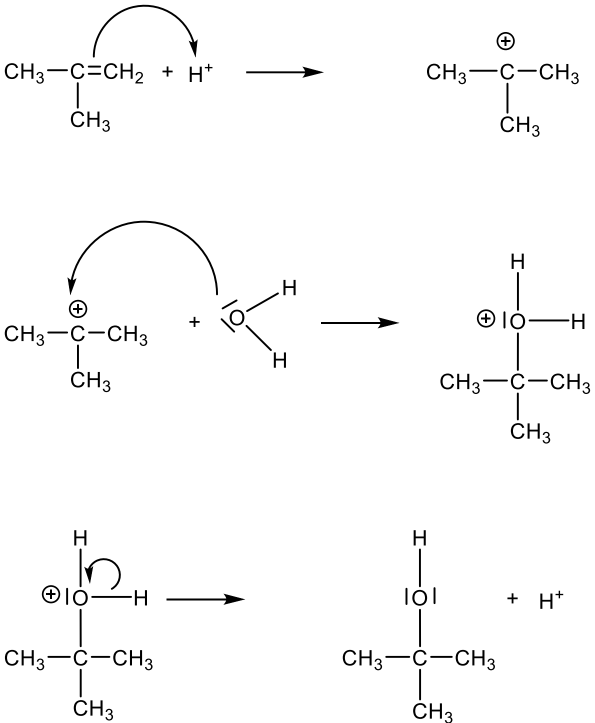
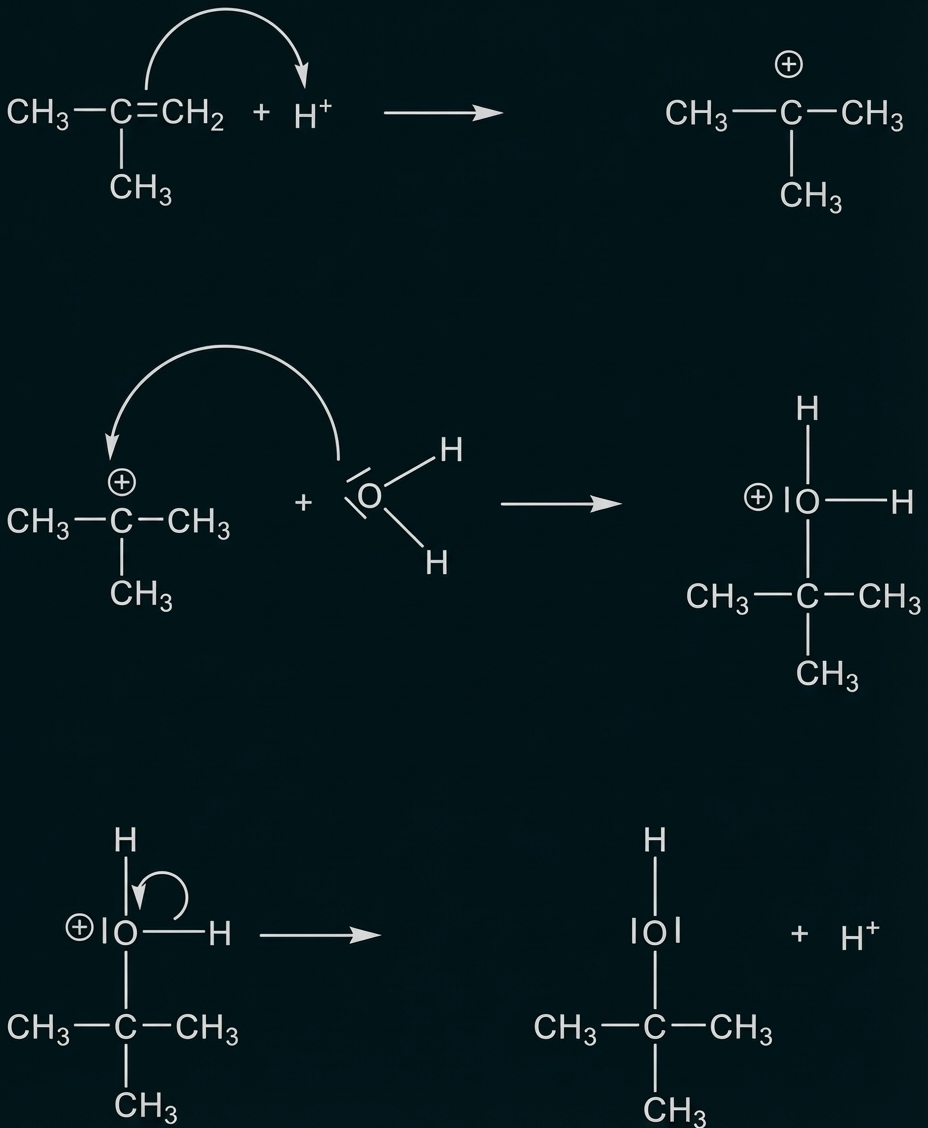
Erklären der Löslichkeit
-
Die Eignung des Ethanols als Lösungsmittel wird sowohl von der Hydroxygruppe als auch von der Ethylgruppe bestimmt.
-
Zwischen der Ethylgruppe des Ethanol-Moleküls und dem unpolaren Teil des Butansäure-Moleküls können sich Van-der-Waals- Wechselwirkungen ausbilden.
-
Das positiv polarisierte Wasserstoff-Atom der Hydroxygruppe des Ethanol-Moleküls und die freien Elektronenpaare des negativ polarisierten Sauerstoff-Atoms der Carbonylgruppe des Butansäure- Moleküls können Wasserstoffbrücken ausbilden.
Ableiten des pKS-Werts
-
gleicher pH-Wert bedeutet gleiche Oxonium-Ionen-Konzentration
-
d. h. gleich gute Abspaltbarkeit von Wasserstoff-Ionen aus der Carboxygruppe bzw. nahezu gleiche Polarität der O-H-Bindung in der Carboxygruppe in beiden Molekülen bzw. nahezu gleiche Säurestärke
-
pKS-Wert ist ein Maß für die Säurestärke, somit ist pKS ≈ 4,82
Berechnen des Heizwerts
Angeben der Reaktionsgleichung:
Berechnen der Änderung der Enthalpie:
Berechnen der Stoffmenge für 1 kg Brennstoff:
Berechnen der Änderung der Enthalpie für 1 kg Brennstoff:
Angeben des Heizwerts:
Diskutieren der Verwendung von Biobutanol anhand von 3 Argumenten
Angeben von mindestens einem Pro-Argument, z. B.:
-
Holz, Getreide etc. sind nachwachsende Rohstoffe
-
Kohlenstoffdioxidemission nur so groß wie vorher Kohlenstoffdioxid im Brennstoff gebunden wurde
-
kein fossiler Brennstoff, nicht endlich
-
Anbau von Getreide in Deutschland möglich, kurze Transportwege
Angeben von mindestens einem Contra-Argument, z. B.:
-
Flächenkonkurrenz zur Nahrungsmittelproduktion (Teller-Tank- Problematik)
-
Monokulturen
-
Kohlenstoffdioxidemission auch durch Anbau, Transport und Verarbeitung zu Biobutanol
-
Heizwert schlechter als bei fossilen Kraftstoffen
Abwägen der Argumente und Fällen eines sachlogischen Fazits