Aufgabe 3 – Zink und Eisen – zusammen stark gegen Rost
Zink als Gebrauchsmetall für Eimer, Schüsseln und Münzen begleitet den Menschen schon seit dem Altertum. Zwar werden auch heute noch viele Alltagsgegenstände aus Zink hergestellt, doch der Großteil allen gewonnenen Zinks wird als Korrosionsschutz für Eisenbauteile verwendet. Die Nachfrage für Zink auf dem Weltmarkt ist seit Jahren konstant hoch und das Interesse für Recycling steigt.
Beschreibe die beim Rosten von Eisen zur Materialermüdung führende stoffliche Veränderung (M 1).
Begründe die beim Rosten abnehmende Verformbarkeit auf Teilchenebene (M 1).
Erkläre unter Einbeziehung von Standardpotenzialen den Sachverhalt, dass selbst beschädigte Zinküberzüge Eisenbauteile noch vor Korrosion schützen (M 1).
Skizziere ein Schema der einzelnen Reaktionsschritte bei der Gewinnung von Zink und berücksichtige Primär- und Sekundärproduktion. Gib darin sämtliche Produkte und Edukte an, ausgenommen bei der Elektrolyse (M 2).
Gib zwei Gemeinsamkeiten und zwei Unterschiede der Primär- und Sekundärproduktion an (M 2).
Beurteile die Empfehlung zum Neuverzinken von Eisenbauteilen (M 3).
Führe die in M 4 beschriebenen Experimente durch.
Gib deine Beobachtungen an und werte diese unter Einbeziehung von Reaktionsgleichungen aus.
Hinweis: Für den Fall, dass du keine auswertbaren Beobachtungen erzielt hast, kannst du dir Ersatzbeobachtungen unter Abzug von 3 BE geben lassen.
Formuliere die Reaktionsgleichung der großtechnischen Elektrolyse von Zink(II)-sulfat-Lösung (M 5).
Begründe zwei Versuchsbedingungen der industriellen Elektrolysezelle, die gegenüber dem Experiment abgeändert wurden, damit eine großtechnische Gewinnung von Zink gelingt (M 4, M 5).
Hinweis: Größenverhältnisse der Anlage bzw. eingesetzte Massen sind nicht zu betrachten.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Material 1: Korrosion von Eisen und Korrosionsschutz durch Verzinken
Korrosion führt zur Beschädigung von metallischen Bauteilen und verursacht Materialermüdung, die bis zur Funktionsuntüchtigkeit (Ermüdungsbruch) reichen kann.
Beim Eisen nennt man diesen Vorgang „Rosten“ und das Ergebnis „Rost“. Rost ist vereinfacht ein Stoffgemisch aus Eisen(II)-oxid, Eisen(III)-oxid und Eisen(II)-hydroxid. Frischer Rost ist hellbraun gefärbt, voluminös und spröde. Er wölbt sich mit der Zeit auf und blättert vom Bauteil ab.
Korrosion verursacht einen enormen wirtschaftlichen Schaden von jährlich mehreren Milliarden Euro in Deutschland (Schätzung).
Das Verzinken ist ein sehr effektives Verfahren des Korrosionsschutzes für Eisen. Das Eisenbauteil wird dabei vollständig mit einer dünnen, fest haftenden Zinkschicht versehen. Man macht sich zunutze, dass Zink bereits bei 419 °C geschmolzen vorliegt und taucht die gereinigten Eisenbauteile kurz in die Zinkschmelze ein. Alternativ kann das Verzinken durch Elektrolyse erfolgen. Der Korrosionsschutz ist selbst bei Beschädigung der Zinkschicht noch gegeben (Abbildung 1).
Zink ist bei Raumtemperatur fest und silberglänzend. An feuchter Luft läuft es in Folge oberflächlicher Bildung von Zink(II)-oxid bzw. Zink(II)-carbonat matt-grau an, wodurch das darunterliegende Zink weitgehend vor witterungsbedingten Einflüssen geschützt wird.
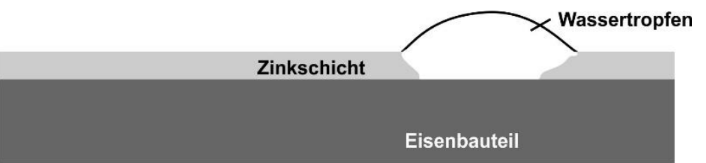
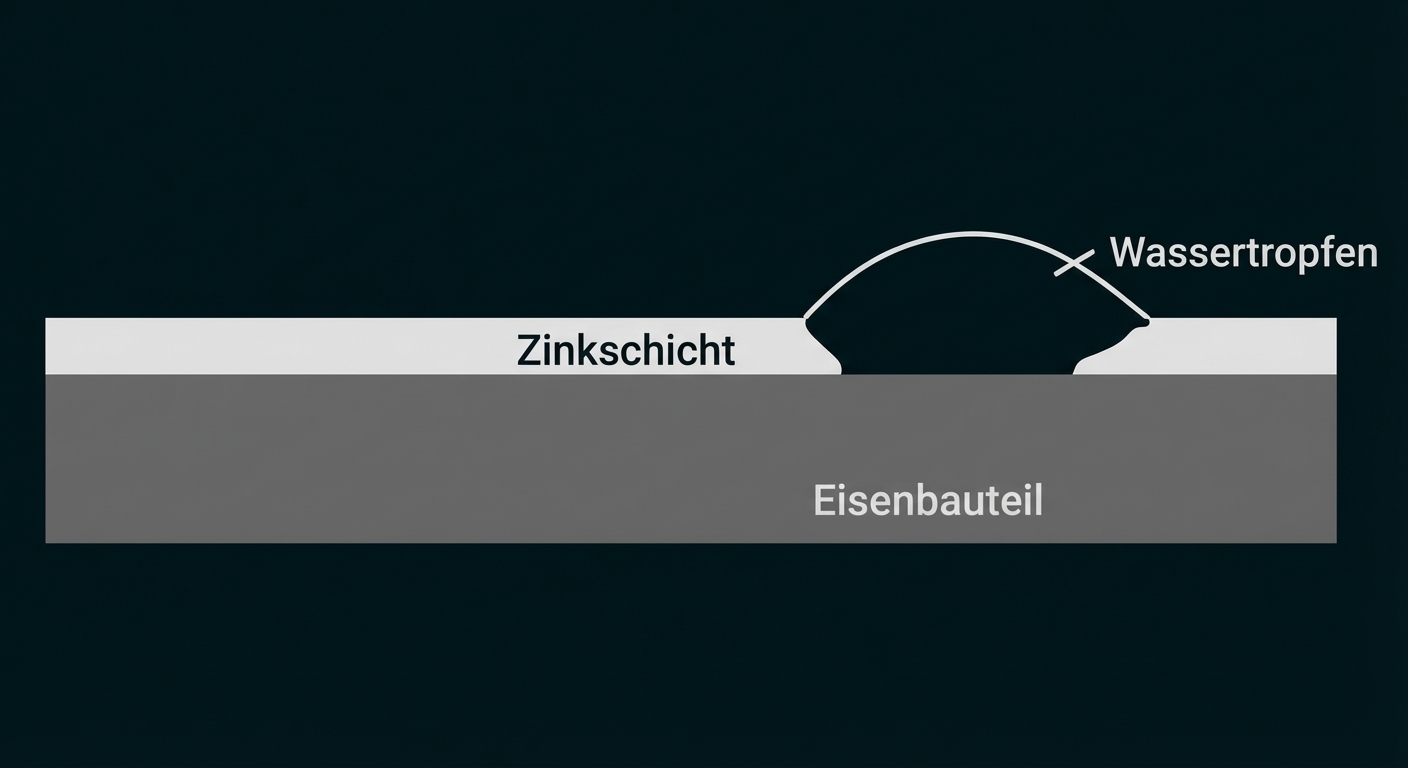
Abb. 1: verzinktes Eisenbauteil, rechts Zinkschicht verletzt und von Wassertropfen benetzt
Material 2: Synthesewege für Zink
Die Herstellung von Zink beruht seit Jahrhunderten auf der Verarbeitung der Zinkerze Zink(II)-sulfid und Zink(II)-carbonat
Diese werden durch Erzbergbau gewonnen und in einem ersten Schritt in Zink(II)-oxid
überführt. Im Fall von Zink(II)- sulfid wird das Erz bei 900 °C mit Sauerstoff aus der Luft zur Reaktion gebracht („Rösten“). Hierbei wird giftiges Schwefeldioxid freigesetzt. Im Fall von Zink(II)-carbonat wird das Erz in Abwesenheit von Luft in einem Ofen auf 1000 °C erhitzt („Brennen“), wobei Kohlenstoffdioxid abgegeben wird.
Für die sich anschließende Gewinnung von elementarem Zink aus Zink(II)-oxid gibt es ebenfalls zwei Verfahren: das thermische und das hydrometallurgische Verfahren. Beim thermischen Verfahren wird Zink(II)-oxid bei knapp 1000 °C mit Kohlenstoffmonooxid zur Reaktion gebracht, es bildet sich als Nebenprodukt Kohlenstoffdioxid. Beim hydrometallurgischen Verfahren wird Zink(II)-oxid mit Schwefelsäure versetzt und die damit erzeugte Zink(II)-sulfat-Lösung im Anschluss elektrolysiert.
Zur bislang beschriebenen sogenannten Primärproduktion, der Rohstoffgewinnung auf Basis natürlicher Grundstoffe wie Erzen, gewinnt in jüngerer Zeit auch die Sekundärproduktion an Bedeutung. Darunter versteht man die Rohstoffgewinnung auf Basis recycelter Materialien, im Fall von Zink aus zinkhaltigem Schrott. Dieser wird im Elektrolichtbogen bei etwa 1800 °C eingeschmolzen. Enthaltenes Zink entweicht bei diesen Temperaturen gasförmig und reagiert umgehend mit Sauerstoff aus der Luft zum Zink(II)-oxid, welches als Staub anfällt und gesammelt wird.
Material 3: Ökobilanzstudie empfiehlt Neuverzinken
Die an Straßen verbauten Schutzplanken bestehen aus verzinktem Eisen. Sind diese am Ende ihrer verhältnismäßig langen Gebrauchsdauer dennoch zu ersetzen, empfiehlt sich nach einer Ökobilanzstudie des niederländischen Forschungsinstituts CE Delft ein Neuverzinken, sofern die Beschädigungen nicht die Stabilität betreffen. Hierbei bleibt das Eisengerüst erhalten und wird nach einer Oberflächenbearbeitung einfach erneut verzinkt. Die Studie kommt zum Schluss, dass mit den neuverzinkten Schutzplanken im Vergleich zu neu hergestellten Modellen ein deutlich geringerer Fußabdruck einhergeht und signifikant weniger Energie benötigt wird.
Material 4: Experiment
Geräte:
-
Becherglas (V = 100 mL)
-
Kupferblech
-
Graphitstab
-
Spannungsquelle, Spannungsmesser
-
Verbindungskabel und Krokodilklemmen
-
Halterung zur Fixierung der Elektroden
Chemikalien:
-
Zink(II)-sulfat-Lösung
Durchführung Teilexperiment 1:
Befülle das Becherglas gut zur Hälfte mit Zink(II)-sulfat-Lösung und tauche darin den Graphitstab und das Kupferblech bis zum Boden ein. Schließe den Minuspol der Spannungsquelle an den Graphitstab, den Pluspol an das Kupferblech an und elektrolysiere ca. 5 Minuten lang bei angelegter Spannung von
Durchführung Teilexperiment 2:
Beende die Elektrolyse und schalte ein Spannungsmessgerät an die beiden Elektroden von Teilexperiment 1. Achte darauf, dass kein Kurzschluss eintritt und vermeide ruckartige Bewegungen der Elektroden. Führe eine Spannungsmessung durch.
Material 5: Großtechnische Elektrolyse von wässriger Zink(II)-sulfat-Lösung
Bei möglichst niedriger Spannung von wird reine Zink(II)-sulfat-Lösung elektrolysiert. Diese fließt kontinuierlich der industriellen Elektrolysezelle zu. Entsprechend fließt Elektrolyt-Lösung kontinuierlich aus der Zelle ab, wodurch eine Anreicherung der sich beim Elektrolyseprozess bildenden Schwefelsäure verhindert wird.
Je industrieller Elektrolysezelle sind bis zu 48 plattenförmige Kathoden geschaltet. Das sich hieran abscheidende Zink wird nach ein oder zwei Tagen mechanisch abgestreift. Das Material von Anode und Kathode ist so gewählt, dass beide sich durch die Elektrolysevorgänge nicht verändern (sogenannte Inert-Elektroden). An der Anode scheidet sich Sauerstoff ab.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Beschreiben der stofflichen Veränderung
-
Vor dem Rosten liegt ein Eisenbauteil vor (Metall).
-
Nach dem Rosten ist ein Stoffgemisch aus Eisenoxiden und Eisenhydroxid (Ionenverbindungen) entstanden.
Begründen der abnehmenden Verformbarkeit
Metall
-
Metall-Kationen sind in Elektronengas eingebettet.
-
Bindungskräfte bleiben nach Druck bzw. Stoß erhalten, da Verschiebung von Gitterebenen nicht zu Abstoßungskräften führt.
Rost (salzartig)
-
Metall-Kationen und Oxid- bzw. Hydroxid-Anionen bilden Ionengitter.
-
Verschiebung von Gitterebenen führt zu nebeneinander liegenden, gleich geladenen Ionen und daher zu Abstoßungskräften.
Erklären des Korrosionsschutzes
-
Zink leichter als Eisen oxidierbar, da
-
Lokalelement bildet sich aus: Zink-Atome reagieren zu Zink(II)-Ionen, die in Lösung gehen (Oxidation).
-
Zinkschicht wird verbraucht, Eisen wird vorerst nicht oxidiert.
Skizze eines Schemas
-
Erfassen der Grobstruktur des Schemas (Übersichtlichkeit)
-
5 Syntheseschritte mit jeweils sämtlichen Produkten und Edukten
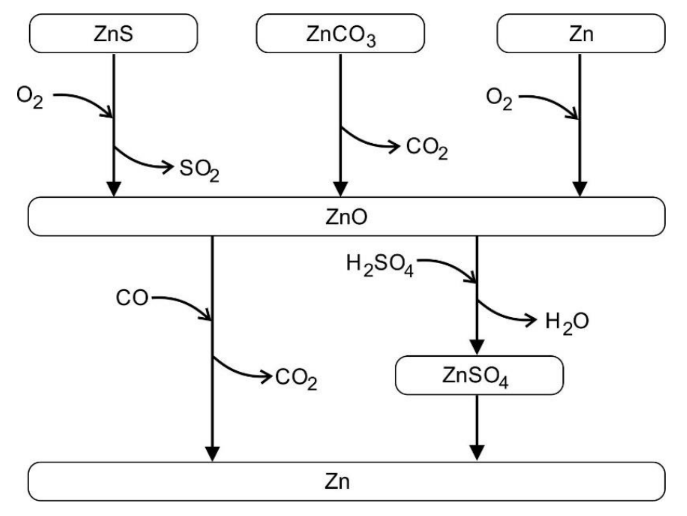
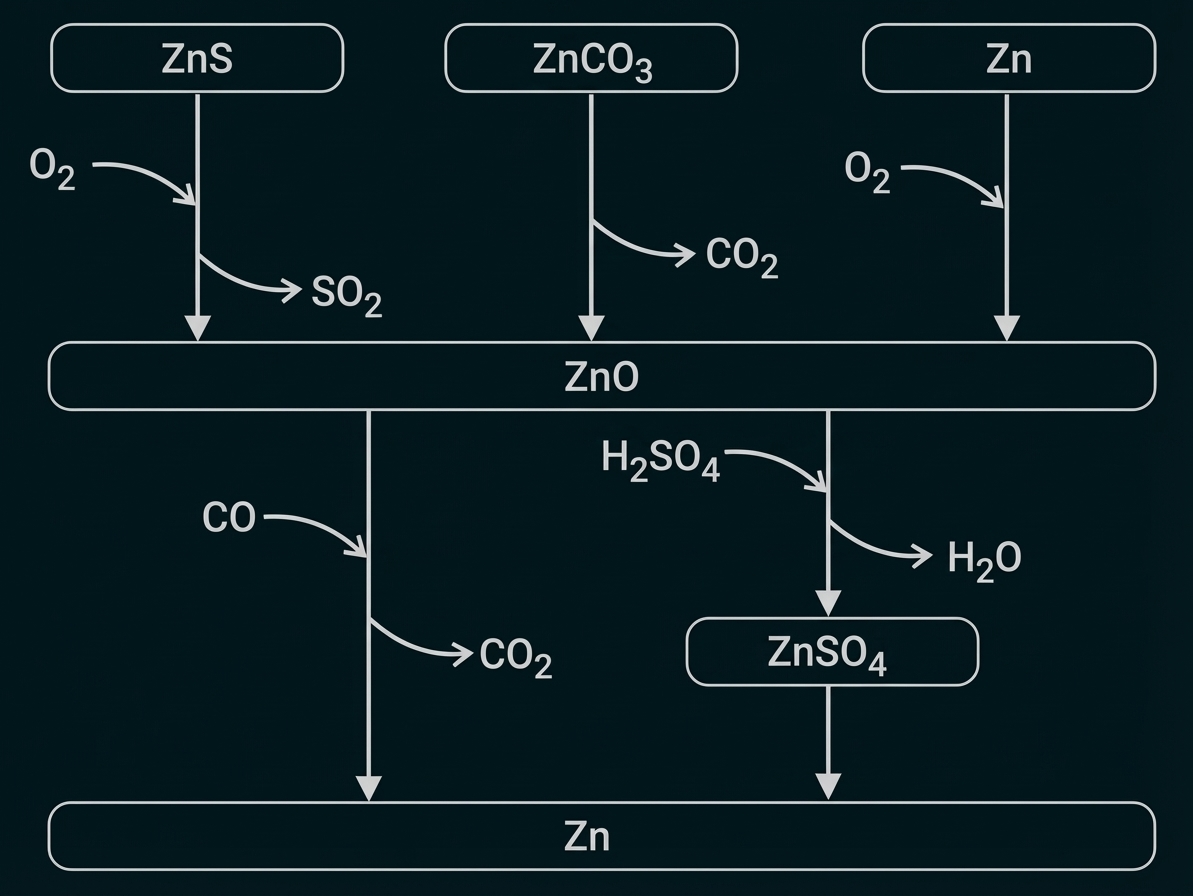
Angeben von Gemeinsamkeiten und Unterschieden
Gemeinsamkeiten:
-
beide energieintensiv
-
beide mit gleichem Zwischenprodukt Zink(II)-oxid
Unterschiede:
-
Synthesewege aus Erzen setzen umweltgefährdende Gase frei, Aufbereitung des zinkhaltigen Altmetalls dagegen nicht.
-
Synthesewege aus Erzen erfordern neue Ressourcen, Aufbereitung aus zinkhaltigem Altmetall ist dagegen ressourcenschonend.
Beurteilen der Empfehlung des Neuverzinkens
-
Herstellung von Metallen (z. B. Eisen) ist energieintensiv
-
Verfahren ist nachhaltiger, da die
-Emmission sinkt und signifikant weniger Energie benötigt wird.
-
Sachurteil: Neuverzinkung kann sinnvoll sein
Durchführen des Experiments
-
Durchführung des Teilexperiments 1 entsprechend der Vorgabe
-
Durchführung des Teilexperiments 2 entsprechend der Vorgabe
-
Einhalten des Arbeitsschutzes
Angeben der Beobachtungen
Teilexperiment 1:
-
Graphit-Elektrode überzieht sich mit grauer Schicht.
-
Elektrolyt-Lösung färbt sich schwach hellblau.
Teilexperiment 2:
-
Spannungsmesswert
Auswerten der Beobachtungen
Teilexperiment 1:
-
Reduktion von Zink(II)-Ionen der Lösung zu Zink-Atomen, die sich an der Elektrode als grauer Überzug abscheiden
-
-
Kupfer-Atome der Elektrode werden zu Kupfer(II)-Ionen oxidiert und verursachen hellblaue Färbung der Elektrolyt-Lösung.
-
Teilexperiment 2:
-
Spannung aufgrund Ausbildung eines galvanischen Elementes
-
Formulieren der Reaktionsgleichung
Begründen zweier Versuchsbedingungen zur großtechnischen Gewinnung, z. B.
-
Inert-Elektrode statt Kupfer-Elektrode, da diese zur Bildung von Kupfer- Ionen im Elektrolyten führt (würden sich abscheiden und der Reinheit des Zinks schaden) und stets ersetzt werden müsste (Elektrode verbraucht sich.)
-
kontinuierlicher Elektrolyseprozess mit kontinuierlichem Zufluss an Zink(II)-Ionen-Lösung, da diese sich beim Elektrolyseprozess verbrauchen und im Schülerexperiment endlich sind (Abscheidung des Zinks endet.)
-
Geringere Spannung, da dies eventuelle Nebenreaktionen (z. B. Wasserstoffbildung) verhindert.