Aufgabe 4 – Milchsäure
Milchsäure dient der Säuerung und Konservierung von Lebensmitteln sowie zur Herstellung von Futtermitteln. Des Weiteren ist sie für den menschlichen Stoffwechsel bedeutsam.
Gib drei Aussagen zum Bau eines Kohlenstoff-Atoms an, die sich aus der Stellung des Elements im Periodensystem ableiten lassen.
Erkläre eine Oxidationszahl vom Kohlenstoffteilchen in einer Verbindung unter Einbeziehen der Elektronenkonfiguration.
Gib den systematischen Namen und die Valenzstrichformel (Lewis-Formel) für ein Milchsäure-Molekül an (M 1).
Formuliere die Reaktionsgleichungen für drei Reaktionen von Milchsäure, die in M 2 benannt sind.
Erläutere an einem Beispiel aus M 2 das Donator-Akzeptor-Prinzip.
Berechne für eine Milchsäure-Lösung mit
-
die Ausgangskonzentration der Milchsäure-Lösung sowie
-
die Stoffmengenkonzentrationen der Oxonium-Ionen und der Hydroxid- Ionen.
Hinweise: Milchsäure-Moleküle protolysieren unvollständig. pKS (Milchsäure) = 3,9
Erkläre die Änderung des pH-Werts einer Milchsäure-Lösung bei Zugabe einer Lösung, die Lactat-Ionen enthält, anhand des Massenwirkungsgesetzes des Protolysegleichgewichts (M 3).
Beurteile die Aussagen in M 3.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Material 1: Milchsäure
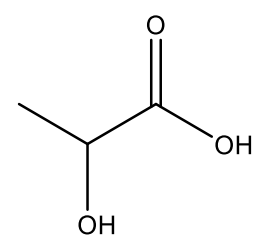
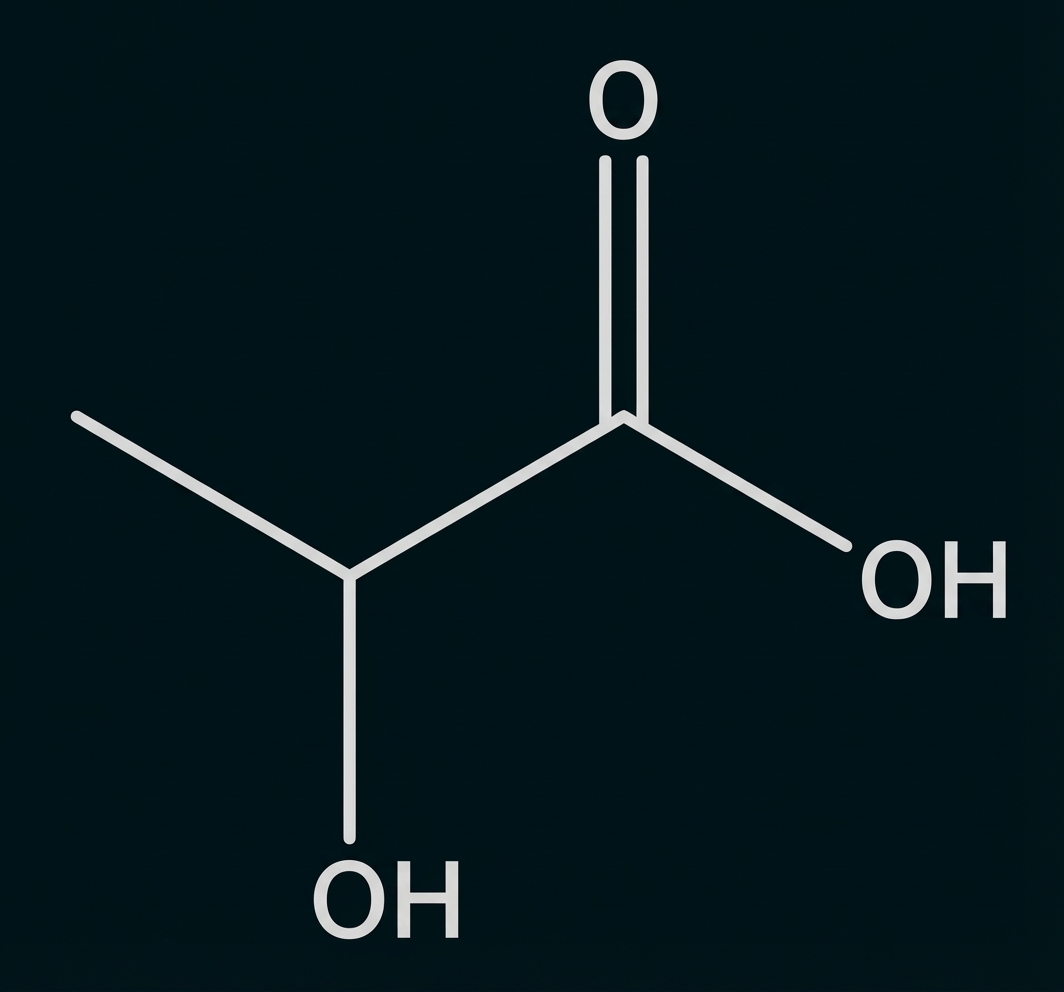
Abbildung 1: Strukturformel eines Milchsäure-Moleküls
Material 2: Reaktionen der Milchsäure
Milchsäure kann an verschiedenen chemischen Reaktionen teilnehmen, die sich aus der Struktur des Milchsäure-Moleküls ableiten lassen, z. B.:
-
Dissoziation nach der Säure-Base-Theorie von Arrhenius,
-
Neutralisation,
-
Veresterung,
-
katalytische Reduktion zu Propan-1,2-diol,
-
Bilden eines Zwitter-Ions durch intramolekulare Protonenwanderung,
-
Reaktion mit geeignetem Metall oder Metalloxid zu einem Salz (Lactat).
Material 3: Milchsäure und Lactat
Der pH-Wert des Blutes wird im Körper in einem engen Bereich (zwischen pH = 7,35 und pH = 7,45) gehalten, um eine optimale Funktion der biochemischen Prozesse zu gewährleisten. Milchsäure und ihre gelösten Salze (Lactate) spielen eine wichtige Rolle bei der Aufrechterhaltung dieses pH-Wert-Bereichs.
In einer verdünnten Milchsäure-Lösung wurde ein pH-Wert von pH = 5,13 und nach dem Zusatz von Natriumlactat ein pH-Wert von pH = 7,4 gemessen.
Tabelle 1: pOH-Wert und Stoffmengenkonzentrationen für pH = 7,4
|
|
|
|
|
|
|
|
|
|
|
|
Aussagen:
Die Lösung aus Milchsäure und Natriumlactat verändert bei Zugabe geringer Volumina einer Natriumhydroxid-Lösung ihren pH-Wert kaum.
Bei Zugabe großer Volumina ändert sich der pH-Wert deutlich.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Angeben der drei Aussagen
-
6 Protonen im Atomkern und 6 Elektronen in der Atomhülle
-
2 besetzte Energieniveaus
-
4 Valenzelektronen
Erklären einer Oxidationszahl
-
Angeben der Elektronenkonfiguration: 6C: 1s2 2s2 2p2
-
Nennen einer Oxidationszahl, z. B. +IV
-
bei +IV hat das Kohlenstoff-Teilchen die Elektronen vom 2s- und 2p-Orbital abgegeben
-
vollbesetztes 1s-Orbital, Teilchen mit Edelgaskonfiguration sind stabil
Angeben des systematischen Namens
-
2-Hydroxypropansäure
Angeben der Valenzstrichformel
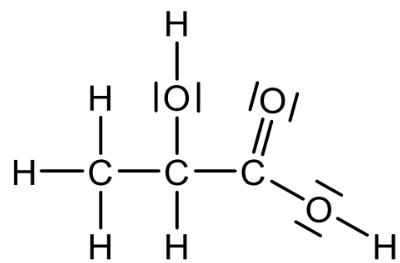
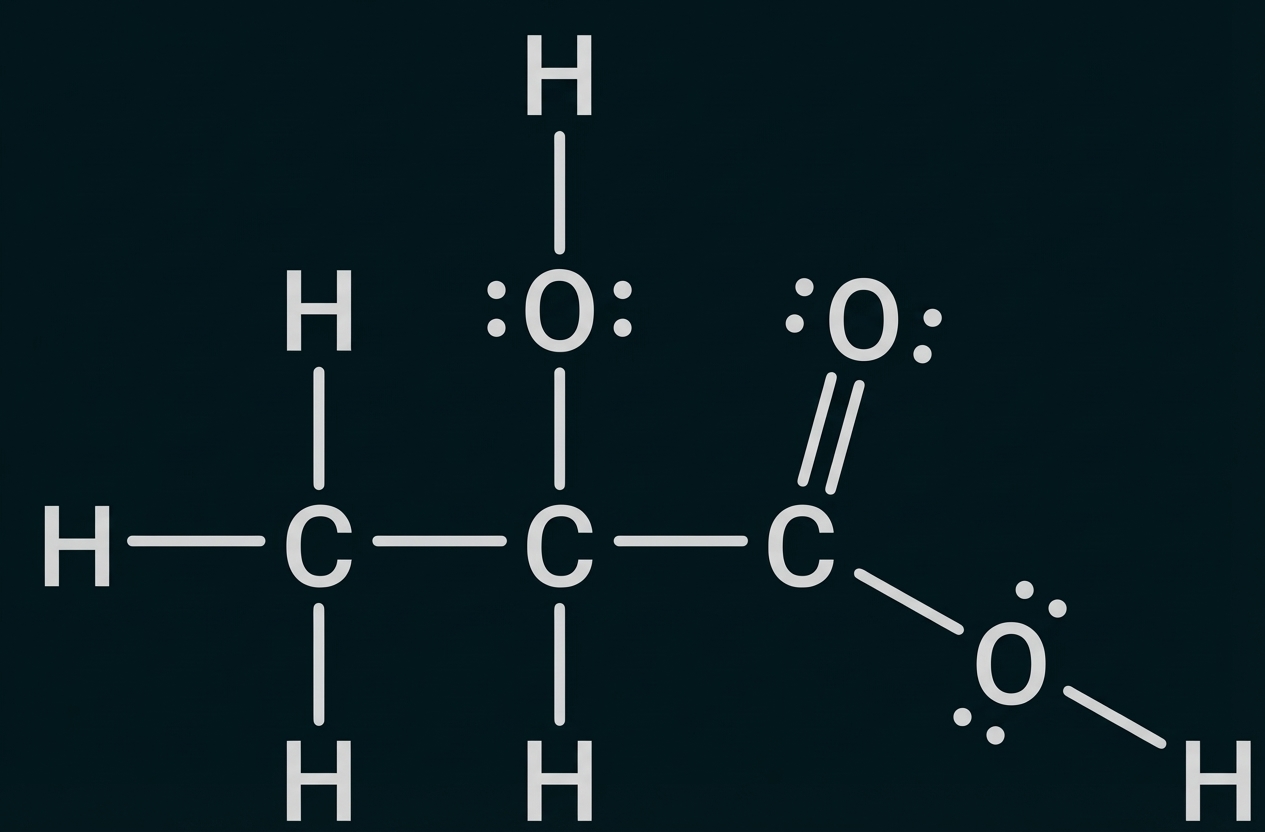
Formulieren von drei Reaktionsgleichungen, z. B.
-
Dissoziation nach der Säure-Base-Theorie von Arrhenius
-
Neutralisation
-
Veresterung
-
katalytische Reduktion zu Propan-1,2-diol
-
Bilden eines Zwitter-Ions
-
Reaktion mit unedlem Metall
-
Reaktion mit einem Metalloxid
Erläutern des Donator-Akzeptor-Prinzips, z. B.
-
Das Milchsäure-Molekül ist der Protonendonator, weil es ein Proton abgibt.
-
Das Hydroxid-Ion ist der Protonenakzeptor, weil es ein Proton aufnimmt.
-
Protonenübergang von einem Milchsäure-Molekül auf ein Hydroxid-Ion.
Berechnen der Ausgangskonzentration
Berechnen der Stoffmengenkonzentration
Erklären der Änderung des pH-Werts
-
steigt.
-
Damit
konstant bleibt, wird
kleiner.
-
Infolgedessen steigt der pH-Wert.
Beurteilen der Aussagen
-
Aussage
-
Hydroxid-Ionen reagieren mit Oxonium-Ionen (Neutralisation)
-
fällt, Hinreaktion wird gefördert
-
Nachbilden von Oxonium-Ionen aus Protolyse der Milchsäure-Moleküle (schwache Säure) und Wiedereinstellen des Protolysegleichgewichts
-
steigt wieder ungefähr auf Ausgangswert
-
pH-Wert ändert sich kaum
-
-
Aussage
-
Hydroxid-Ionen reagieren mit Oxonium-Ionen (Neutralisation) – ohne BE
-
fällt bis nahezu alle Oxonium-Ionen reagiert haben
-
Nachbilden von Oxonium-Ionen aus Protolyse der Milchsäure-Moleküle zu gering
-
Pufferkapazität überschritten,
steigt
-
pH-Wert wird größer
-
Sachurteil zur gesamten Aussage