HT 1 – Phosphorsäure und Phosphate – vielfach verwendete Lebensmittelzusatzstoffe
Phosphorsäure wird in einigen Nahrungsmitteln als Zusatzstoff mit der Nummer E 338 verwendet. Sie ist z. B. für den typischen Geschmack von Cola mitverantwortlich und ist in einigen Lebensmitteln als Säuerungs- und Konservierungsmittel enthalten. Doch seit einigen Jahren kommen Zweifel hinsichtlich der Unbedenklichkeit des ungebremsten Konsums an Phosphorsäure und ihren Salzen auf.
Formuliere eine Reaktionsgleichung für die zweite Stufe der Protolyse von Phosphorsäure-Molekülen in wässriger Lösung.
Erläutere an diesem Beispiel das Säure-Base-Konzept nach Brønsted und am Beispiel des Dihydrogenphosphat-Ions den Begriff „Ampholyt“ (M 1).
Begründe, dass für den pH-Wert einer wässrigen Phosphorsäurelösung hauptsächlich die erste Protolysestufe ausschlaggebend ist (M 1).
Begründe die Notwendigkeit, die Cola-Probe vorzubereiten (M 2).
Beurteile die genannten Möglichkeiten der Probenvorbereitung anhand von zwei Aspekten (M 2).
Beschreibe das Prinzip einer Säure-Base-Titration.
Erläutere die pH-Werte in den beiden markierten Punkten A und B in der aufgenommenen Titrationskurve (M 2).
Begründe, weshalb sich zur Bestimmung der Phosphorsäurekonzentration in Cola eine Titration mit Indikator nicht eignet.
Ermittle die Stoffmengenkonzentration der Phosphorsäure in der untersuchten Cola unter der Annahme, dass keine weiteren Säuren in der Probe enthalten sind (M 2).
Überprüfe die Herstellerangabe bezüglich der Masse an zugesetzter Phosphorsäure (M 2).
Beurteile gesundheitliche Gefahren durch Aufnahme von Phosphor in Verbindungen, sollte ein Jugendlicher mit einem Körpergewicht von täglich einen Liter der in Aufgabe 4 untersuchten Cola zu sich nehmen (M 2, M 3).
Hinweis: Sollte die Berechnung in Aufgabe 4 keine Ergebnisse liefern, gehe von Phosphorsäure in einem Liter Cola aus.
M 1: Phosphorsäure
Phosphorsäure ist in einigen Nahrungsmitteln als Lebensmittelzusatzstoff enthalten. Phosphorsäure-Moleküle können stufenweise bis zu drei Protonen in Säure-Base-Reaktionen abgeben. Bei den einzelnen Deprotonierungsstufen bilden sich ausgehend vom Phosphorsäure-Molekül nacheinander das Dihydrogenphosphat-Ion, das Hydrogenphosphat-Ion und das Phosphat-Ion.
M 2: Bestimmung des Gehaltes an Phosphorsäure in Cola
Cola ist ein kohlensäure- und phosphorsäurehaltiges Erfrischungsgetränk. In Cola sind bis zu Phosphorsäure pro Liter zulässig. Ein Hersteller gibt an, dass einem Liter Cola bei der Herstellung
Phosphorsäure zugesetzt werde und der
-Wert
betrage. Im Labor soll die Cola dieses Herstellers auf ihren Phosphorsäure-Gehalt überprüft werden.
Zur Vorbehandlung der Cola werden zwei verschiedene Möglichkeiten vorgeschlagen:
- eine Probe von
Cola in einem großen Gefäß über Nacht stehen lassen,
- Cola längere Zeit am Sieden halten, abkühlen lassen und danach eine Probe von
entnehmen.
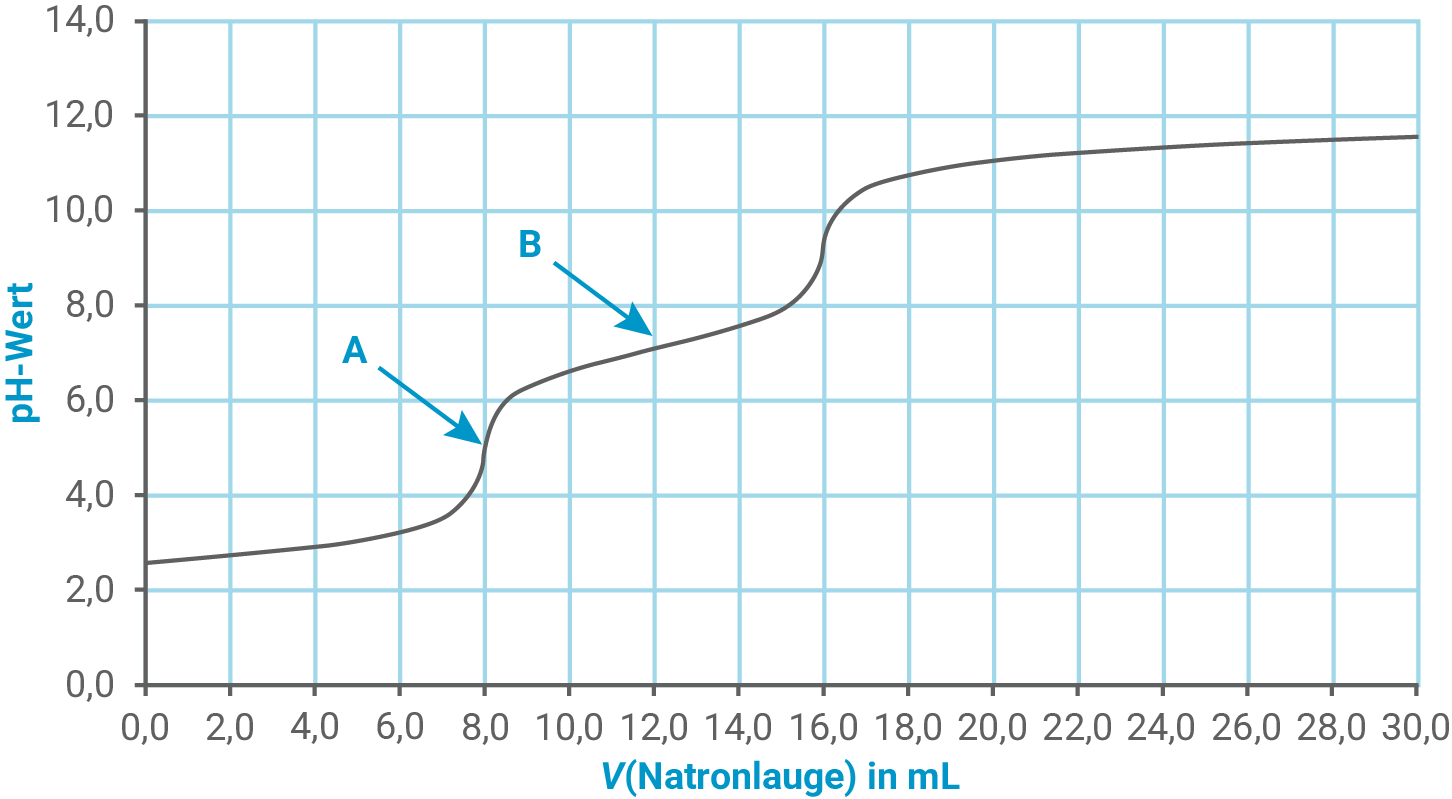
Eine Cola-Probe wird vorbehandelt und danach mit einer Natronlauge-Maßlösung der Stoffmengenkonzentration titriert. Dabei erhält man folgende Titrationskurve (Abbildung 1):
M 3: Phosphorsäure, Phosphate und unsere Gesundheit
Ein vermeidbares Gesundheitsproblem verbirgt sich hinter der verbreiteten Verwendung von Phosphorsäure und deren Salzen als Zusatzstoffe in Nahrungsmitteln. Dieses „freie“ Phosphat wird sehr effektiv vom Körper aufgenommen. Neben der Verwendung der Phosphorsäure in Cola werden in fast allen verarbeiteten Fleischprodukten (wie z. B. Brühwürste und Kochschinken), aber auch in Schmelzkäse und anderen Käsezubereitungen sowie in vielen Fertiggerichten Phosphate eingesetzt, um Wasser zu binden.
Im Jahr 2019 wurde deshalb ein ADI-Wert, bezogen auf die Aufnahme von Phosphor in Verbindungen (z. B. Phosphorsäure, Phosphate, Polyphosphate oder Ähnliches), festgelegt. Der ADI-Wert (acceptable daily intake) ist die geschätzte Menge eines Stoffes in Lebensmitteln pro Kilogramm Körpergewicht, die täglich im Laufe eines Lebens konsumiert werden kann, ohne dass sie ein merkliches Risiko für die Gesundheit birgt. Der ADI-Wert für Phosphor in Verbindungen beträgt pro kg Körpergewicht.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Protolyse des Dihydrogenphosphat-Ions
Erläuterung des Brønsted-Konzepts
Laut dem Säure-Base-Konzept nach Brønsted sind Säuren Protonendonatoren und Basen Protonenakzeptoren
Die Abgabe bzw. Aufnahme von Protonen
führt zur Bildung entsprechender korrespondierender Säure-Base-Paare
bzw.
Darüber hinaus bezeichnet der Begriff „Ampholyt“ eine Substanz, die sowohl als Säure als auch als Base wirken kann. Hierzu zählt beispielsweise das Dihydrogenphosphat-Ion, da es zum einen, wie oben in der Reaktionsgleichung zu sehen, als Säure wirken kann, gleichzeitig durch Aufnahme eines Protons jedoch auch zurück zu Phosphorsäure und somit als Base reagieren kann.
Bedeutung der ersten Protolysestufe für den pH-Wert
Die erste Protolyse hat den höchsten Protolysegrad, da eine mittelstarke Säure ist. Die zweite und dritte Stufe verlaufen deutlich weniger vollständig; die zugehörigen KS-Werte sinken in der Protolysereihe, die zugehörigen pKS-Werte steigen in der Protolysereihe. Schon im zweiten Protolyseschritt nämlich zählt Dihydrogenphosphat schon zu den schwachen Säuren. Daher entstehen die meisten Hydronium-Ionen
durch die erste Stufe, was den pH-Wert hauptsächlich beeinflusst.
Begründung der Notwendigkeit der Probenvorbereitung
Cola enthält neben Phosphorsäure auch Kohlensäure, welche die Phosphorsäuretitration und somit die Bestimmung der Äquivalenzpunkte ohne Vorbehandlung stören würde. Ziel der Vorbereitung ist es also, so viel Kohlensäure wie möglich aus der Cola-Probe als zu verflüchtigen.
Bewertung der beiden vorgeschlagenen Verfahren
- Über-Nacht-Stehenlassen bei Raumtemperatur
Dies ist das schonendere Verfahren mit einfacherer Handhabung. Dafür erfolgt die Entfernung vonnur unvollständig, da nur passive Entgasung stattfindet.
- Längeres Sieden, danach Abkühlen
Hierbei wirdeffektiv vollständig ausgetrieben, das Verfahren ist dafür jedoch aufwendiger und man muss eher darauf achten, dass nicht die gesamte Probe verdampft.
Hinweis: Zur Erreichung der vollen Punktzahl ist auch eine Wahl anderer Aspekte, sofern sinnvoll, zur Beurteilung möglich.
Prinzip der Säure-Base-Titration
Das Ziel der Säure-Base-Titration ist es, die Konzentration einer Säure (bzw. einer Base) durch Messung des verbrauchten Volumens der Maßlösung zu bestimmen.
Die Säure (bzw. Base) unbekannter Konzentration wird hierbei so lange mit einer starken Base (bzw. Säure) mit bekannter Konzentration, der sogenannten Maßlösung, versetzt, bis der Äquivalenzpunkt erreicht wurde. Dieser Punkt, an dem die zugegebenen Hydroxid- bzw. Oxonium-Ionen stöchiometrisch mit den Teilchen der zu bestimmenden Lösung reagieren, lässt sich durch Indikatoren oder pH-Elektroden anzeigen.
Analyse der markierten Punkte A und B in der Titrationskurve
In der Titrationskurve markiert Punkt A den ersten Äquivalenzpunkt, an dem die erste Protolyse von abgeschlossen (bzw. der erste Protolyseschritt vollständig neutralisiert) ist und
als Produkt vorliegt; der pH-Wert liegt dabei im schwach sauren Bereich bei ca. 5.
Punkt B liegt nicht am zweiten Äquivalenzpunkt, sondern auf dem Pufferpunkt (auch Halbäquivalenzpunkt) der zweiten Protolyse, wo und
in gleicher Konzentration vorliegen; hier entspricht der pH-Wert dem pKS-Wert von Dihydrogenphosphat (ca. 7,2).
Warum sich ein Indikator nicht eignet
Da Phosphorsäure dreiprotonig ist, treten mehrere Äquivalenzpunkte auf, deren pH-Sprünge vergleichsweise flach ausfallen und sich nicht eindeutig mit einem einzigen Indikator erfassen lassen. Hinzu kommt, dass die in Cola enthaltenen Farbstoffe den Farbumschlag zusätzlich erschweren. Daher eignet sich zur genauen Bestimmung der Äquivalenzpunkte keine Indikatorlösung, sondern eine pH-Messung mit Elektrode.
Bestimmung der Phosphorsäurekonzentration in Cola
Der erste Äquivalenzpunkt lässt sich in der Titrationskurve leicht ablesen, mit einer verbrauchten Maßlösung von . Hier liegt eine 1:1-Stöchiometrie zwischen verbrauchter Maßlösung und Probelösung
vor und die gesuchte Phosphorsäurekonzentration lässt sich einfach wie folgt berechnen:
Gegeben
Berechnung
Für die Stoffmenge an Phosphorsäure der Cola Probelösung gilt
Mit dem Volumen der Probelösung bedeutet das final für die Konzentration
Überprüfung der Herstellerangabe
Mithilfe der berechneten Konzentration lässt sich über die Molmasse die enthaltene Masse an Phosphorsäure in Cola bestimmen:
Dieser berechnete Wert an Phosphorsäure beträgt mehr als das doppelte vom Wert laut Herstellerangaben Nichtsdestotrotz liegt dieser Wert weiterhin unter dem erlaubten Grenzwert von
und ist somit rechtlich zulässig.
Beurteilung der gesundheitlichen Gefahr durch Trinken von Cola
Ein Jugendlicher mit einem Körpergewicht von kann laut ADI-Wert täglich
Phosphor aufnehmen. Mit
pro Liter Cola liegt man bei einem Konsum von einem Liter pro Tag darunter und hat damit nicht mit gesundheitlichen Gefahren aufgrund der Aufnahme von Phosphor durch Cola zu rechnen.
Jedoch ist hierbei festzuhalten, dass sich diese Betrachtung lediglich auf den Inhaltsstoff Phosphorsäure bezieht und durchaus eine gesundheitliche Gefahr eines solchen täglichen Konsums durch andere Inhaltsstoffe, zum Beispiel des Zuckers, entstehen kann.