Aufgabe 1 – Biodiesel
Biodiesel ist ein Biokraftstoff, der als Alternative zu fossilem Dieselkraftstoff entwickelt wurde. Zur Herstellung von Biodiesel werden pflanzliche Öle, z. B. Rapsöl, mit Methanol umgesetzt.
Gib den systematischen Namen (nach IUPAC) von Glycerin an (M 1).
Beurteile die Löslichkeit von Glycerin in Wasser (M 1).
Formuliere das Massenwirkungsgesetz für die Gleichgewichtsreaktion (M 1).
Berechne ausgehend von den gegebenen Informationen die Gleichgewichtskonstante (M 1, M 2).
Hinweis: Für die Berechnung können in diesem Fall Stoffmengen anstelle der Stoffmengenkonzentrationen verwendet werden.
Gib an, welche Information über die Lage eines chemischen Gleichgewichts aus dem Zahlenwert der zugehörigen Gleichgewichtskonstante abgeleitet werden kann.
Erkläre die Auswirkung der Zugabe von weiterem Methanol auf die Ausbeute an Biodiesel (M 1, M 2).
Gib die Funktion von Natriummethanolat an, und begründe, dass es keinen Einfluss auf die Gleichgewichtskonzentrationen der Reaktionsteilnehmer hat (M 2).
Gib an, welche Produkte in Tank 1 und in Tank 2 vorliegen und welches der Produkte mit Rapsöl verunreinigt ist (M 2).
Berechne die Wärmemenge Q1, die im beschriebenen Experiment vom Wasser aufgenommen wird (M 3).
Ermittle die Wärmemenge Q2, die im beschriebenen Experiment laut Hersteller abgegeben wird (M 3).
Erkläre die stark unterschiedlichen Beträge von Q1 und Q2 anhand von drei Aspekten (M 3).
Berechne den Brennwert von fossilem Dieselkraftstoff (M 4).
Bewerte die Nachhaltigkeit von fossilem Diesel und von Biodiesel anhand von drei Aspekten (M 3, M 4, M 5).
Material M 1: Vom Rapsöl zum Biodiesel
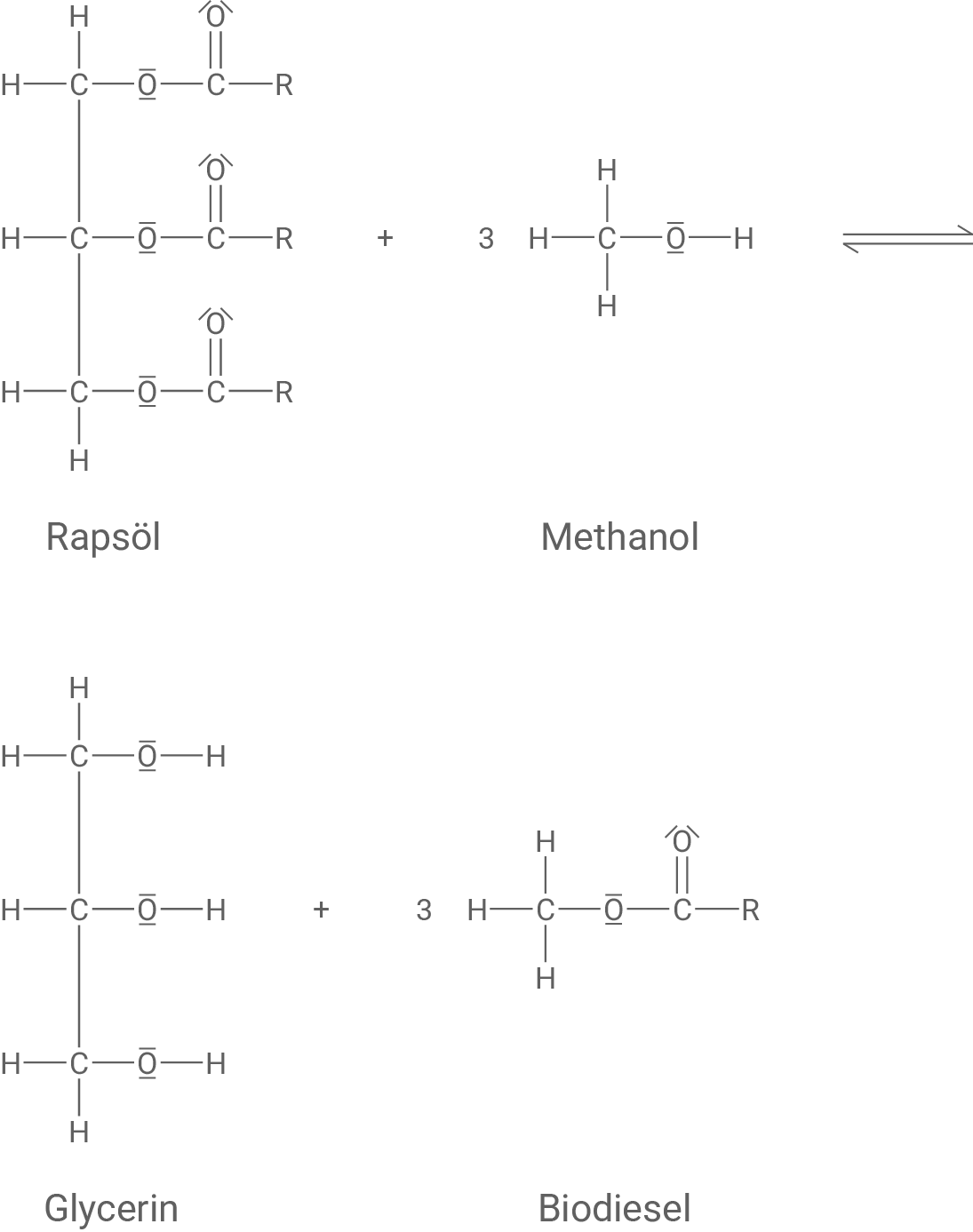
Zur Herstellung von Biodiesel wird Rapsöl mit Methanol umgesetzt. Dabei stellt sich ein chemisches Gleichgewicht ein (Abbildung 1). Zur Vereinfachung wird hier davon ausgegangen, dass die langkettigen Fettsäurereste (R) in den Rapsöl-Molekülen identisch sind.
Material M 2: Industrielle Herstellung von Biodiesel
Die industrielle Herstellung von Biodiesel verläuft in mehreren Schritten. Der Gesamtprozess kann durch ein Fließdiagramm dargestellt werden (Abbildung 2).
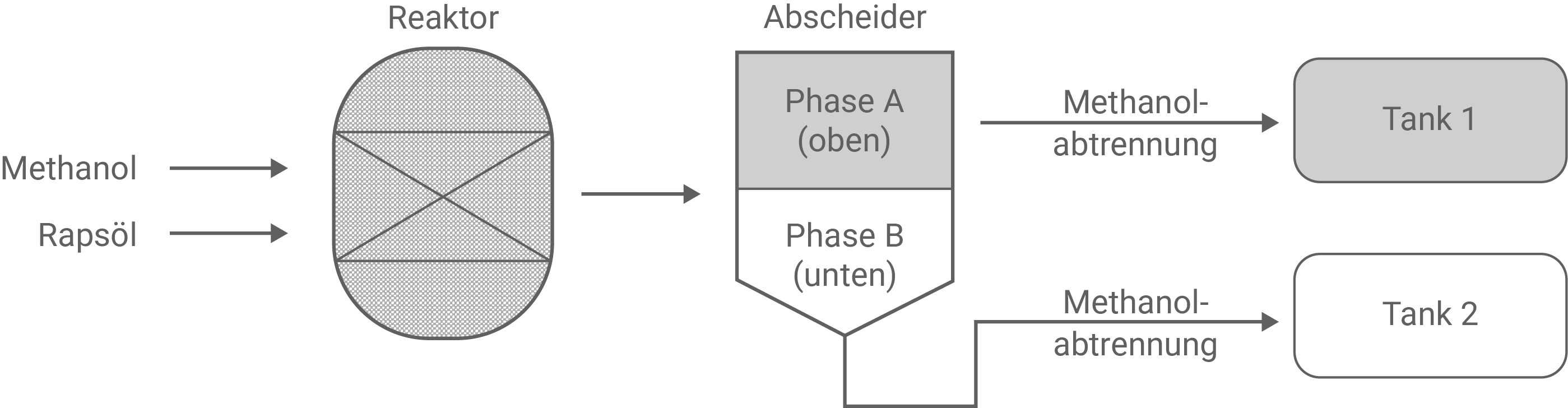
Folgende chemische Aspekte sind dabei relevant:
- Rapsöl und Methanol werden in einem beheizten Reaktor zur Reaktion gebracht. Es bildet sich ein Gemisch aus Rapsöl, Methanol, Glycerin und Biodiesel, das mehrere Stunden lang bei Temperaturen zwischen
und
gerührt wird.
- Nach Einstellung eines chemischen Gleichgewichts wird weiteres Methanol zugegeben. Insgesamt wird die doppelte Stoffmenge an Methanol eingesetzt, die für einen vollständigen Umsatz erforderlich wäre. Auf diese Weise werden bis zu
des eingesetzten Rapsöls umgesetzt. Wenn z. B.
Rapsöl mit
Methanol zur Reaktion gebracht wird, bleiben nach Einstellung des Gleichgewichts nur
Rapsöl im Reaktionsgemisch.
- Damit sich das chemische Gleichgewicht schnell genug einstellt, wird dem Reaktionsgemisch Natriummethanolat
zugesetzt. Das Natriummethanolat nimmt an der Reaktion teil, geht aber unverändert aus ihr hervor.
- Das Reaktionsgemisch wird nach dem Abkühlen in einen Abscheider geleitet (Abbildung 2). Entsprechend der Löslichkeitsverhältnisse und der Dichten der Reaktionsteilnehmer (Tabelle 1) teilt es sich in zwei Phasen A und B auf.
Tabelle 1: Dichten der Reaktions-
teilnehmerStoff Dichte in
beiRapsöl Methanol Glycerin Biodiesel - Nach der Methanolabtrennung erhält man zwei Produkte, die in Tanks abgefüllt werden. Eines der beiden Produkte ist geringfügig mit nicht umgesetztem Rapsöl verunreinigt.
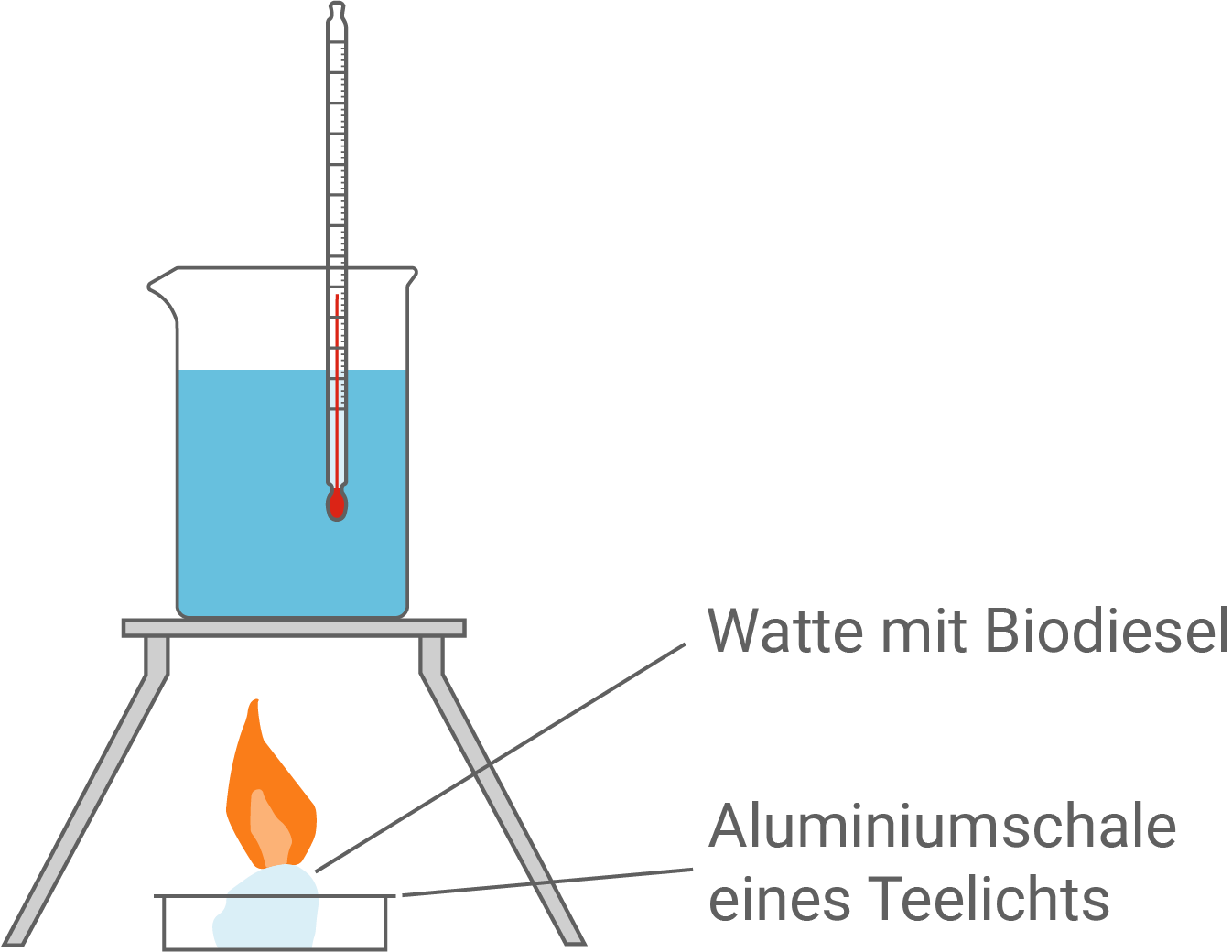
Material M 3: Kalorimetrie mit Biodiesel
Dazu wird
Die Wassertemperatur steigt von
Material M 4: Fossiler Dieselkraftstoff
bildungsenthalpien
Material M 5: Nachhaltigkeit
Im Zusammenhang mit der Diskussion über zukunftsfähige Antriebssysteme im Individualverkehr wird häufig über den Begriff der Nachhaltigkeit gesprochen.
Unter Nachhaltigkeit versteht man eine Zukunftsentwicklung, die die Bedürfnisse der Gegenwart so befriedigt, dass die Möglichkeiten zukünftiger Generationen nicht eingeschränkt werden.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Systematischer Name von Glycerin
Propan-1,2,3-triol
Beurteilung der Wasserlöslichkeit von Glycerin
Eine gute Löslichkeit setzt voraus, dass die Teilchen der beteiligten Stoffe miteinander starke Wechselwirkungen ausbilden können. Da Glycerin-Moleküle jeweils drei polare Hydroxy-Gruppen aufweisen, können sie Wasserstoffbrücken mit Wasser-Molekülen ausbilden. Somit ist Glycerin gut in Wasser löslich.
Formulierung des Massenwirkungsgesetzes
Berechnung der Gleichgewichtskonstanten
Hinweis: Für die Berechnung können in diesem Fall Stoffmengen anstelle der Stoffmengenkonzentrationen verwendet werden.
Laut M 2 werden bis zu des Rapsöls umgesetzt, bei einer eingesetzten Stoffmenge von
Rapsöl verbleiben also lediglich
nach Einstellung des chemischen Gleichgewichts im Reaktionsgemisch. Dies bedeutet, dass
Glycerin entstehen.
Pro Rapsöl-Molekül entstehen drei Biodiesel-Moleküle, d. h. die Stoffmenge an gebildetem Biodiesel beträgt:
Aussage über Lage des chemischen Gleichgewichts
Wenn der Zahlenwert der Gleichgewichtskonstante größer als
ist, liegt das chemische Gleichgewicht auf der Seite der Produkte. Wenn der Zahlenwert kleiner als
ist, dann liegt das chemische Gleichgewicht auf der Seite der Edukte.
Erklärung der Auswirkung einer Konzentrationserhöhung
Nach dem Prinzip von Le Chatelier bewirkt eine Erhöhung der Konzentration eines Edukts die Erhöhung der Konzentration der Produkte, da das System diesem Zwang ausweicht. Bei diesem chemischen Gleichgewicht bewirkt die Zugabe von weiterem Methanol also eine höhere Ausbeute an Biodiesel.
Funktion von Natriummethanolat
Laut M 2 beschleunigt Natriummethanolat die Einstellung des chemischen Gleichgewichts bei der Umsetzung von Rapsöl mit Methanol zu Biodiesel, geht jedoch unverändert aus der Reaktion hervor. Es fungiert hier also als Katalysator, der zwar die Reaktionsrate der Hin- und Rückreaktion gleichermaßen erhöht, aber keinen Einfluss auf die Lage des chemischen Gleichgewichts hat.
Angabe der Stoffe in den Tanks
Tank 1: Biodiesel (verunreinigt mit Rapsöl)
Tank 2: Glycerin
Es entstehen zwei Phasen, da sich das hydrophile Glycerin nicht gut mit dem hydrophoben Rapsöl und Biodiesel vermischen kann. Da Glycerin laut M 2 eine höhere Dichte als Rapsöl und Biodiesel hat, sinkt es im Abscheider in die untere Phase B ab. Rapsöl und Biodiesel haben ähnliche Dichten und bilden die obere Phase A.
Berechnung der Wärmemenge Q1
Die spezifische Wärmekapazität von Wasser beträgt:
Ermittlung der Wärmemenge Q2
Laut M 3 beträgt der Brennwert des Biodiesels:
Erklärung der Differenz
Bei diesem einfachen Versuchsaufbau wird ein Großteil der abgegebenen Wärme nicht auf das Wasser übertragen.
Dazu kommt bei der angegebenen Durchführung, dass bei rußender Flamme keine vollständige Verbrennung erfolgt.
Das Wasser, das sich bei der Verbrennung des organischen Stoffes bildet, liegt gasförmig als Wasserdampf vor, d. h. die in der Brennwertangabe des Herstellers erfasste Kondensationsenergie wird hier nicht erfasst.
Berechnung des Brennwerts von Dieselkraftstoff
Bei der Verbrennung eines Undecan-Moleküls entstehen elf Kohlenstoffdioxid-Moleküle und zwölf Wasser-Moleküle. Mit den gegebenen Standardbildungsenthalpien
in M 4 lässt sich die Reaktionsenthalpie
für
Undecan berechnen:
Bewertung der Nachhaltigkeit
Hier können verschiedene Aspekte betrachtet werden. Grundsätzlich sind nachwachsende Brennstoffe wie Biodiesel nachhaltiger als fossiler Dieselkraftstoff, weil sie auch zukünftigen Generationen zur Verfügung stehen. Zwar hat herkömmlicher Dieselkraftstoff einen leicht höheren Brennwert im Vergleich zu Biodiesel, gleichzeitig aber auch höhere Treibhausgasemissionen. Beim Anbau der für Biodiesel benötigten Pflanzen (z. B. Raps) wird Kohlenstoffdioxid zum Teil wieder gebunden, wodurch die CO2-Bilanz von Biodiesel besser ausfällt. Allerdings benötigt der Anbau dieser Pflanzen große landwirtschaftliche Flächen, die folglich nicht für andere Zwecke genutzt werden können.
Insgesamt betrachtet stellt Biodiesel jedoch die nachhaltigere Option dar.