Aufgabe 4 – Gewinnung von Reinkupfer
Kupfer ist ein vielfältig einsetzbares Metall, das aus natürlich vorkommendem Kupfererz gewonnen wird. Insbesondere für eine Verwendung in der Elektroindustrie ist so genanntes Reinkupfer mit einem besonders hohen Reinheitsgrad erforderlich.
Stelle die Reaktionsgleichungen für Reaktionen 1 und 2 auf (M 1).
Begründe mit Hilfe von Oxidationszahlen, welche Atome bei Reaktion 2 oxidiert und welche reduziert werden (M 1).
Stelle eine Reaktionsgleichung für die Gewinnung von Kupfer aus „Zementwasser“ auf (M 1, M 2).
Erkläre mit Hilfe von Standardpotenzialen, dass diese chemische Reaktion freiwillig abläuft.
Erkläre die Vorgänge sowie die Beobachtungen im Verlauf des Schulversuchs auf Teilchenebene (M 3).
Begründe, dass eine Überschreitung der angelegten Spannung zu metallischen Verunreinigungen des Reinkupfers führen kann (M 3).
Ermittle die zu erwartende Massenzunahme der Reinkupfer-Elektrode im Verlauf der Elektrolyse (M 3).
Beurteile, ob die Vermutungen der drei Schüler (A – C) jeweils plausibel sind (M 3, M 4).
Hinweis: Sulfat-Ionen nehmen nicht am Elektrodenprozess teil.
Beschreibe ein experimentelles Vorgehen zur Überprüfung der Vermutung von Schüler A.
Material M 1: Chemische Verarbeitung von Kupfererz durch Bioleaching
Bei der chemischen Verarbeitung von Kupfererz (vereinfacht: Kupfer(II)-sulfid, CuS) zu elementarem Kupfer gewinnt das sogenannte „Bioleaching“ (to leach: auswaschen) zunehmend an Bedeutung. Ziel dieses Verfahrens ist das „Auswaschen“ von Cu2+-Ionen aus dem wasserunlöslichen Erz unter Beteiligung von Mikroorganismen. Dazu wird zerkleinertes kupfererzhaltiges Gestein aufgehäuft und mit einer wässrigen Suspension besprüht, welche unter anderem Fe3+-Ionen sowie spezielle Mikroorganismen enthält. Während die Suspension nach unten sickert, laufen verschiedene Reaktionen ab. Diese lassen sich vereinfacht wie folgt beschreiben:
| Reaktion 1: | Die in der Suspension enthaltenen Fe3+-Ionen reagieren mit den im Kupfererz enthaltenen Sulfid-Ionen, wobei Fe2+-Ionen und Schwefel-Atome entstehen. |
| Reaktion 2: | Schwefel-Atome aus Reaktion 1 reagieren mit Sauerstoff-Molekülen und Wasser-Molekülen zu Sulfat-Ionen (SO42−) und Oxonium-Ionen. |
Material M 2: Gewinnung von Reinkupfer aus „Zementwasser“
Im nächsten Schritt wird dem „Zementwasser“ Eisen zugesetzt, welches mit dem „Zementwasser“ unter Bildung von Kupfer reagiert. Dieses Kupfer enthält noch metallische Verunreinigungen und wird als Rohkupfer bezeichnet. Das Rohkupfer wird in einem weiteren Schritt elektrolytisch zu Reinkupfer verarbeitet (Abb. 1).

Material M 3: Schulversuch zur elektrolytischen Raffination von Rohkupfer
In einem Schulversuch wird das Prinzip der elektrolytischen Raffination von Rohkupfer angewendet. In Abbildung 2 sind die bei der Elektrolyse ablaufenden Vorgänge schematisch dargestellt.
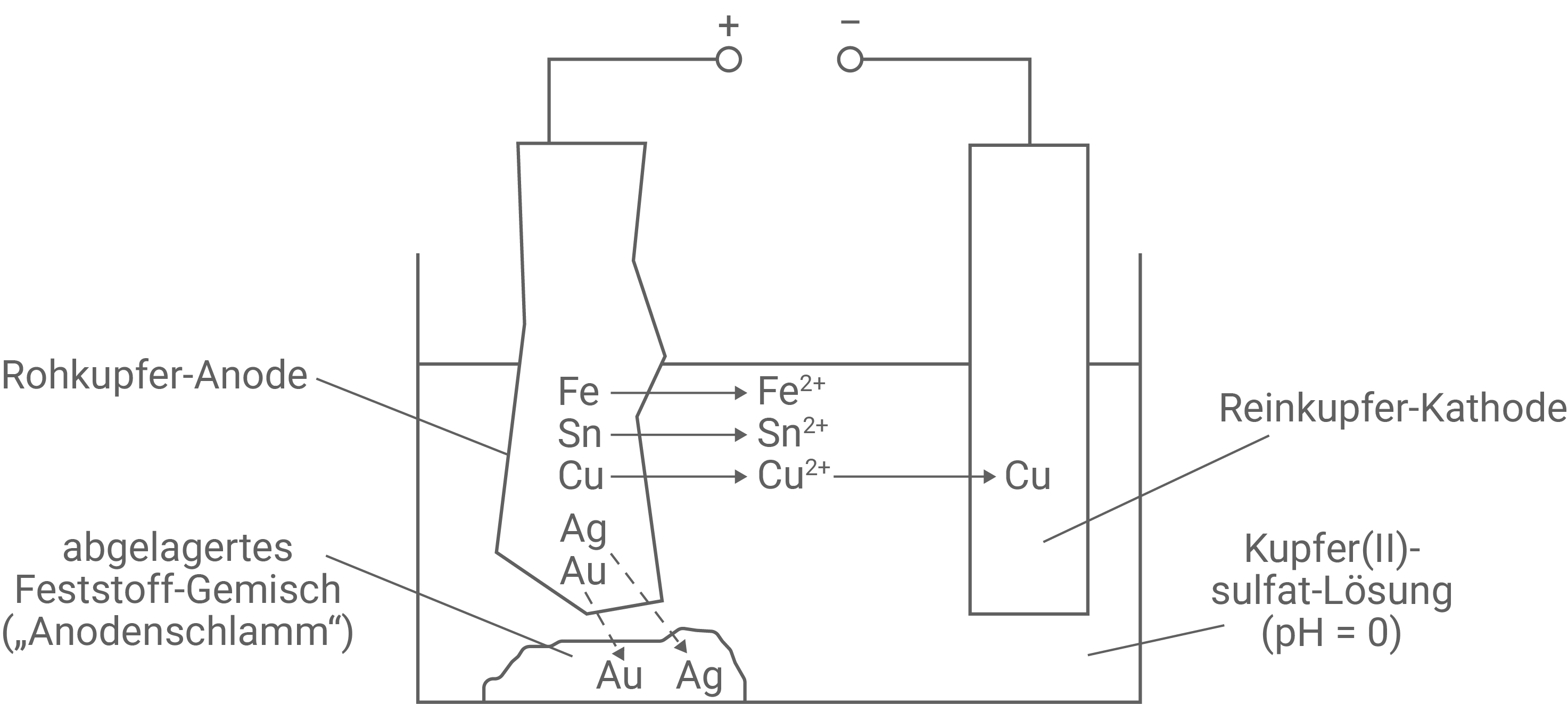
Im Verlauf der Elektrolyse kann beobachtet werden, dass die Rohkupfer-Anode „dünner“ und die Reinkupfer-Kathode „dicker“ wird. Außerdem bildet sich unterhalb der Rohkupfer-Anode der sogenannte „Anodenschlamm“.
Als Elektrolyt dient eine schwefelsaure Kupfer(II)-sulfat-Lösung Es wird für eine Dauer von
bei einer Spannung von
und einer Stromstärke von
unter Standardbedingungen elektrolysiert. Zur Vermeidung von metallischen Verunreinigungen im entstehenden Reinkupfer darf die angelegte Spannung den Wert von
nicht wesentlich überschreiten.
Material M 4: Schulversuch zur Elektrolyse einer Kupfer(II)-sulfat-Lösung
Der Versuchsaufbau aus Abbildung 2 wird abgewandelt, indem anstelle der Rohkupfer-Elektrode eine Kohlenstoff-Elektrode verwendet wird. Bei Anlegen einer Spannung wird an der Kohlenstoff-Elektrode die Bildung eines Gases beobachtet. Schüler äußern dazu folgende Vermutungen:

Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?| Reaktion 1: | |
| Reaktion 2: |
Begründung von Oxidation und Reduktion bei Reaktion 2
Das Schwefel-Atom erhöht seine Oxidationszahl von 0 zu +VI im Sulfat-Anion, es wird durch die Abgabe von sechs Elektronen oxidiert.
Die Oxidationszahl des Sauerstoff-Atoms im Sauerstoff-Molekül sinkt hingegen durch die Aufnahme von zwei Elektronen von 0 zu −II im Sulfat-Anion. Das Sauerstoff-Atom des Wasser-Moleküls ändert seine Oxidationszahl im Vergleich mit dem Oxonium-Ion nicht.
Reaktionsgleichung
Erklärung mithilfe von Standardpotenzialen
Das Redoxpaar weist ein Standardpotenzial
von
auf, wohingegen das Standardpotenzial
von
beträgt. Somit hat das Redoxpaar
ein positiveres Standardpotential als das Redoxpaar
weshalb Kupfer(II)-Ionen durch Eisen-Atome reduziert werden bzw. Eisen-Atome durch Kupfer(II)-Ionen oxidiert werden können.
Erklärung der Vorgänge und Beobachtungen des Schulversuchs
An der Rohkupfer-Anode findet die Oxidation statt, daher gehen dort die Kupfer-Kationen sowie die Ionen von Eisen
und Zinn
in Lösung über, weswegen die Anode dünner wird.
An der Reinkupfer-Kathode hingegen werden Kupfer-Ionen zu elementarem Kupfer reduziert, die Ionen der unedleren Metalle Eisen und Zinn jedoch nicht. Durch die Kupferabscheidung wird die Kathode dicker.
Die Metalle Silber und Gold
welche ebenfalls im Rohkupfer enthalten sind, sind edler als Kupfer. Sie werden daher nicht an der Anode oxidiert. Beim Auflösen der Rohkupfer-Anode lösen sie sich aus dem Metallatomgitter und sinken zu Boden, wo sie sich als Anodenschlamm ablagern.
Begründung der Verunreinigung bei Überschreitung der Spannung
An der Reinkupfer-Kathode werden diejenigen Kationen reduziert, die das größte Bestreben dazu haben. Die Standardpotenziale von Zinn und Eisen
sind negativer als das Standardpotenzial von Kupfer, weshalb sie bei der gegebenen Spannung in Lösung bleiben. Wenn die angelegte Spannung erhöht wird, können an der Reinkupfer-Kathode neben Kupfer(II)-Ionen auch die Ionen der unedleren Metalle reduziert werden, wodurch das sich abscheidende Reinkupfer verunreinigt würde.
Ermittlung der Massenzunahme der Reinkupfer-Elektrode
Die Masse des während der Elektrolyse abgeschiedenen Kupfers entspricht der Massenzunahme an der Reinkupfer-Elektrode. Laut dem Faradayschen Gesetz gilt bei der Elektrolyse: ist hierbei die Ladungsmenge,
die Stoffmenge,
die Ladungszahl bzw. Wertigkeit des Ions, und
die Faraday-Konstante. Die innerhalb einer Zeitspanne
fließende Ladungsmenge
ergibt die elektrische Stromstärke
, daher gilt:
Somit lässt sich die Stoffmenge des abgeschiedenen Kupfers berechnen:
Beurteilung der Vermutungen
Die Vermutung von Schüler A, dass das gebildete Gas Sauerstoff sei, ist plausibel, denn bei der Kohlenstoff-Elektrode handelt es sich um die Anode. Dort kann dementsprechend Wasser zu Sauerstoff oxidiert werden:
Beschreibung des experimentellen Vorgehens
Sauerstoff kann z. B. mithilfe der Glimmspanprobe nachgewiesen werden. Hierfür fängt man das gebildete Gas auf und taucht einen zuvor entzündeten, glühenden Holzspan (Glimmspan) hinein. Flammt der Glimmspan auf, so handelt es sich um Sauerstoff und die Vermutung wurde bestätigt.