HT 3 – Neurobiologie, Genetik
Thema: Ivermectin-Überempfindlichkeit bei Hunden
1.
Beschreibe die Abläufe an einer hemmenden chemischen Synapse und erkläre auf molekularer Ebene die Wirkung von Ivermectin bei Wirbellosen (Material A).
(12 Punkte)
2.
Vergleiche die Verteilung von Ivermectin in den verschiedenen Geweben der Mäuse (Tabelle 1) und leite die Funktion des MDR1-Proteins bei Säugetieren ab (Materialien A und B). Ermittle die Aminosäuresequenz der in Tabelle 2 dargestellten DNA-Sequenzen sowie den Mutationstyp (Materialien C und E). Erläutere die Auswirkungen für das MDR1-Protein und die betroffenen Hunde (Materialien A bis C).
(24 Punkte)
3.
Stelle die wesentlichen Schritte der Polymerase-Kettenreaktion (PCR) dar und erkläre die Funktion der Primer im dargestellten Diagnoseverfahren (Abbildung 1, Materialien C und D). Werte Abbildung 2 im Hinblick auf die Genotypen der untersuchten Hunde aus (Material D). Erläutere mögliche Konsequenzen für die Hundezucht (Materialien A bis D).
(18 Punkte)
Material A: Ivermectin
Hunde können von Parasiten wie Läusen, Milben oder Zecken befallen werden. Zur Bekämpfung dieser Parasiten wird zum Beispiel Ivermectin eingesetzt. Ivermectin ist ein Neurotoxin, das insbesondere auf Wirbellose tödlich wirkt. Es bindet an Glutamat-gesteuerte Chloridionen-Kanäle in der postsynaptischen Membran und öffnet sie dauerhaft. Glutamat-gesteuerte Chloridionen-Kanäle kommen nur bei Wirbellosen vor. Auf Wirbeltiere wirkt Ivermectin weniger toxisch und wird daher auch bei Hunden zur Bekämpfung parasitären Befalls angewendet. Es ist ein fettlöslicher Wirkstoff, der durch die Zellmembran diffundiert. Er reichert sich in Leber und Fettgewebe der behandelten Tiere an und wird von dort langsam freigesetzt. Der Wirkstoff zirkuliert dann in geringer Menge im Blut der behandelten Tiere und wird von den Parasiten aufgenommen.Material B: Überempfindlichkeit gegen Ivermectin
Ivermectin kann bei höheren Konzentrationen auch an GABA-gesteuerte Chloridionen-Kanäle bei Wirbeltieren binden und diese aktivieren. Insbesondere im Zentralnervensystem von Wirbeltieren kann dies zu neurotoxischen Effekten führen. Bei Collies und anderen Hunderassen wurden nach einer Behandlung mit Ivermectin häufig Symptome wie Bewegungsstörungen, Krämpfe und Benommenheit bis hin zu Komazuständen beobachtet. Da nicht alle Hunde einer Rasse gleichermaßen davon betroffen sind, wurden die individuellen Ursachen für diese Überempfindlichkeit analysiert.
Die Ursache dieser Überempfindlichkeit konnte auf eine Veränderung im MDR1-Gen zurückgeführt werden. Um Erkenntnisse über die Funktion von MDR1 bei Säugetieren zu gewinnen, wurden Experimente mit Mäusen durchgeführt. Es handelte sich um Wildtyp-Mäuse und gentechnisch veränderte Mäuse, deren MDR1-Gen ausgeschaltet worden war. Bei beiden Gruppen wurden nach Behandlung mit Ivermectin die Wirkstoff-Konzentrationen in verschiedenen Geweben bestimmt (Tabelle 1).
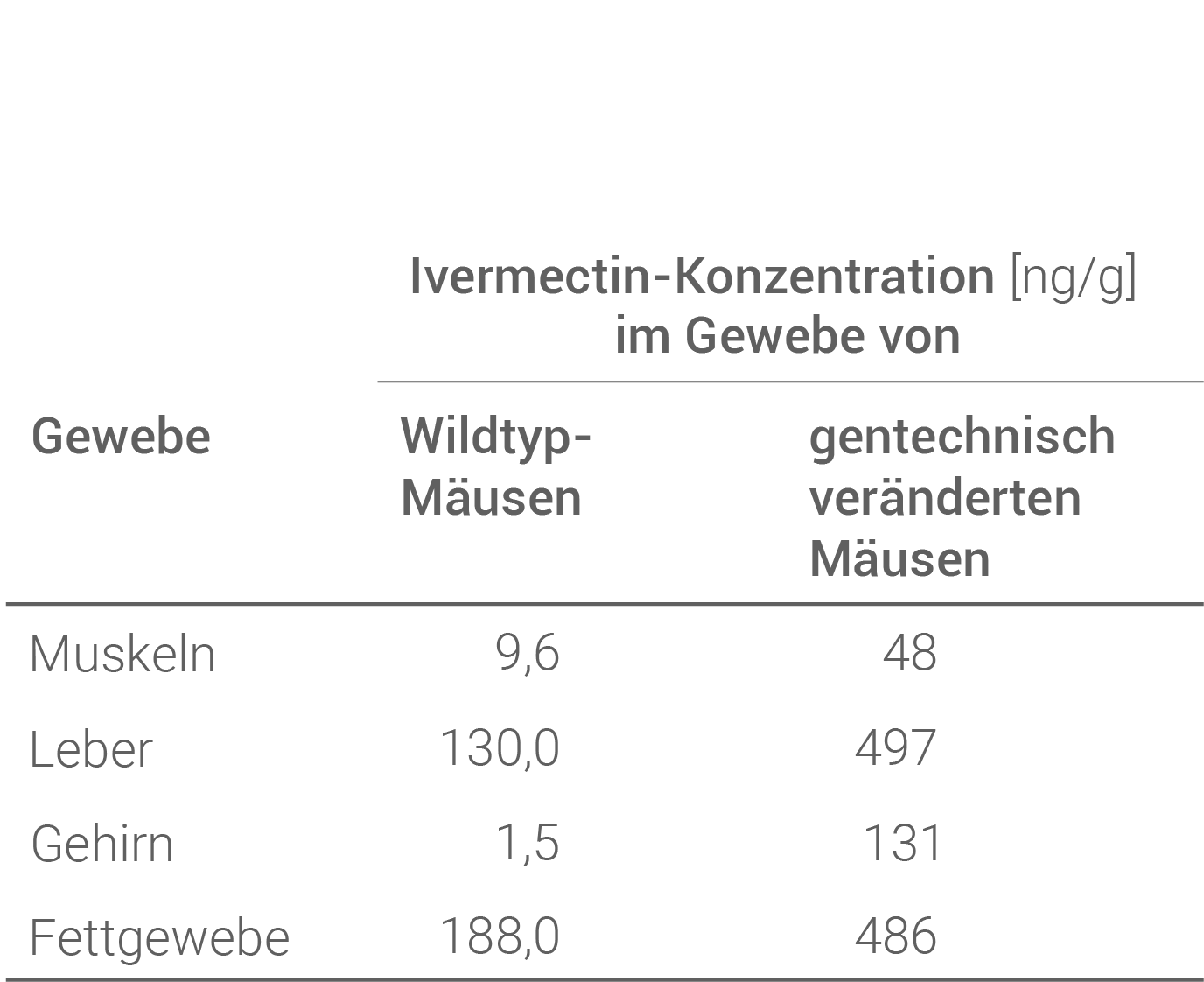
Tab. 1: Ivermectin-Konzentration bei Wildtyp-Mäusen und gentechnisch veränderten Mäusen
Material C: MDR1-Mutation bei Collies
Genetische Analysen des MDR1-Gens bei Collies, die gegenüber Ivermectin überempfindlich sind, zeigten die in Tabelle 2 dargestellten Ergebnisse. Das gesamte MDR1-Protein hat eine Länge von 1281 Aminosäuren.
Tab. 2: Ausschnitt aus dem nicht-codogenen Strang des MDR1-Gens. Die Nummerierung der Tripplets bezieht sich auf das Wildtyp-Allel.

Material D: Nachweis der MDR1-Allele
Die Ivermectin-Überempfindlichkeit wird autosomal-rezessiv vererbt. Mithilfe der Polymerase-Kettenreaktion (PCR) wurden DNA-Proben verschiedener Hunde untersucht. Die jeweiligen Primer-Paare sowie die erwartete Größe der vervielfältigten Fragmente sind in Abbildung 1 dargestellt. Die Ergebnisse einer Gelelektrophorese der PCR-Produkte zeigt Abbildung 2.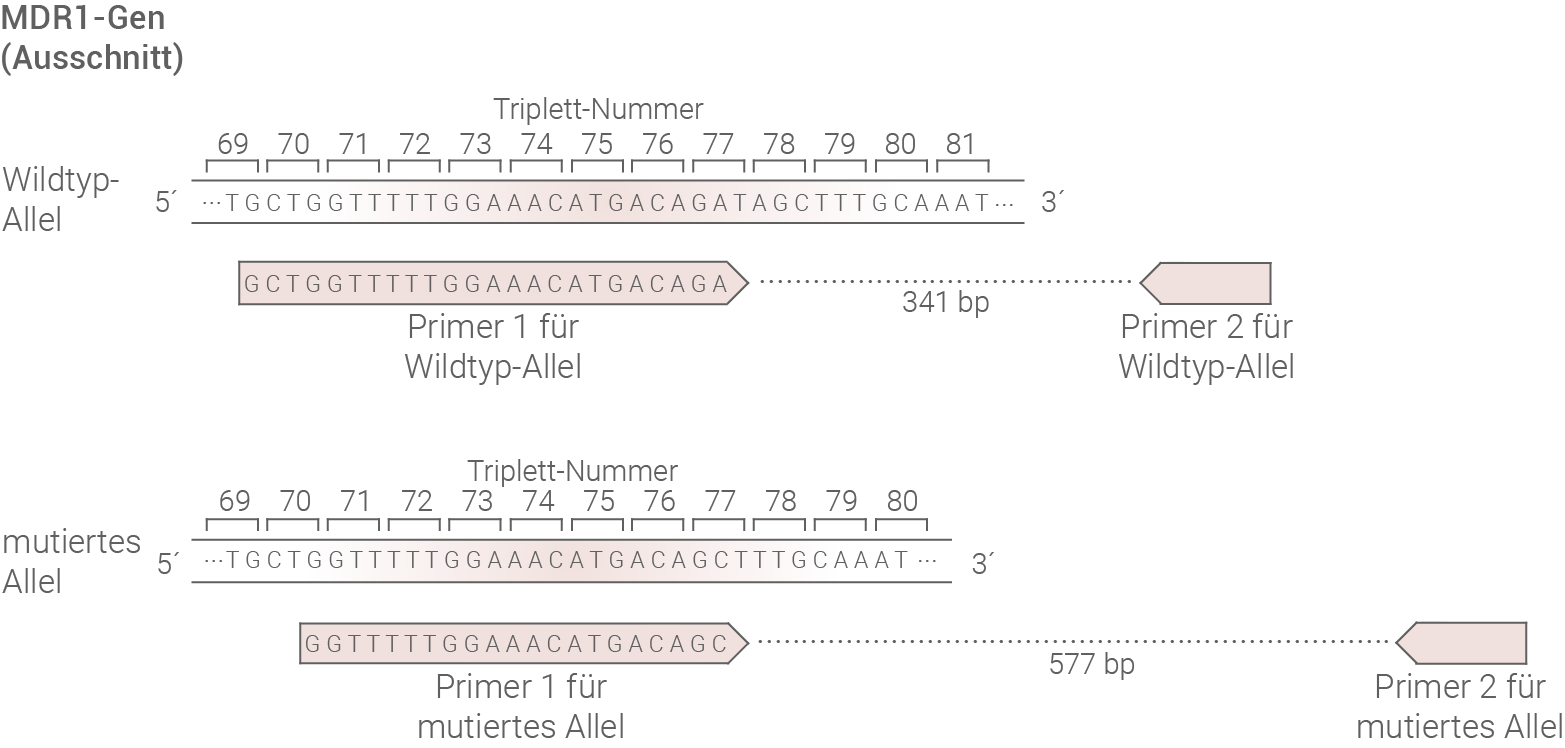
Abb. 1: Schematische Darstellung der Lage der PCR-Primer und der Größe des jeweils vervielfältigten DNA-Fragments. Aus Gründen der Übersichtlichkeit ist der codogene DNA-Strang hier nicht dargestellt.
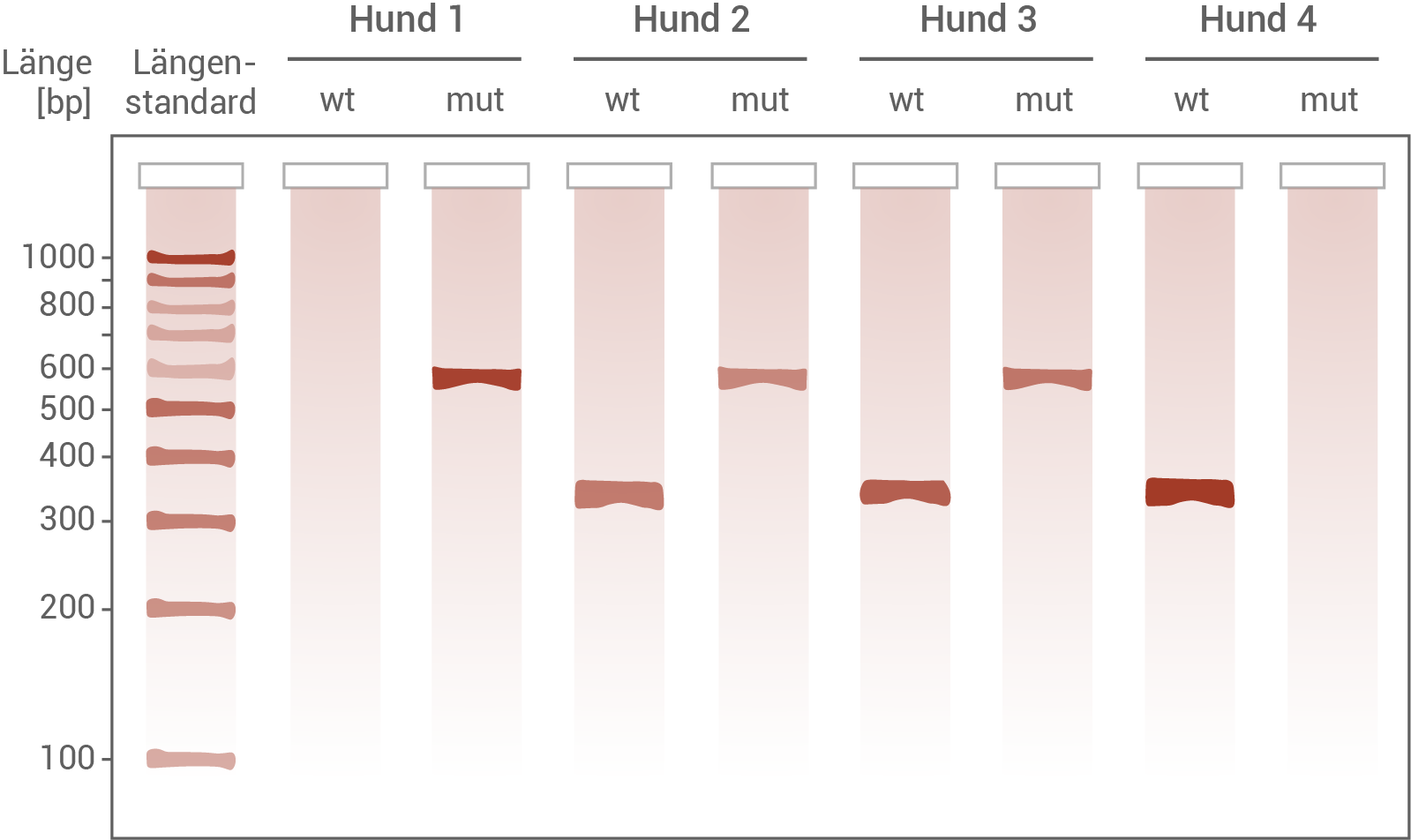
Abb. 2: Ergebnis der Gelelektrophorese von PCR-Produkten verschiedener Hunde mit Primer-Paaren zum Nachweis des Wildtyp-Allels (wt) und des mutierten Allels (mut)
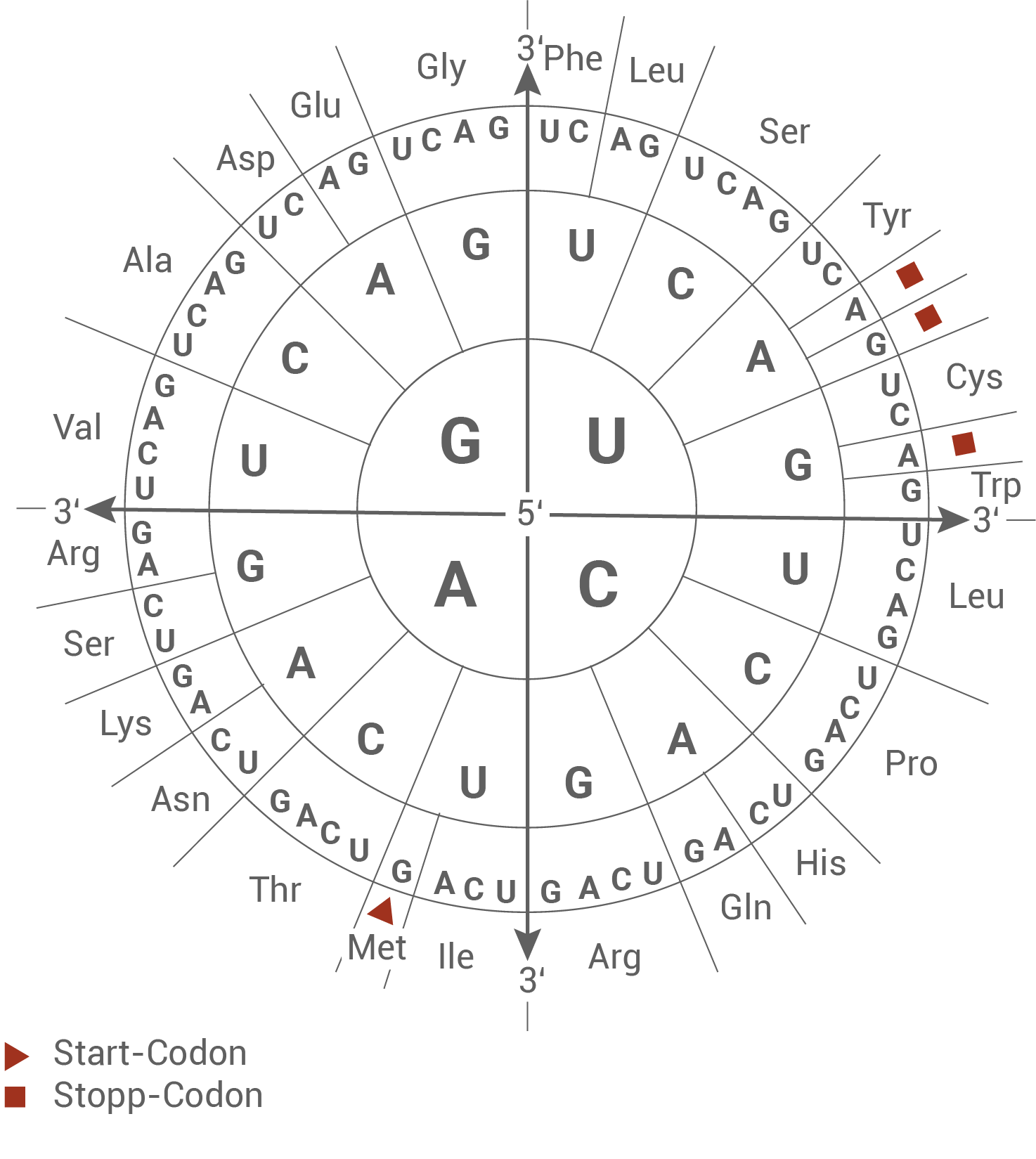
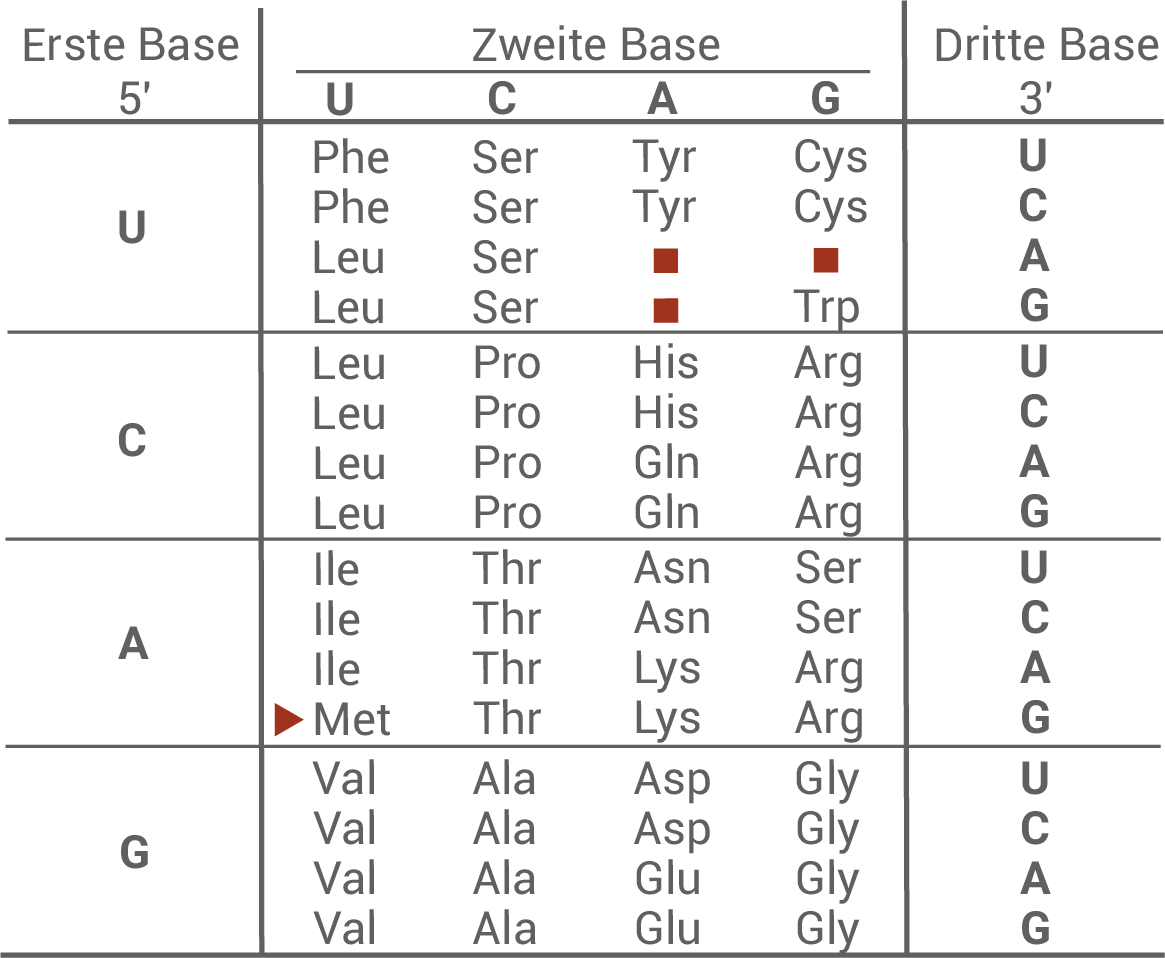
Material E: Codesonne und Tabelle zum genetische Code
| Ala | Alanin |
|---|---|
| Arg | Arginin |
| Asn | Asparagin |
| Asp | Asparaginsäure |
| Cys | Cystein |
| Gln | Glutamin |
| Glu | Glutaminsäure |
| Gly | Glycin |
| His | Histidin |
| Ile | Isoleucin |
| Leu | Leucin |
| Lys | Lysin |
| Met | Methionin |
| Phe | Phenylalanin |
| Pro | Prolin |
| Ser | Serin |
| Thr | Threonin |
| Trp | Tryptophan |
| Tyr | Tyrosin |
| Val | Valin |
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?
1.
Abläufe an hemmenden chemischen Synapsen:
- In der Präsynapse kommt ein Aktionspotenzial an. Es löst dort die Öffnung spannungsabhängiger Calciumionenkanäle aus.
- Der Einstrom von Calciumionen in die Zelle löst das Verschmelzen der mit Transmittermolekülen gefüllten Vesikel mit der präsynaptischen Membran aus.
- Transmitterstoffe werden in den synaptischen Spalt entlassen. Die Transmittermoleküle gelangen durch Diffusion an die Rezeptoren der postsynaptischen Membran und bewirken durch das Andocken ein Öffnen der Chloridionen-Kanäle.
- Durch den Einstrom der negativen Chloridionen in die Zelle wird eine Hyperpolarisation ausgelöst.
- So entsteht ein inhibitorisches postsynaptisches Potenzial (IPSP), welches sich passiv unter Abschwächung ausbreitet.
- Ivermectin besitzt vermutlich eine ähnliche chemische Struktur wie die Neurotransmitter, die bei der Erregungsleitung genutzt werden. Es bindet an die Glutamat-gesteuerten Chloridionenkanäle und wirkt somit analog zu einem Neurotransmitter.
- Werden bei den Wirbellosen Glutamat-gesteuerte Chloridionen-Kanäle in der postsynaptischen Membran dauerhaft geöffnet, so befindet sich die Zelle im Zustand der Hyperpolarisation. Es kann dadurch keine Erregungsweiterleitung mehr stattfinden.
- Das liegt daran, dass im Axonhügel inhibitorische postsynaptische Potenziale mit erregenden Potenzialen verrechnet werden.
- Ein Ausbleiben der Erregungsweiterleitung führt bei den Tieren zu Lähmungen, und kann den Tod hervorrufen.
2.
Vergleich der Verteilung von Ivermectin in den verschiedenen Geweben der Mäuse:
- Bei gentechnisch veränderten Mäusen ist die Konzentration von Ivermectin in allen untersuchten Gewebetypen deutlich höher als in den Geweben der Wildtypmäuse.
- Besonders signifikant ist der Unterschied im Gehirngewebe zwischen den untersuchten Mäusen.
- Im Allgemeinen ist die Konzentration in Leber und Fettgewebe am höchsten.
- Das MDR1-Protein ist im Körper für die Resorption körperfremder Stoffe aus der Zelle ins Blut zuständig.
- Es kommt vor allem in den Blutgefäßen der Blut-Hirn-Schranke vor, wo es das dauerhafte Eindringen körperfremder Stoffe in das Nervengewebe des Gehirns unterbindet. Das ZNS soll dadurch vor gefährlichen Stoffen geschützt werden.
- Ivermectin ist ein lipophiler Stoff. Er ist dadurch in der Lage, durch die Biomembran von Blutgefäßzellen zu diffundieren und in ihr Inneres zu gelangen.
- Dort wird Invermectin von den MDR1-Proteinen gebunden und zurück ins Blut transportiert. So gelangt Invermectin nicht oder nur in geringem Maße in das Gehirn und andere Gewebe.
- Wildtyp-Sequenz: Gly-Asn-Met-Thr-Asp-Ser-Phe-Ala-Asn
- mutiertes Allel: Gly-Asn-Met-Thr-Ala-Leu-Gln-Met
- Das veränderte MDR1-Protein bei Collies weist ab der 77. Triplett-Nummer eine veränderte Aminosäuresequenz auf.
- Beim mutierten MDR1-Allel liegt eine Deletion von vier Nukleotiden vor. Dies verschiebt das Leseraster, und wird dementsprechend als Rasterschubmutation bezeichnet.
- Eine veränderte Aminosäuresequenz führt zu einer veränderten Raumstruktur und damit zu einer eingeschränkten Funktion des Proteins.
- Es besteht zudem die Möglichkeit, dass vorzeitig Stoppcodons eingebaut werden, und die Polypeptidkette verkürzt ist.
- Das mutierte Allel sorgt für die Expression eines veränderten Proteins. Es ist nicht mehr in der Lage, körperfremde Stoffe aus den Zellen von Blutgefäßen zu filtern.
- Von der Überempfindlichkeit gegen Ivermectin sind nur Hunde betroffen, die homozygote Träger des mutierten Allels sind.
- Sie können kein funktionstüchtiges MDR1-Protein ausbilden. Die Resorption körperfremder Stoffe kann bei ihnen nicht stattfinden. Dadurch reichert sich Ivermectin im Hirngewebe der Tiere an.
- Die hohe Konzentration im Hirngewebe kann zu einer Bindung von Ivermectin an GABA-gesteuerte Chloridionen-Kanäle führen. Dies führt zu einer übermäßigen Hemmung der postsynaptischen Zellen.
- Dadurch lassen sich Symptome wie Bewegungsstörungen, Benommenheit und Koma bei Hunden mit einer Überempfindlichkeit erklären.
3.
Wesentliche Schritte der Polymerase-Kettenreaktion:
- Denaturierung: Die Doppelhelix wird bei einer Temperatur von ca. 95 °C in ihre beiden Einzelstränge aufgespalten. Das liegt daran, dass bei dieser Temperatur die Wasserstoffbrücken zwischen den einzelnen Basenpaaren aufgelöst werden.
- Hybridisierung: Hier werden bei 55 bis 60 °C Primer komplementär an die zu vervielfältigenden Abschnitte angelagert.
- Polymerisation: Die sogenannte Taq-Polymerase synthetisiert bei 72 °C ausgehend von dem 3'-Ende des DNA-Primers einen zum Matrizenstrang komplementären DNA-Strang.
- Dieser Zyklus wird so oft wiederholt, bis die gewünschte Menge des zu replizierenden DNA-Abschnittes entstanden ist.
- Verwendet werden zwei unterschiedliche Primerpaare. Ein Paar ist dabei spezifisch für das Wildtyp-Allel, und das andere Paar für das mutierte Allel.
- Die Fragmente, die bei der PCR entstehen sind unterschiedlich lang. Je nachdem, ob das Wildtyp-Allel oder das mutierte Allel vorliegt.
- So können Wildtyp-Allel und mutiertes Allel in zwei PCR-Reaktionen der Proben-DNA eines Hundes detektiert werden.
- Bei Hund 1 ist keine Bande für das Wildtyp-Allel zu erkennen, dafür eine deutliche Bande für das mutierte Allel. Der Hund ist somit homozygot für das mutierte Allel.
- Bei den Hunden 2 und 3 ist je eine Bande für das Wildtyp-Allel und das mutierte Allel zu erkennen. Sie sind somit heterozygot.
- Bei Hund 4 ist eine Bande für das Wildtyp-Allel zu erkennen, aber keine für das mutierte Allel. Somit ist dieser Hund homozygot für das Wildtyp-Allel, und kein Träger des mutierten Allels.
- Bevor Hunderassen, die von der Überempfindlichkeit auf Ivermectin betroffen sind, zur Zucht zugelassen werden, sollte mittels eines PCR-Tests überprüft werden, ob sie Träger des mutierten Allels sind.
- Hunde, die heterozygot betroffen sind, erkranken selbst nicht, haben jedoch eine 50 %ige Wahrscheinlichkeit, das mutierte Allel an ihre Nachkommen weiterzugeben.
- Hunde, die homozygote Träger des mutierten Allels sind, werden das Allel auf jeden Fall an ihre Nachkommen weitergeben.
- Für die Zucht ist es daher wichtig zu wissen, ob ein Tier Träger des mutierten Allels ist.
- Darüber hinaus sollten auch die zukünftigen Besitzer des Hundes darüber informiert werden, ob das Tier Träger des mutierten Allels ist. Sie sollten dann andere Behandlungsmöglichkeiten gegen Parasiten einsetzen.