Aufgabe 2 – Beton – Ein Werkstoff für die Ewigkeit?
Jedes Jahr werden weltweit zwölf Kubikkilometer Beton produziert, genug, um eine 30 cm dicke und über tausend Meter hohe Mauer einmal um den Äquator herum zu bauen. Jedoch scheint dieser Superwerkstoff nicht ewig haltbar und stabil zu sein, sondern kommt im Laufe der Jahre an seine Grenzen.
Begründe das basische Milieu von ausgehärtetem Beton (M 1).
Erkläre die Funktionsweise des Schnelltests zur Feststellung des Fortschritts der Carbonatisierung (M 1, M 2, M 3, M 4).
Formuliere die Reaktionsgleichung für die Carbonatisierung von Beton (M 3).
Nenne das Prinzip von Le Chatelier.
Begründe auf dieser Grundlage den sinkenden pH-Wert bei zunehmender Carbonatisierung des Betons (M 3).
Skizziere ein Übersichtsschema (z. B. ein Fließdiagramm) zu den chemischen Vorgängen, die zum „Sulfattreiben“ führen (M 5).
Erläutere am Beispiel der Reaktion von Schwefelwasserstoff mit Wasser das Säure-Base-Konzept nach Brönsted unter Angabe einer Reaktionsgleichung (M 5).
Berechne die Massenkonzentration an Calciumhydroxid im Filtrat der Aufschlämmung der Betonprobe.
Beurteile darüber den Qualitätszustand des Betonteils (M 6).
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Material 1: Das Aushärten von Beton
Für Beton werden Kies, Sand und das Bindemittel Zement vermengt und anschließend mit Wasser versetzt. Dabei dient das Wasser nicht allein dazu, eine gut verarbeitbare Masse an Beton zu erhalten, sondern ist notwendig für dessen Aushärteprozess durch die sogenannte Hydratation des Zements. Hierbei kommt es zur Bildung von Calciumhydroxid das neben anderen Bestandteilen in dem noch frischen Beton für relativ hohe pH-Werte zwischen 12,5 und 13,5 sorgt.
Material 2: Stahlbeton
Die Zugfestigkeit von Betonbauteilen lässt sich entscheidend verbessern, wenn in die Betonmasse Stahlstäbe oder Stahlgitter (sogenannte Stahlbewehrungen) einbetoniert werden. Dabei wird der Stahl durch das stark basische Milieu der ihn umgebenden Betonmasse vor Korrosion geschützt, indem sich eine Schutzschicht auf dem Stahl ausbildet.


Abb. 1: Bewehrungsstahl vor dem Einbau
Material 3: Carbonatisierung von Beton
Unter Carbonatisierung versteht man die Gleichgewichtsreaktion von gelöstem Calciumhydroxid mit Kohlenstoffdioxid aus der Umgebungsluft zu schwerlöslichem Calciumcarbonat (Kalkstein, und Wasser.
Durch die Kalksteinbildung erhöht sich zwar die Festigkeit des Betons, jedoch ist das stark basische Milieu des Betons nicht mehr gegeben. Der -Wert des angefeuchteten Betons sinkt von
auf unter
Ab einem
-Wert deutlich unter
beginnt der im Beton verbaute Stahl bei eindringender Feuchtigkeit zu rosten. Die Folge davon ist möglicherweise ein Stabilitätsverlust der Konstruktion sowie das Abplatzen von Betonteilen an der Oberfläche.


Abb. 2: Betonabplatzung durch oxidierte Stahlstäbe
Material 4: Schnelltest zur Überprüfung des Fortschrittes der Carbonatisierung
An frischen Betonbruchstellen wird der Fortschritt der Carbonatisierung in der Regel durch Besprühen mit einer Lösung des Säure-Base-Indikators Phenolphthalein sichtbar gemacht. Hierüber lässt sich eine Aussage zum noch vorhandenen Schutz des Baustahles vor Korrosion treffen.
Material 5: Schäden durch „Sulfattreiben“ in Abwasserkanälen
Beim Durchfließen von relativ warmem Haushaltsabwasser durch erdverlegte, kühle Abwasserrohre aus Beton kommt es zur Kondensation von Wasser im oberen Teil der inneren Rohrfläche. Abwasserrohre führen Schwefelwasserstoff-Gas mit, das bei der biologischen Zersetzung von Eiweißen im Haushaltswasser anfällt.
Dieses Gas bildet in Gegenwart bestimmter Schwefelbakterien, dem Kondenswasser und dem Sauerstoff aus der Luft das Reaktionsprodukt Schwefelsäure. Aus dem im Beton enthaltenen Calciumhydroxid wird durch die Reaktion mit Schwefelsäure festes Calciumsulfat gebildet. Dadurch kommt es zu einer Volumenvergrößerung gegenüber dem Calciumhydroxid, wodurch der Beton aufquillt und hiernach Risse und Abplatzungen bekommt (siehe Abb. 3). Dies ist in der Fachwelt als sogenanntes „Sulfattreiben“ bekannt.
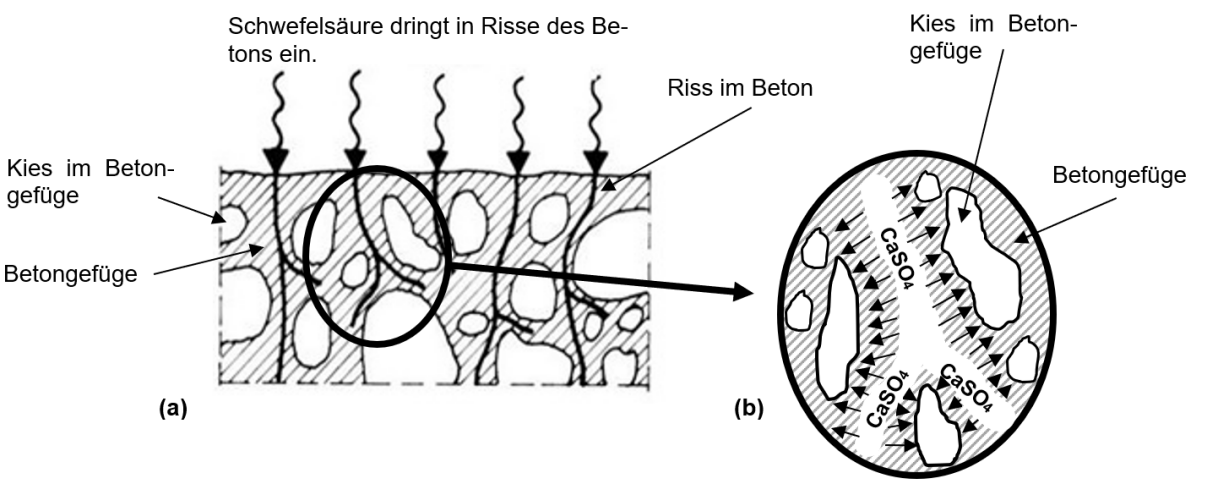
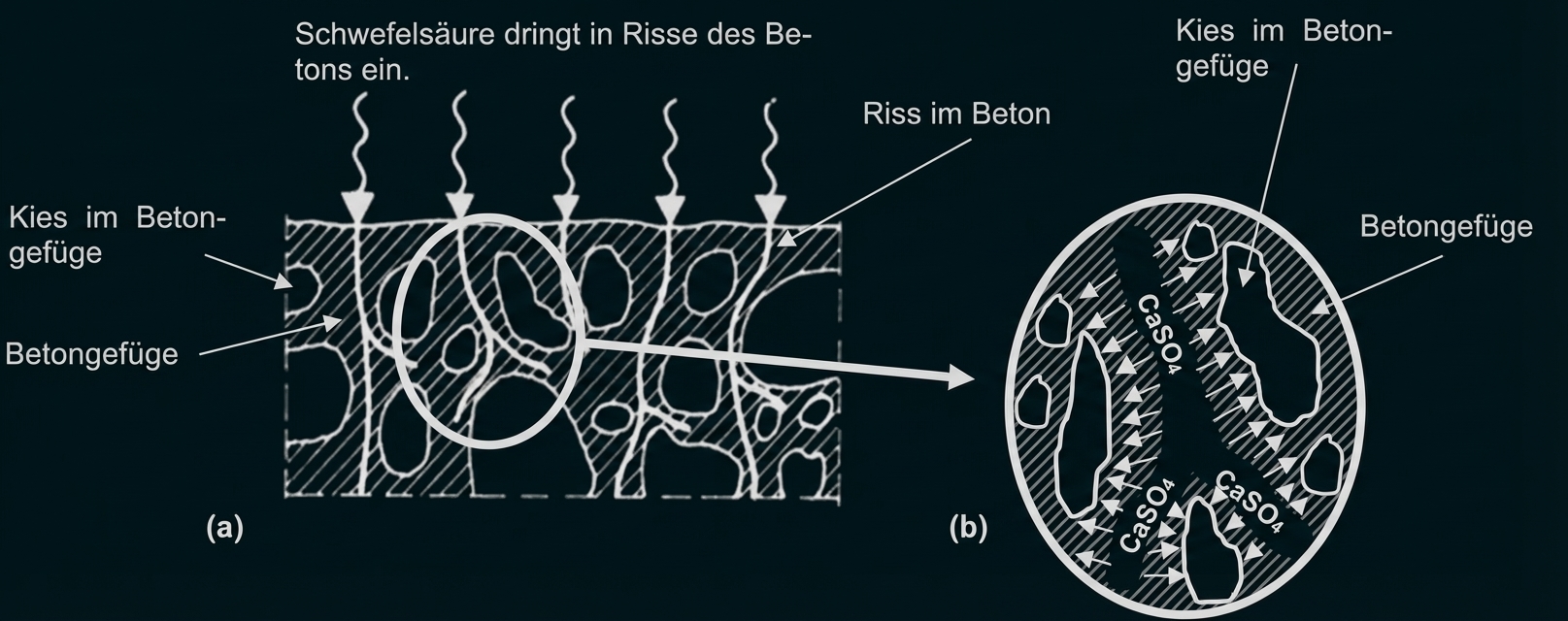
Abb. 3: (a) schematische Abbildung zum Sulfattreiben; (b) vergrößerter Ausschnitt
Material 6: Analyse einer Betonprobe
Bei Kenntnis des Massenanteils an Calciumhydroxid einer Betonprobe kann auf den Zustand des Betons geschlossen werden. Ist der Calciumhydroxid-Anteil infolge der Carbonatisierung zu niedrig, fehlt der Korrosionsschutz für den Baustahl. Dadurch ist die Tragfähigkeit eines Stahlbetonteils nicht mehr dauerhaft gewährleistet. In dem nachfolgenden Diagramm ist eine Referenzgerade abgebildet, die die zum Erhalt des Korrosionsschutzes notwendigen Mindestanteile an Calciumhydroxid im Beton bezogen auf dessen Alter ausweist.
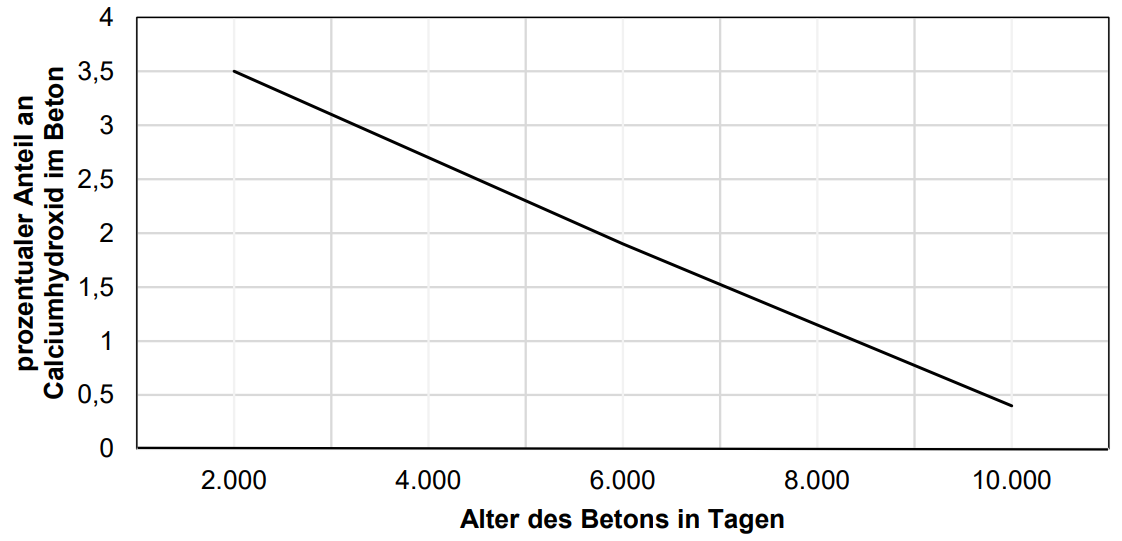
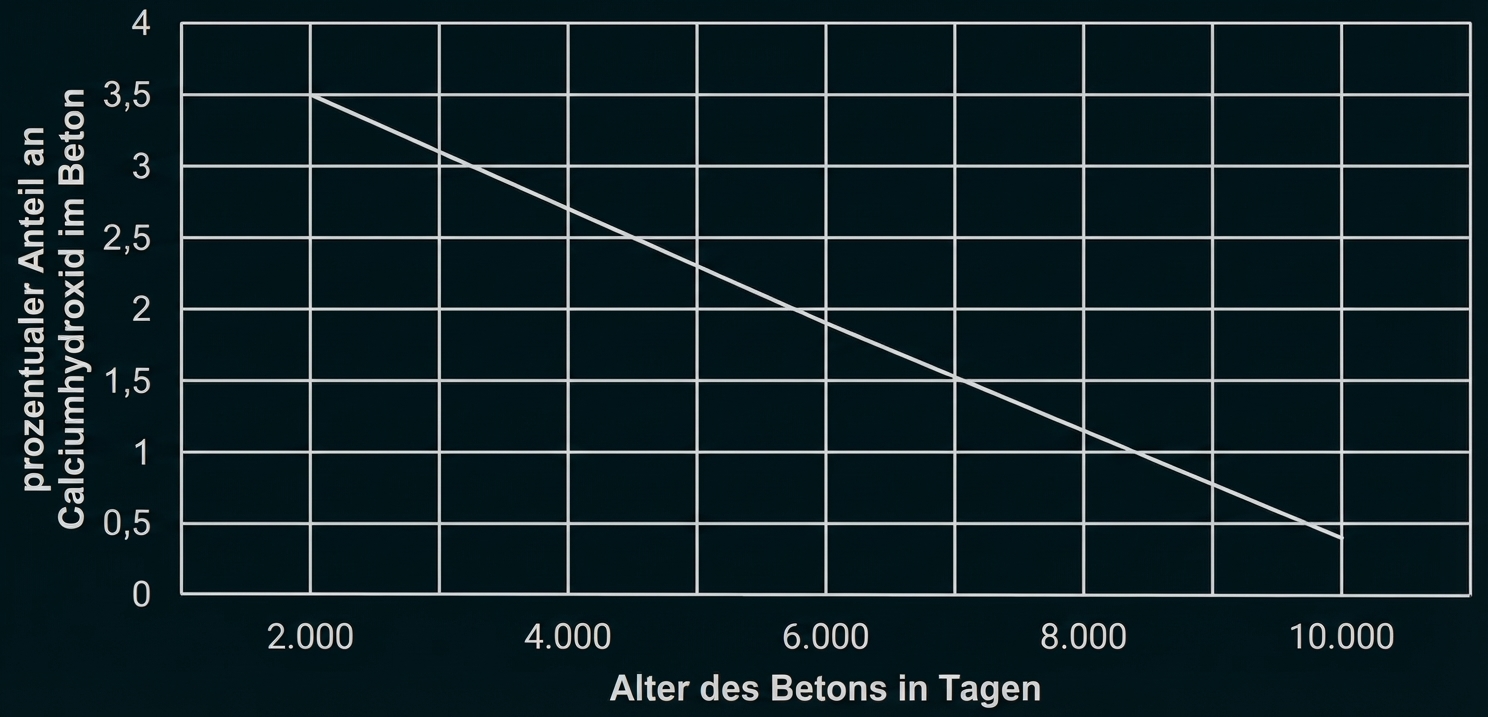
Abb. 4: zeitabhängige Entwicklung des Mindestanteils an Calciumhydroxid in Beton nach der Aushärtezeit
Untersuchung einer Betonprobe:
Von einer 27 Jahre (ca. 10.000 Tage) alten Brücke wurde eine Bohrkernprobe genommen und pulverisiert. Davon wurden 100 g Betonpulver in 1,0 L Wasser aufgeschlämmt.
Diese Aufschlämmung wurde so lange stehen gelassen, bis das gesamte Calciumhydroxid der Probe gelöst war, und anschließend filtriert. Der pH-Wert des Filtrates betrug 12,36.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Begründung des basischen Milieus von Beton
-
Das sich beim Abbindeprozess bildende Calciumhydroxid dissoziiert in dem im Beton enthaltenen Wasser unter Abspaltung von Hydroxid-Ionen, die das basische Milieu bewirken.
Erklärung der Funktionsweise des Schnelltests
-
Ohne Farbumschlag wäre der
-Wert mit höchstens
zu niedrig. Der Stahl im Beton ist nicht mehr vor Korrosion geschützt.
-
Ist eine deutliche Purpurfärbung zu sehen, liegt der
-Wert mindestens bei
was bedeutet, dass der Stahl vor Korrosion geschützt ist.
Formulierung der Reaktionsgleichung zur Carbonatisierung
Nennung des Prinzips von Le Chatelier
Nach dem Prinzip von Le Chatelier weicht ein im Gleichgewicht
befindliches System einem äußeren Zwang so aus, dass der Zwang
minimiert wird.
Begründung des sinkenden pH-Werts
-
Durch die Bildung von schwerlöslichem Calciumcarbonat werden Calcium- und Hydroxid-Ionen aus dem chemischen Gleichgewicht entfernt.
-
Dadurch und durch die Zufuhr von
läuft die Hydroxid-Ionen verbrauchende Reaktion bevorzugt ab, d. h. deren Konzentration wird verringert. Daher nimmt der pH-Wert ab.
Skizze eines Übersichtsschemas zu den chemischen Vorgängen, die zum „Sulfattreiben“ führen
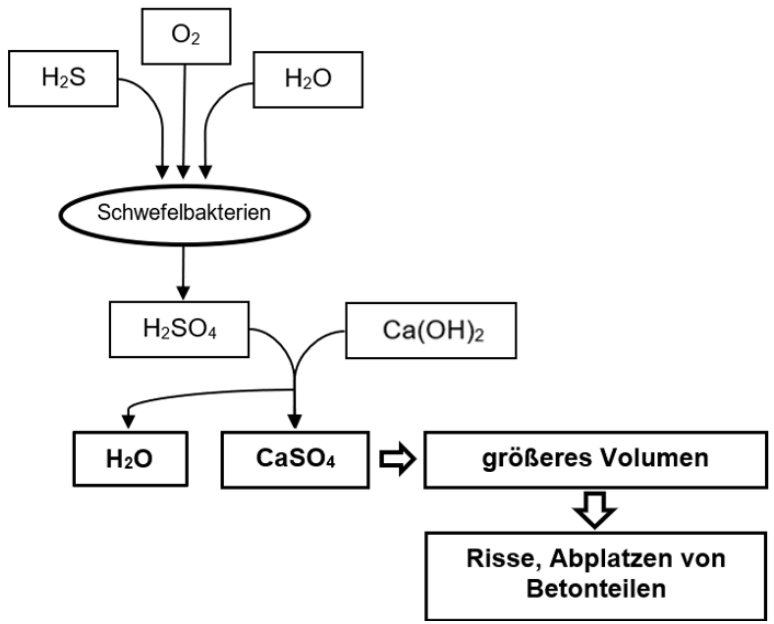
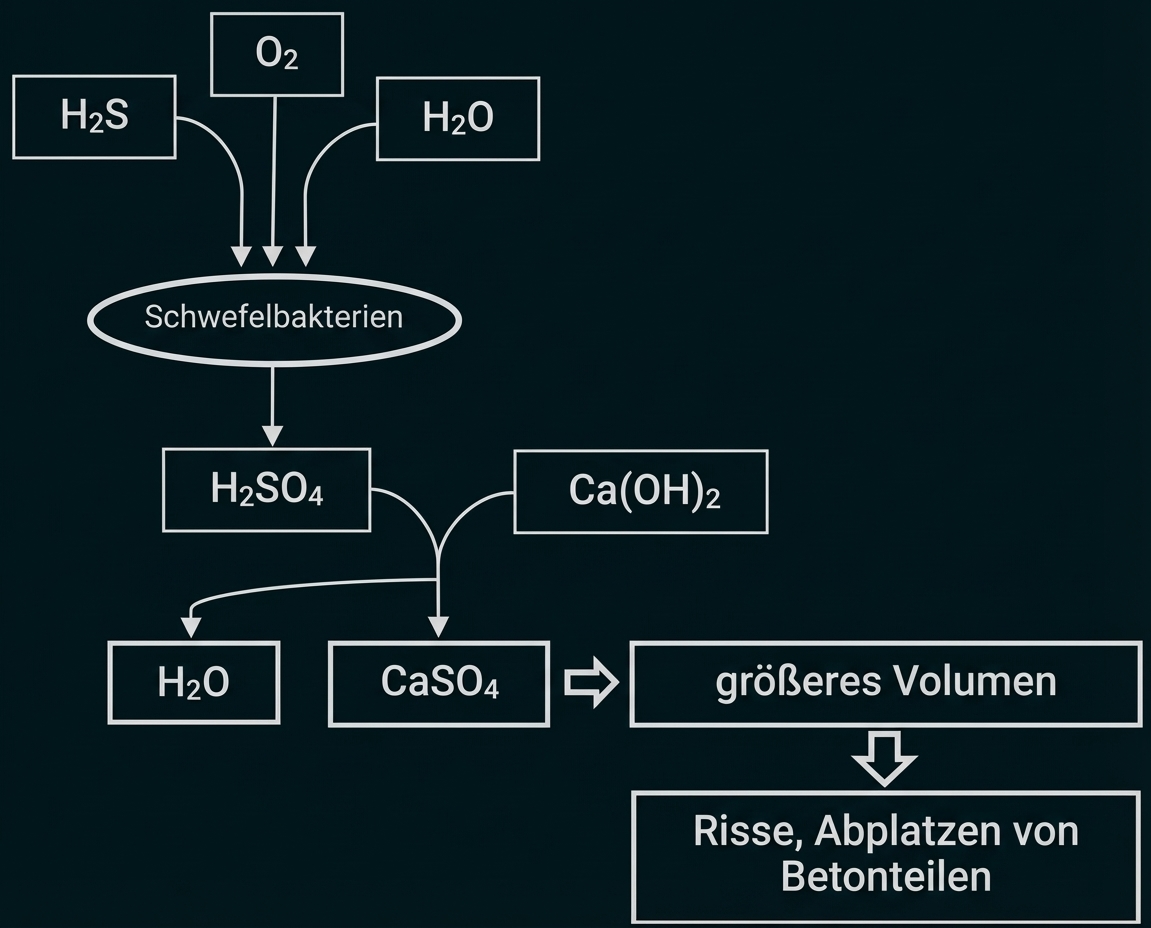
Erläuterung des Säure-Base-Konzepts nach Brönsted
-
Das Schwefelwasserstoff-Molekül ist eine Brönsted-Säure, weil es Protonen abgibt (Protonendonator).
-
Das Wasser-Molekül ist eine Brönsted-Base, weil es Protonen aufnimmt (Protonenakzeptor).
-
Insgesamt handelt es sich um eine Protonenübertragungsreaktion.
Angabe einer Reaktionsgleichung
Berechnung der Massenkonzentration an Calciumhydroxid
Berechnung der Hydroxid-Ionen-Konzentration:
Berechnung der Stoffmengenkonzentration:
Berechnung der Massenkonzentration:
In einem Liter Filtrat sind Calciumhydroxid enthalten, was dem Calciumhydroxid-Gehalt von
des Bohrkerns entspricht. Das entspricht einem prozentualen Anteil von
Beurteilung des Qualitätszustandes des Betonteils
-
Laut Diagramm müsste eine 27 Jahre (10.000 Tage) alte Betonprobe einen Calciumhydroxid-Gehalt von mindestens
aufweisen.
-
Die Mindestanforderung ist damit noch erfüllt.