Aufgabe 3 – Wahlaufgabe
Hinweis: Von den nachfolgenden Aufgabenteilen 3.A und 3.B soll in der Prüfung nur einer bearbeitet werden.
Aufgabe 3.A – Citronensäure und ihre Verbindungen
Citronensäure ist ein natürlicher Bestandteil vieler Früchte und tritt als Stoffwechselprodukt in Organismen auf. Die Säure und ihre Verbindungen werden vielfältig verwendet z. B. als Säuerungsmittel in Lebensmitteln und in Kosmetika.
Begründe anhand des Baus der Moleküle eine der genannten Eigenschaften des Stoffs (M A1).
Bestätige die in der Werbung getroffenen Aussagen anhand eines selbst hergestellten Brausepulvers experimentell (M A2).
Weise das gasförmige Reaktionsprodukt nach (M A2).
Plane dazu dein experimentelles Vorgehen (M A2).
Werte deine Beobachtungen unter Einbeziehung von Reaktionsgleichungen aus.
Beschreibe das Vorgehen zum kalorimetrischen Ermitteln des physikalischen Brennwerts (M A3).
Berechne die Reaktionsenthalpie für die Verbrennung reiner Citronensäure aus dem kalorimetrisch ermittelten Messwert (M A1, M A3).
Formuliere die Reaktionsgleichung für die Gleichgewichtsreaktion zur Herstellung von Triethylcitrat (M A4).
Begründe zwei Maßnahmen, um die Ausbeute dieses Esters zu erhöhen.
Bewerte den Einsatz von Triethylcitrat gegenüber Aluminiumsalzen in Deodorants (M A4).
Aufgabe 3.B – Kupfer
Ein Elektrofahrzeug enthält etwa dreimal so viel Kupfer wie ein vergleichbares Fahrzeug mit Verbrennungsmotor. Auch für die Infrastruktur zum Aufladen von Elektrofahrzeugen besteht ein hoher Bedarf an Kupfer.
Fertige vom Bau der Metalle eine beschriftete Skizze an.
Leite davon ausgehend eine Eigenschaft von Metallen ab.
Begründe für eine der beiden Reaktionen des Garblasens das Vorliegen einer Redoxreaktion. Nutze deine Kenntnisse über Oxidationszahlen (M B1).
Diskutiere die Bestrebungen zum Abbau von Kupfererzen in Deutschland (M B1).
Formuliere für die Elektrodenreaktionen des Daniell-Elements die Teilgleichungen (M B2).
Berechne die Zellspannung unter Standardbedingungen (M B2).
Führe die Experimente zum Kupferkreislauf durch (M B3).
Gib jeweils deine Beobachtungen an.
Werte diese unter Einbeziehung von Reaktionsgleichungen aus.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Material A1: Citronensäure
Citronensäure (2-Hydroxypropan-1,2,3-tricarbonsäure) ist eine farblose, wasserlösliche Carbonsäure, die zu den Fruchtsäuren zählt. Im wasserfreien Zustand bildet sie rhombische Kristalle. Sie ist sehr leicht löslich in Wasser und gut löslich in Ethanol. Eine wässrige Lösung der Citronensäure leitet den elektrischen Strom, feste Citronensäure und die Schmelze jedoch nicht.
Die molare Masse der Citronensäure beträgt
Als Formel für Citronensäure-Moleküle kann vereinfachend die Symbolik H3cit verwendet werden.
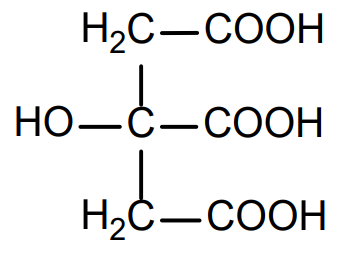
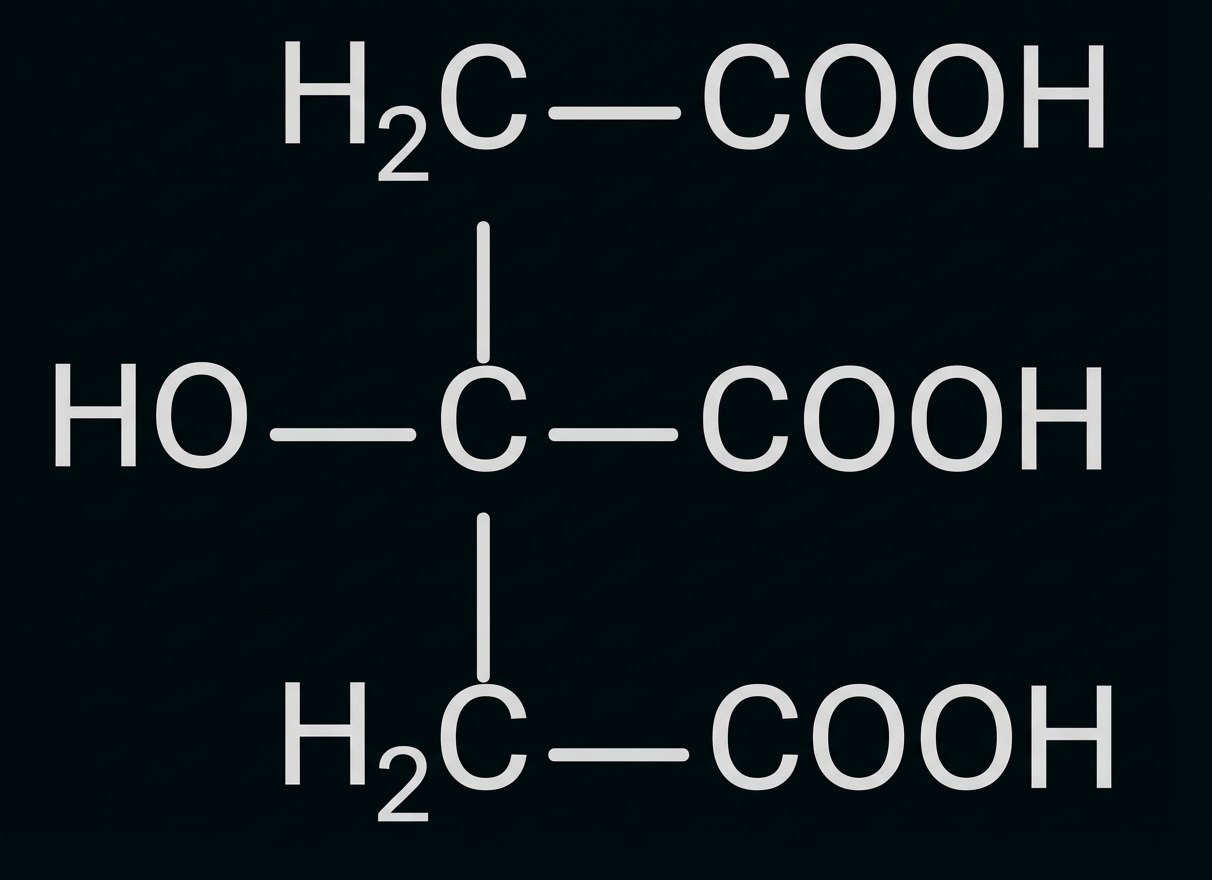
Abb. A1: Strukturformel eines Citronensäure-Moleküls
Material A2: Brausepulver
Brausepulver ist ein Gemisch aus mehreren Stoffen. Laut Werbung kann aus diesem mit Wasser ein sprudelndes und kühlendes Getränk hergestellt werden.
Zur experimentellen Bestätigung der in der Werbung getroffenen Aussagen stehen Ihnen die folgenden Geräte und Chemikalien zur Verfügung.
Geräte:
-
Reagenzgläser
-
Reagenzglasständer
-
Bechergläser
-
Tropfpipetten
-
Spatellöffel
-
Thermometer
-
Glasrührstab
-
Stopfen
Chemikalien:
-
Natriumhydrogencarbonat
-
Citronensäure
-
Saccharose (Zucker)
-
Bariumhydroxid-Lösung (gesättigt)
-
Wasser
Material A3: Bestimmung des physikalischen Brennwertes
In Lebensmitteln spielt der physikalische und physiologische Brennwert eine wichtige Rolle. Der physikalische Brennwert entspricht der Enthalpieänderung für die vollständige Verbrennung einer Stoffportion in reinem Sauerstoff. Dieser Wert kann kalorimetrisch mit Hilfe eines Verbrennungskalorimeters ermittelt werden.
Bei der Verbrennung von 1 g reiner Citronensäure im Kalorimeter erhöhte sich die Temperatur der Kalorimeterflüssigkeit um 12,1 K. Im Kalorimeter befanden sich 200 g Wasser als Kalorimeterflüssigkeit.
Kalorimetrische Gleichung:
Spezifische Wärmekapazität des Wassers:
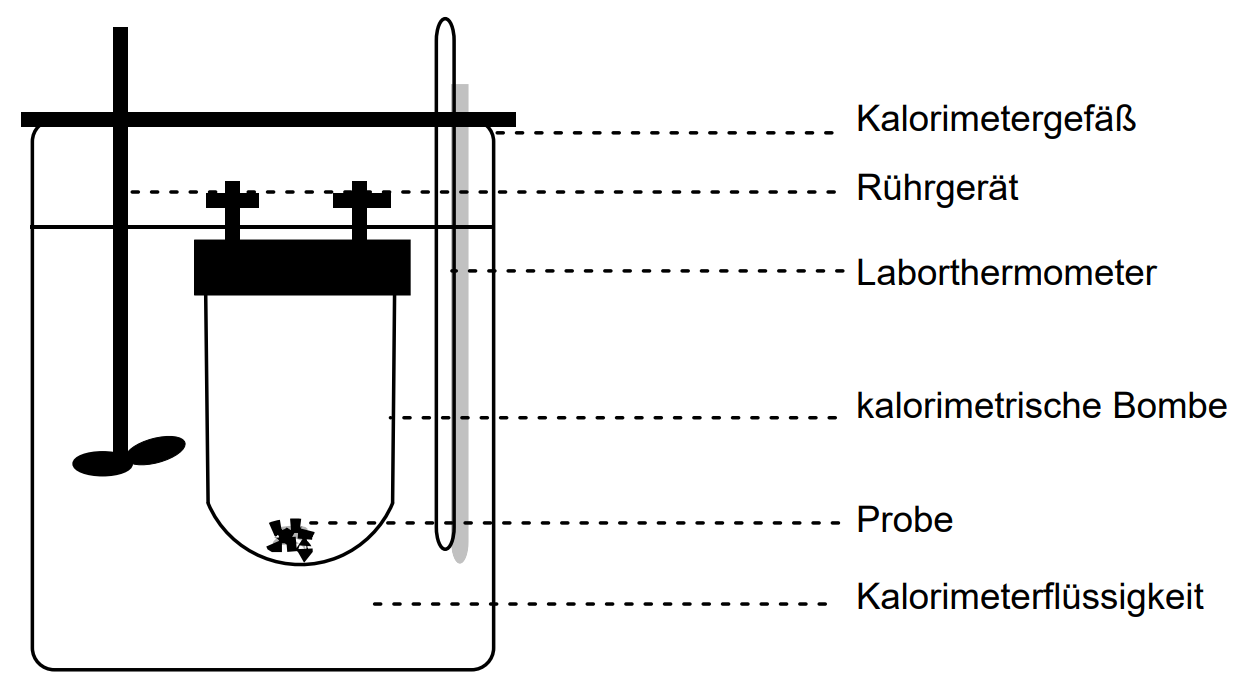
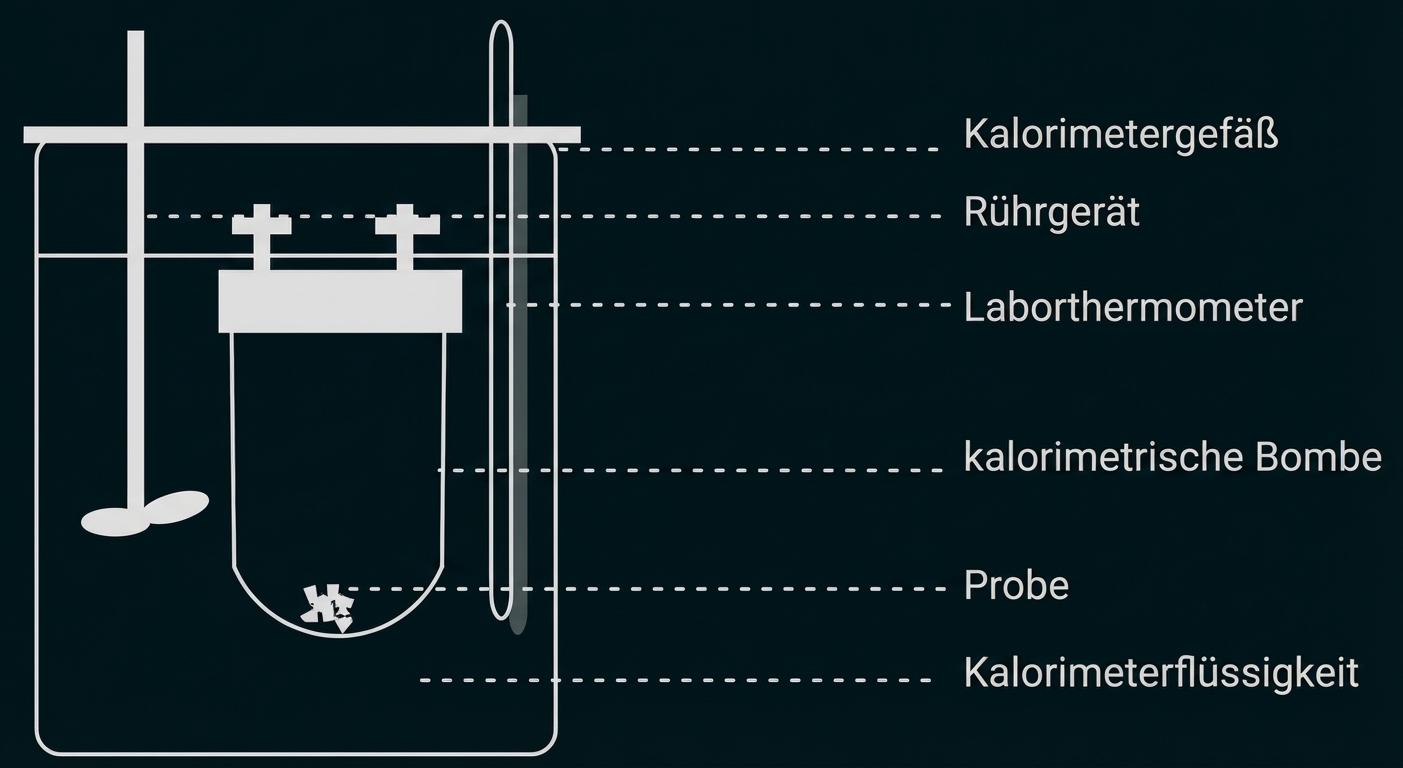
Abb. A2: Aufbau eines Verbrennungskalorimeters
Material A4: Triethylcitrat
Triethylcitrat (TEC), auch Citronensäuretriethylester, wird durch eine exotherme Reaktion von Ethanol mit Citronensäure hergestellt und als künstlicher Trägerstoff und Stabilisator, z. B. in Deodorants, verwendet. TEC verhindert, dass sich mit der Zeit unangenehmer Schweißgeruch bildet. Er wirkt in diesem Fall als eine Art Enzymblocker, der die Bildung der für die Schweißzersetzung so wichtigen Bakterienenzyme hemmt. Die natürliche Hautflora wird dabei geschont, die Verträglichkeit ist in der Regel ausgesprochen gut. Triethylcitrat wird in erster Linie in natürlichen Bio-Deodorants eingesetzt. Konventionelle Deodorants setzen dagegen noch häufig auf Aluminiumsalze. Sie blockieren temporär die Schweißporen, so dass das Schwitzen unter den Achseln eingeschränkt wird. Zudem wirken sie auf die den Schweiß zersetzenden Bakterien antibakteriell, so dass der Schweißgeruch vermindert wird.
Aluminiumverbindungen stehen im Verdacht, an gesundheitlichen Beeinträchtigungen wie z. B. Allergien beteiligt zu sein.
Material B1: Kupfergewinnung
Deutschland gehört zu den führenden Kupferproduzenten. Etwa 50 % der hierzulande hergestellten Kupferprodukte stammen aus recyceltem Alt-Kupfer.
Da in Deutschland aktuell kein Kupferbergbau betrieben wird, müssen Kupfererze u. a. aus Südamerika importiert werden.
Seit einigen Jahren findet die Erkundung von Kupferlagerstätten z. B. im Süden Brandenburgs und in Thüringen statt. Der Abbau von Kupfererzen soll auch in Deutschland wieder erfolgen.
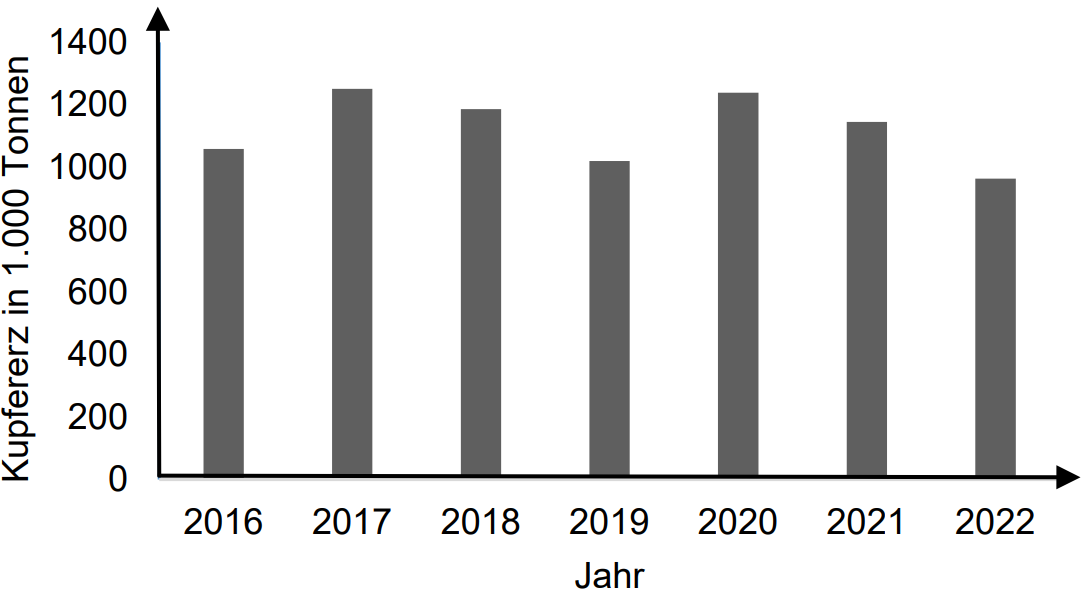
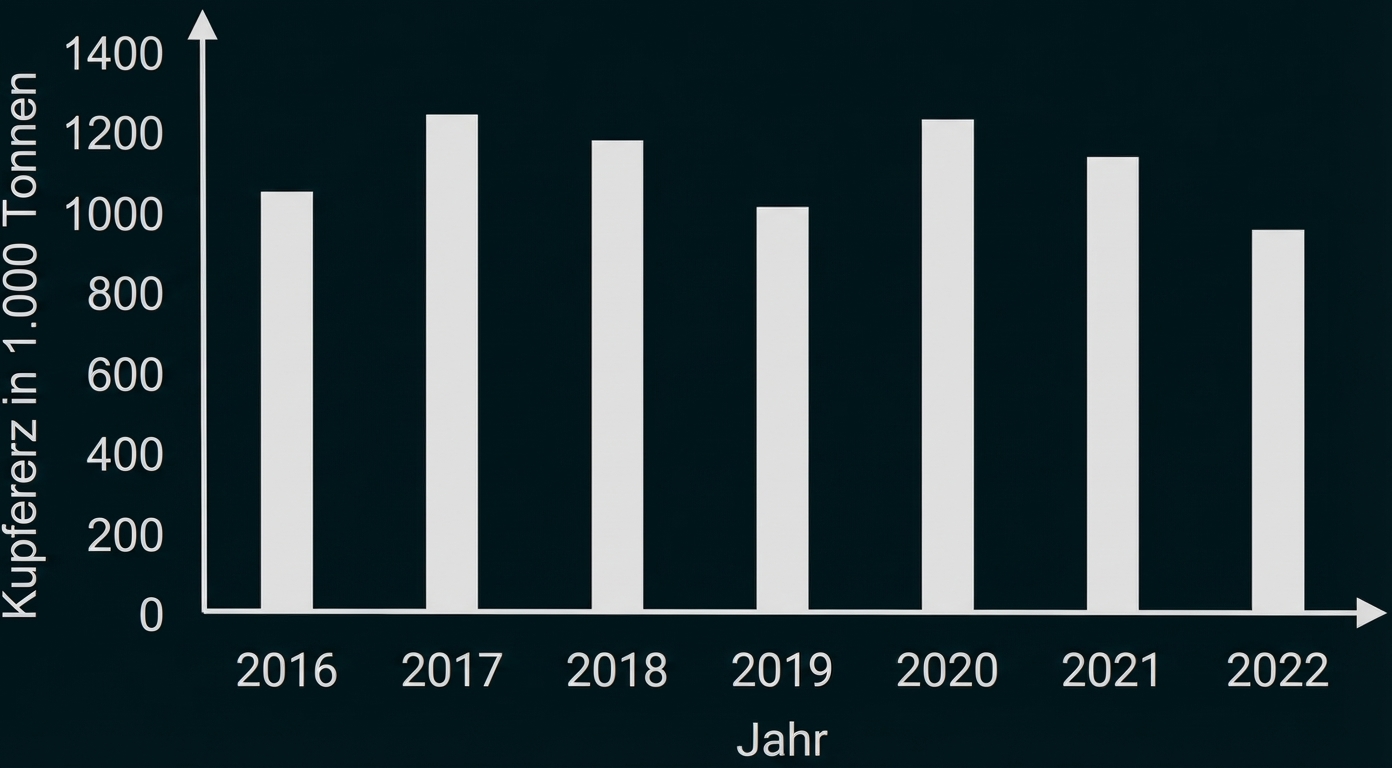
Abb. B1: nach Deutschland importiertes Kupfererz von 2016 bis 2022
Sulfidische Kupfererze werden in mehreren Schritten zum Rohkupfer verarbeitet. Im Röstprozess erfolgt zunächst bei 700 bis 800 °C eine Umsetzung der Erze mit Sauerstoff. Das Schmelzen und Schlackenblasen entfernt anschließend eisenhaltige Bestandteile. Im letzten Schritt, dem Garblasen, führen die beiden chemischen Reaktionen a) und b) zum Rohkupfer.
a)
b)
Material B2: Daniell-Element
In der ersten Hälfte des 19. Jahrhunderts entwickelte der britische Physikochemiker John Frederic Daniell (1790 – 1845) ein nach ihm benanntes galvanisches Element, das Daniell-Element. Es besteht aus einer Kupfer- und einer Zink-Halbzelle, deren Standardpotenziale und
betragen.
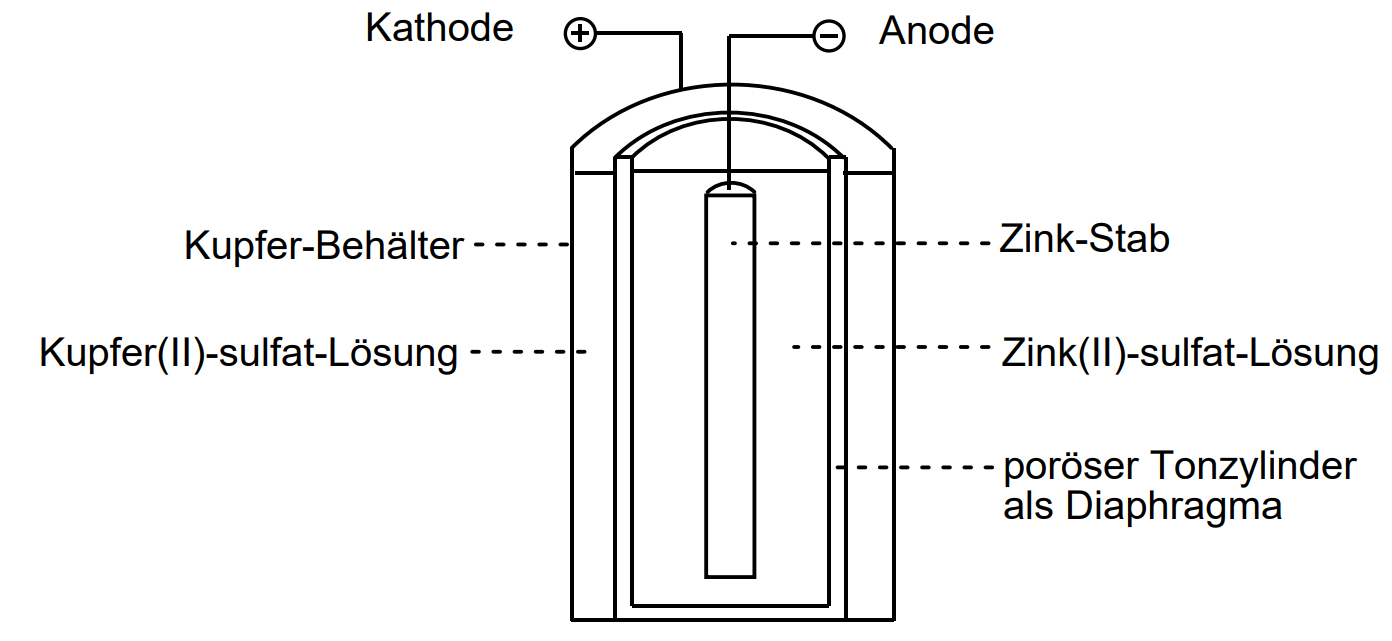

Abb. B2: Aufbau eines Daniell-Elements
Material B3: Kupferkreislauf
Untersuche die chemischen Reaktionen des dargestellten Kupferkreislaufs.
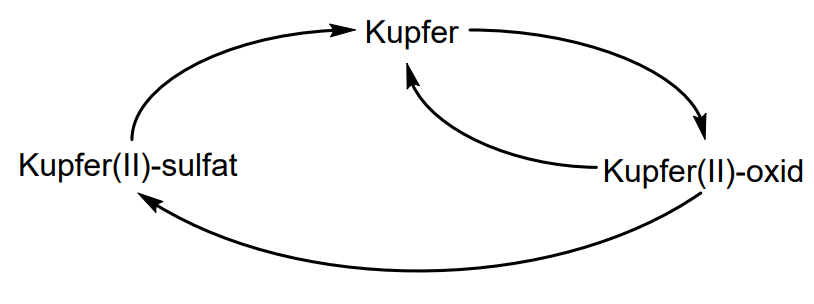
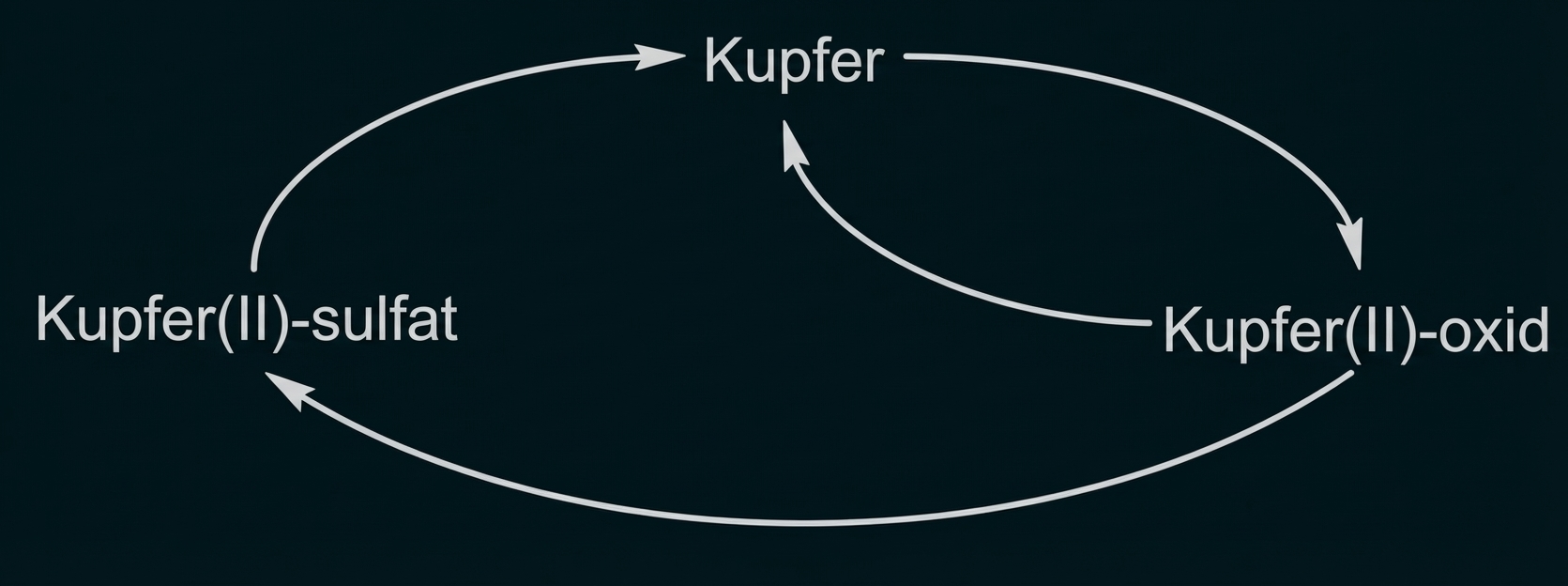
Abb. B3: Darstellung des Kupferkreislaufs
Geräte:
-
Reagenzglasständer
-
schwer schmelzbare Reagenzgläser
-
Reagenzglashalter
-
Becherglas (30 bis 50 mL)
-
Messzylinder (10 mL)
-
Tropfpipetten
-
Spatel
-
Pinzette
-
Stoppuhr
-
Brenner
-
Tiegelzange
Chemikalien:
-
Eisennagel
-
Kohlenstoff (Pulver)
-
Kupferdraht
-
Kupfer(II)-oxid
-
Siedesteinchen
-
Schwefelsäure-Lösung
Experiment A
Erhitze einen Kupferdraht in der Brennerflamme bis zum Glühen und kühle ihn in der Luft ab.
Experiment B
Mische in einem Reagenzglas zwei Spatel Kupfer(II)-oxid mit zwei Spateln Kohlenstoff. Erhitze das Gemisch mit dem Brenner bis zum Glühen. Auf den Nachweis des entstehenden Kohlenstoffdioxids wird verzichtet.
Experiment C
Erhitze in einem Reagenzglas eine Spatelspitze Kupfer(II)-oxid mit ca. 5 mL Schwefelsäure-Lösung bis zum Sieden. Verwende dabei Siedesteinchen.
Kühle das Reagenzglas vorsichtig im Wasserbad ab.
Dekantiere die Lösung aus dem Reagenzglas in ein kleines Becherglas. Stelle zum Schluss einen Eisennagel ca. fünf Minuten in die Lösung.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Begründen einer genannten Eigenschaft
-
polare Hydroxy- und Carboxy-Gruppen in Citronensäure-Molekülen
-
Ausbildung von Wasserstoffbrücken zwischen Citronensäure-Molekülen, Citronensäure fest bei Raumtemperatur
Planung des Vorgehens
-
Lösen eines Gemischs aus Citronensäure und Natriumhydrogen-carbonat in Wasser, Messung der Temperaturänderung
-
Einleiten des Gases in gesättigte Bariumhydroxid-Lösung
Durchführung der Experimente nach Plan
Beobachtungen
-
Temperaturverringerung
-
Gasentwicklung beim Lösen des Gemischs in Wasser
-
weißer Niederschlag in Bariumhydroxid-Lösung
Auswertung
-
endothermer Vorgang
-
Gasentwicklung durch Bildung von Kohlenstoffdioxid
-
-
Bildung von Bariumcarbonat
-
Beschreiben der kalorimetrischen Bestimmung
-
vollständige Verbrennung einer bestimmten Masse an Citronensäure im Kalorimeter
-
die dabei frei werdende Wärme erhöht die Temperatur des Wassers, diese Temperaturänderung wird bestimmt
-
mithilfe der kalorimetrischen Gleichung wird aus diesem Wert die Enthalpieänderung berechnet, diese entspricht dem physikalischen Brennwert
Berechnung
Formulieren der Reaktionsgleichung

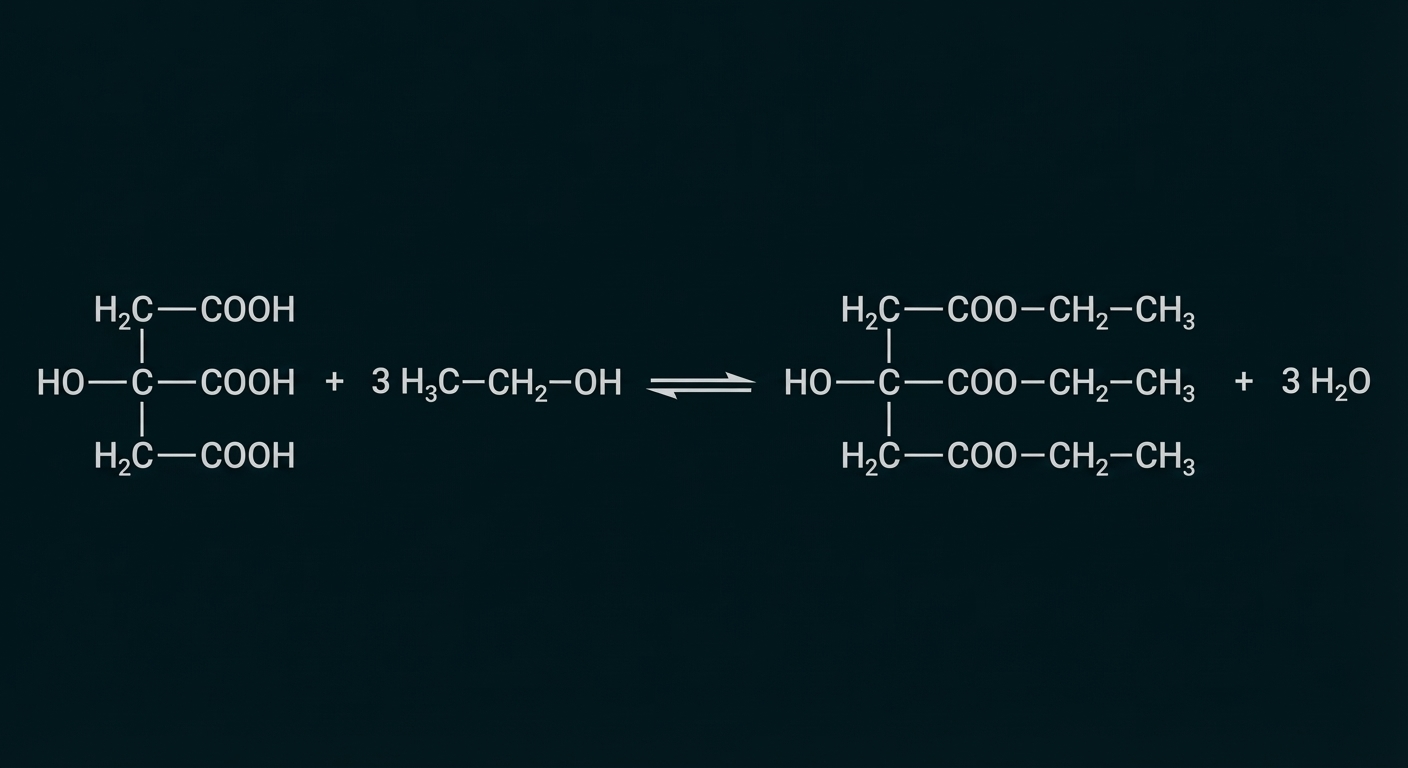
Begründen von zwei Maßnahmen
-
Temperatursenkung
-
Begünstigung exothermer Hinreaktion
-
Erhöhung der Konzentration von z. B. Ethanol
-
Begünstigung der Reaktion unter Verbrauch von Ethanol
Bewerten
-
Deodorants mit Triethylcitrat gut verträglich
-
Deodorants mit Aluminiumsalzen stehen im Verdacht, gesundheitsschädlich zu sein und Allergien auszulösen
-
Werturteil
Beschriftete Skizze
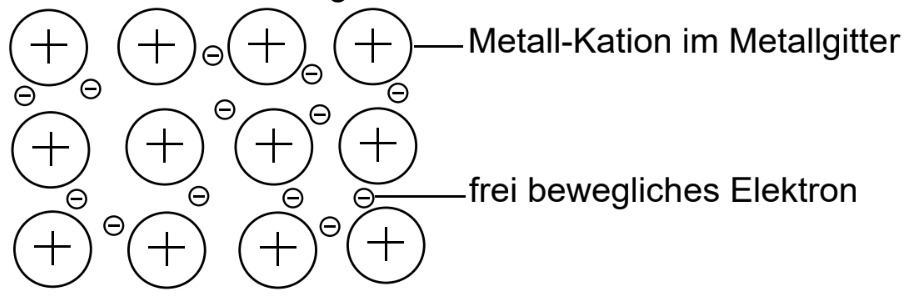
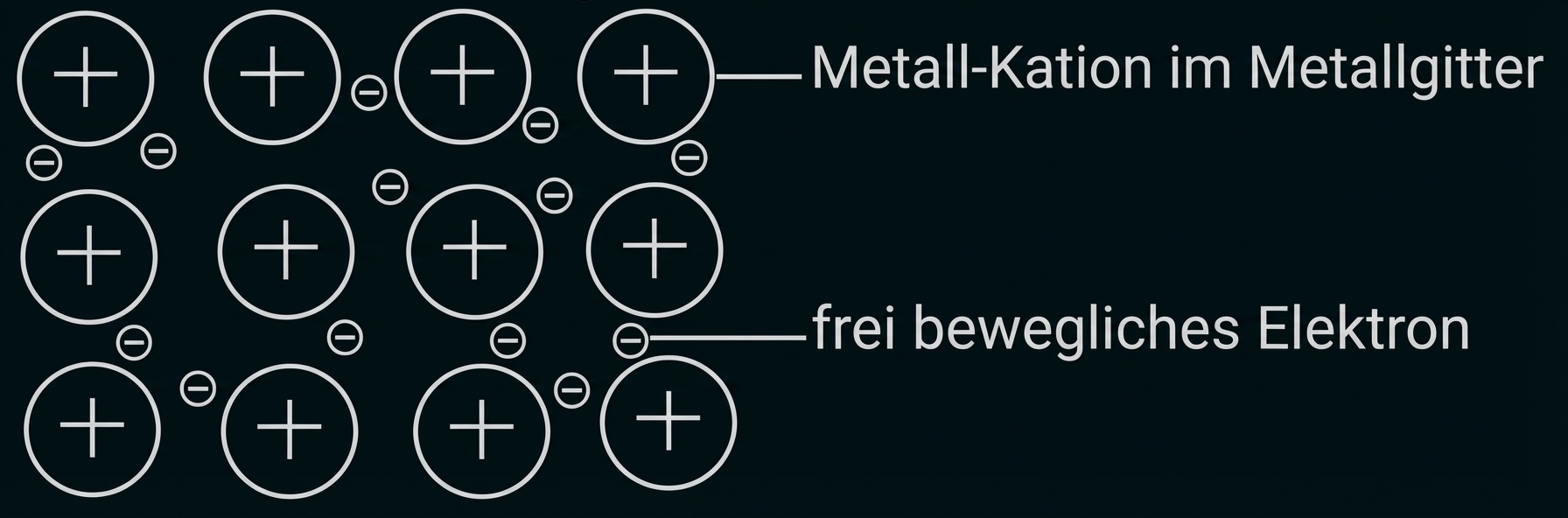
Ableiten einer Eigenschaft von Metallen
-
freibewegliche Elektronen
-
elektrische Leitfähigkeit
Begründung Redoxreaktion
Eine Redoxreaktion liegt vor, wenn sich die Oxidationszahlen der beteiligten Atome im Verlauf der Reaktion ändern, was auf einen Übergang von Elektronen hindeutet.
Reaktionsgleichung (Röstschritt a) )
Bestimmung der Oxidationszahlen
-
Edukte:
-
In
: Kupfer (
) hat die Oxidationszahl +I, Schwefel (
) hat -II.
-
In
: Als Element hat Sauerstoff die Oxidationszahl 0.
-
-
Produkte:
-
In
: Kupfer bleibt bei +I, Sauerstoff hat die Oxidationszahl -II.
-
In
: Sauerstoff hat die Oxidationszahl -II, Schwefel steigt auf +IV.
-
Analyse der Teilprozesse
-
Reduktion (Elektronenaufnahme):
-
Die Oxidationszahl von Sauerstoff sinkt von 0 (in
) auf -II (in
und
). Sauerstoff nimmt somit Elektronen auf.
-
-
Oxidation (Elektronenabgabe):
-
Die Oxidationszahl von Schwefel steigt von -II (in
) auf +IV (in
). Schwefel gibt somit Elektronen ab.
-
Fazit
Da Schwefel oxidiert und Sauerstoff reduziert wird, liegt eine Redoxreaktion vor. Das Kupfer ändert in diesem ersten Schritt (dem Rösten) seine Oxidationszahl noch nicht.
Reaktionsgleichung (Reduktionsschritt b) )
Bestimmung der Oxidationszahlen
-
Edukte:
-
In
: Schwefel hat die Oxidationszahl -II, Kupfer hat +I.
-
In
: Sauerstoff hat die Oxidationszahl -II, Kupfer hat +I.
-
-
Produkte:
-
In elementarem
: Kupfer hat als Element die Oxidationszahl 0.
-
In
: Sauerstoff hat die Oxidationszahl -II, Kupfer hat +I.
-
Analyse der Teilprozesse
-
Reduktion (Elektronenaufnahme):
-
Die Oxidationszahl von Kupfer sinkt von +I (in
und
) auf 0 (in
). Kupfer-I-Ionen nehmen also Elektronen auf und werden zu elementarem Kupfer reduziert.
-
-
Oxidation (Elektronenabgabe):
-
Die Oxidationszahl von Schwefel steigt von -II (in
) auf +IV (in
). Schwefel gibt somit Elektronen ab und wird oxidiert.
-
Fazit
Da sowohl eine Oxidation (Schwefel) als auch eine Reduktion (Kupfer) gleichzeitig stattfinden, handelt es sich eindeutig um eine Redoxreaktion.
Hinweis: Zur Erreichung der vollen Punktzahl muss nur eine der beiden Gleichungen erklärt worden sein.
Diskussion zum Kupferabbau
-
Pro: Unabhängigkeit von Lieferketten
-
Contra: Umweltbelastung
-
Fazit
Formulieren der Teilgleichungen
Anode:
Kathode:
Berechnen der Zellspannung
Durchführung
Beobachtungen
Experiment A:
-
Bildung eines grau-schwarzen Belags am Kupfer
Experiment B:
-
Bildung eines rot-braunen Feststoffs
Experiment C:
-
Bildung einer blauen Lösung, Bildung eines rot-braunen Belags am Eisennagel
Auswertung
Experiment A:
-
Reaktion des Kupfers mit dem Sauerstoff der Luft zu schwarzem Kupfer(II)-oxid
-
Experiment B:
-
Reaktion des Kupfer(II)-oxids mit Kohlenstoff unter Bildung von Kupfer und Kohlenstoffoxid
-
Experiment C:
-
Reaktion des Kupfer(II)-oxids mit Schwefelsäure-Lösung unter Bildung von Kupfer(II)-sulfat-Lösung
-
-
Bildung eines Kupferüberzugs durch elektrochemische Fällung von Kupfer aus der Kupfer(II)-sulfat-Lösung durch unedleres Eisen
-