Vorschlag B – Ethin und andere Alkine
Ethin (früher auch Acetylen) ist eine Grundchemikalie der chemischen Industrie und lässt sich vielseitig verwenden. Die Herstellung von Ethin kann auf verschiedenen Wegen erfolgen.
Früher wurde Ethin bevorzugt aus Calciumcarbid hergestellt. Die im Calciumcarbid neben den Calcium-Ionen vorliegenden Acetylid-Anionen beinhalten ebenfalls jeweils eine Dreifachbindung, da sich ihre Struktur vom Ethin ableitet.
Heute erfolgt die Herstellung von Ethin unter anderem aus Methan. Wird Ethin in einer Verbrennungsreaktion mit reinem Sauerstoff umgesetzt, wird die Flamme bis zu  heiß, weshalb Ethin auch beim sogenannten „autogenen Schweißen“ zum Einsatz kommt.
In seiner Bedeutung als Ausgangsverbindung für chemische Synthesen dient Ethin heute auch zur Kunststoffherstellung. Früher wurde Benzol (Benzen) aus Ethin in einem von Walter Reppe entwickelten Verfahren hergestellt.
Aufgrund der in allen Alkinen vorkommenden Dreifachbindung verhalten sich verschiedene Alkine in chemischen Reaktionen ähnlich.
heiß, weshalb Ethin auch beim sogenannten „autogenen Schweißen“ zum Einsatz kommt.
In seiner Bedeutung als Ausgangsverbindung für chemische Synthesen dient Ethin heute auch zur Kunststoffherstellung. Früher wurde Benzol (Benzen) aus Ethin in einem von Walter Reppe entwickelten Verfahren hergestellt.
Aufgrund der in allen Alkinen vorkommenden Dreifachbindung verhalten sich verschiedene Alkine in chemischen Reaktionen ähnlich.
 -Ionen
-Ionen zusammensetzt, mit Wasser zur Reaktion gebracht. Dabei entstehen Ethin und Calciumhydroxid.
Im zweiten Verfahren reagiert Methan ohne weiteren Reaktionspartner zu Ethin und einem weiteren gasförmigen Reaktionsprodukt.
zusammensetzt, mit Wasser zur Reaktion gebracht. Dabei entstehen Ethin und Calciumhydroxid.
Im zweiten Verfahren reagiert Methan ohne weiteren Reaktionspartner zu Ethin und einem weiteren gasförmigen Reaktionsprodukt.
 (Pikometer), im Ethin-Molekül hingegen
(Pikometer), im Ethin-Molekül hingegen  In einem Fachtext steht: „Die C–H-Bindung im Ethin-Molekül ist kürzer als die im Ethen-Molekül. Dies liegt daran, dass Form und Anteil der s- und p-Orbitale Einfluss auf die Form der daraus gebildeten Hybrid-Orbitale haben.“
Hinweis
In einem Fachtext steht: „Die C–H-Bindung im Ethin-Molekül ist kürzer als die im Ethen-Molekül. Dies liegt daran, dass Form und Anteil der s- und p-Orbitale Einfluss auf die Form der daraus gebildeten Hybrid-Orbitale haben.“
Hinweis
 entspricht
entspricht 
2.1
Formuliere für beide Verfahren zur Herstellung von Ethin (Material 1) jeweils die Reaktionsgleichung unter Verwendung von Strukturformeln für die organischen Verbindungen.
Entwickle die Lewis-Formel für das Acetylid-Ion  -Ion
-Ion
(4 BE)
2.2
Formuliere für jede der Reaktionen in Material 2 eine Reaktionsgleichung unter Verwendung von Strukturformeln für die organischen Verbindungen.
Berechne die Masse an Brom, die man für die vollständige Bromierung der Methyl-Gruppen (Reaktion C) von  1,3,5-Trimethylbenzol benötigt.
Formuliere für Reaktion C den Reaktionsmechanismus und benenne diesen sowie die einzelnen Reaktionsschritte.
Hinweis
1,3,5-Trimethylbenzol benötigt.
Formuliere für Reaktion C den Reaktionsmechanismus und benenne diesen sowie die einzelnen Reaktionsschritte.
Hinweis
Der Mechanismus soll im ersten und im zweiten Reaktionsschritt stellvertretend jeweils mit der Umsetzung eines Brom-Moleküls dargestellt werden. Nicht an der Reaktion beteiligte Molekülteile können durch „R“ für Rest abgekürzt werden.
Der Mechanismus soll im ersten und im zweiten Reaktionsschritt stellvertretend jeweils mit der Umsetzung eines Brom-Moleküls dargestellt werden. Nicht an der Reaktion beteiligte Molekülteile können durch „R“ für Rest abgekürzt werden.
(14 BE)
2.3
Ethen und Ethin eignen sich als Brennstoffe und werden darüber hinaus zur Herstellung von Kunststoffen verwendet.
Formuliere die Reaktionsgleichung für die vollständige Verbrennung von Ethin. Gib für die Reaktion die wesentlichen Oxidationszahlen an und zeige anhand der Elektronenübergänge, dass es sich um eine Redoxreaktion handelt.
Formuliere für Polyethen und für trans-Polyethin jeweils einen Strukturformelausschnitt aus vier Monomer-Einheiten und erläutere für Polyethen das Verhalten beim Erwärmen.
(9 BE)
2.4
Erläutere die Bindungsverhältnisse im Ethin-Molekül mithilfe des Orbitalmodells.
Begründe die unterschiedliche Länge der  -Bindung im Ethen- und Ethin-Molekül mihilfe der Aussage des Fachtextes (Material 3).
-Bindung im Ethen- und Ethin-Molekül mihilfe der Aussage des Fachtextes (Material 3).
(8 BE)
2.5
Formuliere für Reaktion A der Alkylierung (Material 4) eine Reaktionsgleichung.
Hinweis
Verwenden Sie für alle beteiligten Teilchen Strukturformeln. Begründe, nach welchem Mechanismus Reaktion B wahrscheinlich abläuft bzw. nicht abläuft und formuliere den Reaktionsmechanismus.
Verwenden Sie für alle beteiligten Teilchen Strukturformeln. Begründe, nach welchem Mechanismus Reaktion B wahrscheinlich abläuft bzw. nicht abläuft und formuliere den Reaktionsmechanismus.
(10 BE)
2.6
Von Hexin gibt es insgesamt sieben Konstitutionsisomere (Strukturisomere) mit jeweils einer Dreifachbindung, zu denen unter anderem Hex-1-in, Hex-2-in und Hex-3-in gehören.
Entwickle für die übrigen vier Konstitutionsisomere jeweils die Strukturformel.
In der Struktur von einem dieser Konstitutionsisomere liegt ein asymmetrisches Kohlenstoff-Atom vor.
Beschrifte in der Struktur des entsprechenden Konstitutionsisomeren das asymmetrische Kohlenstoff-Atom mit einem Stern.
(5 BE)
(50 BE)
Material 1
Herstellungsverfahren für Ethin
Im ersten Verfahren wird Calciumcarbid, das sich aus Calcium-Ionen und Acetylid-IonenMaterial 2
Reaktionen von Alkinen
| Reaktion A: | Reaktion von Ethin zu Benzol (Benzen) ohne weiteren Reaktionspartner. |
| Reaktion B: | Reaktion von Propin zu 1,3,5-Trimethylbenzol ohne weiteren Reaktionspartner. |
| Reaktion C: | Reaktion von 1,3,5-Trimethylbenzol mit Brom unter Einwirkung von Licht und Wärme, wobei ausschließlich die Methyl-Gruppen bromiert werden. Nehmen Sie an, dass es zu einer vollständigen Bromierung aller Methyl-Gruppen kommt. |
Material 3
Bindungslängen der Kohlenstoff-Wasserstoff-Bindungen in Ethen und Ethin
Im Ethen-Molekül beträgt die Bindungslänge aller C–H-BindungenMaterial 4
Alkylierung von Pent-1-in
| Reaktion A: | Unter Wirkung starker Basen können Alkine am C1-Atom deprotoniert werden. So reagiert Pent-1-in mit Amid-Ionen |
| Reaktion B: | Das so erhaltene Anion reagiert mit Bromethan in einer Substitutionsreaktion zu Hept-3-in. |
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?
2.1
Formulierung der Reaktionsgleichungen
Reaktion von Calciumcarbid mit Wasser:
 Ethin-Synthese aus Methan:
Ethin-Synthese aus Methan:
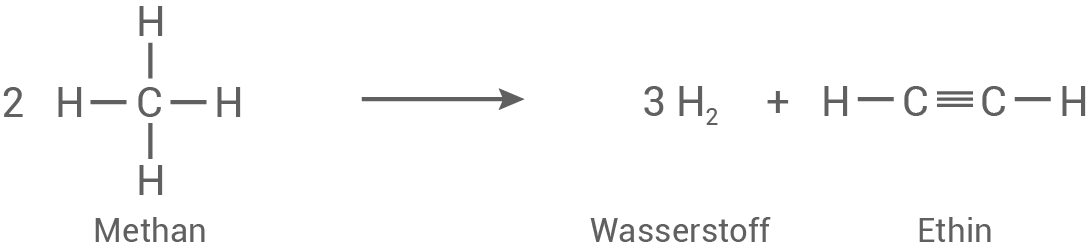 Entwicklung der Lewis-Formel
Entwicklung der Lewis-Formel
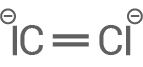


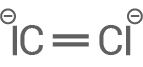
Acetylid-Ion (auch: Carbid-Ion)
2.2
Reaktionsgleichungen zu den drei beschriebenen Reaktionen
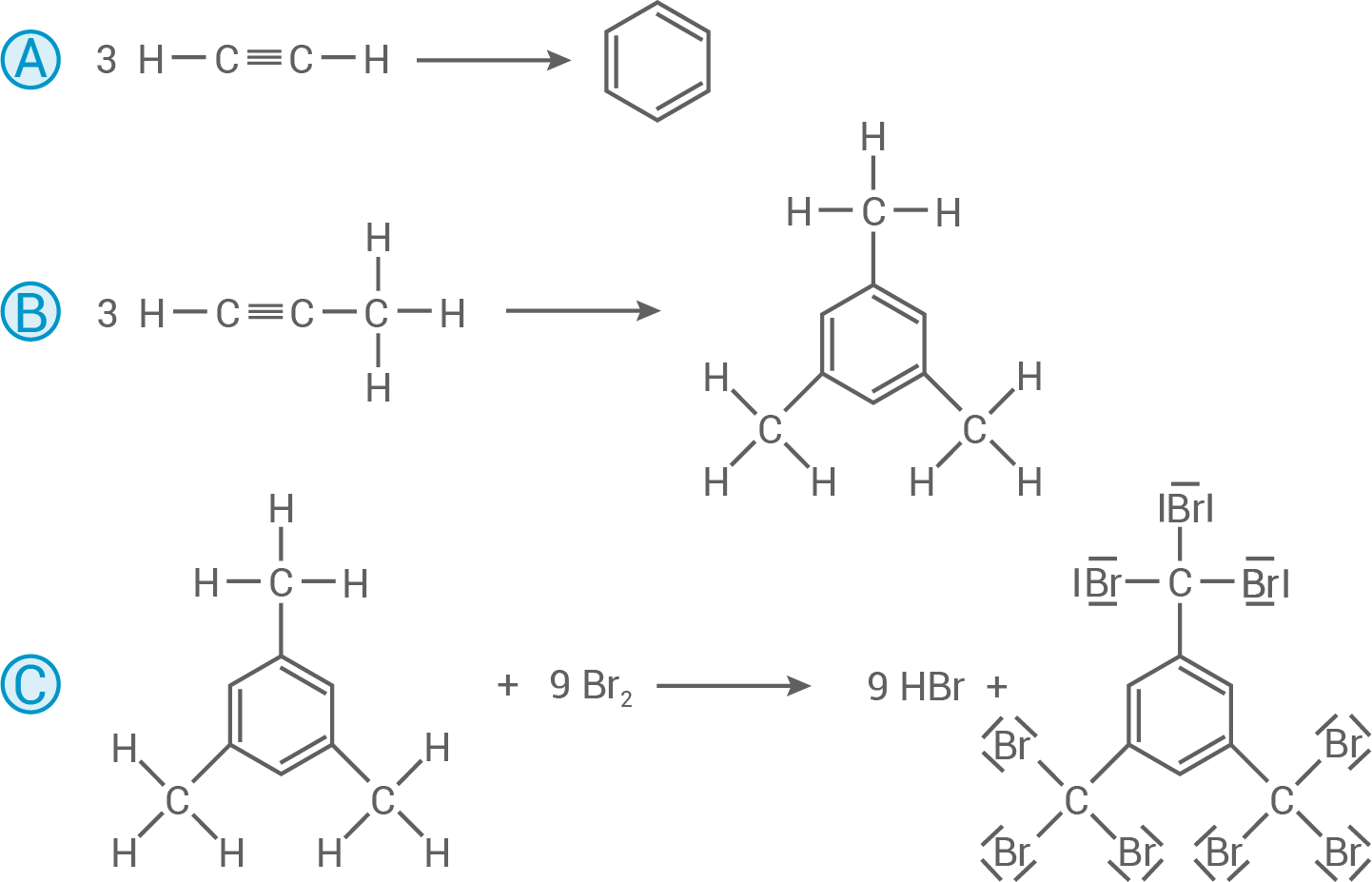 Berechnung der Masse an Brom
Zunächst wird die Stoffmenge
Berechnung der Masse an Brom
Zunächst wird die Stoffmenge  von 1,3,5-Trimethylbenzol berechnet:
Mit
von 1,3,5-Trimethylbenzol berechnet:
Mit  und
und  gilt:
gilt:
![\(\begin{array}[t]{rll}
n \,\text{(Trimethylbenzol)}&=& \dfrac{5\,\text{g}}{120 \,\text{g} \cdot \text{mol}^{-1}} & \\[5pt]
&=& 0,0417 \,\text{mol}
\end{array}\)](https://www.schullv.de/resources/formulas/acd070efd5875bedfaf57b845f06a00b57504b307f536381b3f38ece15455160_light.svg) Der Reaktionsgleichung zeigt folgenden Zusammenhang:
Der Reaktionsgleichung zeigt folgenden Zusammenhang:
![\(\begin{array}[t]{rll}
n\,\text{(Brom)} &=& n \,\text{(Trimethylbenzol)} \cdot 9 & \\[5pt]
&=& 0,0417 \,\text{mol} \cdot 9 & \\[5pt]
&\approx& 0,375 \,\text{mol}
\end{array}\)](https://www.schullv.de/resources/formulas/e52cd645e78a8f89e2dc2572734f01bc465fae2c45d56a24bd01fa4d09edb384_light.svg) Mit
Mit  und
und  gilt:
gilt:
![\(\begin{array}[t]{rll}
m\,\text{(Brom)}&=& 0,375\,\text{mol} \cdot 159,8 \,\text{g} \cdot \text{mol}^{-1} & \\[5pt]
&=& 59,93 \,\text{g}
\end{array}\)](https://www.schullv.de/resources/formulas/17a78e8d4e540383a50b79ba0c017150cb1090637b98bbe47d752dcfca2f3719_light.svg) Damit werden für die vollständige Bromierung der Methyl-Gruppen in Reaktion C ca.
Damit werden für die vollständige Bromierung der Methyl-Gruppen in Reaktion C ca.  benötigt.
Benennung des Reaktionsmechanismus und der einzelnen Schritte
benötigt.
Benennung des Reaktionsmechanismus und der einzelnen Schritte
 Die Reaktion unterliegt bei diesen Bedingungen dem Mechanismus der radikalischen Substitution.
Die Reaktion unterliegt bei diesen Bedingungen dem Mechanismus der radikalischen Substitution.

- Startreaktion: homolytische Spaltung

- Kettenreaktion: an der Seitengruppe des Trimethylbenzols
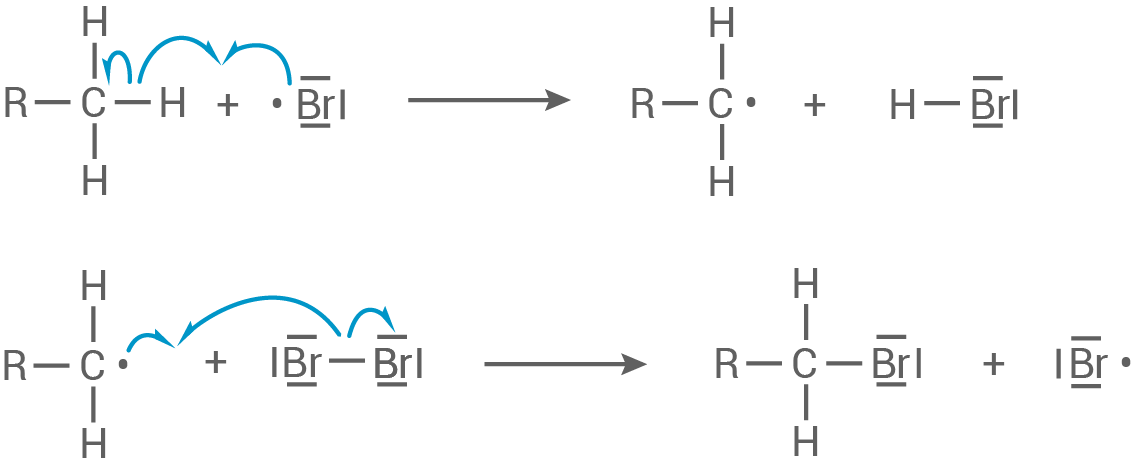
- Kettenabbruch:
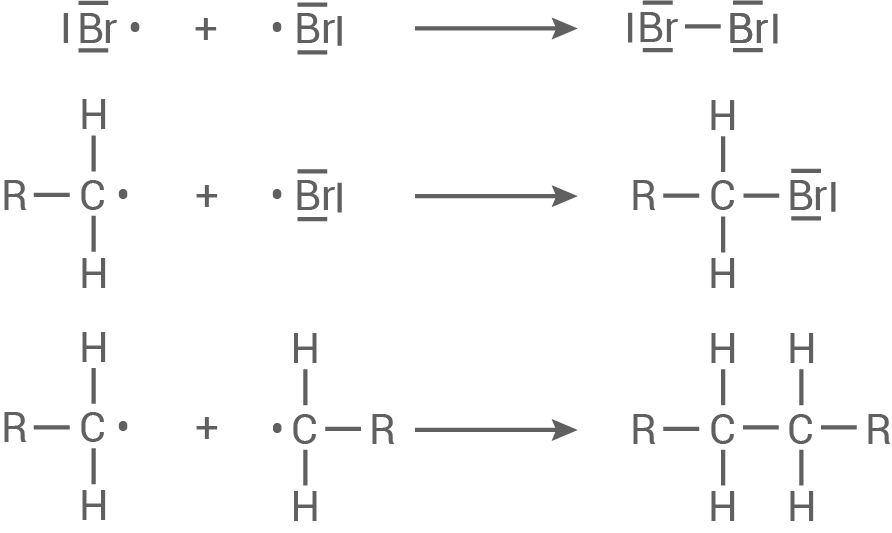
2.3
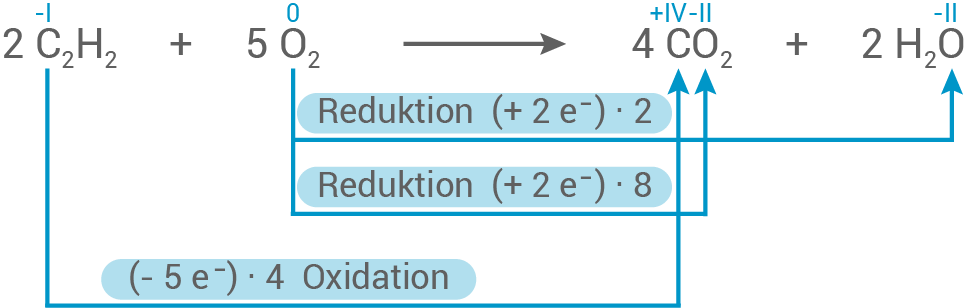
Die vollständige Verbrennung von Ethin
 Das Verhalten von Polyethen beim Erwärmen (thermisches Verhalten)
Das Verhalten von Polyethen beim Erwärmen (thermisches Verhalten)

- Die Oxidationszahl im Kohlenstoffdioxid-Molekül steigt von -I auf +IV. Der Kohlenstoff gibt also
Elektronen ab und es findet eine Oxidation statt.
- Die Oxidationszahl des Sauerstoffs sinkt von 0 auf -II. Der Sauerstoff nimmt die vom Kohlenstoff abgegebenen Elektronen auf und es findet eine Reduktion statt.
- Es handelt sich also um eine Redoxreaktion, in der insgesamt
Elektronen übertragen werden.

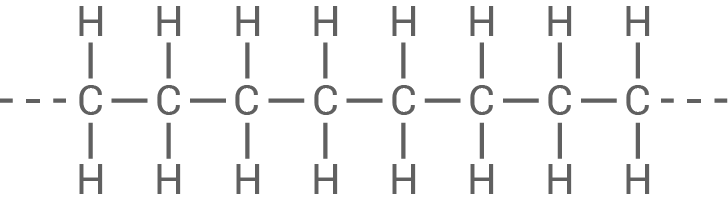
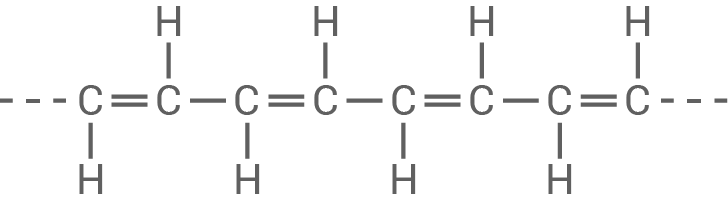
Polyethen

trans-Polyethin
- Der Kunststoff Polyethen (PE) ist ein Thermoplast.
- Der Strukturformelausschnitt zeigt eine lineare, unverzweigte Polymerkette, wobei nur schwache VAN-DER-WAALS-Kräfte wirken.
- Beim Erhitzen, also der Zufuhr von Wärmeenergie, werden die zwischenmolekulare Kräfte durch starke thermische Bewegungen überwunden.
- Dadurch gleiten die Molekülketten aneinander vorbei und es kommt zur Erweichung.
- Bei stärkerem Erhitzen ist auf Stoffebene das Schmelzen des Kunststoffs zu beobachten.
2.4
Bindungsverhältnisse im Ethin-Molekül
Das Ethin-Molekül weist eine Dreifachbindung auf, die sich aus einer  - und zwei
- und zwei  -Bindungen zusammensetzt. Bei den beiden Einfachbindungen handelt es sich um
-Bindungen zusammensetzt. Bei den beiden Einfachbindungen handelt es sich um  -Bindungen:
-Bindungen:
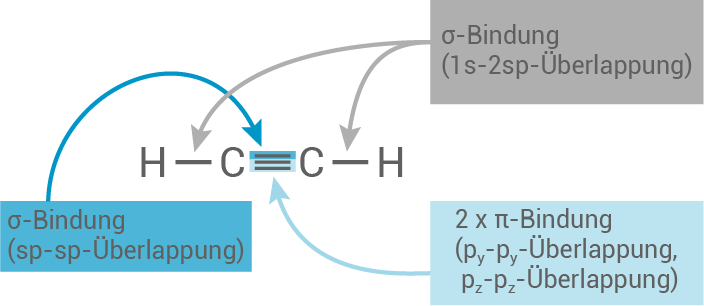

- Die
-Atome des Ethins sind
-hybridisiert, wobei eines der beiden
-Hybridorbitale mit einem
-Hybridorbital des anderen
-Atoms überlappt. Hieraus ergibt sich die
-Bindung.
- Durch symmetrie- und richtungsgleiche Überlappung der unhybridisierten
-Orbitale entstehen die beiden
-Bindungen
oder
- Die
-Einfachbindungen sind ebenfalls
-Bindungen, die durch Überlappung des
-Orbitals des Wasserstoff-Atoms mit dem zweiten
-Hybridorbital des Kohlenstoff-Atoms entstehen.
- Als Grundlage dienen unterschiedliche
- und
-Anteile in den kovalenten Bindungen.
- Im Ethin sind die Kohlenstoff-Atome
- und im Ethen
-hybridisiert.
- Während der
- und
- Ánteil im
-Hybridorbital des Ethins gleich groß sind, überwiegt im
-Hybridorbital des Ethens der
-Anteil.
- In der verbildlichten Darstellung sind die
-Orbitale kugelförmig und die
-Orbitale eher hantelförmig.
- Im Ethin-Molekül sind die
-Hybridorbitale daher kugelförmig und die
-Hybridorbitale im Ethen-Molekül weniger kugelförmig (höherer
-Anteil).
- Bei der Überlappung der jeweiligen Hybridorbitale mit dem
-Orbital des Wasserstoff-Atoms ergibt sich für das Ethen eine Bindungslänge von
und ist somit größer als die
des Ethins.
2.5
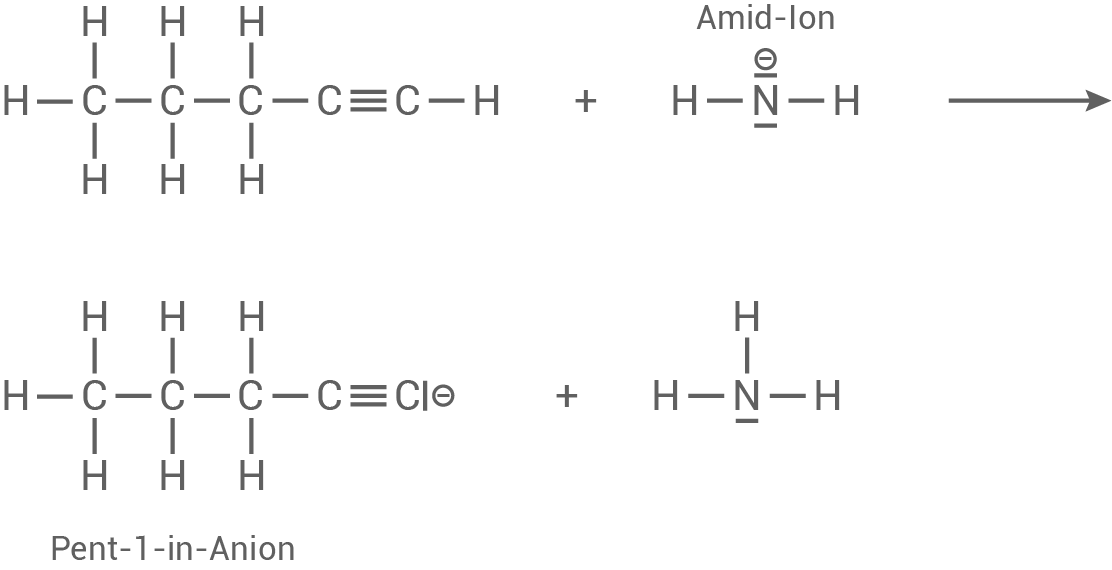
Reaktionsgleichung für Reaktion A der Alkylierung
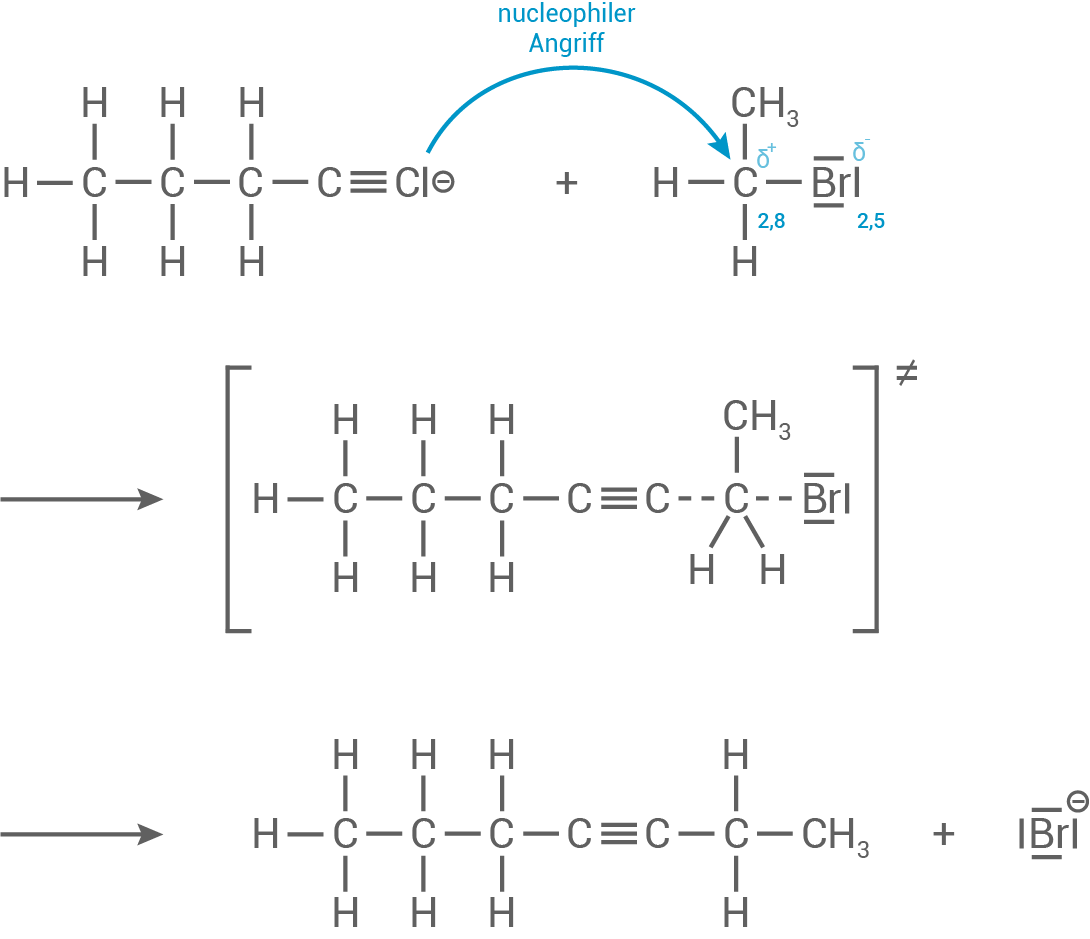
 Reaktionsmechanismus für Reaktion B
Reaktionsmechanismus für Reaktion B
 Begründung für den Ablauf einer
Begründung für den Ablauf einer  -Reaktion
-Reaktion

Deprotonierung von Pent-1-in durch das Amid-Ion

Reaktion des Anions mit Bromethan nach dem  -Mechanismus
-Mechanismus
- Die Reaktion findet an einem primären
-Atom statt, wodurch kurzzeitig im Übergangszustand 5 Substituenten an diesem binden.
- Würde es sich um ein tertiäres
-Atom handeln, wäre ein
-Mechanismus aufgrund des sterischen Anspruchs nicht möglich.
- Bei einem
-Mechanismus wird als Zwischenprodukt ein Carbenium-Ion gebildet. Dieses wird nur durch den +I-Effekt der Methylgruppe und damit sehr schlecht stabilisiert.
- Weiterhin ist Pent-1-in als gutes Nucleophil an der Reaktion beteiligt.
- Das bedeutet, der nucleophile Angriff kann stattfinden, bevor sich durch die Abspaltung der Abgangsgruppe ein Carbenium-Ion bildet.
- Somit unterliegt die Reaktion dem
-Mechanismus.
2.6
Entwicklung der Konstitutionsisomere
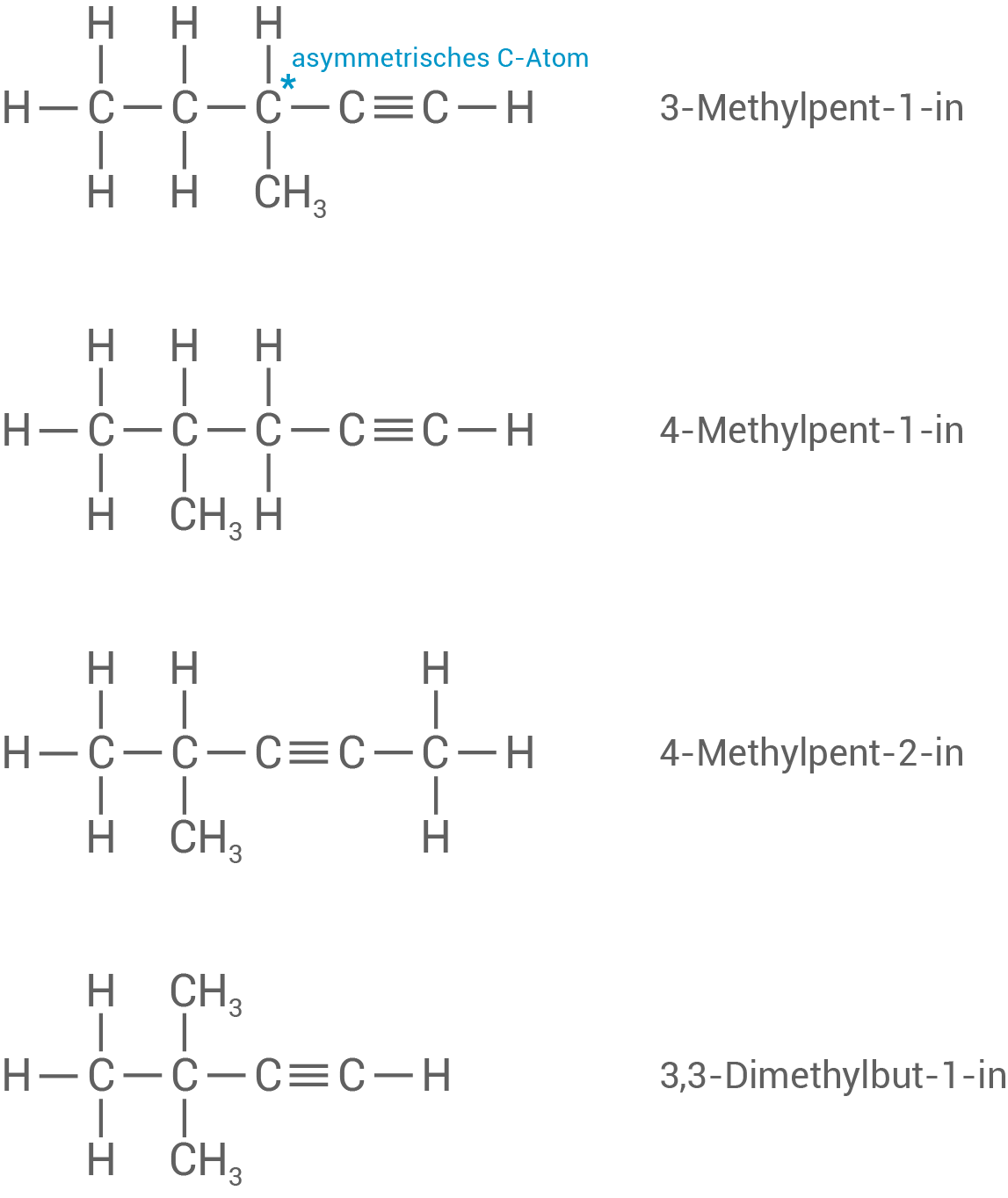 Das asymmetrische
Das asymmetrische  -Atom ist mit * gekennzeichnet und im 3-Methylpent-1-in vorzufinden. Hier besitzt das primäre
-Atom ist mit * gekennzeichnet und im 3-Methylpent-1-in vorzufinden. Hier besitzt das primäre  -Atom vier verschiedene Substituenten/Bindungspartner.
-Atom vier verschiedene Substituenten/Bindungspartner.
