Aufgabe 2 – Die Spannungsreihe der Metalle
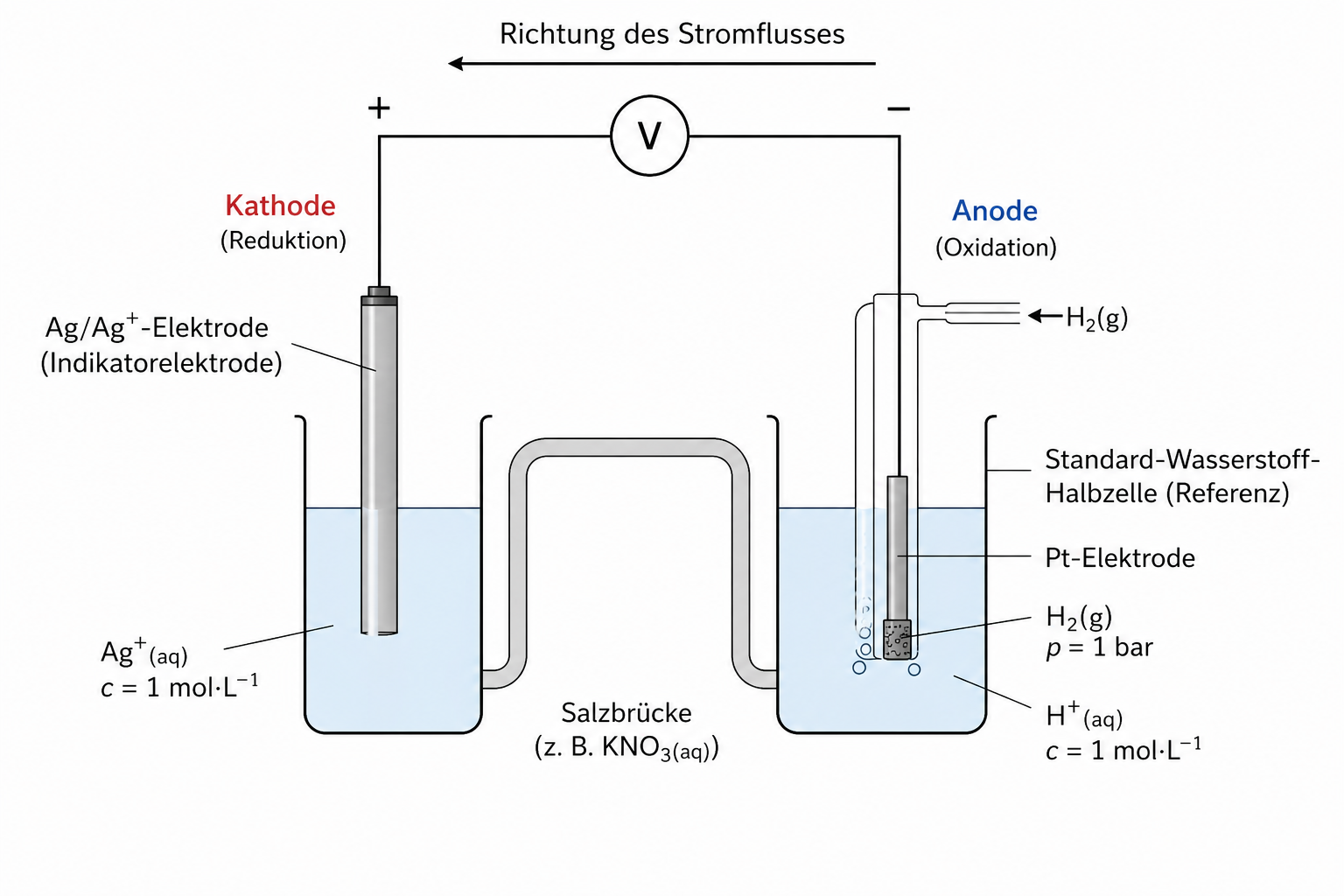
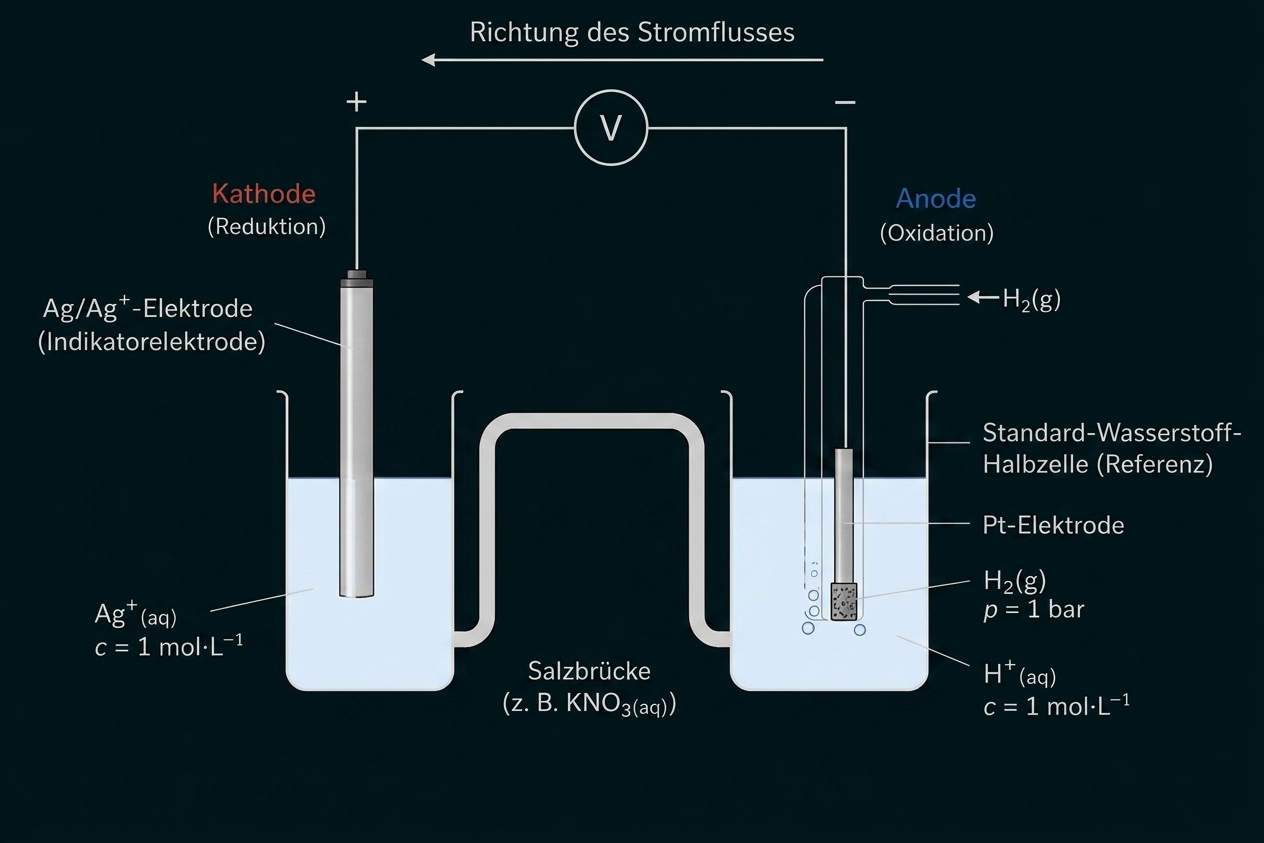
Zur Bestimmung der Standardpotentiale benutzt man als Referenz die „Standard-Wasserstoff-Halbzelle“.
Zeichne und beschrifte den Aufbau einer Galvanischen Zelle zur Bestimmung des Standardpotenzials einer -Elektrode und gib die Richtung des Stromflusses an.
Erläutere die Entstehung eines elektrochemischen Potenzials und Faktoren, die das Potenzial beeinflussen.
Plane ein Gedankenexperiment, mit dem man die Metalle Zink, Kupfer, Zinn und Eisen entsprechend ihres Redoxpotenzials in eine Reihe ordnen kann.
In Deutschland sind viele Brücken sanierungsbedürftig, weil unter anderem im Stahlbeton Eisenstangen, von Beton umhüllt, anfangen zu rosten.
In der Regel ist Zement basisch und hat einen hohen pH-Wert (ca. pH = 12).
Bröckelt jedoch der Beton, tritt Luft und Wasser an die Eisenteile. Das geschieht u.a. durch Frost und Streusalze.
Beschreibe das Rosten von Eisen an der Skizze mithilfe von Reaktionsgleichungen.
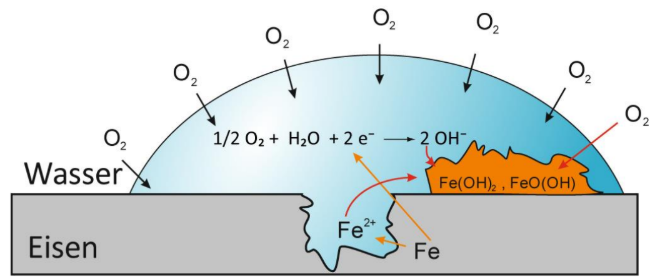
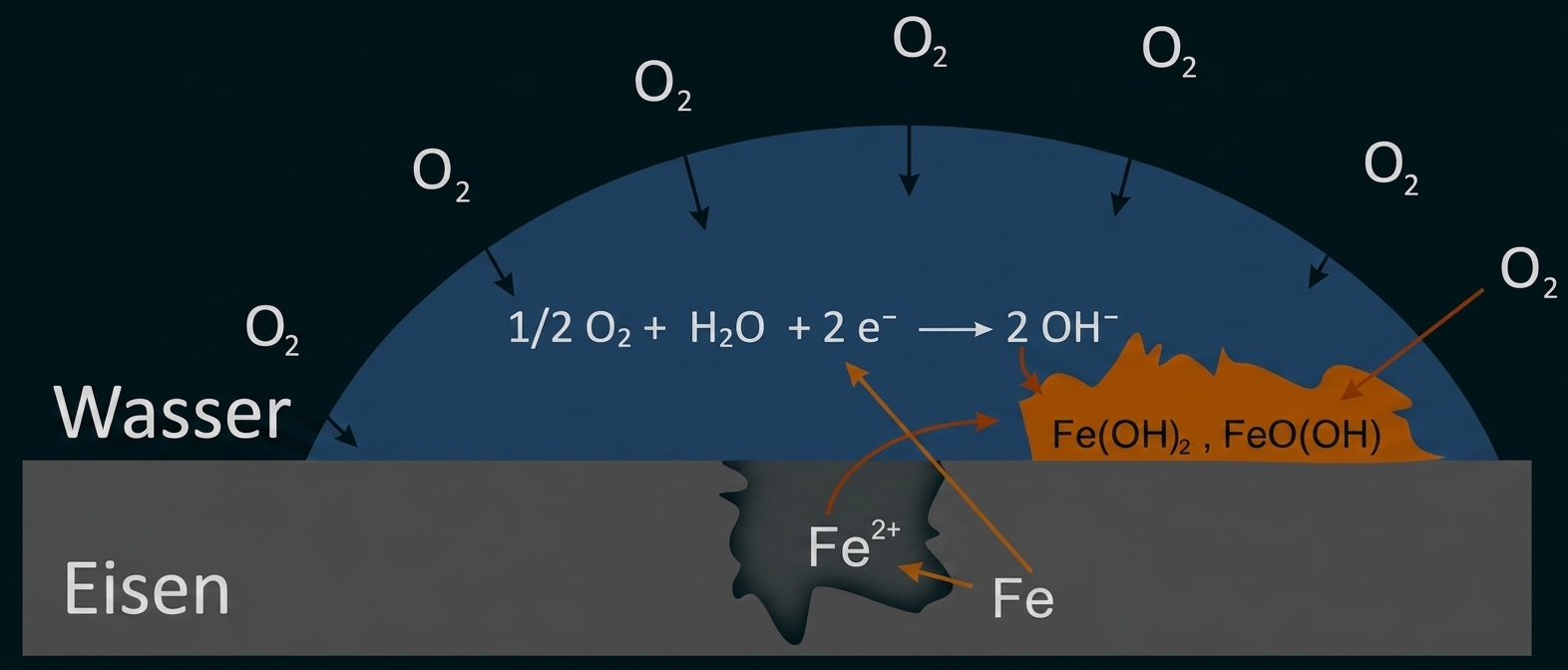
Abbildung: Rostvorgang
Erläutere den Einfluss des pH-Wertes und der Unversehrtheit des Betons auf den Rostprozess.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Skizze
Entstehung eines elektrochemischen Potenzials
Das elektrochemische Potenzial entsteht an der Grenzfläche zwischen einer Elektrode (Metall) und einer Elektrolytlösung durch die Ausbildung einer elektrischen Doppelschicht. Dieser Prozess lässt sich in Teilschritte untergliedern:
-
Lösungsdruck: Jedes Metall hat das Bestreben, Metall-Ionen in die Lösung abzugeben. Dabei bleiben Elektronen im Metallgitter zurück, wodurch sich die Elektrode negativ auflädt. Beispiel:
.
-
Abscheidungsdruck (Oszillationsdruck): Gleichzeitig neigen die in der Lösung befindlichen Metall-Ionen dazu, sich wieder an der Elektrode anzulagern und Elektronen aufzunehmen. Beispiel:
.
-
Dynamisches Gleichgewicht: Nach kurzer Zeit stellt sich ein Gleichgewicht zwischen diesen beiden Vorgängen ein.
-
Elektrische Doppelschicht: Durch die Ladungstrennung (negative Elektrode vs. positiv geladene Lösungsschicht direkt davor) entsteht eine Potenzialdifferenz, die als elektrochemisches Potenzial bezeichnet wird.
Faktoren, die das Potenzial beeinflussen
Das messbare Potenzial einer Halbzelle ist keine starre Größe, sondern hängt von verschiedenen Parametern ab:
-
Art des Metalls (Standardpotenzial): Das Material bestimmt die Lage des Gleichgewichts (Edelmetalle haben einen geringen Lösungsdruck, unedle Metalle einen hohen).
-
Konzentration der Ionen: Je höher die Konzentration der Metall-Ionen in der Lösung ist, desto stärker wird der Abscheidungsdruck (Prinzip von Le Chatelier), was das Potenzial zu positiveren Werten verschiebt. Dies wird quantitativ durch die Nernst-Gleichung beschrieben.
-
Temperatur: Die thermische Energie beeinflusst die Beweglichkeit der Ionen und die Gleichgewichtslage. In der Standard-Wasserstoff-Halbzelle ist
(
) als Standardbedingung definiert.
-
Druck: Bei Gas-Elektroden (wie der Wasserstoff-Halbzelle) beeinflusst der Partialdruck des Gases das Potenzial.
Prinzip des Gedankenexperiments
Das Experiment basiert auf dem Eintauchen eines Metalls in die Salzlösung eines anderen Metalls. Eine Reaktion findet nur dann freiwillig statt, wenn das elementare Metall unedler ist als das Metall-Ion in der Lösung (das unedlere Metall reduziert das edlere Metall-Ion).
Versuchsaufbau und Durchführung
-
Materialien: Proben der Metalle Zink (
), Kupfer (
), Zinn (
) und Eisen (
) sowie entsprechende 1-molare Salzlösungen (z. B. Sulfate oder Chloride dieser Metalle).
-
Vorgehen: Jedes Metall wird nacheinander in die Lösungen der jeweils drei anderen Metalle getaucht.
-
Beobachtung: Es wird notiert, ob sich ein Belag auf dem Metall bildet (Reaktion) oder ob keine Veränderung eintritt.
Erwartete Beobachtungen (Matrix)
Basierend auf den Standardpotenzialen ergeben sich folgende Reaktionen:
|
Metall |
|
|
|
|
Anzahl Reaktionen |
|
Zink ( |
- |
Reaktion |
Reaktion |
Reaktion |
3 |
|
Eisen ( |
keine |
- |
Reaktion |
Reaktion |
2 |
|
Zinn ( |
keine |
keine |
- |
Reaktion |
1 |
|
Kupfer ( |
keine |
keine |
keine |
- |
0 |
Auswertung und Einordnung
-
Das Metall mit den meisten Reaktionen ist das unedlste (stärkstes Reduktionsmittel), da es die meisten anderen Ionen reduzieren kann.
-
Das Metall mit keiner Reaktion ist das edlste (schwächstes Reduktionsmittel).
-
Reihenfolge (nach steigendem Redoxpotenzial):
Beispielhafte Reaktionsgleichung
Stellvertretend für eine beobachtete Reaktion (z. B. Zink in Kupfersulfatlösung):
-
Oxidation:
-
Reduktion:
-
Redoxreaktion:
Der Korrosionsvorgang an der Skizze
Das Rosten von Eisen ist ein elektrochemischer Prozess, bei dem sich auf der Metalloberfläche winzige Kurzschlusszellen (Lokalelemente) bilden. Wasser dient dabei als Elektrolyt.
Teilschritte der Korrosion
Der Gesamtvorgang lässt sich in Redox-Teilreaktionen untergliedern:
-
Anodische Teilreaktion (Oxidation): An der Stelle des Eisenmetalls, an der der Beton bröckelt oder Defekte vorliegen, werden Eisenatome zu Eisen(II)-Ionen oxidiert. Diese wandern in den Wassertropfen:
-
Kathodische Teilreaktion (Reduktion): An den Rändern des Wassertropfens, wo ausreichend Luftsauerstoff gelöst ist, findet die Reduktion von Sauerstoff statt. Dabei bilden sich Hydroxid-Ionen:
-
Bildung von Eisen(II)-hydroxid: Die
-Ionen und
-Ionen diffundieren zueinander und bilden schwerlösliches Eisen(II)-hydroxid:
Bildung von Rost
Das primär entstandene Eisen(II)-hydroxid reagiert mit weiterem Sauerstoff und Wasser zu dem komplexen Gemisch, das wir als Rost bezeichnen:
-
Durch weitere Oxidation entsteht wasserhaltiges Eisen(III)-oxid-hydroxid (
):
Einfluss des pH-Wertes (Passivierung)
-
Basisches Milieu: Zement hat im unversehrten Zustand einen hohen pH-Wert von ca.
.
-
Schutzschichtbildung: In diesem stark alkalischen Bereich bildet sich auf der Oberfläche der Eisenstangen eine extrem dünne, dichte Oxidschicht (Passivschicht).
-
Korrosionsschutz: Diese Passivschicht verhindert den Kontakt des Eisens mit Sauerstoff und Wasser, wodurch das Eisen vor Korrosion geschützt bleibt, selbst wenn Feuchtigkeit vorhanden ist.
Einfluss der Unversehrtheit des Betons
-
Barrierefunktion: Ein unversehrter Beton dient als mechanische Barriere gegen das Eindringen von Reaktionspartnern wie
und
.
-
Depassivierung durch Risse: Bröckelt der Beton (z. B. durch Frost oder Streusalze), entstehen Risse, durch die Luft und Wasser direkt an das Eisen gelangen können.
-
Karbonatisierung: Durch eindringendes
aus der Luft sinkt der pH-Wert im Beton ab (
).
-
Folge: Sinkt der pH-Wert unter einen kritischen Bereich (ca.
), wird die schützende Passivschicht instabil und zerstört.
-
Elektrolytwirkung: Streusalze (Ionen) erhöhen zudem die Leitfähigkeit des eindringenden Wassers, was die Geschwindigkeit der elektrochemischen Korrosionsprozesse massiv beschleunigt.