Aufgabe 4 – Elektrochemische Prozesse
Ein galvanisches Element soll unter Standardbedingungen eine Zellspannung von mindestens liefern.
Wähle geeignete Elektroden aus und begründe die Wahl.
Fertige für das ausgewählte galvanische Element eine beschriftete Skizze an und erläutere das Zustandekommen der Zellspannung unter Verwendung der chemischen Zeichensprache.
Ein Zinkstab wird
in eine Magnesiumchlorid-Lösung und
in eine Silbernitrat-Lösung getaucht.
Begründe die zu erwartenden Reaktionen und formuliere die Reaktionsgleichungen.
Beschreibe den Unterschied zwischen einem Primär- und einem Sekundärelement.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Auswahl geeigneter Elektroden
Die Zellspannung soll mindestens
betragen.
Geeignete Elektrodenmaterialien sind z. B. Magnesium und Silber, denn die Differenz ihrer Standardpotentiale gewährleistet eine Zellspannung von über
Anfertigen einer beschrifteten Skizze des galvanischen Elements
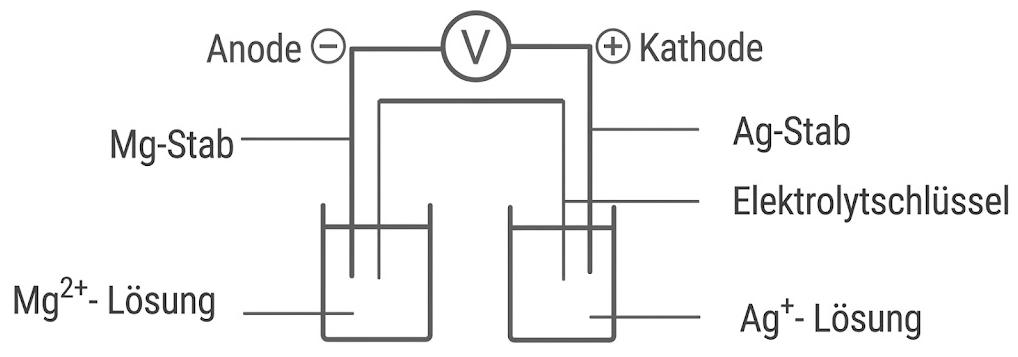
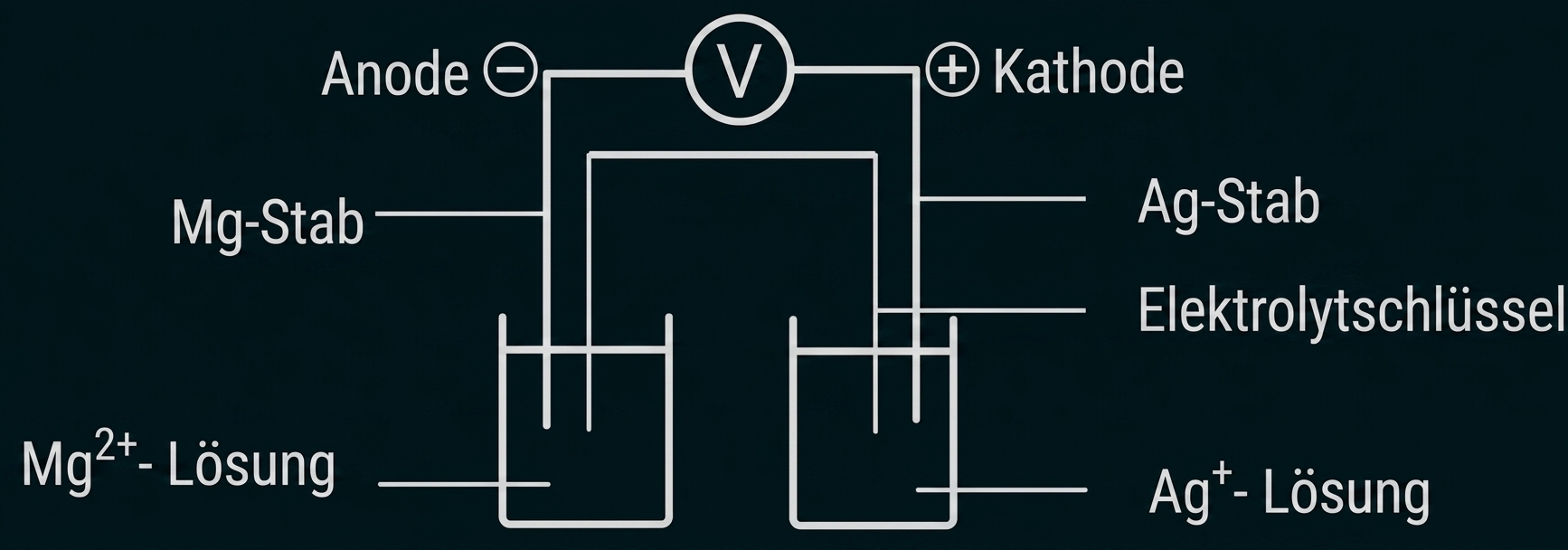
Erläuterung des Zustandekommens der Zellspannung
|
Kathode: |
|
|
Anode: |
|
Die Donatorhalbzelle lädt sich positiv auf und die Akzeptorhalbzelle lädt sich negativ auf. Elektronen wandern von der Donatorhalbzelle über den Leiter zur Akzeptorhalbzelle. Es erfolgt ein Ladungsausgleich durch Ionenwanderung über den Elektrolytschlüssel. Dadurch entsteht ein geschlossener Stromkreis.
keine Reaktion, da das Standardpotential von Magnesium nicht ausreicht, um Zink zu oxidieren:
Zink wird zu Zn2+-Ionen oxidiert und Ag+-Ionen werden zu elementarem Silber reduziert:
Unterschied in der Umkehrbarkeit:
-
Primärelement: Funktion als galvanische Zelle, bis Ausgangsstoffe umgesetzt sind
-
Sekundärelement: durch Zufuhr von elektrischer Energie Rückkehr zum Ausgangszustand; erneut als Spannungsquelle nutzbar