Aufgabe 2 – Schwefelsäure
Die Schwefelsäure ist mit einer Jahresproduktion von 3 Millionen Tonnen weltweit eine der wichtigsten Chemikalien. Sie wird unter anderem für die Produktion von Düngemitteln, für die Herstellung von Papiererzeugnissen und für die Farbstoffindustrie benötigt.
Formuliere die Reaktionsgleichungen für die Schritte zur Herstellung von Schwefelsäure.
Bestimme die jeweilige Reaktionsart für die ersten drei Schritte (M 4).
Berechne das Volumen von Schwefeldioxid, das bei der Oxidation von 2 Tonnen Eisen(II)-sulfid entsteht.
Stelle die Formel für das Massenwirkungsgesetz des Kontaktverfahrens auf.
Interpretiere die Temperaturabhängigkeit des Verfahrens (M 5).
Erläutere zwei Gründe für den Einsatz eines Katalysators beim Kontaktverfahren.
Verdünnt man konzentrierte Schwefelsäure mit Wasser, steigt die Leitfähigkeit der Lösung an.
Erkläre die Aussage zur Erhöhung der Leitfähigkeit mit Hilfe von Reaktionsgleichungen.
Erläutere die Säure-Base-Theorie nach Brønsted an einer Protolysestufe.
Experiment:
Weise Sulfat-Ionen in verdünnter Schwefelsäure-Lösung nach.
Fordere die benötigten Materialien an und fertige ein vollständiges Protokoll an.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?M 4: Herstellung der Schwefelsäure
Im ersten Schritt wird Schwefeldioxid hergestellt. Dazu röstet man sulfidische Erze. Zum Beispiel entsteht beim Erhitzen von Eisen(II)-sulfid unter Luftzufuhr neben Schwefeldioxid auch Eisen(III)-oxid.
Im weiteren Prozess zur Herstellung der Schwefelsäure nutzt man das Kontaktverfahren, bei dem das Schwefeldioxid in Gegenwart des Kontaktkatalysators Vanadiumpentoxid mit Luft zu Schwefeltrioxid oxidiert.
Schwefeltrioxid löst sich nicht besonders gut in Wasser. Aus diesem Grund leitet man das Gas in konzentrierte Schwefelsäure, mit der es zur Dischwefelsäure reagiert.
Durch Zugabe von Wasser zerfällt die Dischwefelsäure wieder in Schwefelsäure.
M 5: Temperaturabhängigkeit des SO2/SO3-Gleichgewichtes
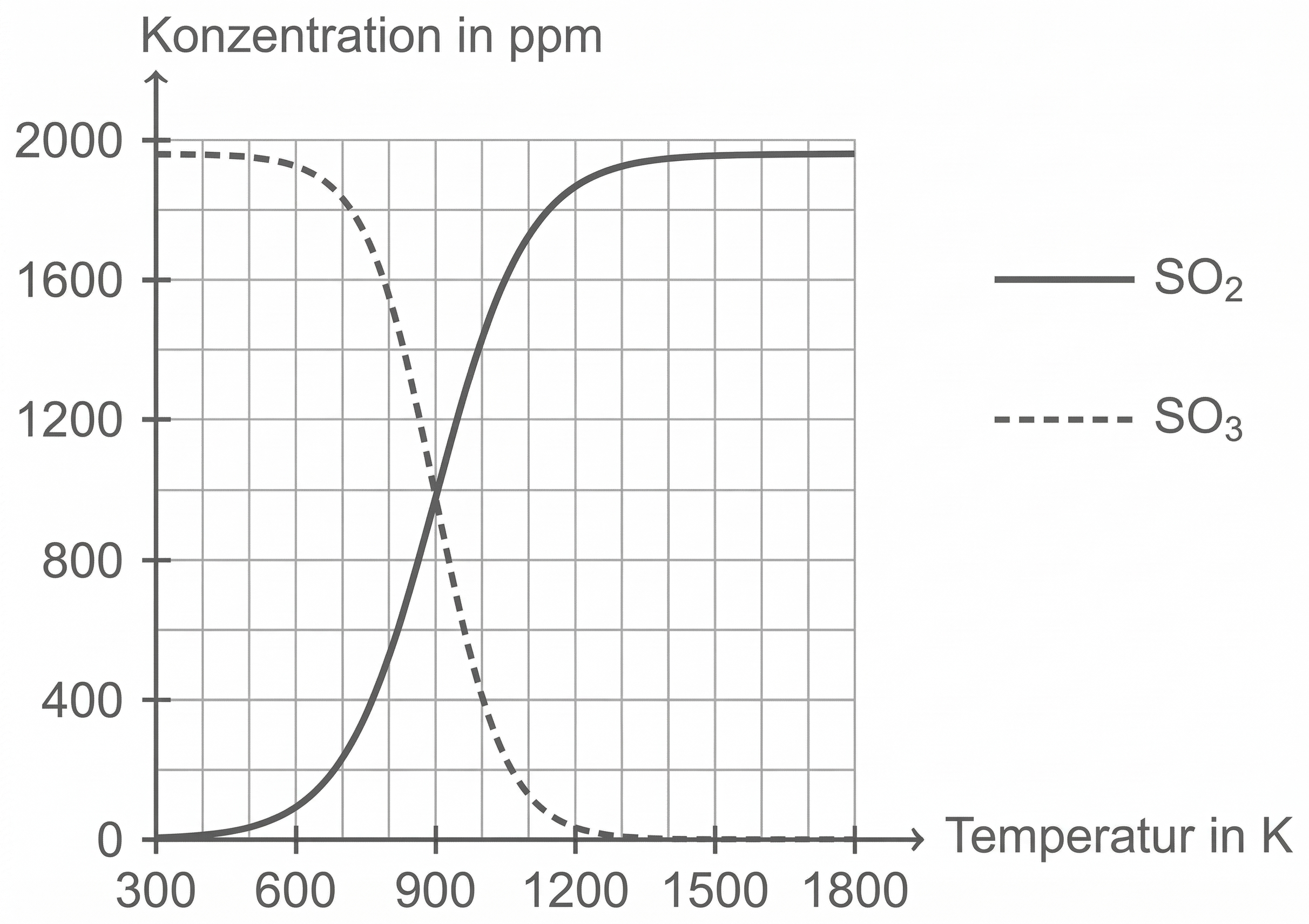
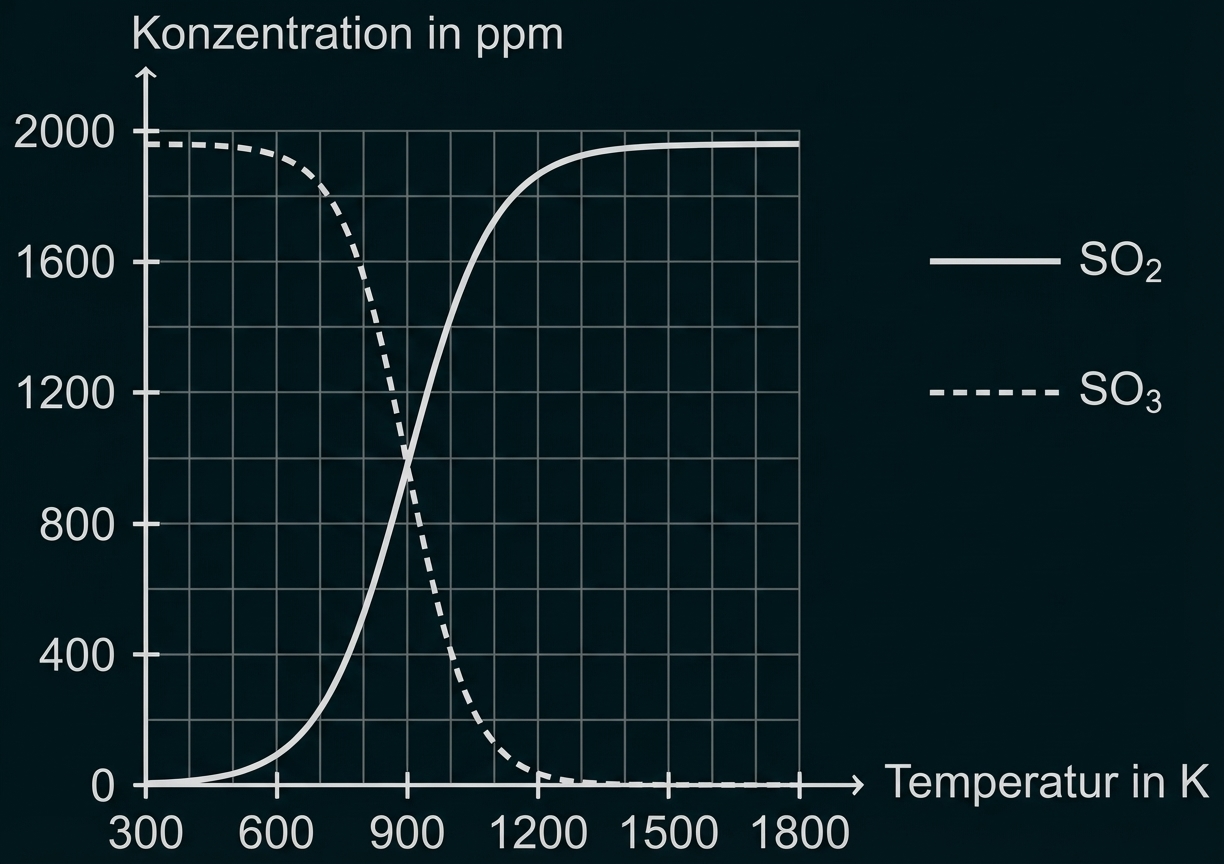
Abb. 1: Temperaturabhängigkeit des SO2/SO3-Gleichgewichtes [2]
Quellen (ggf. verändert):
[2] https://www.researchgate.net/figure/a-Equilibrium-concentrations-for-SO-3-and-SO-2-with-the-gas-composition-in-the-Oxy3-case_fig15_260565612 (Zugriff am 25.11.2023)
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Redoxreaktion: Änderung der Oxidationszahlen
Protolyse: keine Änderung der Oxidationszahlen
Redoxreaktion
Redoxreaktion
Protolyse
Redoxreaktion: Änderung der Oxidationszahlen
Protolyse: keine Änderung der Oxidationszahlen
Gegeben:
Gesucht:
Aufstellen der Formel für das MWG
Interpretation der Temperaturabhängigkeit des Verfahrens
-
Darstellung des Schwefeldioxid-Schwefeltrioxid-Gleichgewichts in Abhängigkeit von der Temperatur
-Achse: Temperatur in
-Achse: Konzentration in
-
Mit zunehmender Temperatur (ab ca.
sinkt der Anteil an Schwefeltrioxid im Gleichgewichtsgemisch.
-
Gleichzeitig steigt der Anteil an Schwefeldioxid im Gemisch.
-
Daraus kann geschlussfolgert werden, dass die Bildung von Schwefeltrioxid exotherm und die Rückreaktion endotherm verläuft.
-
Katalysatoren sind Stoffe, die neue Reaktionswege ermöglichen und damit die Aktivierungsenergie für die Reaktion herabsetzen, damit beschleunigen sie die Reaktion.
-
Dadurch kann Energie eingespart werden.
-
Dadurch wird Zeit eingespart, d.h., in gleicher Zeit werden mehr Reaktionsprodukte hergestellt.
Erklärung der Zunahme der Leitfähigkeit mithilfe von Reaktionsgleichungen
Bei der Reaktion mit Wasser entstehen in zwei Stufen Oxonium-Ionen. Nacheinander werden Hydrogensulfat- und Sulfat-Ionen gebildet. Alle diese Ionen tragen zur Erhöhung der Leitfähigkeit bei.
Erläuterung der Säure-Base-Theorie nach Brønsted
-
Säuren sind Protonendonatoren, sie geben ein Proton ab.
-
Basen sind Protonenakzeptoren, sie nehmen ein Proton auf.
-
Protonenabgabe:
-
Protonenaufnahme:
-
Korrespondierende Säure-Base-Paare:
und
Experiment:
Anfordern: Bariumchlorid-Lösung, Reagenzglas, Reagenzglasständer, Probe, Pipette
Protokoll:
-
Durchführung
-
Beobachtung: weißer Niederschlag
-
Auswertung:
-
Nachweis möglich, da Bariumsulfat ein schwer lösliches Salz ist, was durch die Fällungsreaktion sichtbar gemacht wird