Aufgabe 4 – Ammoniumnitrat
Am 04.08.2020 kam es in Beirut zu einer Explosionskatastrophe. Weite Teile des Hafens wurden zerstört, in der Stadt richtete sie große Schäden an. Bei Schweißarbeiten in einem Lagerraum soll durch Funkenflug ein Feuer ausgebrochen sein, das dort gelagerte Feuerwerkskörper zur Explosion brachte. Diese verursachte wiederum Explosionen von 2750 Tonnen daneben gelagerten Ammoniumnitrats.
Beim Erhitzen über 300 °C und Normdruck zerfällt Ammoniumnitrat in Wasserdampf, Stickstoff und Sauerstoff.
Formuliere die Reaktionsgleichung.
Erläutere den ersten Hauptsatz der Thermodynamik an dieser Reaktion unter Normbedingungen.
Stelle deine Ergebnisse in einem Energiediagramm graphisch dar.
Um das Ausmaß der Druckwelle deutlich zu machen, müssen die gegebenen Reaktionsbedingungen beachtet werden.
Berechne die Volumenarbeit unter den angegebenen Bedingungen, und für die Masse von 2750 Tonnen des Salzes.
Erläutere das Prinzip der Kalorimetrie.
Fertige dazu eine Skizze der Apparatur an und benenne die Teile.
Nenne zwei Voraussetzungen dafür, dass eine Reaktion für dieses Verfahren geeignet ist.
In einem Kalorimeter werden 5 g Ammoniumnitrat in 25 mL Wasser gelöst.
Berechne die zu erwartende Temperaturdifferenz.
Hinweis: Die Lösungsenthalpe beträgt
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Reaktionsgleichung des Ammoniumnitratzerfalls
Ammoniumnitrat () zerfällt beim Erhitzen über
in die gasförmigen Produkte Wasserdampf, Stickstoff und Sauerstoff:
Erläuterung des ersten Hauptsatzes der Thermodynamik
Der erste Hauptsatz der Thermodynamik ist der Energieerhaltungssatz. Er besagt, dass Energie in einem abgeschlossenen System weder erschaffen noch vernichtet, sondern nur von einer Form in eine andere umgewandelt werden kann. Für chemische Reaktionen gilt:
-
Innere Energie: Die Änderung der inneren Energie (
) eines Systems entspricht der Summe der mit der Umgebung ausgetauschten Wärme (
) und Arbeit (
):
.
-
Enthalpie: Da die Reaktion unter Normdruck (isobar) abläuft, wird die freigesetzte Wärme als Reaktionsenthalpie (
) bezeichnet.
-
Energieumwandlung: Bei der Explosion von Ammoniumnitrat wird die in den chemischen Bindungen gespeicherte Energie (chemische Energie) schlagartig in thermische Energie (Wärme) und mechanische Energie (Volumenarbeit durch die Gasexpansion) umgewandelt.
-
Volumenarbeit: Da aus einem Feststoff große Mengen Gas entstehen, verrichtet das System Arbeit gegen den äußeren Luftdruck (
).
Energiediagramm der Reaktion
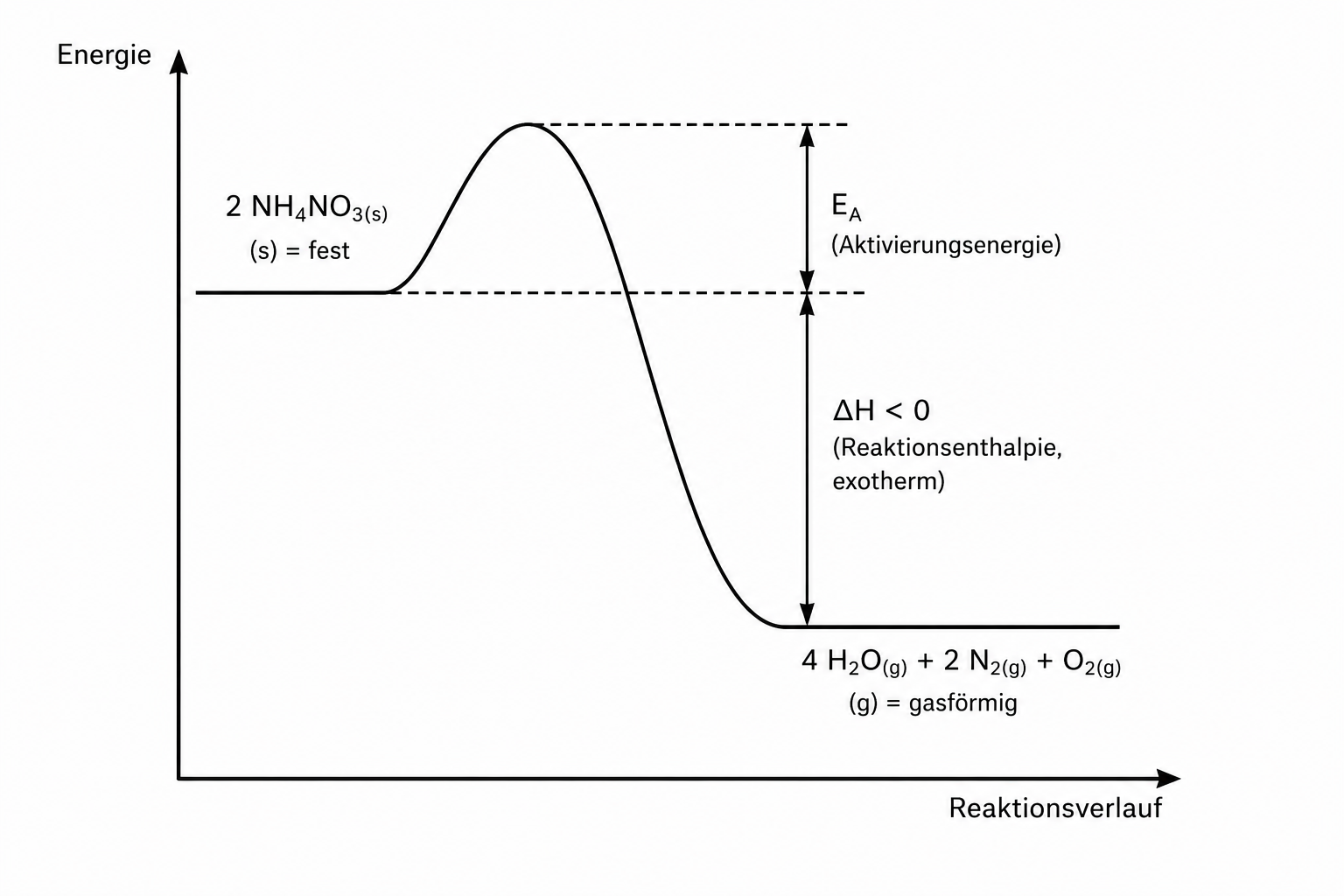
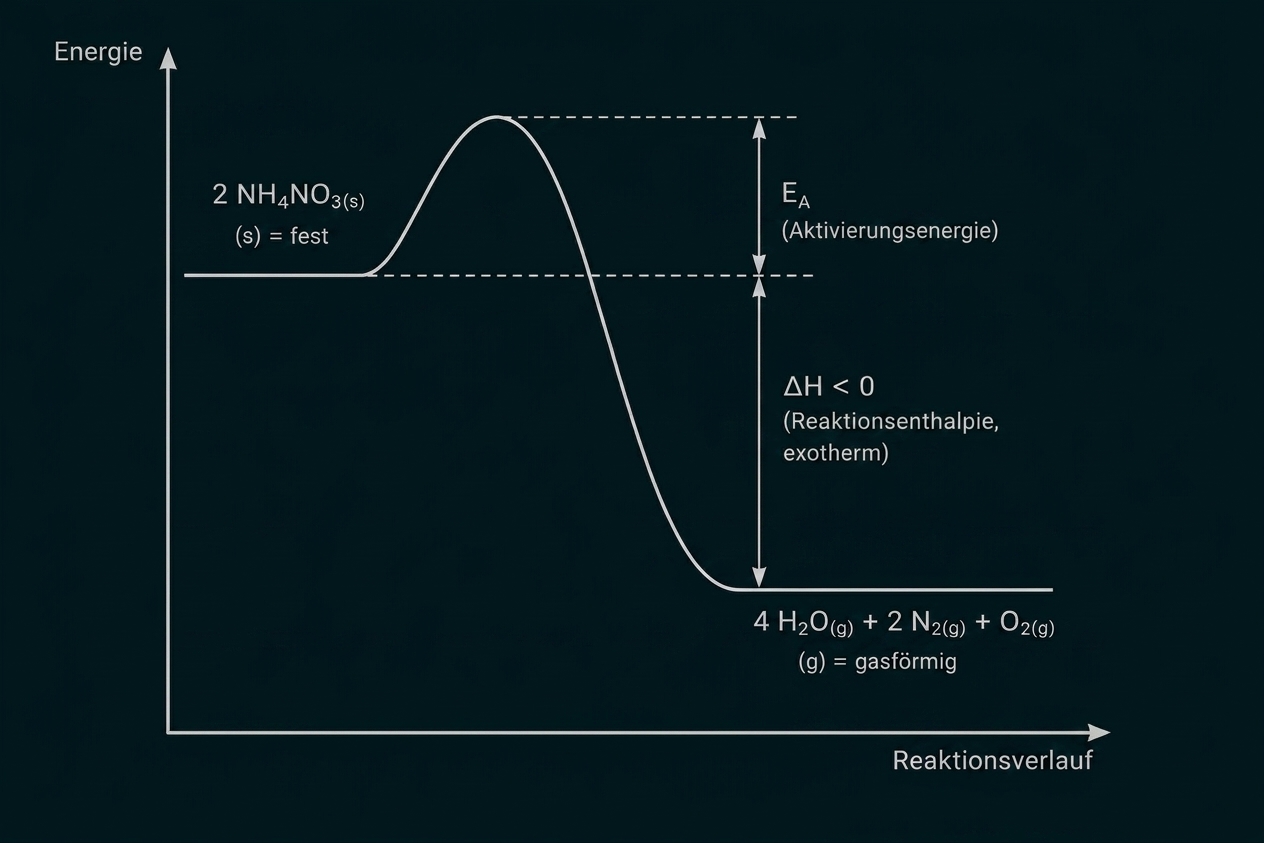
Gegebene Werte und Vorbereitung
-
Masse des Salzes (
):
.
-
Molare Masse (
):
(berechnet aus Tabellenwerten).
-
Molares Volumen der Gase:
.
-
Druck (Normdruck):
.
Schritt 1: Berechnung der Stoffmenge Ammoniumnitrat
Zuerst bestimmen wir, wie viele Mole des Salzes vorhanden sind:
Schritt 2: Bestimmung der Stoffmenge der entstandenen Gase
Laut Reaktionsgleichung () entstehen aus
Feststoff insgesamt
Gas (
). Das Stoffmengenverhältnis beträgt also
.
Schritt 3: Berechnung der Volumenänderung ()
Da das Volumen des Feststoffs gegenüber dem Gasvolumen vernachlässigbar ist, entspricht dem Volumen der entstandenen Gase:
Schritt 4: Berechnung der Volumenarbeit ()
Die Volumenarbeit berechnet sich nach der Formel:
Interpretation des Ergebnisses
-
Das negative Vorzeichen zeigt an, dass das System Energie in Form von Arbeit an die Umgebung abgibt (Expansion).
-
Der enorme Wert von über
Gigajoule verdeutlicht die gewaltige Zerstörungskraft der Druckwelle in Beirut.
Prinzip der Kalorimetrie
Bei der Kalorimetrie wird die bei einer chemischen Reaktion aufgenommene oder abgegebene Wärmeenergie über eine Temperaturänderung bestimmt. Dazu läuft die Reaktion in einem möglichst gut isolierten Gefäß ab, sodass kaum Energie mit der Umgebung ausgetauscht wird.
Gibt die Reaktion Wärme ab (exotherm), steigt die Temperatur der Lösung. Nimmt die Reaktion Wärme auf (endotherm), sinkt die Temperatur.
Die aufgenommene oder abgegebene Wärmeenergie berechnet man mit:
mit:
-
Wärmeenergie
-
spezifische Wärmekapazität
-
Masse
-
Temperaturänderung
Skizze eines Kalorimeters
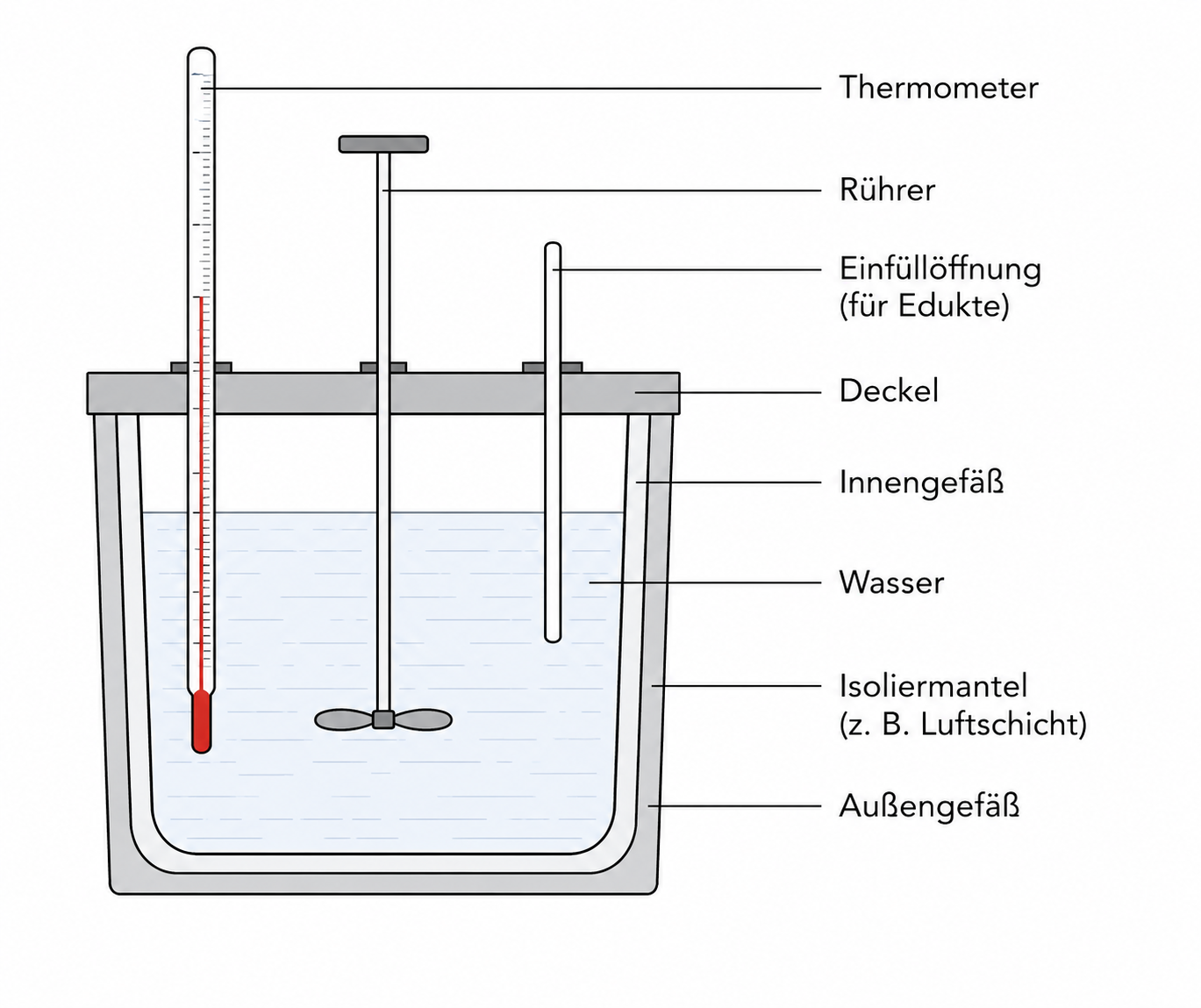
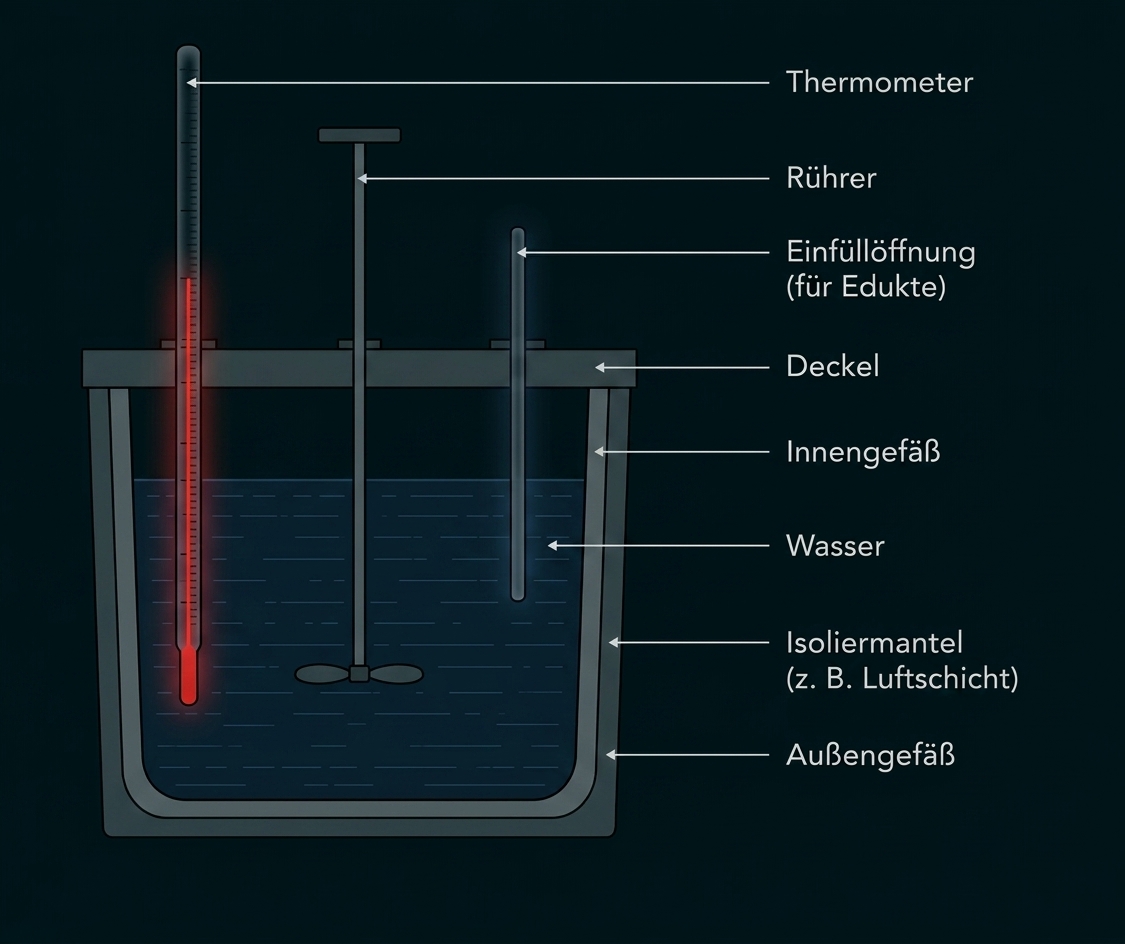
Zwei Voraussetzungen, z.B.:
-
Schneller Ablauf: Die Reaktion sollte schnell ablaufen, damit die Wärmemenge in kurzer Zeit freigesetzt wird, bevor nennenswerte Wärmeverluste an die Umgebung auftreten.
-
Vollständiger Umsatz: Die Reaktion muss möglichst quantitativ (vollständig) ablaufen, damit die gemessene Wärme exakt der Stoffmenge (n) zugeordnet werden kann.
-
Ausreichend große Wärmetönung: Die Reaktion muss eine genügend große Menge an Wärme freisetzen (exotherm) oder aufnehmen (endotherm), um eine messbare Temperaturdifferenz
zu erzeugen.
-
Keine Nebenreaktionen: Es sollten keine unkontrollierten Nebenreaktionen ablaufen, welche das Ergebnis verfälschen.
1. Gegebene Werte:
-
Masse Ammoniumnitrat:
-
Volumen Wasser:
-
Molare Lösungsenthalpie:
-
Spezifische Wärmekapazität Wasser:
-
Molare Masse
:
(aus Tabelle:
)
2. Berechnung der Stoffmenge :
3. Berechnung der aufgenommenen Wärmemenge :
4. Umstellung der Kalorimetergleichung nach :
Die Formel lautet: .
Ergebnis: Die zu erwartende Temperaturdifferenz beträgt ca. (bzw.
). Da der Vorgang endotherm ist, sinkt die Temperatur im Kalorimeter um diesen Betrag.