Aufgabe 3 – Wasser – ein vielseitiger Stoff
Wasser ist einer der wichtigsten Stoffe für den Menschen. Reines Wasser hat unter Standardbedingungen einen -Wert von
Erläutere anhand einer Reaktionsgleichung den Begriff der Autoprotolyse.
Begründe mit Hilfe des Diagramms (siehe Abbildung 1), ob die Autoprotolyse des Wassers exotherm oder endotherm verläuft.
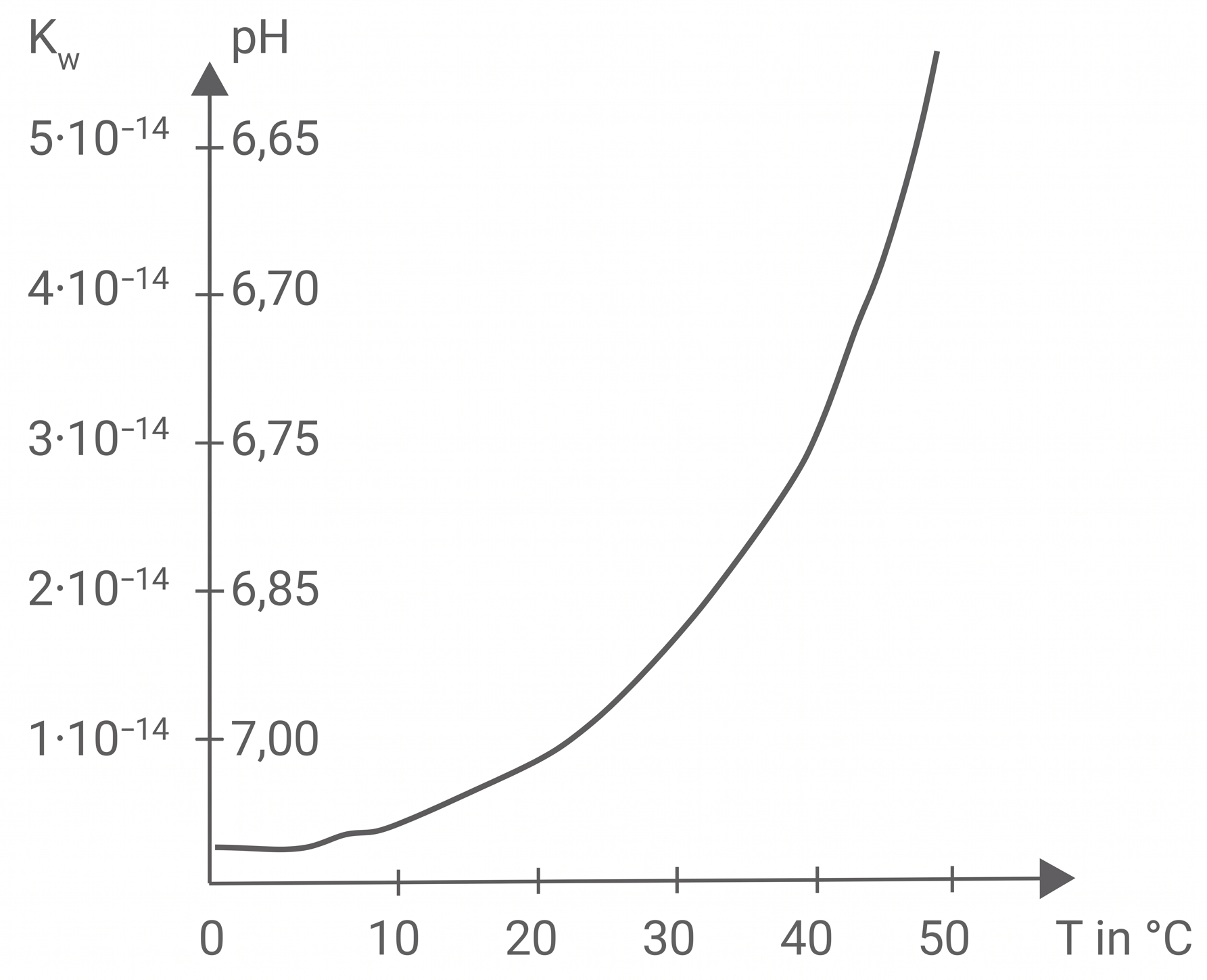
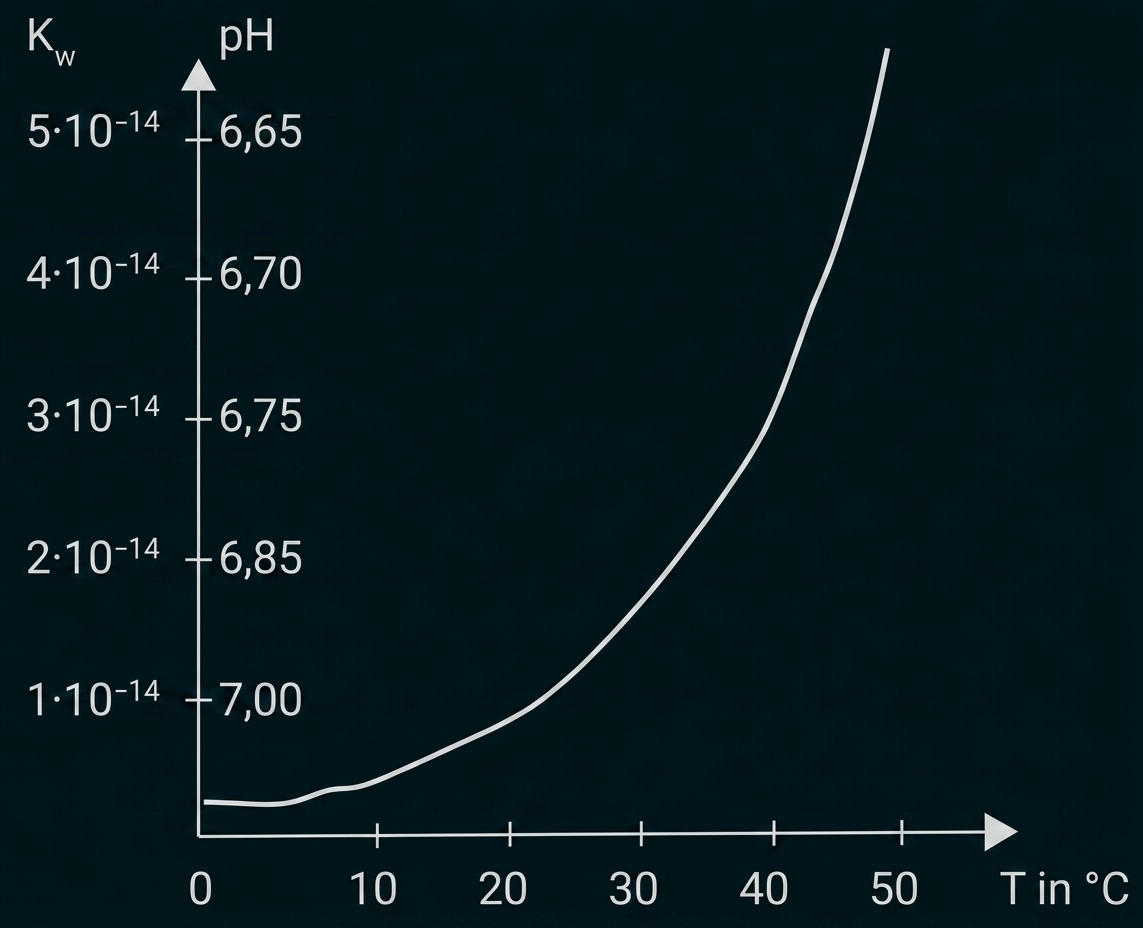
Abbildung 1: Temperaturabhängigkeit des Ionenprodukts von Wasser
Der pH-Wert einer Lösung steigt, wenn
Ammoniak in Wasser eingeleitet wird oder
Calcium mit Wasser reagiert, wobei auch Wasserstoff entsteht.
Begründe diese Aussagen unter Verwendung von Reaktionsgleichungen.
Nenne jeweils die Reaktionsart.
Vergleiche die beiden Reaktionen unter vier Gesichtspunkten.
Berechne die Konzentrationen der Hydroxid- und Hydronium-Ionen in einer Calciumhydroxid-Lösung mit einem -Wert von
Erläutere die Bedeutung des pH-Wertes an zwei Beispielen.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Autoprotolyse: Amphotere Teilchen reagieren mit sich selbst in einer Säure-Base-Reaktion, wobei ein Teilchen der Protonendonator und das andere Teilchen der Protonenakzeptor ist.
Bei etwa beträgt das Ionenprodukt des Wassers
und bei etwa
ist
Da mit zunehmender Temperatur das Ionenprodukt größer wird, handelt es sich bei der Autoprotolyse des Wassers um einen endothermen Vorgang.
Begründen der Aussagen und Nennen der Reaktionsart
Bei der Reaktion mit Wasser entstehen Hydroxid-Ionen, wodurch die Lösung basischer wird und der pH-Wert steigt.
Da sich die Oxidationszahlen nicht ändern, handelt es sich um eine Protolyse, wobei Protonen übertragen werden.
Bei der Reaktion mit Wasser entstehen Hydroxid-Ionen, wodurch die Lösung basischer wird und der pH-Wert steigt.
Die Oxidationszahlen ändern sich. Somit handelt es sich um eine Redoxreaktion, wobei Elektronen übertragen werden.
Vergleichen der beiden Reaktionen
|
Kriterium |
Protolyse |
Redoxreaktion |
|---|---|---|
|
Gemeinsamkeiten Teilchenaustausch |
Teilchen werden zwischen den reagierenden Stoffen ausgetauscht. Es gibt einen Donator (Teilchenabgabe) und einen Akzeptor (Teilchenaufnahme). |
|
|
Unterschiede ausgetauschte Teilchen |
Protonen |
Elektronen |
|
Oxidationszahlen |
ändern sich nicht |
ändern sich |
Hinweis: Es können ebenso andere Kriterien zum Vergleich herangezogen werden, z. B.:
Protonenabgabe = Säurereaktion
Elektronenabgabe = Oxidation
Berechnung der Konzentrationen der Oxonium- und Hydroxid-Ionen
Gesucht:
Gegeben:
Die Konzentration der Oxonium-Ionen beträgt und die Konzentration der Hydroxid-Ionen beträgt
Erläuterung des pH-Werts an Beispielen
-
Blut: konstanter pH-Wert von
für den Sauerstoff- und CO2-Transport
-
Wasser: pH-Wert im neutralen Bereich, damit die Fische atmen können
-
Boden: pH-Wert spezifisch für das Wachstum von Pflanzen
-
Verdauung: Aktivität der Verdauungsenzyme abhängig vom pH-Wert