Aufgabe 4 – Kohlenstoffdioxid und die „Versauerung“ der Meere
In den letzten Jahrzehnten wurde von den Meeren vermehrt Kohlenstoffdioxid aus der Atmosphäre aufgenommen. Dadurch sinkt der pH-Wert des Meerwassers. Diesen Prozess bezeichnet man als „Ozeanversauerung“. Für Organismen, die ihre Schalen und Skelette aus Kalk aufbauen, wie z. B. Muscheln, Schnecken oder Korallen, stellt diese „Ozeanversauerung“ eine Gefährdung dar.
Erkläre die im Modellexperiment genannten Farbveränderungen des Indikators unter Einbeziehung von Reaktionsgleichungen (M 10).
Beschreibe das in Material 11 dargestellte Diagramm.
Begründe das stärkere Absinken des pH-Wertes der Meere im Bereich der Arktis und Antarktis im Vergleich zu anderen Meeresregionen.
Erläutere den Einfluss der sich erwärmenden Meere auf die Erderwärmung.
Beurteile unter Berücksichtigung der Oxonium-Ionen-Konzentrationen den umgangssprachlichen Ausdruck „Das Meerwasser wird also um etwa 150 Prozent saurer werden…“ (M 12).
Gib dazu eine fachwissenschaftlich korrekte Aussage an.
Gib das Prinzip von Le Chatelier wieder.
Erläutere unter Anwendung dieses Prinzips die Auswirkungen einer Erhöhung der Konzentration an gelöstem Kohlenstoffdioxid im Meerwasser auf die genannten Meeresorganismen (M 13).
Berechne den prozentualen Massenanteil an Calciumcarbonat in den untersuchten Muschelschalen (M 14).
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?M 10: Ein Modellexperiment zur „Ozeanversauerung“
In einer Broschüre des Helmholtz-Zentrums für Ozeanforschung in Kiel wird ein Modellexperiment zur Veranschaulichung der „Ozeanversauerung“ beschrieben. Beobachtungen aus dem Versuch lassen sich mit den Prozessen in Verbindung bringen, die zwischen den obersten Wasserschichten der Meere und der Atmosphäre ablaufen.
Das Modell-Experiment läuft wie in der Abbildung dargestellt ab:
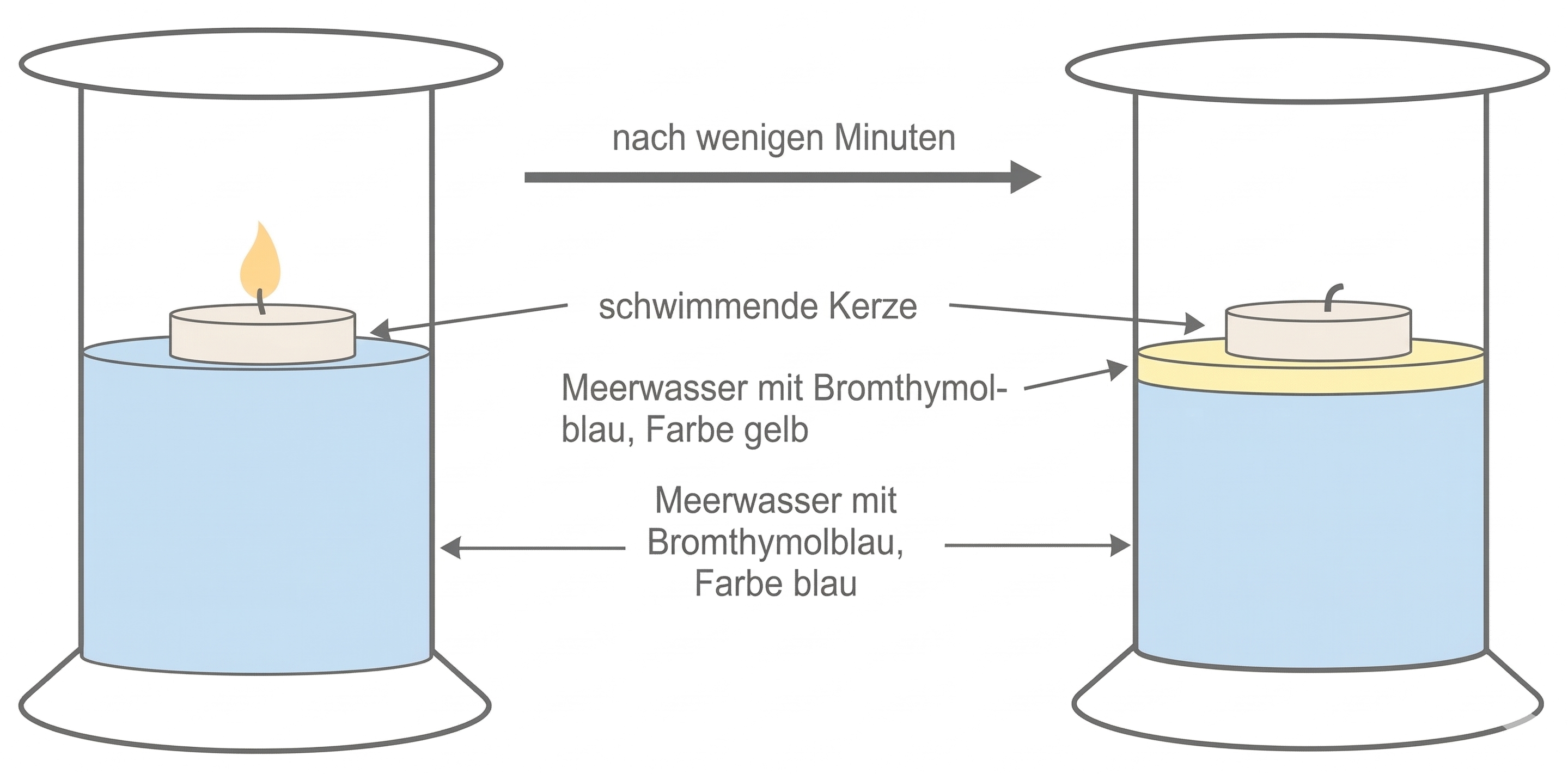
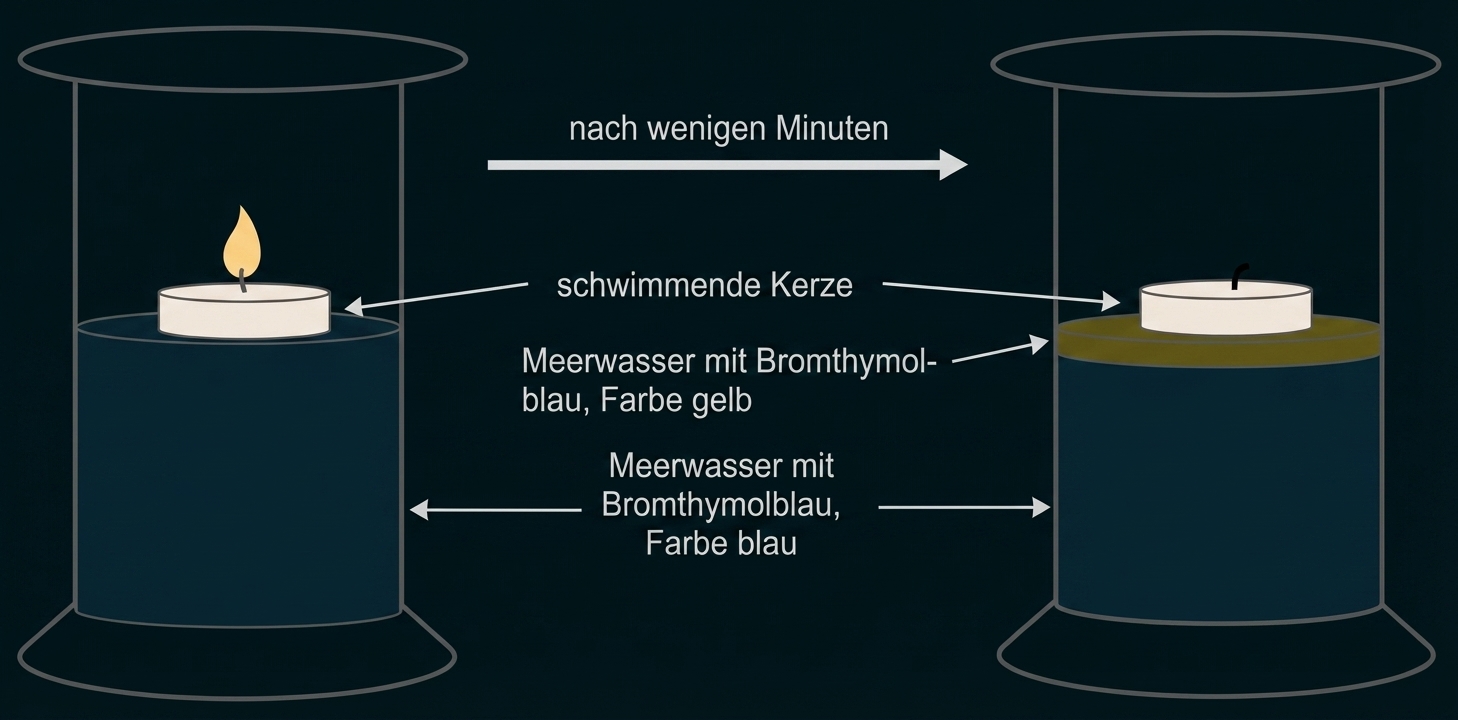
Abb. 2: Ablauf des Experiments
M 11: Die Löslichkeit von Kohlenstoffdioxid in Wasser
Die Ozeane sind die „blauen“ Lungen unseres Planeten. In ihnen lösen sich jährlich mehr als 25 Prozent des weltweit freigesetzten Kohlenstoffdioxids.
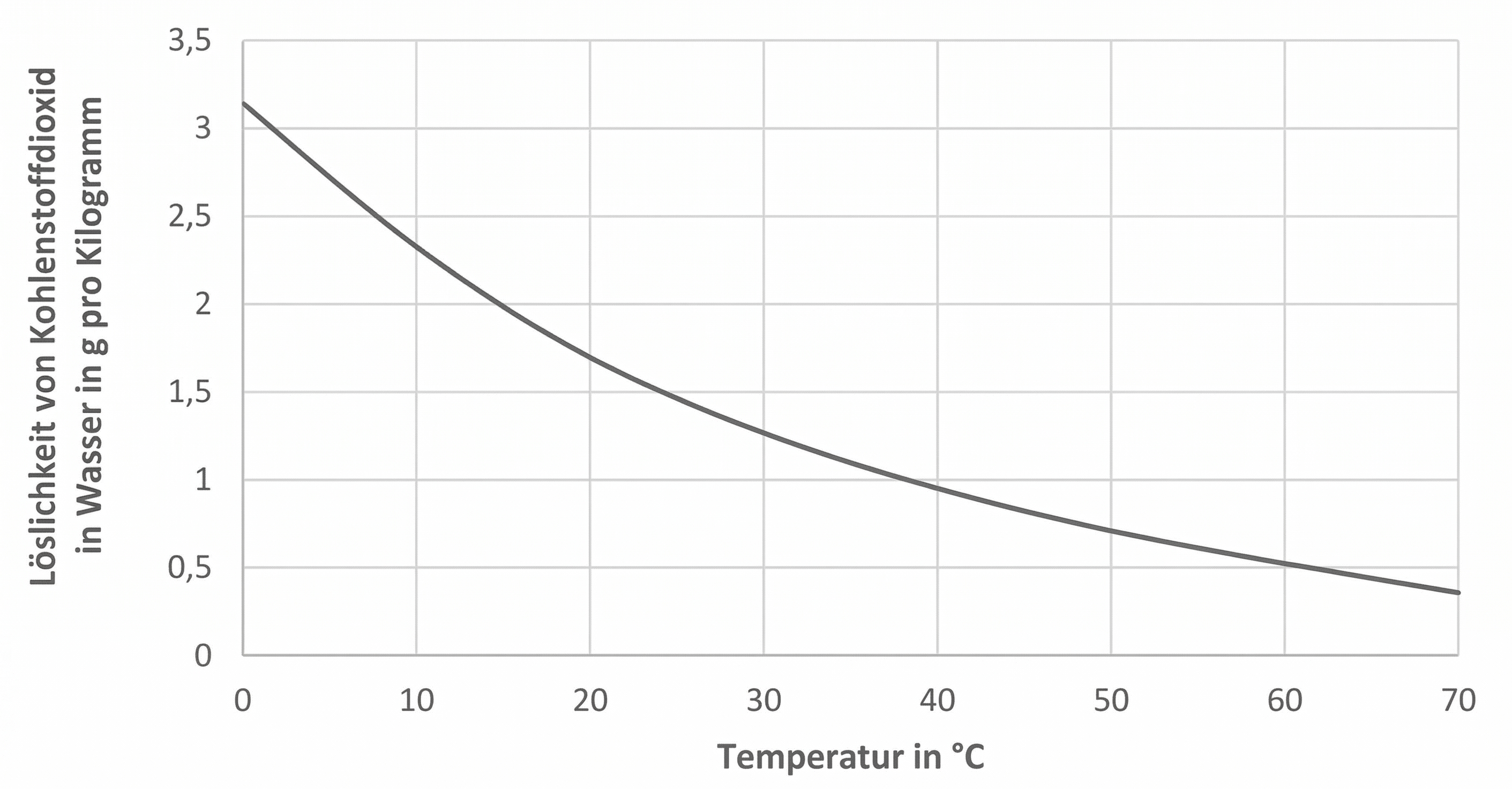
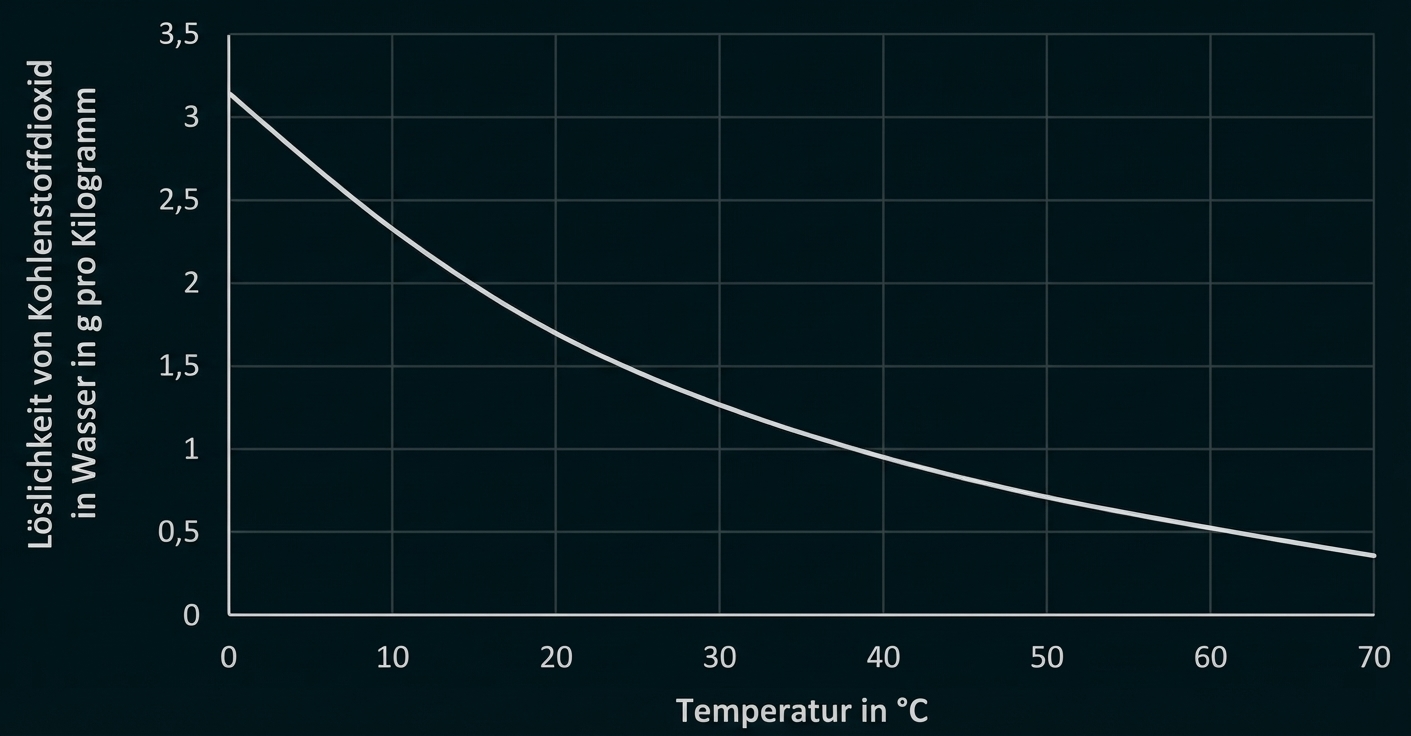
Abb. 3: Temperaturabhängigkeit der Löslichkeit von Kohlenstoffdioxid in Wasser
[4]
M 12: Der Begriff „Versauerung“
Mit einem durchschnittlichen -Wert von derzeit
ist Meerwasser leicht basisch. Bis zum Jahr 2100 wird der
-Wert der Ozeane bei unverminderten Kohlenstoffdioxid-Emissionen voraussichtlich auf einen Wert von
sinken.
In manchen Artikeln findet man dazu nicht selten fachwissenschaftlich zweifelhafte Aussagen wie „Das Meerwasser wird also um etwa 150 Prozent saurer werden…“.
[5]
M 13: Carbonat-Hydrogencarbonat-Gleichgewicht
Der überwiegende Anteil kohlenstoffhaltiger Verbindungen im Ozean liegt in Form von Hydrogencarbonaten und Carbonaten vor. Die Anionen dieser Verbindungen stehen mit dem gelösten Kohlenstoffdioxid und Wasser in einem chemischen Gleichgewicht, das man vereinfachend gemäß folgender Reaktionsgleichung beschreibt:
Im Meer lebende Organismen wie Muscheln, Schnecken, Tintenfische, aber auch bestimmte Korallen nutzen die im Meerwasser vorhandenen Carbonat-Ionen zum Aufbau ihrer Schalen und Skelette.
[6], [7]
M 14: Ein Experiment zur Bestimmung des Calciumcarbonat-Gehalts einer Muschelschale
Muschelschalen bestehen überwiegend aus Calciumcarbonat das mit einer organischen Substanz verkittet ist.
In einem einfachen Schulexperiment soll der Gehalt an Calciumcarbonat in Muscheln aus der Nordsee bestimmt werden. Dazu wird folgender Versuch durchgeführt:
Die Schalen einiger Muscheln werden fein zermahlen und anschließend werden des Muschelschalenpulvers abgewogen.
Nach Zugabe von Salzsäure der Konzentration
hat das enthaltene Calciumcarbonat vollständig reagiert, da keine Gasentwicklung von frei werdendem Kohlenstoffdioxid mehr zu beobachten ist.
Die Reaktion läuft gemäß folgender Reaktionsgleichung ab:
[8]–[10]
Quellen (ggf. verändert):
[4] Hamm, J. (2021, 2. Februar). Löslichkeit von Kohlenstoffdioxid. Chemie.Schule. https://www.chemie.schule/WP/wp03-Mineralwasser/wp03-ab/ab_loeslichkeit_kohlenstoffdioxid_wasser.htm (Zugriff am: 07.12.2023)
[5] Alfred-Wegner-Institut (2022, 16. Dezember). Fakten zur Ozeanversauerung: Saurer ist nicht gleich sauer. AWI. https://www.awi.de/im-fokus/ozeanversauerung/fakten-zur-ozeanversauerung.html (Zugriff am: 31.03.2024)
[6] Der Kohlenstoffkreislauf im Ozean (o. D.). https://bildungsserver.hamburg.de/themenschwerpunkte/klimawandel-und-klimafolgen/klimawandel/treibhausgase/kohlenstoffkreislauf-ozean-artikel-253332 (Zugriff am 18.08.2023)
[7] Altmayer, W. et al. (2012). Salters Chemie: Chemical Storylines. Schülerband. Schroedel.
[8] Musterkristalle in der Muschel (2014, 31. Oktober). MPG. https://www.mpg.de/muschelschale_mikrostruktur (Zugriff am: 23.03.2024)
[9] Biologische Auswirkungen von Ozeanversauerung: Gesellschaftliche Folgen der Ozeanversauerung (o. D.). Bioacid. https://www.bioacid.de/gesellschaftliche-folgen/ (Zugriff am: 23.03.2024)
[10] „Das Meer wird allmählich versauern“ (2017, 11. August). BMBF. https://www.bmbf.de/bmbf/shareddocs/kurzmeldungen/de/das-meer-wird-allmaehlich-versauern.html (Zugriff am: 18.08.2023)
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Reaktionsgleichungen:
-
Das bei der Verbrennung der Kerze freigesetzte Kohlenstoffdioxid-Gas löst sich (teilweise) in der oberen Wasserschicht und reagiert (teilweise) mit Wasser zu Kohlensäure, welche anschließend (teilweise) protolysiert.
-
Dadurch steigt die Konzentration an Oxonium-Ionen in der oberen Wasserschicht und der pH-Wert sinkt, wodurch sich die Farbe des Indikators an der Wasseroberfläche von blau nach gelb verändert.
Beschreibung des Diagramms
-
Im Diagramm wird die Abhängigkeit der Löslichkeit von Kohlenstoffdioxid-Gas in Wasser von der Temperatur dargestellt.
-
Im dargestellten Temperaturbereich nimmt die Löslichkeit von Kohlenstoffdioxid in Wasser (von ca.
Kohlenstoffdioxid pro
Wasser bei
zunächst stark ab,
-
dann im Verlauf weniger stark (bis auf ca.
Kohlenstoffdioxid pro
Wasser bei
ab.
Begründung des stärkeren Absinkens des pH-Wertes in Arktis und Antarktis
-
Im Bereich der Arktis und Antarktis herrschen niedrigere Temperaturen als in anderen Meeresregionen der Welt.
-
Folglich löst sich dort im kälteren Meerwasser auch mehr Kohlenstoffdioxid, was schlussendlich zu einer höheren Konzentration an Kohlensäure bzw. Oxonium-Ionen im Meerwasser führt. Dadurch sinkt der pH-Wert stärker.
Erläuterung des Einflusses auf die Erderwärmung
Durch die Erwärmung der Meere löst sich weniger Kohlenstoffdioxid im Meerwasser. Damit entsteht ein höherer Kohlenstoffdioxidanteil in der Atmosphäre. Weil es sich um ein Treibhausgas handelt, schreitet die Erderwärmung schneller voran.
Beurteilung der Aussage zur „Versauerung“ der Meere
Für die Oxonium-Ionen-Konzentration gilt:
Bei beträgt die Konzentration der Oxonium-Ionen
Bei beträgt die Konzentration der Oxonium-Ionen
Das Verhältnis der beiden Konzentrationen beträgt:
Die Aussage ist folglich nur korrekt, wenn sie auf die Oxonium-Ionen-Konzentration bezogen wird und nicht auf den pH-Wert.
Angeben einer fachwissenschaftlich korrekten Aussage
Die Oxonium-Ionen-Konzentration nimmt um zu.
Angeben des Prinzips von Le Chatelier
Nach dem Prinzip von Le Chatelier weicht ein im Gleichgewicht befindliches System einem äußeren Zwang so aus, dass der Zwang minimiert wird.
Erläutern der Auswirkungen einer erhöhten Kohlenstoffdioxid-Konzentration im Meerwasser
Steigt die Konzentration an Kohlenstoffdioxid, läuft vermehrt die Rückreaktion ab. Die Stoffmengenkonzentration der Carbonat-Ionen sinkt dadurch. Eine geringere Konzentration an Carbonat-Ionen im Meer erschwert in der Folge den Aufbau der Schalen/Skelette
Für die Stoffmenge der verbrauchten Salzsäure gilt:
Für die Stoffmenge des Calciumcarbonats gilt laut der Reaktionsgleichung:
Damit lässt sich die Stoffmenge des Calciumcarbonats berechnen:
Mit der molaren Masse von Calciumcarbonat kann nun die Masse des Calciumcarbonats berechnet werden:
Die Muschelschalen bestehen zu aus Calciumcarbonat.