Aufgabe 3 – β-Alanin
β-Alanin gehört zu nicht proteinogenen Aminosäuren und ist die einzige natürlich vorkommende Aminosäure ihrer Art. Die Struktur von β-Alanin zeigt die Abbildung 1:
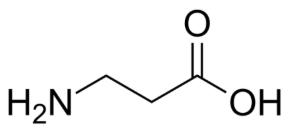
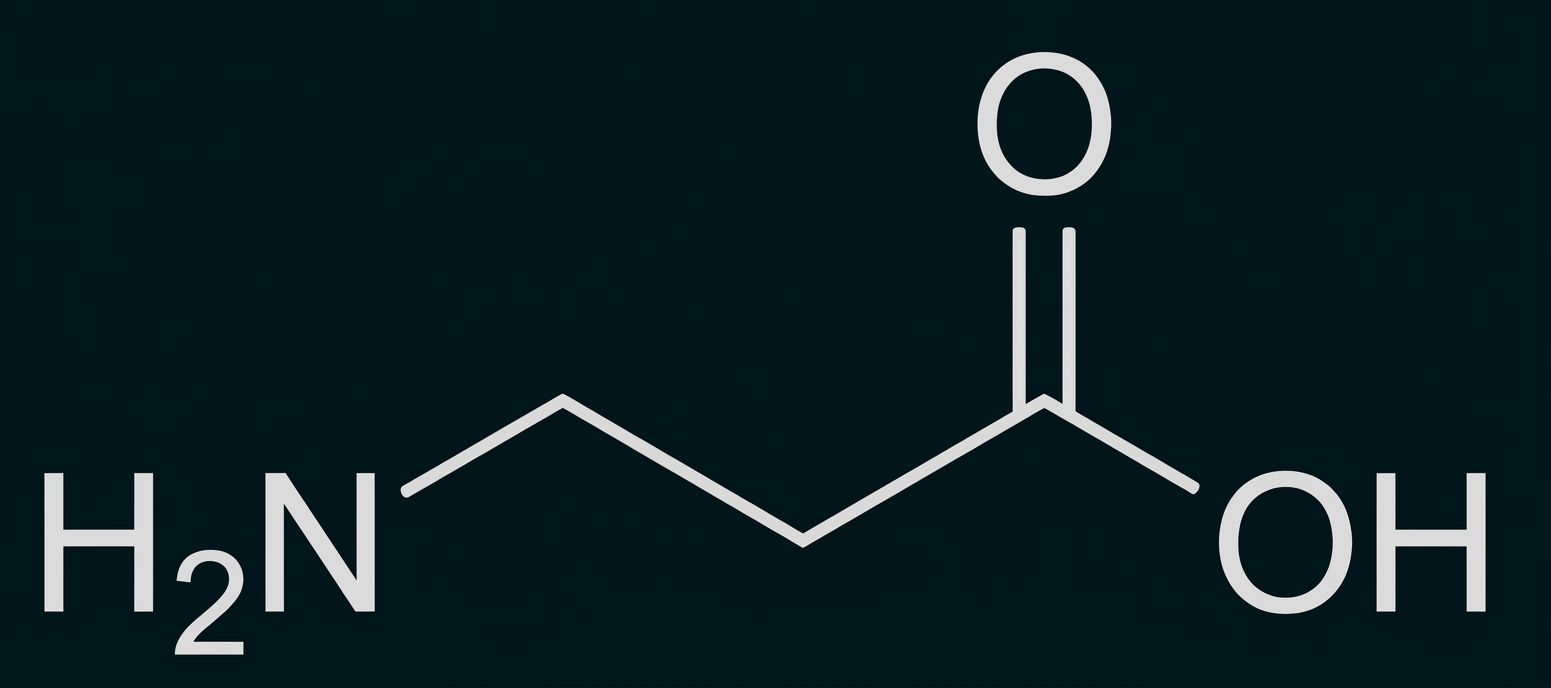
Abb. 1: Strukturformel von β-Alanin
Benenne die charakteristischen funktionellen Gruppen in β-Alanin.
Leite zwei Eigenschaften von β-Alanin anhand seiner Struktur ab.
Vergleiche die Struktur von β-Alanin mit der Struktur der proteinogenen Aminosäure 𝛼-Alanin in zwei Aspekten.
Proteinogene Aminosäuren können Enzyme bilden, die zu wichtigen Katalysatoren gehören.
Erläutere die Wirkungsweise und nenne die Merkmale eines Katalysators.
Zeichne ein Energie-Diagramm, indem du für eine Reaktion mit Katalysator und ohne Katalysator den Energieverlauf grafisch darstellst.
Die Enzyme sind Proteine und weisen eine komplexe Struktur auf.
Beschreibe die verschiedenen Strukturebenen der Proteine.
Nenne die Bindungsart und die Wechselwirkungen, die diese Strukturebenen ermöglichen.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Charakteristische funktionelle Gruppen in -Alanin
Anhand der Strukturformel lassen sich zwei wesentliche funktionelle Gruppen identifizieren:
-
Aminogruppe (
): Diese Gruppe befindet sich am
-C-Atom der Kohlenstoffkette.
-
Carboxygruppe (auch Carboxylgruppe,
): Diese Gruppe ist charakteristisch für organische Säuren.
Ableitung von Eigenschaften aus der Struktur
Aus dem Bau des Moleküls lassen sich folgende physikalische und chemische Eigenschaften ableiten:
-
Zwitterionenbildung und hoher Schmelzpunkt:
-
Da das Molekül sowohl eine saure Carboxygruppe als auch eine basische Aminogruppe besitzt, findet eine intramolekulare Protonenübertragung statt.
-
Es bildet sich ein Zwitterion (
).
-
Die starken elektrostatischen Anziehungskräfte (Ionenbindung) im Kristallgitter führen dazu, dass
-Alanin bei Raumtemperatur ein Feststoff mit einem vergleichsweise hohen Schmelzpunkt ist.
-
-
Gute Wasserlöslichkeit:
-
Die polaren funktionellen Gruppen (
und
) bzw. die Ladungen des Zwitterions können Wasserstoffbrückenbindungen oder Dipol-Ion-Wechselwirkungen mit Wassermolekülen eingehen.
-
Aufgrund dieser hohen Polarität ist der Stoff gut in dem polaren Lösungsmittel Wasser löslich.
-
-
Amphoterer Charakter:
-
Aufgrund der beiden unterschiedlichen funktionellen Gruppen kann
-Alanin sowohl als Säure (Protonendonator) als auch als Base (Protonenakzeptor) reagieren, abhängig vom pH-Wert der Umgebung.
-
Vergleich von -Alanin und
-Alanin
Der strukturelle Vergleich lässt sich in den folgenden zwei wesentlichen Aspekten zusammenfassen:
-
Position der Aminogruppe:
-
Bei
-Alanin ist die Aminogruppe (
) am zweiten Kohlenstoffatom (dem
-C-Atom), also direkt benachbart zur Carboxygruppe, gebunden.
-
Bei
-Alanin hingegen ist die Aminogruppe am dritten Kohlenstoffatom (dem
-C-Atom) positioniert, wodurch die funktionellen Gruppen durch eine zusätzliche
-Gruppe getrennt sind.
-
-
Chiralität und optische Aktivität:
-
-Alanin besitzt ein asymmetrisches Kohlenstoffatom (
), an dem vier verschiedene Reste gebunden sind (
,
,
,
). Es ist daher chiral und optisch aktiv.
-
-Alanin besitzt kein chirales Zentrum, da alle Kohlenstoffatome in der Kette mindestens zwei identische Bindungspartner (Wasserstoffatome) aufweisen. Es ist somit achiral.
-
Merkmale eines Katalysators
Ein Katalysator ist ein Stoff, der eine chemische Reaktion beeinflusst, ohne dabei dauerhaft verbraucht zu werden. Zu seinen wesentlichen Merkmalen gehören:
-
Herabsetzung der Aktivierungsenergie: Er ermöglicht einen neuen Reaktionsweg mit geringerem Energiebedarf.
-
Erhöhung der Reaktionsgeschwindigkeit: Die Reaktion läuft bei gleicher Temperatur deutlich schneller ab.
-
Unveränderbarkeit: Nach der Reaktion liegt der Katalysator chemisch unverändert wieder vor.
-
Keine Beeinflussung des Gleichgewichts: Die Lage des chemischen Gleichgewichts bleibt unverändert; es wird lediglich schneller erreicht.
-
Spezifität (bei Enzymen): Biokatalysatoren weisen eine hohe Substrat- und Wirkungsspezifität auf.
Wirkungsweise eines Katalysators
Die Wirkungsweise basiert auf der Veränderung des Reaktionsmechanismus:
-
Der Katalysator bildet mit den Edukten (bei Enzymen: Substraten) einen energetisch instabilen Übergangszustand oder einen Enzym-Substrat-Komplex.
-
Dieser Zwischenschritt erfordert eine wesentlich geringere Aktivierungsenergie (
) als der direkte Weg der Edukte zum Produkt.
-
Nach der Umwandlung wird das Produkt freigesetzt und der Katalysator steht für einen neuen Zyklus zur Verfügung.
Energiediagramm
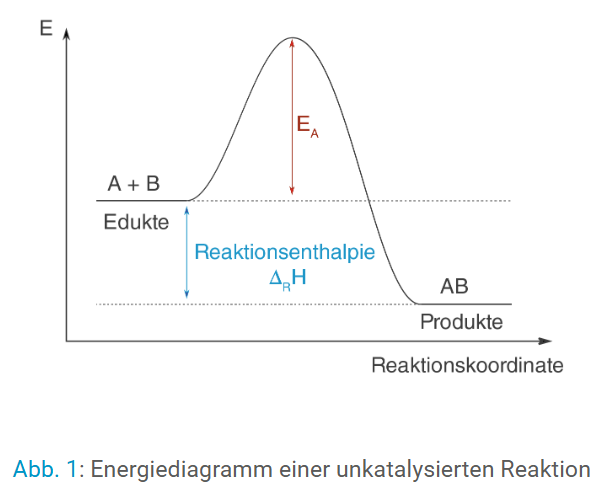
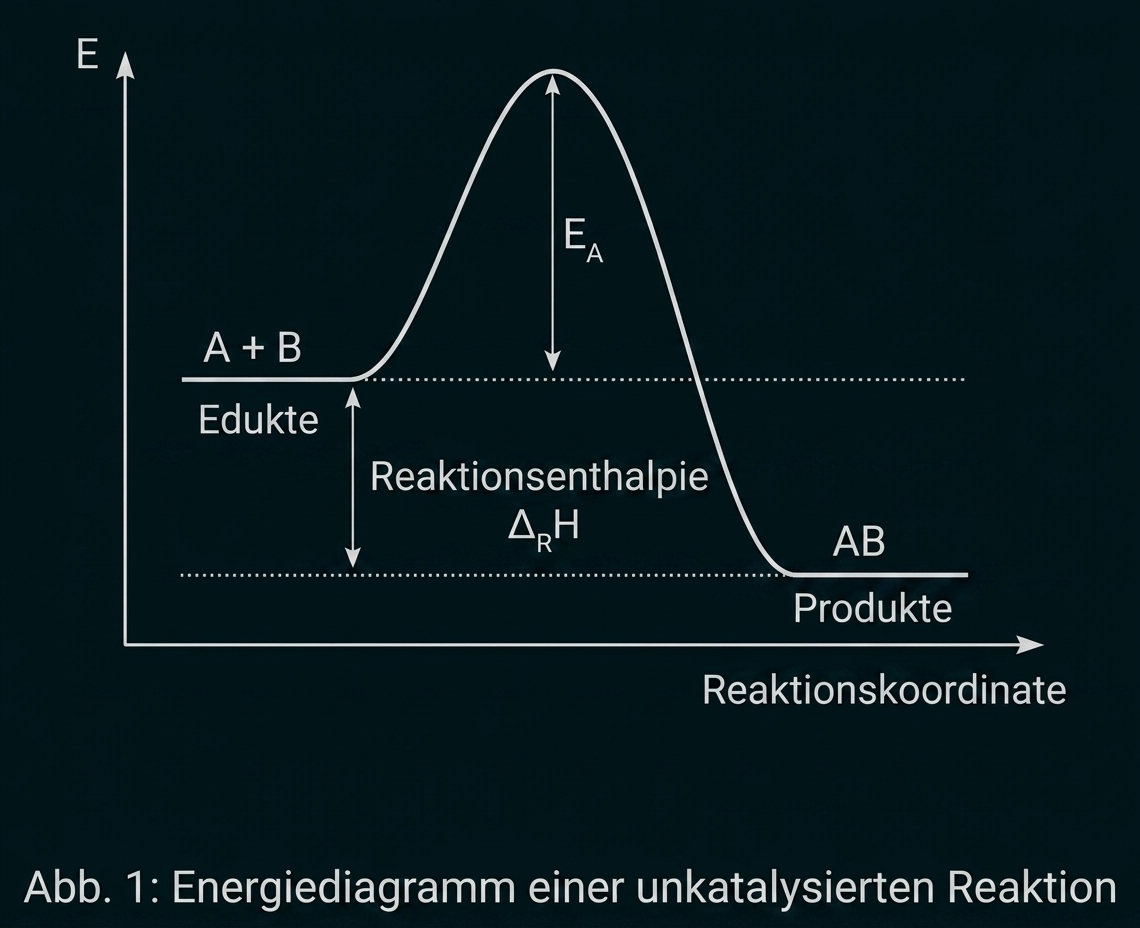
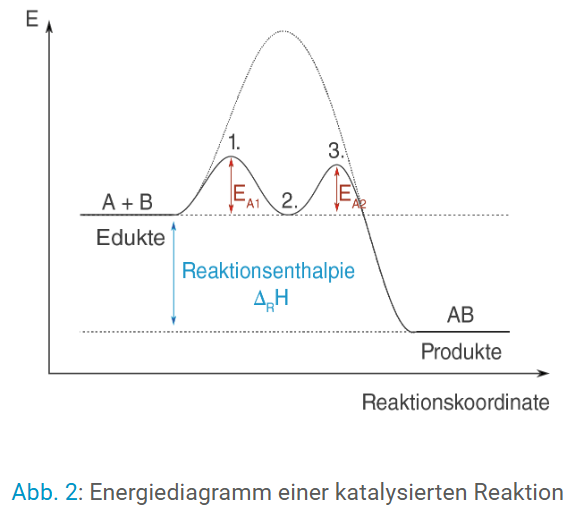
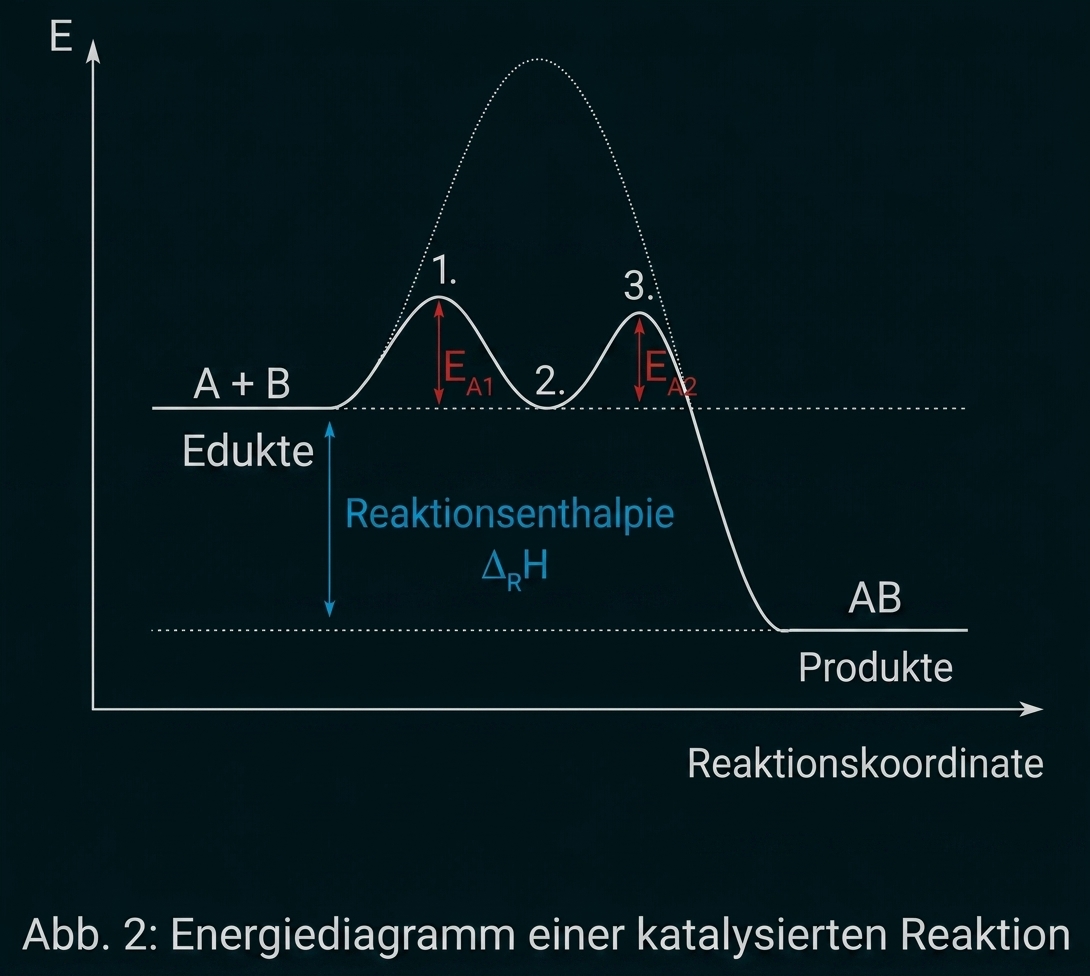
Mit:
-
EA → Aktivierungsenergie
-
→ Reaktionsenthalpie
Strukturebenen der Proteine
Proteine weisen eine komplexe, in vier Ebenen unterteilte Struktur auf, die ihre spezifische Funktion als Enzyme bestimmt.
-
Primärstruktur:
-
Beschreibung: Dies ist die exakte Abfolge (Sequenz) der einzelnen Aminosäuren in einer Polypeptidkette.
-
Bindungsart: Die Aminosäuren sind über kovalente Peptidbindungen miteinander verknüpft.
-
-
Sekundärstruktur:
-
Beschreibung: Lokale räumliche Anordnung der Polypeptidkette in regelmäßige Strukturen. Die häufigsten Formen sind die
-Helix (schraubenförmig) und das
-Faltblatt (zickzackförmig).
-
Wechselwirkung: Diese Strukturen werden maßgeblich durch Wasserstoffbrückenbindungen zwischen den Carbonyl-Gruppen (
) und den Amino-Gruppen (
) des Peptidrückgrats stabilisiert.
-
-
Tertiärstruktur:
-
Beschreibung: Die vollständige, unregelmäßige räumliche Faltung der gesamten Polypeptidkette zu einer stabilen, meist globulären (kugelförmigen) Gestalt.
-
Bindungen/Wechselwirkungen: Die Stabilisierung erfolgt durch Wechselwirkungen zwischen den Resten (Seitenketten) der Aminosäuren:
-
Van-der-Waals-Kräfte (hydrophobe Wechselwirkungen).
-
Wasserstoffbrückenbindungen.
-
Ionenbeziehungen (Salzbrücken).
-
Disulfidbrücken (kovalente Bindungen zwischen Cystein-Resten).
-
-
-
Quartärstruktur:
-
Beschreibung: Räumliche Anordnung von zwei oder mehr eigenständigen Polypeptidketten (Untereinheiten), die zusammen ein funktionelles Protein bilden.
-
Wechselwirkungen: Die Untereinheiten werden durch die gleichen zwischenmolekularen Kräfte wie bei der Tertiärstruktur (v. a. Wasserstoffbrücken, Ionenbeziehungen und hydrophobe Wechselwirkungen) zusammengehalten.
-