Aufgabe 2 – Rost und Wärmepflaster
Formuliere die Elektronenkonfiguration des Eisenatoms und leite die zwei häufigsten Oxidationsstufen des Eisens ab.
Eisen- und Stahlkonstruktionen werden mit der Zeit durch den Rostvorgang beschädigt.
Erkläre mit Hilfe einer Skizze die ablaufenden Vorgänge bei der Sauerstoffkorrosion des Eisens.
Erläutere das Wesen der Reaktionsart.
Begründe, dass ein Zinküberzug vor Korrosion schützt.
Im Wärmepflaster wird durch chemische Reaktionen über einen längeren Zeitraum Wärme abgegeben. Die Inhaltsstoffe Eisen, Aktivkohle, Wasser und Kochsalz reagieren miteinander, wenn durch Entfernen der Schutzfolie Sauerstoff an die Ausgangsstoffe gelangt. In der folgenden Abbildung sind die Vorgänge vereinfacht dargestellt.
Interpretiere diese Abbildung 1.
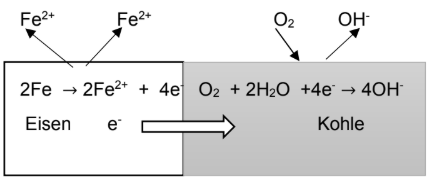
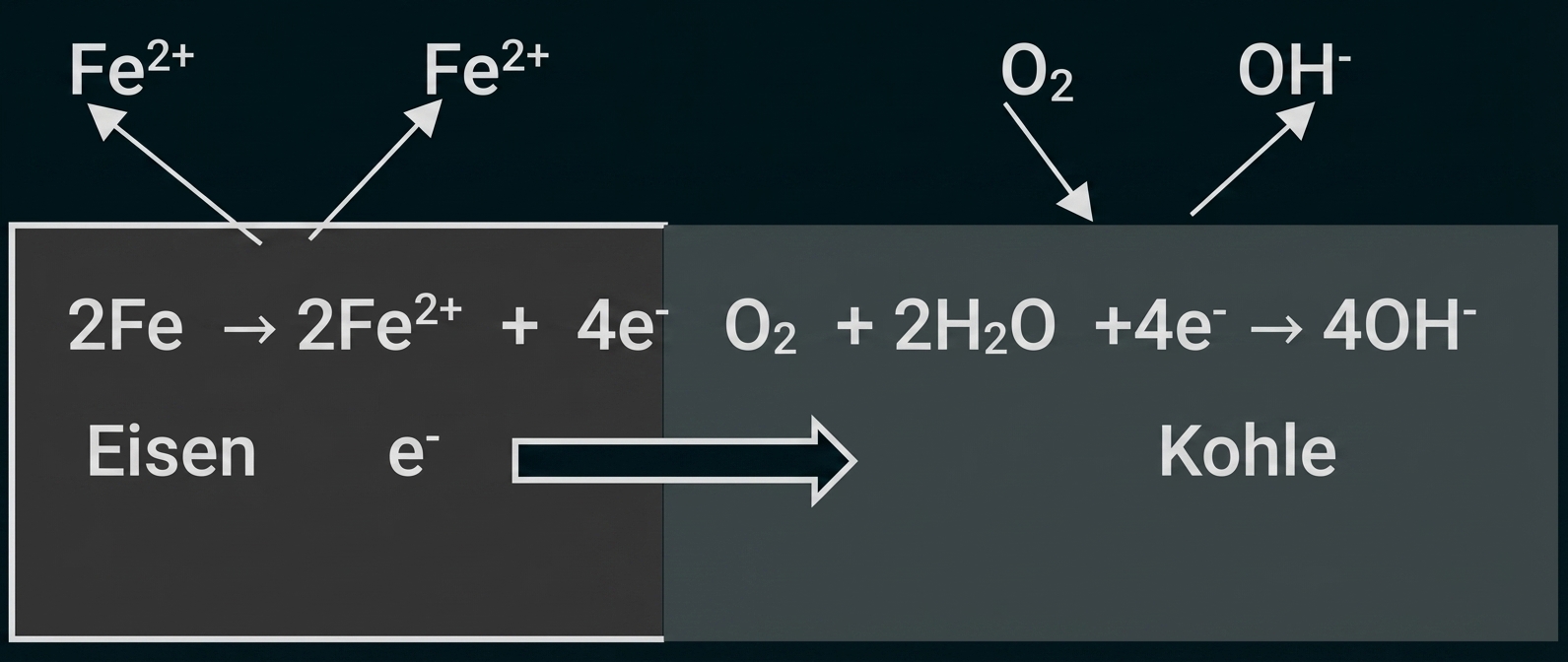
Abb.1
Kochsalz (Natriumchlorid) ist nur zu ca. 1 % enthalten, darauf verzichten kann man jedoch nicht.
Nenne die Rolle des Kochsalzes bei diesen Reaktionen.
Vergleiche die Vorgänge des Rostens und die im Wärmepflaster miteinander.
Berechne die Reaktionsenthalpie, wenn 20 Gramm Eisen mit Sauerstoff vereinfachter Weise vollständig zu Eisen(III)-oxid reagieren.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Formulierung der Elektronenkonfiguration:
-
Vollständige Schreibweise:
-
Edelgasschreibweise (verkürzt):
Ableitung der zwei häufigsten Oxidationsstufen:
Die Oxidationsstufen ergeben sich aus der energetischen Stabilität der resultierenden Elektronenkonfigurationen bei der Abgabe von Elektronen. Wichtig ist hierbei die Regel, dass bei den Nebengruppenelementen die Elektronen des äußersten Energieniveaus () zuerst abgegeben werden.
-
Oxidationsstufe +II (
):
-
Ableitung: Das Eisenatom gibt die zwei Elektronen des
-Orbitals ab.
-
Konfiguration:
.
-
-
Oxidationsstufe +III (
):
-
Ableitung: Zusätzlich zu den zwei
-Elektronen wird ein weiteres Elektron aus dem
-Orbital abgegeben.
-
Konfiguration:
.
-
Begründung: Die
-Konfiguration entspricht einer halb besetzten d-Unterschale. Dieser Zustand ist energetisch besonders stabil (Symmetrie und minimierte Elektronenabstoßung).
-
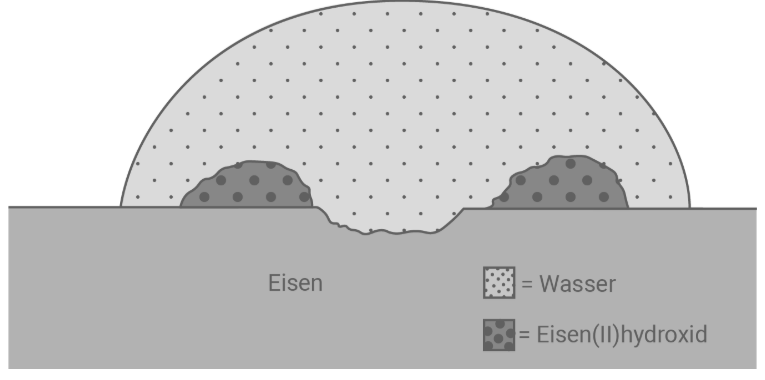
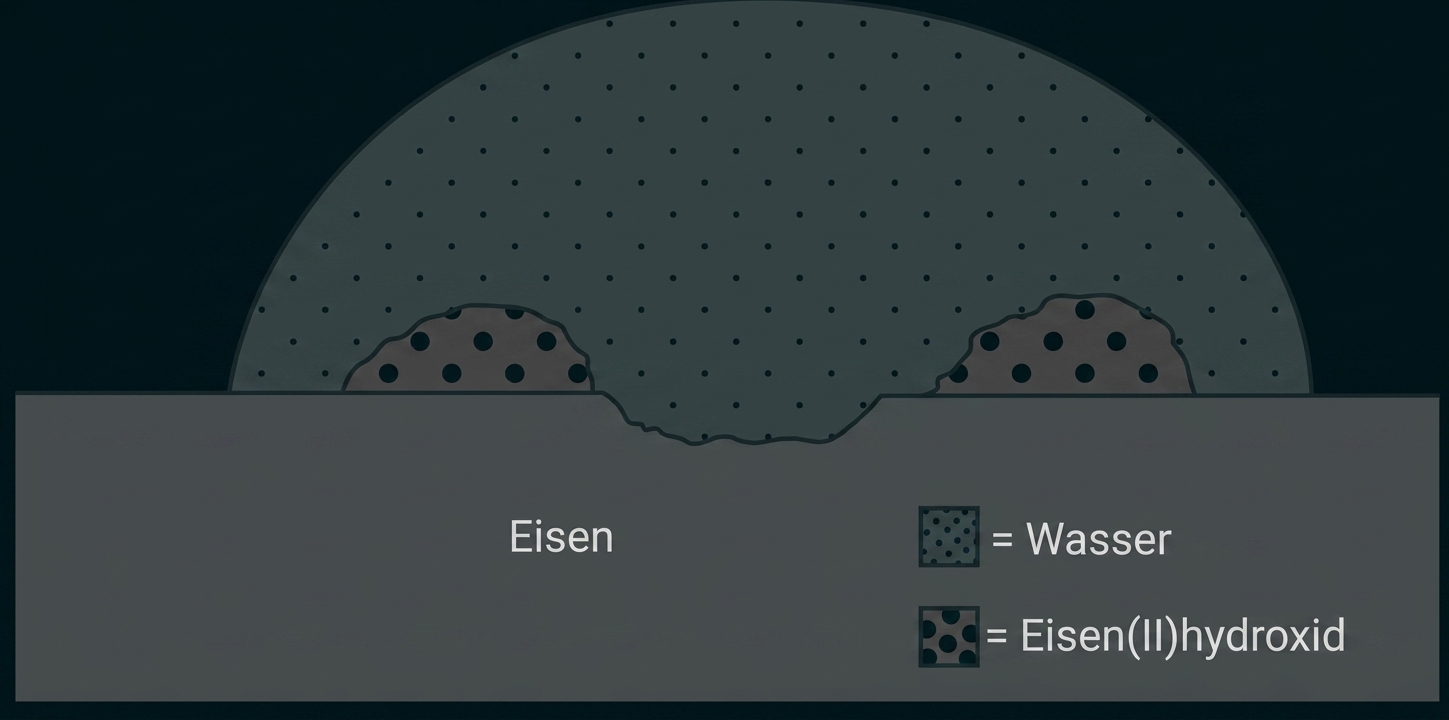
Erklärung der ablaufenden Vorgänge anhand einer Skizze
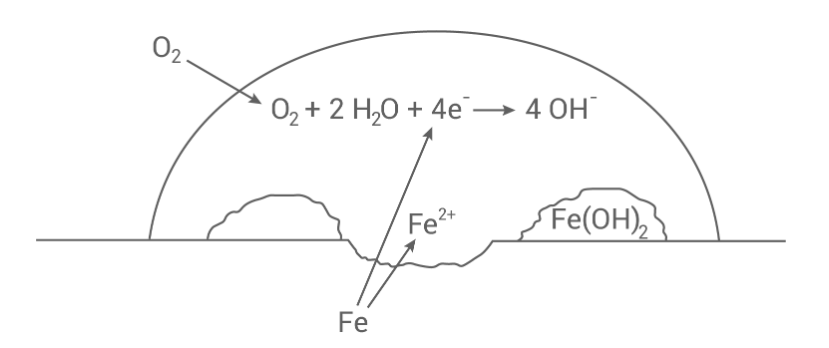
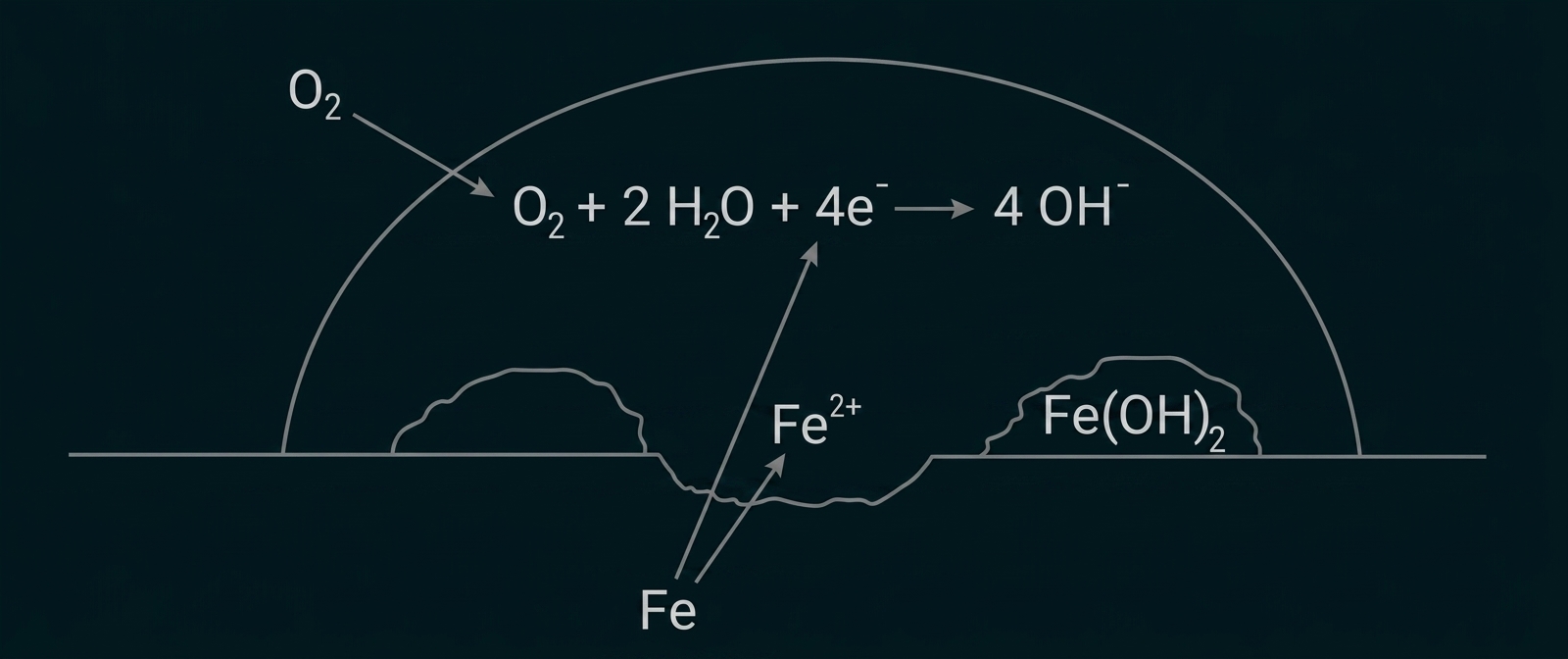
-
Anodischer Bereich (Oxidation): An einer Fehlstelle des Metalls gehen Eisenatome als Ionen in Lösung. Die Elektronen verbleiben im Metall.
-
Kathodischer Bereich (Reduktion): An einer anderen Stelle (oft verunreinigt durch edlere Metalle oder Kohlenstoff) reagiert der im Wasser gelöste Sauerstoff mit den herangewanderten Elektronen und Wasser zu Hydroxid-Ionen.
-
Folgereaktion: Die
-Ionen und
-Ionen diffundieren zueinander und bilden Eisen(II)-hydroxid, das durch weiteren Sauerstoff zu Hydratisierten Eisen(III)-oxiden (Rost) weiterreagiert.
Wesen der Reaktionsart:
-
Es handelt sich um eine Redoxreaktion.
-
Das Wesen dieser Reaktion ist der Elektronenübergang vom Reduktionsmittel (Eisen) auf das Oxidationsmittel (Sauerstoff).
-
Da die Teilreaktionen (Oxidation und Reduktion) räumlich getrennt ablaufen, spricht man von einem elektrochemischen Vorgang.
Begründung des Korrosionsschutzes durch Zink
Der Schutz durch einen Zinküberzug (Verzinken) beruht auf zwei Mechanismen:
-
Abschirmung (Passivierung): Zink bildet an der Luft eine dichte Oxid- bzw. Carbonatschicht aus, die das darunterliegende Metall vor direktem Kontakt mit Sauerstoff und Wasser schützt.
-
Opferanode (Kathodischer Korrosionsschutz): Laut der Tabelle der Standardelektrodenpotenziale hat Zink ein negativeres Potenzial
als Eisen
-
Wird die Zinkschicht beschädigt, bildet sich ein Lokalelement, in dem Zink als das unedlere Metall die Anode bildet und oxidiert wird.
-
Das Eisen wird dadurch zur Kathode und bleibt vor Oxidation geschützt, solange noch Zink vorhanden ist.
-
Interpretation der Abbildung 1: Vorgänge im Wärmepflaster
Die Abbildung verdeutlicht, dass das Wärmepflaster wie eine kurzgeschlossene galvanische Zelle (Lokalelement) funktioniert, bei der chemische Energie direkt in Wärmeenergie umgewandelt wird.
Analyse der Teilbereiche:
-
Anodischer Prozess (Eisen-Bereich):
-
Das Eisen fungiert als Anode.
-
Hier findet die Oxidation statt: Eisenatome geben Elektronen ab und werden zu Eisen(II)-Ionen (
) oxidiert.
-
Reaktionsgleichung:
.
-
-
Elektronenleitung:
-
Die freigesetzten Elektronen (
) fließen durch den direkten Kontakt vom Eisen zur Aktivkohle (angedeutet durch den dicken Pfeil).
-
-
Kathodischer Prozess (Kohle-Bereich):
-
Die Aktivkohle dient aufgrund ihrer großen Oberfläche als Kathode und stellt den Ort für die Reduktion bereit.
-
Hier findet die Reduktion statt: Luftsauerstoff (
), der nach Entfernen der Schutzfolie eindringt, reagiert mit Wasser (
) und den zugeführten Elektronen zu Hydroxid-Ionen (
).
-
Reaktionsgleichung:
.
-
Zusammenfassung der Interpretation: Das Wärmepflaster nutzt die kontrollierte Sauerstoffkorrosion von Eisenpulver. Die Aktivkohle beschleunigt diesen Prozess massiv, indem sie eine große Oberfläche für die Sauerstoffreduktion bietet. Da die Reaktion insgesamt stark exotherm ist, wird die dabei freiwerdende Reaktionsenthalpie als Nutzwärme abgegeben.
Die Rolle des Kochsalzes ()
Obwohl Kochsalz nur zu ca. 1% enthalten ist, übernimmt es eine essenzielle Funktion für den Ablauf der Reaktion:
-
Elektrolyt: In Verbindung mit dem enthaltenen Wasser bildet das Salz eine elektrisch leitfähige Lösung.
-
Ionentransport: Die gelösten Ionen ermöglichen den Ladungsausgleich zwischen dem anodischen (Eisen) und dem kathodischen Bereich (Kohle). Ohne diesen Elektrolyten käme der Elektronenfluss und damit die Wärmeproduktion sofort zum Erliegen.
Vergleich: Rosten vs. Wärmepflaster
|
Merkmal |
Natürliches Rosten |
Wärmepflaster |
|
Gemeinsamkeit |
Beides sind elektrochemische Redoxreaktionen mit Sauerstoff als Oxidationsmittel. |
Beides sind exotherme Prozesse. |
|
Geschwindigkeit |
Verläuft meist langsam über Jahre hinweg. |
Verläuft beschleunigt und intensiv über Stunden. |
|
Oberfläche |
Reaktion an der kompakten Metalloberfläche. |
Reaktion von fein verteiltem Eisenpulver und Aktivkohle (hohe Oberfläche). |
|
Zielsetzung |
Unerwünschte Korrosion (Schädigung). |
Nutzwärmeabgabe (gewollte Reaktion). |
Berechnung der Reaktionsenthalpie ()
Gegeben: ;
. Vereinfachte Reaktion zu Eisen(III)-oxid (
):
1. Berechnung der molaren Standardreaktionsenthalpie ():
Man nutzt die Bildungsenthalpien aus dem Anhang. Für Elemente im Standardzustand () gilt
.
(bezogen auf den Stoffumsatz laut Gleichung).
2. Berechnung der eingesetzten Stoffmenge Eisen ():
3. Berechnung der Gesamtwärme ():
Laut Gleichung beziehen sich die auf den Umsatz von
Eisen.
Ergebnis: Bei der vollständigen Reaktion von Eisen wird eine Wärmemenge von ca.
frei (
).