Aufgabe 2 – Silber aus Lehm: Aluminium
Aluminium ist mit circa 7,57 % nach Sauerstoff und Silicium das dritthäufigste Element der Erdkruste. Hier kommt es in Verbindungen, niemals in reiner Form vor.
Beschreibe den Aufbau des Aluminiumkristalls auf Teilchenebene.
Erkläre daran vier charakteristische Eigenschaften der Stoffklasse.
Beschrifte die Skizze, übernimm dazu die Zahlen in deine Arbeit (M 4).
Formuliere die Reaktionsgleichungen für:
die Teilreaktionen an den Elektroden,
die Gesamtreaktion der Schmelzflusselektrolyse.
Nenne den systematischen Namen von Kryolith.
Erkläre den Aufbau der Verbindung Kryolith sowie die Struktur und die chemische Bindung im negativ geladenen Teilchen (M 4).
Berechne den Energiebedarf für die gesamte Jahresproduktion an Aluminium und die jährliche Einsparung an Energie durch Recycling (M 4, M 5).
Beurteile die Verwendung von Recyclingaluminium aus ökonomischer und ökologischer Sicht.
Formuliere für alle möglichen Reaktionen an den Elektroden die Reaktionsgleichungen (M 6).
Bestimme die Abscheidungspotentiale und berechne die Zersetzungsspannung (M 7).
Nach dem Abschalten des Stroms ist eine elektrische Spannung nachweisbar.
Erkläre diese Beobachtung.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?M 4: Schmelzflusselektrolyse
1859 gelang dem französischen Chemiker Devill der entscheidende Schritt zur technischen Lösung der Aluminiumelektrolyse durch Elektrolyse eines Gemisches aus Natriumaluminiumchlorid und Kryolith In der Gegenwart gewinnt man Aluminium in Aluminiumhütten in zwei Schritten:
Im Bayerverfahren wird aus reiner Tonerde (Aluminiumoxid) Aluminium gewonnen.
Im Hall-Héroult-Prozess, einer Schmelzflusselektrolyse von Aluminiumoxid, wird reines Aluminium hergestellt. Das Lösungsmittel Kryolith erhöht die Leitfähigkeit sowie die Stromausbeute und senkt die Badtemperatur von auf
Sauerstoff reagiert mit der Graphit-Elektrode zu Kohlenstoffdioxid. Kohlenstoffdioxid reagiert mit dem Graphit weiter zu Kohlenstoffmonooxid.
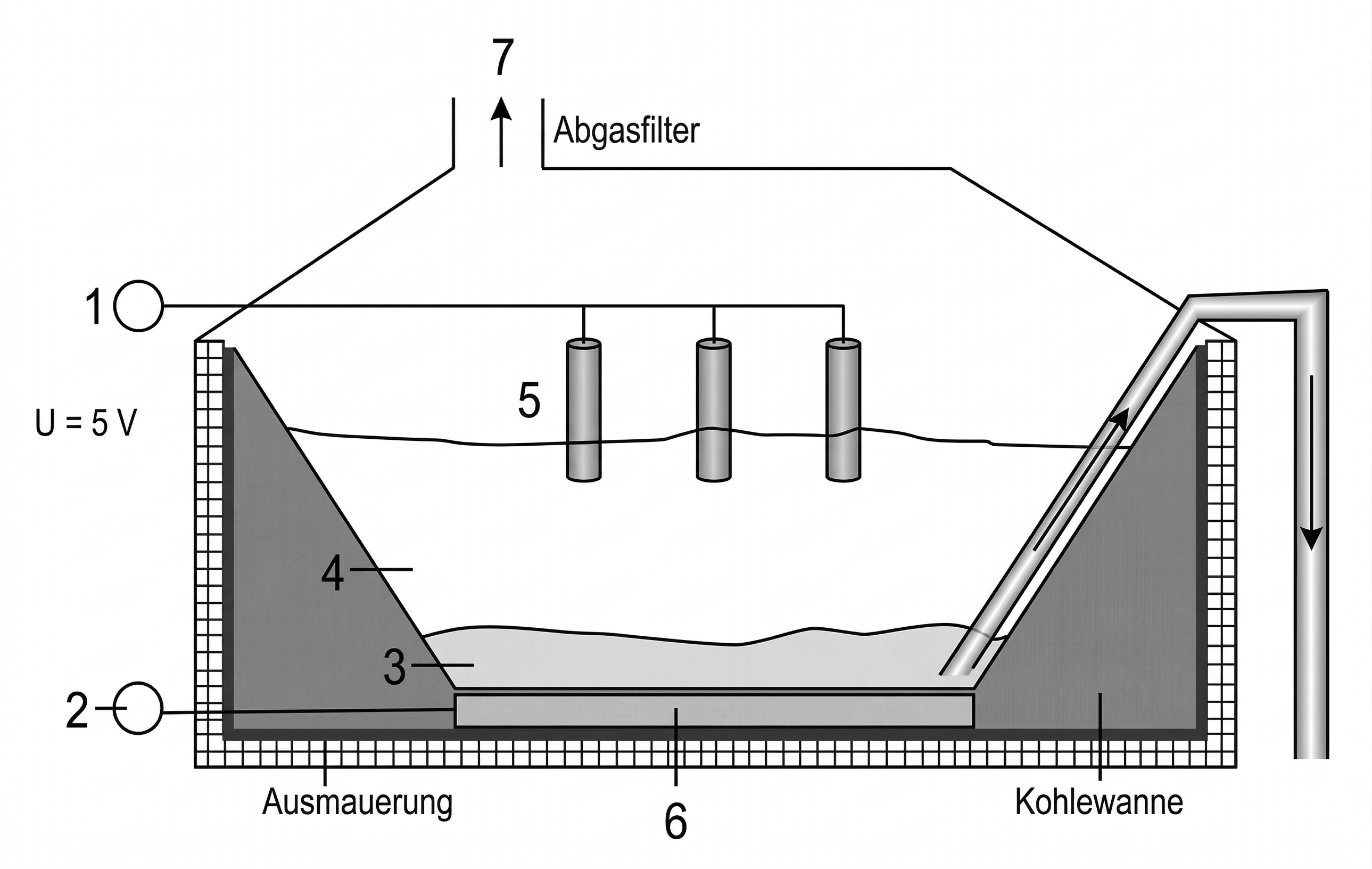
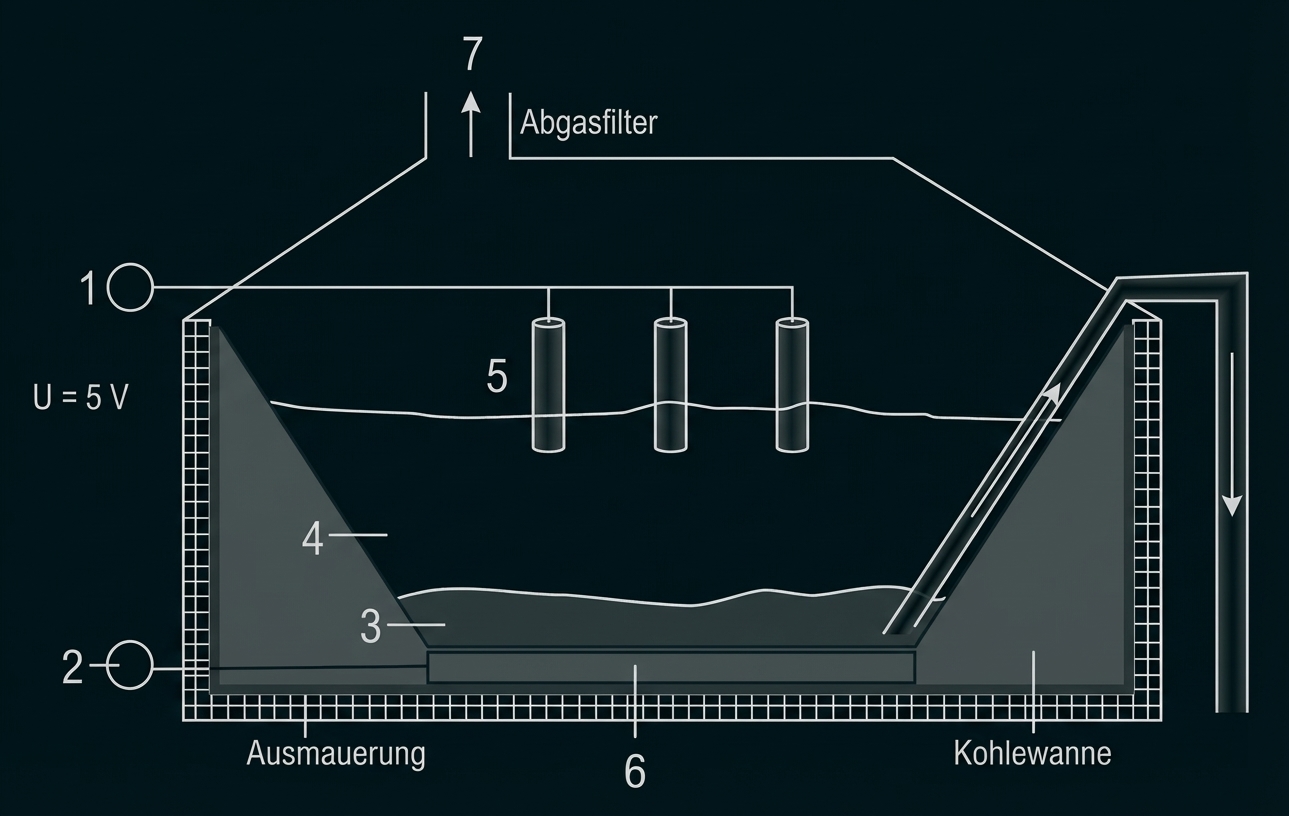
Abb. 4: Schema der Schmelzflusselektrolysezelle zur Aluminiumgewinnung
M 5: Produktionszahlen
Jährlich werden 58 Millionen Tonnen Aluminium produziert. Dazu kommen noch 16 Millionen Tonnen Recyclingaluminium aus Altmetall. Die Stromausbeute beträgt 90 %. Aluminium lässt sich ohne Qualitätsverlust in den Werkstoffkreislauf integrieren. Der Energiebedarf für die Rohmetallgewinnung von Aluminium aus Altmetall beträgt nur 5 % gegenüber der Herstellung aus Aluminiumoxid, da der Schmelzpunkt
beträgt. Neben der Energieeinsparung wird auch die CO2-Emission pro Tonne Aluminium um
gesenkt.
M 6: Gedankenexperiment
Eine Aluminiumchlorid-Lösung soll elektrolysiert werden. Es werden Graphitelektroden verwendet, der pH-Wert der Elektrolyt-Lösung liegt im sauren Bereich.
Geräte: U-Rohr, Kabel, Krokodilklemmen, Stromversorgungsgerät, Spannungsmessgerät, 2 Graphitelektroden
Nach wenigen Minuten wird das Stromversorgungsgerät abgeschaltet und dafür das Spannungsmessgerät angeschlossen (Überspannungen werden vernachlässigt).
M 7: Standardelektrodenpotenziale
Tab. 2: Standardelektrodenpotenziale (bei
|
Element/ Verbindung |
oxidierte Form |
reduzierte Form |
|
|
Aluminium |
|
|
|
|
Chlor |
|
|
|
|
Wasserstoff |
|
|
|
|
Sauerstoff |
|
|
|
|
Sauerstoff |
|
|
|
|
Wasserstoff |
|
|
|
Die Standardelektrodenpotenziale sind alphabetisch geordnet.
[2]
Quellen (ggf. verändert):
[2] ERBRECHT, R., et al. Das große Tafelwerk: Formelsammlung für die Sekundarstufe I und II. 1st ed. Berlin: Volk und Wissen, 1999. ISBN 3-06-020760-7.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Beschreibung des Aufbaus des Aluminiumkristalls
Das Metall Aluminium ist aus Aluminium-Atomen aufgebaut, die regelmäßig angeordnet sind. Da die Außenelektronen nur schwach gebunden sind, können sie sich im Gitter frei bewegen. Die delokalisierten Elektronen werden als Elektronengas, die entstehenden positiv geladenen Metall-Ionen als Metallrümpfe bezeichnet. Zwischen den Metall-Ionen und den frei beweglichen Elektronen wirken starke elektrostatische Anziehungskräfte, die Metallbindung.
Erklären der Eigenschaften der Stoffklasse der Metalle
-
mechanisch verformbar: Wirkt eine Kraft auf das Metallgitter, so können die Gitterebenen aneinander vorbeigleiten.
-
elektrisch leitfähig: Legt man eine Spannung an, wandern die frei beweglichen Elektronen zum Pluspol, der elektrische Strom fließt.
-
metallischer Glanz: Die frei beweglichen Elektronen werden durch die Energie des Lichts angeregt und strahlen es sogleich wieder ab. Es wird reflektiert und die Metalle erscheinen glänzend.
-
wärmeleitfähig: Die Übertragung von Wärme erfolgt durch Stöße der freibeweglichen Elektronen auf die Atomrümpfe.
Beschriften der Skizze
|
1 |
Pluspol |
|
2 |
Minuspol |
|
3 |
flüssiges Aluminium |
|
4 |
Kryolith-Aluminium-Schmelze |
|
5 |
Graphitanode |
|
6 |
Graphitkathode |
|
7 |
Abgase |
Formulieren der Reaktionsgleichungen der Schmelzflusselektrolyse von Aluminiumoxid
|
Kathode (−): |
|
|
Anode (+): |
|
|
Folgereaktionen: |
|
|
Gesamtreaktion: |
|
Kathode (−):
Anode (+):
Folgereaktionen:
Gesamtreaktion:
Nennen des systematischen Namens von Kryolith
ist Natriumhexafluoridoaluminat.
Erklären des Aufbaus von Kryolith und der Struktur des Anions
Es ist ein Ionenkristall, bestehend aus einem Kation und einem Komplexanion
Zwischen ihnen herrscht eine Ionenbindung (elektrostatische Anziehungskräfte zwischen entgegengesetzt geladenen Ionen). Das negativ geladene Komplex-Ion besteht aus einem Zentral-Ion
und den Liganden
Die Koordinationszahl
gibt die Anzahl der Liganden an.
Alle Fluorid-Ionen besitzen nichtbindende Elektronenpaare, mit denen sie sich am Zentral-Ion anlagern, so dass Elektronenpaarbindungen entstehen. Hierbei handelt es sich um koordinative Bindungen.
Berechnung des Energiebedarfs und der jährlichen Einsparung
gegeben:
Stromausbeute
gesucht:
Pro Tonne:
Die Gewinnung von einer Tonne Aluminium aus Altmetall benötigt nur der Energie gegenüber der Herstellung aus Aluminiumoxid:
Für 16 Mio. Tonnen:
Gesamt:
Einsparung durch Recycling pro Tonne:
Für 16 Mio. Tonnen:
Beurteilung der Verwendung von Recyclingaluminium
z. B.: Verwendung von Recyclingaluminium reduziert die Kohlenstoffdioxid-Emission im Jahr um etwa Dadurch wird die Umwelt geschützt und die Erderwärmung bzw. der Klimawandel weniger vorangetrieben.
Aufgrund der Senkung des Energiebedarfs werden Rohstoffe eingespart. Auch das trägt zum Umweltschutz bei, da der Abbau der Rohstoffe reduziert werden kann. Ökonomisch bedeutet es eine Kostensenkung.
Formulieren der möglichen Reaktionsgleichungen an den Elektroden
|
Kathode (−): |
|
|
|
Anode (+): |
|
|
Kathode (−):
Anode (+):
Bestimmen der Abscheidungspotentiale und Berechnen der Zersetzungsspannung
Mithilfe der Nernst-Gleichung lassen sich die Abscheidungspotentiale bestimmen:
Bei gilt:
Für die Zersetzungsspannung gilt:
Erklären der Beobachtung nach Abschalten des Stroms
Nach dem Abschalten der Spannungsquelle ist eine Spannung nachweisbar, weil sich während der Elektrolyse eine Galvanische Zelle aufgebaut hat. Die Donatorzelle ist eine Wasserstoffzelle, die Akzeptorzelle eine Chlorzelle. Der Strom fließt von der Donator- zur Akzeptorzelle.