Aufgabe 5 – Kaliumchlorid
Kaliumchlorid spielt als medizinischer Wirkstoff eine Rolle. Er wird u. a. als Mittel gegen Kaliummangel eingesetzt. Außerdem ist das Salz in zahlreichen Medikamenten als Zusatzstoff enthalten, wie z. B. in isotonischen Lösungen, die als Tropf verabreicht werden. Weiterhin dient es in der Lebensmittelindustrie als Lebensmittelzusatz E 508 zur Geschmacksverstärkung und in der Landwirtschaft als Kalidünger.
Erläutere den Aufbau des Kaliumchlorid-Kristalls.
Erkläre ausführlich das Lösungsverhalten von Kaliumchlorid in Wasser und Benzin (Hauptbestandteil Heptan).
Fertige mit den Werten aus Tabelle 1 ein Diagramm an und interpretiere diesen Sachverhalt.
Tabelle 1: Löslichkeit verschiedener Salze in
|
Temperatur in |
|
|
|
|---|---|---|---|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Berechne die Masse von Kaliumchlorid, die man bei in
Wasser geben muss, damit eine gesättigte Lösung entsteht.
Das Salz Kaliumchlorid kann man u. a. aus Sylvin (ein Erz aus Kaliumchlorid und Natriumchlorid) gewinnen.
Beschreibe ein mögliches Experiment zur Gewinnung von Kaliumchlorid aus Sylvin.
Eine Kaliumchlorid-Schmelze und eine Kaliumchlorid-Lösung werden elektrolysiert.
Formuliere die Reaktionsgleichungen an Graphitelektroden und die Gesamtgleichungen.
Erkläre die unterschiedlichen Reaktionsprodukte.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Erläuterung des Aufbaus des Kaliumchlorid-Kristalls
Kaliumchlorid ist ein Ionenkristall, in dem die Atome sehr regelmäßig angeordnet sind. Es wirken elektrostatische Anziehungskräfte zwischen Kalium-Kationen und Chlorid-Anionen. Der Kristall ist als Ganzes elektrisch neutral.
Erklärung des Lösungsverhaltens in Wasser und Benzin
Es gilt: Ähnliches löst sich in Ähnlichem.
In Wasser löst sich Kaliumchlorid sehr gut:
-
Wassermoleküle sind kleine Dipolmoleküle
-
An Ecken und Kanten des Kristalls lagern sich Wassermoleküle entsprechend der Ionenladung mit der entgegengesetzten Partialladung an die Ionen, setzen die Anziehungskräfte zwischen den Ionen herab und lösen sie aus dem Kristall heraus (Hydratation)
In Benzin dagegen löst sich Kaliumchlorid nicht:
-
Benzin besteht aus unpolaren Kohlenwasserstoffen
-
Salze (wie Kaliumchlorid) sind hingegen ionische Verbindungen
Anfertigen eines Diagramms
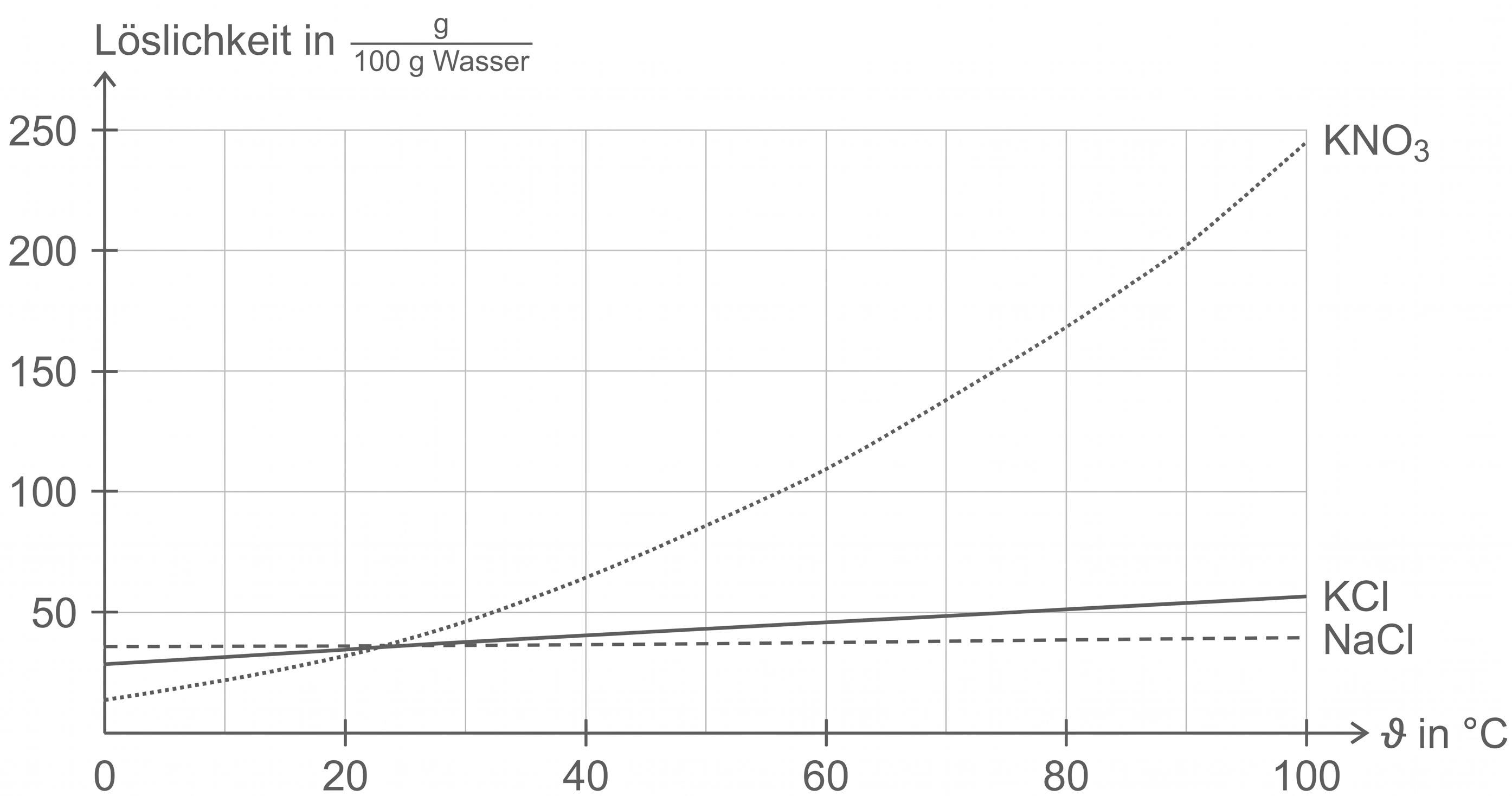
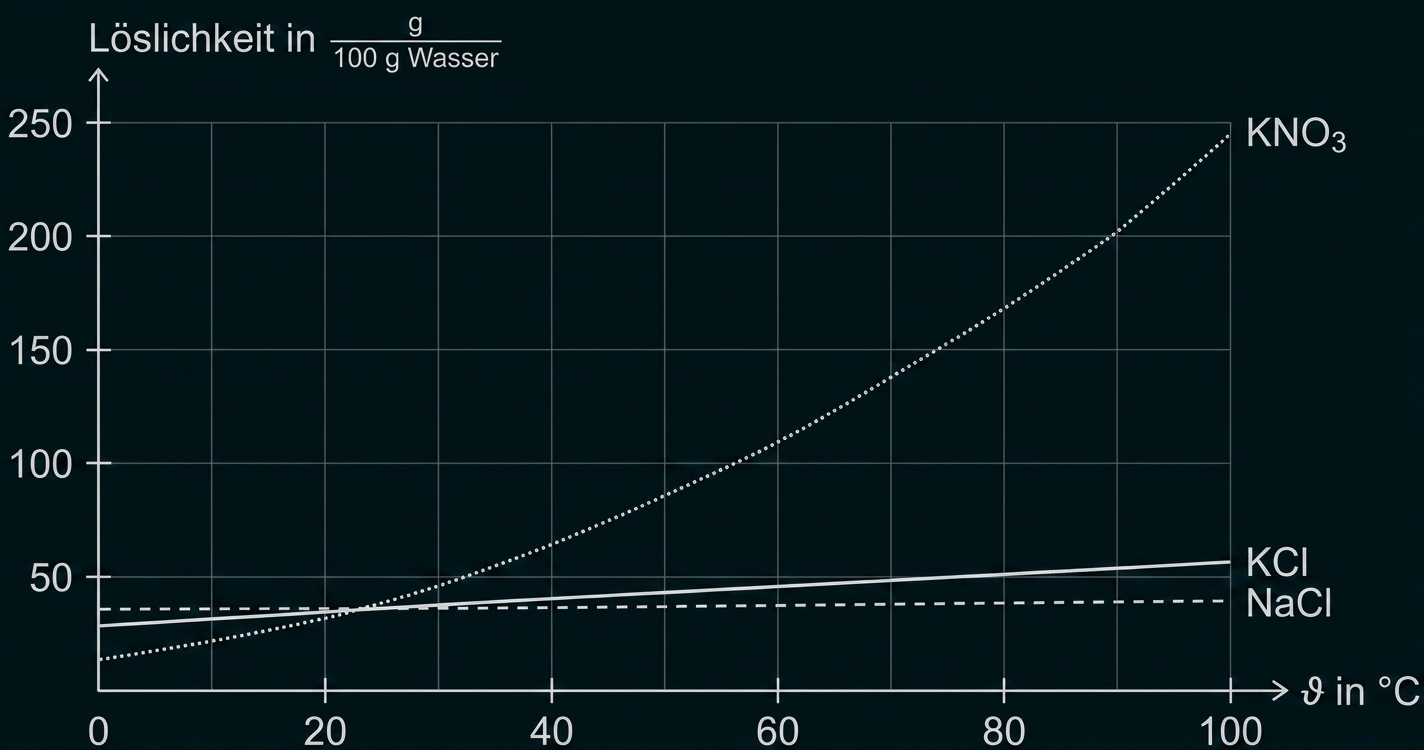
Interpretation des Diagramms
Die Löslichkeit der drei Salze bei unterschiedlichen Temperaturen ist verschieden. Die Löslichkeit von Natriumchlorid ist kaum temperaturabhängig, während sie bei Kaliumchlorid bei höheren Temperaturen leicht größer ist. Bei Kaliumnitrat nimmt die Löslichkeit deutlich mit steigender Temperatur zu.
Die Löslichkeit von bei
beträgt
Wasser entsprechen
Somit ergibt sich für die Masse an Kaliumchlorid:
Bei muss man
Kaliumchlorid in
Wasser geben, um eine gesättigte Lösung herzustellen.
Wenn man Sylvin bei hohen Temperaturen in Wasser löst und die Lösung abkühlen lässt, fällt Kaliumchlorid zuerst aus, da seine Löslichkeit mit sinkender Temperatur leicht abnimmt. Die Löslichkeit von Natriumchlorid hingegen hängt kaum von der Temperatur ab.
Formulieren der Reaktionsgleichungen
Kaliumchlorid-Schmelze:
|
(−) Kathode: |
|
|
(+) Anode: |
|
|
Gesamtreaktion: |
|
Kaliumchlorid-Lösung:
|
(−) Kathode: |
|
|
(+) Anode: |
|
|
Gesamtreaktion: |
|
Erklärung der unterschiedlichen Elektrolyseprodukte
Es läuft immer die Reaktion mit der kleinsten Zersetzungsspannung ab. Die theoretische Zersetzungsspannung von Wasser beträgt wohingegen sie für eine Kaliumchlorid-Schmelze unter Standardbedingungen
betragen würde. Somit würde in einer Kaliumchlorid-Lösung nur Wasser elektrolysiert werden.