Aufgabe 1 – Wasser – das Molekül des Lebens
Wasser gibt es zumindest rein rechnerisch genug auf der Erde. Das ist wichtig, denn ohne Wasser ist kein Leben auf der Erde denkbar. Doch Wasser ist nicht immer nur ein Lebensbringer.
Zeichne die Lewis-Formel von Wasser und erläutere mit deren Hilfe die Bindungsverhältnisse im Molekül sowie die räumliche Anordnung des Moleküls.
Beschreibe den Lösungsvorgang von Natriumchlorid in Wasser auf der Teilchenebene und aus energetischer Sicht
Erkläre die Abhängigkeit der Dichte von der Temperatur mithilfe des Teilchenmodells (M 2).
Erkläre mit Hilfe der Reaktionskinetik und mit der Dichte das Absterben der Zellen bei niedrigen bzw. sehr niedrigen Temperaturen (M 2).
Stelle eine begründete Hypothese für die Verwendung von Trehalose als Frostschutzmittel in lebenden Organismen auf (M 1, M 3).
Nenne den Prozess, der bei Proteinen zum Funktionsverlust führt.
Stelle eine begründete Hypothese für die Verwendung von Trehalose als Schutzmittel gegen die Austrocknung in lebenden Organismen auf (M 1, M 3).
Zeichne die Strukturformel eines beliebigen Fettes.
Erläutere mit der Struktur der Fette die geringe Löslichkeit in Wasser sowie die veränderte Löslichkeit der Spaltprodukte in lebenden Organismen (d. h. bei (M 1).
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?M 1: Wasser als chemische Grundlage
Wasser ist für das Leben auf der Erde unabdingbar. Es ist der Lebensraum für viele Organismen und bildet den Hauptbestandteil der Zellen. Das Wasser kann sogar bis zu 85 % der Zelle ausmachen. In den Zellen dient Wasser als Lösungsmittel für Salze (z. B. Natriumchlorid), Nährstoffe (z. B. für Aminosäuren und Proteine), aber auch als Ausgangsstoff, Produkt und Reaktionsraum für die Reaktionen des Stoffwechsels. Für die mehrzelligen Organismen hat Wasser eine weitere Bedeutung als Transportmittel, da es die benötigten Stoffe zu den Zellen und Abfallprodukte zu den Ausscheidungsorganen befördert.
Nicht alle Stoffe, die dem Organismus bzw. der Zelle gelöst vorliegen müssen, sind auch wasserlöslich. Ein typisches Beispiel sind die Fette, die als Reserve- und Nährstoffe auftreten. Diese werden entweder durch bestimmte Hilfsproteine gelöst bzw. emulgiert oder vorher ganz mithilfe von Wasser aufgespalten. Die Organismen sind bestrebt, ihren Wasservorrat aufrechtzuerhalten, was nicht immer möglich ist. Insbesondere Organismen, die Wasser als Lebensraum nutzen, wurden während der Evolution genötigt, Strategien zu entwickeln, wie sie dem Wassermangel oder gar der Austrocknung begegnen können. Bei Wasserverlust verlieren die Proteine die Hydrathülle, was zur Verklumpung und dem Verlust der räumlichen Struktur und Funktionsfähigkeit führt. Als Folge würden die Zellen und Organismen absterben.
Doch Wasser kann für einen Organismus auch zur Gefahr werden. Das zeigt sich insbesondere bei niedrigen Temperaturen, also bei Frost. Hier sind die Zellen auf Strategien angewiesen, wie sie den Gefahren, die von Wasser ausgehen, wirksam ausweichen können.
M 2: Dichte des Wassers
Tab. 1: Dichte des Wassers
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
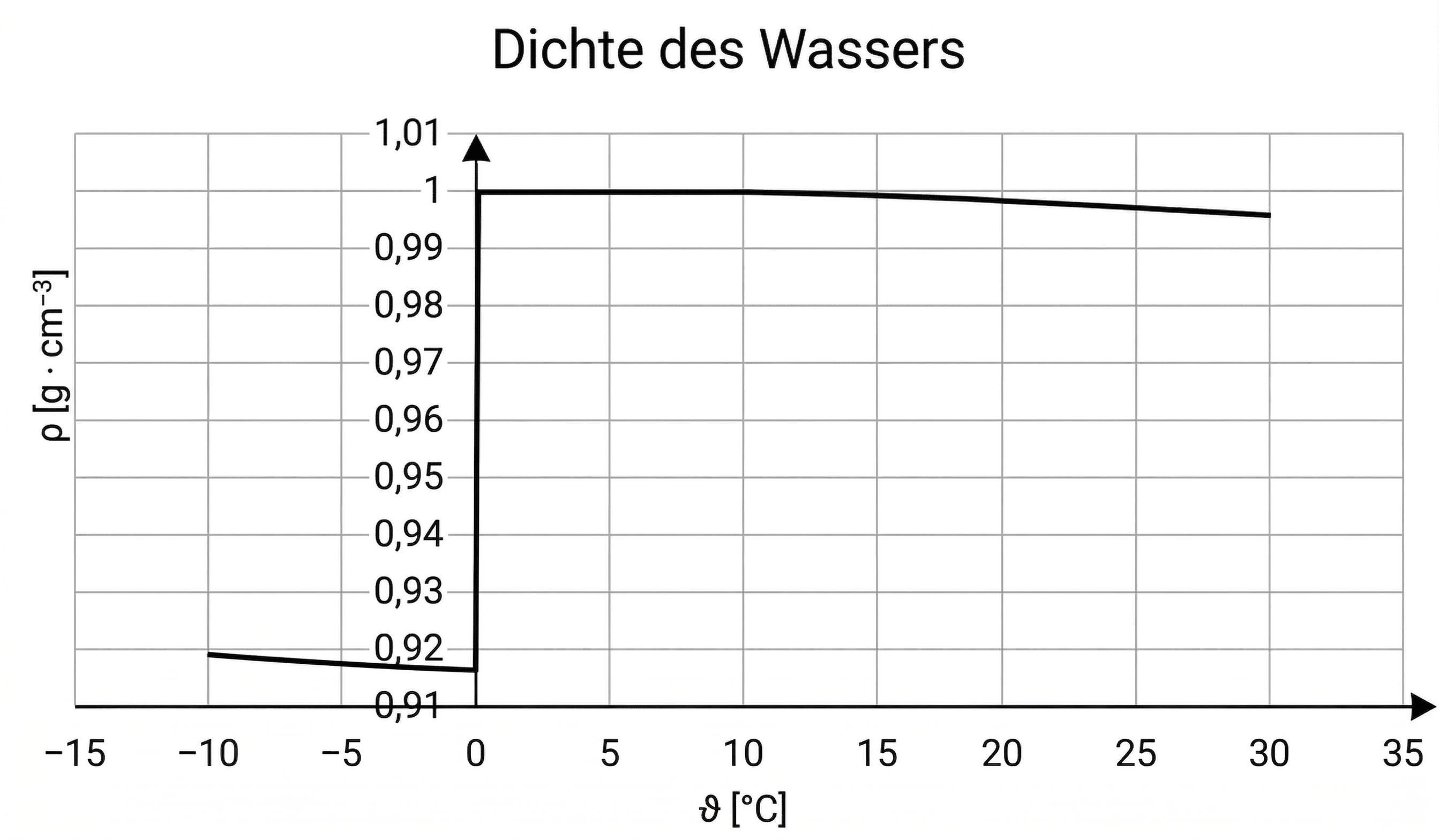
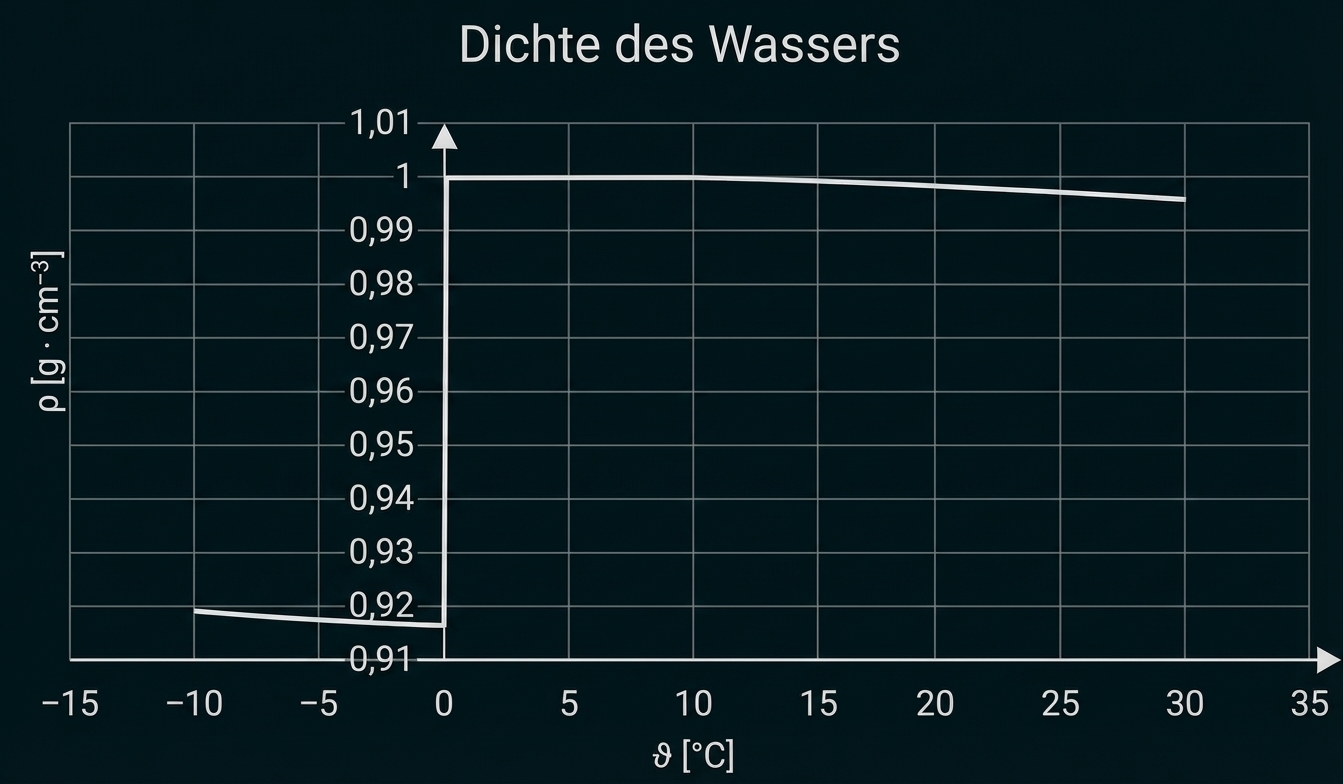
Abb. 1: Dichte des Wassers
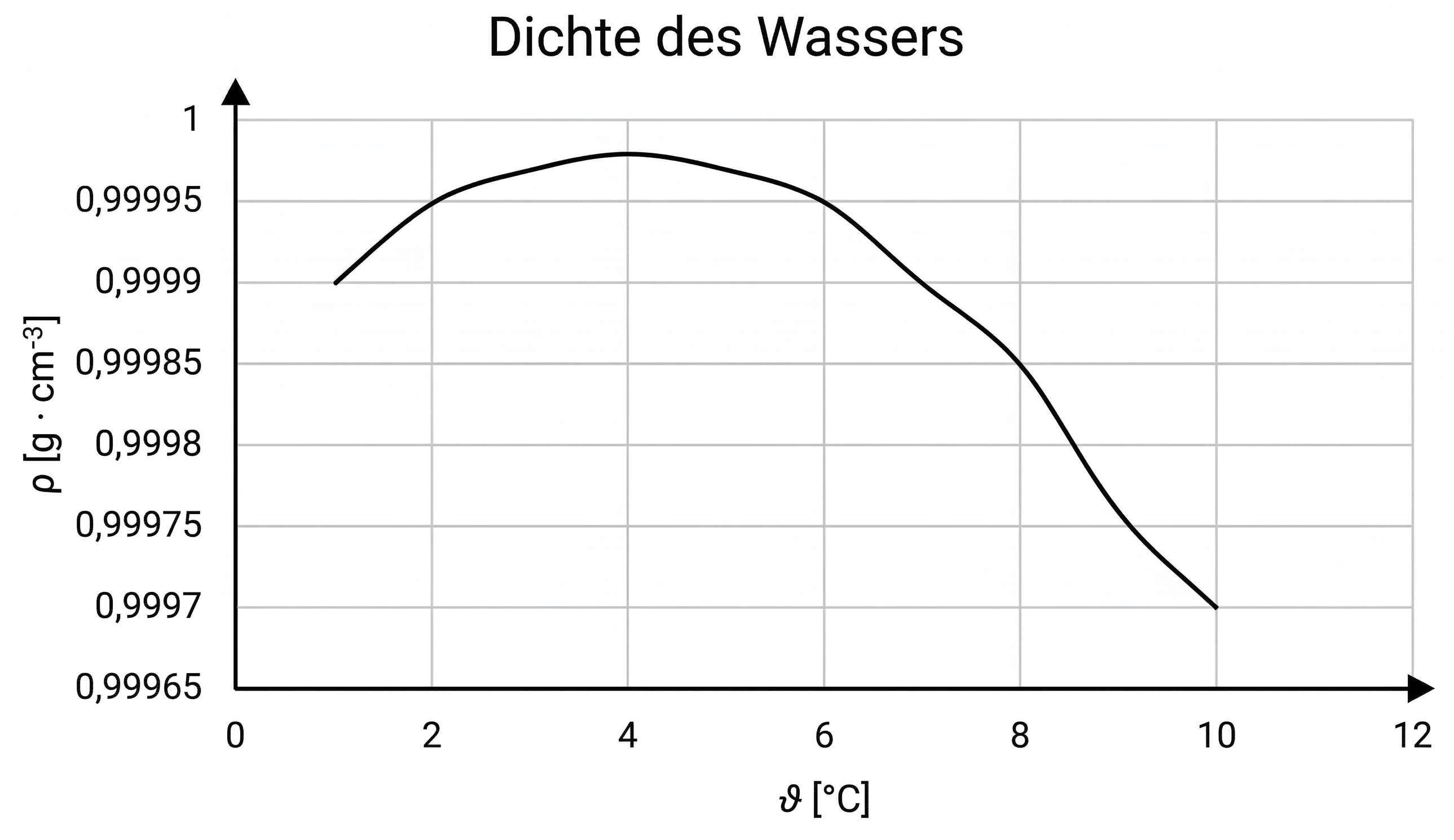
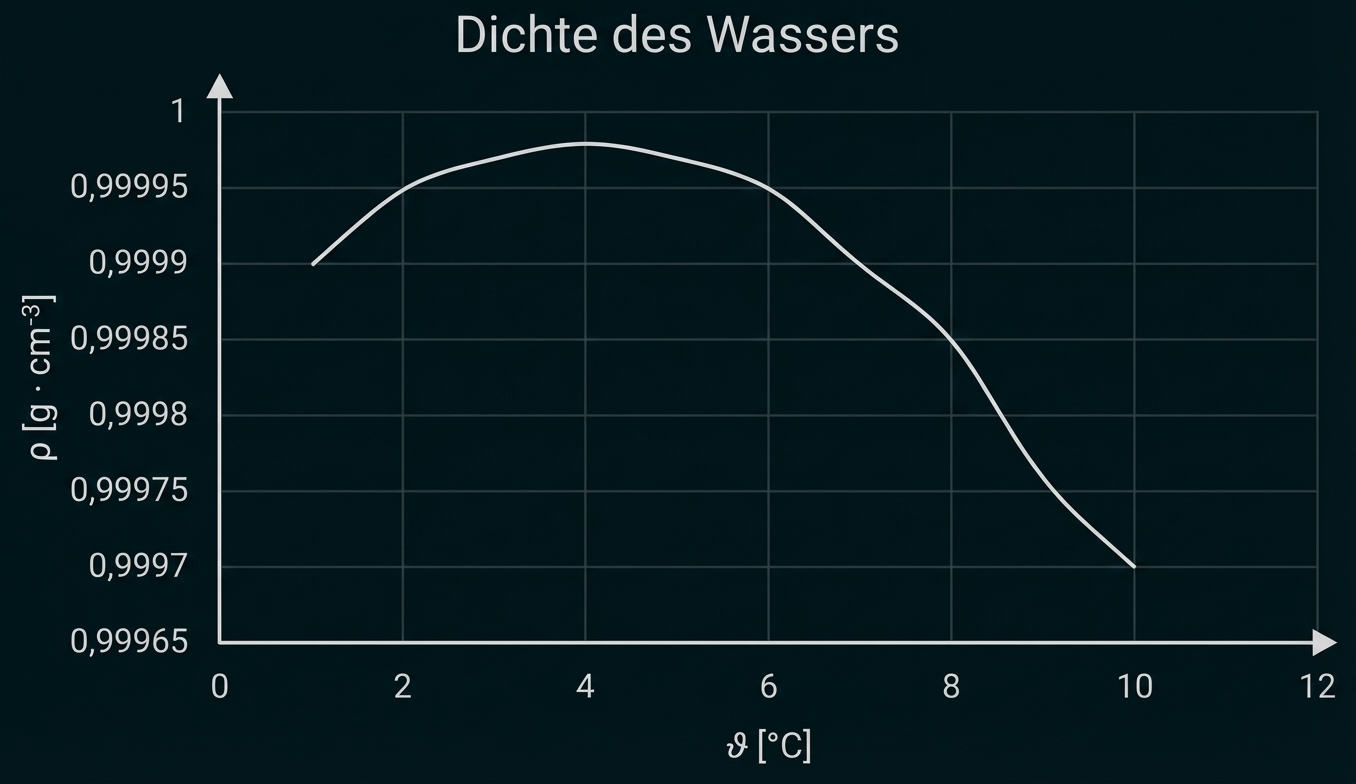
Abb. 2: Dichte des Wassers
[1]
M 3: Trehalose


Abb. 3: Trehalose
Trehalose (siehe Abbildung 3) ist ein Stoff, der auch bei Menschen eine Verwendung findet. Aufgrund seiner hohen Wasserbindungskapazität findet man ihn in den Tränenersatzmitteln (Augenbefeuchtungsmittel). Weiter kann man Trehalose als Zuckeraustauschstoff nutzen. Für die Lebewesen, die Trehalose herstellen können, ist aber dieser Stoff aus anderen Gründen überlebenswichtig. Trehalose wird nämlich als natürliches Frostschutzmittel verwendet. So können z. B. Bärtierchen durch eine Erhöhung des Trehalosegehaltes sehr niedrigen Temperaturen trotzen. Interessanterweise kann Trehalose von einigen Organismen auch als Schutzmittel gegen Austrocknung helfen, so dass sie auch bei einem sehr starken Wasserverlust lebensfähig bleiben. Sie müssen allerdings in einen inaktiven Zustand wechseln, in dem ihre Lebensfunktionen so gut wie zum Stillstand kommen. Nach Wasserzugabe können sie aber in ihren normalen Lebenszustand zurückkehren.
Quellen (ggf. verändert):
[1] Ice - Thermal Properties (engineeringtoolbox.com); abgerufen am 04.11.2023; Wasser-Dichtetabelle (internetchemie.info); Zugriff am 04.11.2023
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Zeichnen der Lewis-Formel


Erläuterung der Struktur
Das Wasser-Molekül besteht aus zwei Wasserstoff-Atomen, die beide an ein Sauerstoff-Atom durch eine polare (kovalente) Bindung gebunden sind. Wie auf dem Bild zu sehen ist, steht somit das Sauerstoff-Atom in der Mitte zwischen beiden Wasserstoff-Atomen. Da Sauerstoff elektronegativer ist als Wasserstoff, sind die Bindungselektronenpaare zum Sauerstoff hingezogen, wodurch Wasserstoff eine partielle positive Ladung, Sauerstoff eine partielle negative Ladung erhält. Man spricht hier von einem Dipol.
Daneben sieht man bei Sauerstoff zwei freie Elektronenpaare. Diese verstärken die negative Ladung im Dipol am Sauerstoff und beeinflussen die räumliche Struktur des Moleküls: Das Wasser-Molekül ist gewinkelt.
Beschreibung des Lösevorgangs auf Teilchenebene
Die Dipole der Wasser-Moleküle lagern sich an die Ionen im Ionengitter des NaCl-Kristalls. Dabei werden die Enden der Dipole zu den entgegengesetzt geladenen Ionen hingezogen (bei Natrium-Ionen wird das negative Ende des Dipols, bei Chlorid-Ionen das positive Ende des Dipols angezogen). Durch das Eindringen der Wasser-Moleküle in das Ionengitter werden einzelne Ionen herausgelöst und von Wasser-Molekülen vollständig ummantelt. Dadurch bildet sich eine Hydrathülle, die ein Wiedereingliedern der Ionen ins Gitter verhindert und die Ionen in der Lösung stabilisiert. Die Wechselwirkung zwischen den Natrium- und Chlorid-Ionen und Wasser-Molekülen wird als Ion-Dipolwechselwirkung bezeichnet und stellt damit die Grundlage für das Auflösen ionischer Verbindungen in Wasser dar.
Beschreibung des Lösevorgangs aus energetischer Sicht
Das Ausbilden von Ion-Dipol-Wechselwirkungen führt zu einer Freisetzung von Energie. Diese führt zur Erhöhung der Teilchenbewegung der betroffenen Ionen im Gitter, was das Eindringen der Wasser-Moleküle ermöglicht. Die anschließende Ausbildung einer kompletten Hydrathülle liefert so viel Energie, dass die Bindungsenergie im Gitter (Gitterenergie) nahezu vollständig aufgehoben wird. Da die freiwerdende Energie bei der Ausbildung einer Ion-Dipol-Wechselwirkung sehr gering ist, ist eine große Anzahl dieser Wechselwirkungen nötig. Beim Natriumchlorid-Kristall ist die Summe dieser freiwerdenden Energie kleiner als die Gitterenergie.
Die Abhängigkeit der Dichte von der Temperatur kann man grob in drei Teile unterteilen, die einzeln beschrieben werden können:
-
Bereich unter dem Gefrierpunkt
-
Bereich zwischen
und
-
Bereich ab
Unter werden im Eis vier Wasserstoffbrücken pro Wasser-Molekül ausgebildet. Diese beanspruchen viel Platz, deshalb ist der Abstand der Wasser-Moleküle im Eis größer als im flüssigen Wasser, d. h., man findet weniger Teilchen in einem Liter Wasser. Der Wert der Dichte ist dadurch kleiner als bei flüssigem Wasser, was man an der Lage der Kurve erkennt.
Weiter beobachtet man eine Dichteabnahme mit der steigenden Temperatur. Dies ist auf die ansteigende Bewegung der Teilchen zurückzuführen, die zu steigenden Abständen und dem Absinken der Dichte führt.
Schmelzen des Eises bei führt zu einem Auflösen eines Teils der Wasserstoffbrücken und dem Zusammenbruch der Kristallstruktur. Die Abstände zwischen den Molekülen verringern sich sprunghaft, was man an dem Dichtesprung merkt.
Der weitere Anstieg der Temperatur verstärkt den Effekt bis zu wo die Bewegung der Teilchen sehr gering ist und die Moleküle sich am nächsten kommen. Die Dichte erreicht ihren maximalen Wert.
Der Anstieg der Temperatur ab verursacht eine immer heftigere Bewegung der Teilchen, die sich dadurch immer weiter voneinander bewegen, wodurch die Abstände zunehmen und die Dichte sinkt.
Erklärung mithilfe der Reaktionskinetik
Der Stoffwechsel ist ein System chemischer Reaktionen. Die chemischen Reaktionen verlaufen bei niedrigen Temperaturen deutlich langsamer – nach der RGT-Regel nimmt die Reaktionsgeschwindigkeit mit jeder Temperaturabsenkung von auf ein Viertel bis eine Hälfte des ursprünglichen Wertes ab. D. h., die chemischen Reaktionen sind für die Aufrechterhaltung der Lebensprozesse zu langsam.
Der Tabelle im M 2 kann man entnehmen, dass unter dem Gefrierpunkt die Dichte des Wassers sprunghaft sinkt, was umgekehrt zu einem Ansteigen des Volumens führt. Im Falle des Gefrierens des Organismus bzw. der Zelle können die Wasserkristalle durch die Volumenzunahme den Körper bzw. die Zelle mechanisch beschädigen (z. B. kann die Zelle platzen).
Bei Frost kristallisiert das Wasser, die Eisstruktur wird durch die Wasserstoffbrücken ausgebildet.
Trehalose enthält nach M 3 viele Hydroxy-Gruppen. Diese ähneln in der Struktur dem Wassermolekül und können demnach auch Wasserstoffbrücken ausbilden.
Aufstellen einer Hypothese
Trehalose bildet in der Lösung zahlreiche Wasserstoffbrücken zu Wasser-Molekülen aus, diese Moleküle stehen dann nicht mehr für die Struktur im Eis zur Verfügung, die Kristalle werden dadurch viel kleiner bzw. können sich ab einer gewissen Konzentration von Trehalose gar nicht mehr ausbilden.
Nennen des Prozesses
Denaturierung
Aufstellen einer Hypothese
Proteine werden in Wasser durch unterschiedliche Wechselwirkungen aufgelöst bzw. in Lösung stabilisiert:
-
Ion-Dipol-Wechselwirkungen
-
Wasserstoffbrücken
Die Trehalose enthält nach M 3 viele Hydroxy-Gruppen, die die gleichen Wechselwirkungen wie Wasser mit den Proteinen ausbilden können.
Aufgrund der Molekülstruktur (großes Molekül mit sehr vielen Wasserstoffbrücken) ist Trehalose aber nicht so flüchtig wie Wasser und kann auch bei hoher Lufttemperatur nicht verdampfen.
Die Trehalose ersetzt also Wasser bei der Stabilisierung der Proteine bzw. Trehalose nimmt den Platz von verdampftem Wasser ein, so dass die Denaturierung verhindert wird.
Zeichnen der Strukturformel eines Fettmoleküls


Erläuterung der Löslichkeit in Wasser
Man sieht, dass ein Fett-Molekül größtenteils aus völlig unpolaren Abschnitten (enthaltene Alkylketten) besteht, die keine starken Wechselwirkungen mit Wasser ausbilden können. Selbst die polaren Teile der Estergruppe können nur begrenzt Wasserstoffbrücken mit Wasser ausbilden, wobei ihre Anzahl nicht ins Gewicht fällt. Dadurch sind die Fette sehr wenig wasserlöslich.
Aus dem Material M 1 geht hervor, dass Fette mit Wasser gespalten werden, d. h., es handelt sich um eine Hydrolyse. Aufgrund des pH-Wertes kann man davon ausgehen, dass die Fettsäuren, die bei der Hydrolyse entstehen (siehe Schema), deprotoniert sind -Wert der organischen Säuren befindet sich im Bereich von


Das entstehende Glycerin ist ein stark polares Molekül mit drei Hydroxy-Gruppen, die zusammen bis zu neun Wasserstoffbrücken mit Wasser ausbilden können. Das begründet die sehr gute Wasserlöslichkeit. Die entstehenden Fettsäuren wären normalerweise wenig wasserlöslich. Da sie aber bei als Carboxylat vorliegen, sorgt die negativ geladene Carboxylat-Gruppe für eine erhöhte Wasserlöslichkeit.