Aufgabe 3 – Viele Wege führen zum Eisen
Eisen ist das häufigste Gebrauchsmetall. Die großtechnische Herstellung im Hochofenprozess ist energieaufwendig und gilt als klimaschädlich. Um die Kohlenstoffdioxid-Emissionen zu verringern, sind alternative Verfahren wie die Herstellung mit Hilfe von Wasserstoff zunehmend von Interesse.
Formuliere die Reaktionsgleichung für die Umsetzung von Koks mit Kohlenstoffdioxid zu Kohlenstoffmonooxid (M 8).
Beschreibe die Abbildung 5 (M 8).
Gib das Prinzip von Le Chatelier an und werte die Abbildung 5 auf dieser Grundlage aus (M 8).
Ermittle unter Verwendung des Satzes von Hess die Änderung der Enthalpie bei der Reduktion von Eisen(III)-oxid mit Kohlenstoffmonooxid zu Eisen(II,III)-oxid und Kohlenstoffdioxid (M 8, Tab. 3).
Berechne, ab welcher Temperatur die Bildung von Eisen und Wasserdampf aus Eisen(III)-oxid und Wasserstoff freiwillig abläuft (M 9).
Erläutere zwei Gründe für die Abweichung zwischen der von dir berechneten Temperatur und den realen Reaktionsbedingungen (M 9).
Berechne die Masse an Kohlenstoffdioxid, die pro produzierter Tonne Eisen aus Eisen(III)-oxid entsteht, wenn dafür „grauer Wasserstoff“ verwendet wird (M 9).
Beurteile
-
die unterschiedlichen Varianten zur Herstellung von Wasserstoff unter dem Aspekt der Nachhaltigkeit (M 9),
-
die ökologischen Auswirkungen der Eisen-Herstellung mit Wasserstoff gegenüber der mit Koks anhand der Kriterien Kohlenstoffdioxid-Vermeidung und Energieeinsparung (M 8, M 9).
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?M 8: Hochofenprozess
Im Hochofenprozess werden Eisenerze zu elementarem Eisen umgesetzt. Wichtige Eisenerze sind Hämatit (Eisen(III)-oxid und Magnetit (Eisen(II,III)-oxid
Ein einmal in Betrieb genommener Hochofen arbeitet 8 bis 10 Jahre ohne Unterbrechung und liefert täglich bis zu 12.000 Tonnen Roheisen.
Im Hochofen werden die Ausgangsstoffe Eisenerz, Koks (ein stark kohlenstoffhaltiger Brennstoff, vereinfacht Kohlenstoff) und Zuschlagsstoffe zur Reaktion gebracht. Zuschlagsstoffe dienen hierbei der Abtrennung unerwünschter Begleitstoffe in Form von Schlacke. Von unten wird heiße Druckluft in den Hochofen eingeblasen. Im Gasstrom laufen die beiden folgenden Reaktionen ab: Zunächst verbrennt der Koks zu Kohlenstoffdioxid, das durch überschüssigen Koks sofort zu Kohlenstoffmonooxid reduziert wird (sogenanntes Boudouard-Gleichgewicht, vgl. Abb. 5).
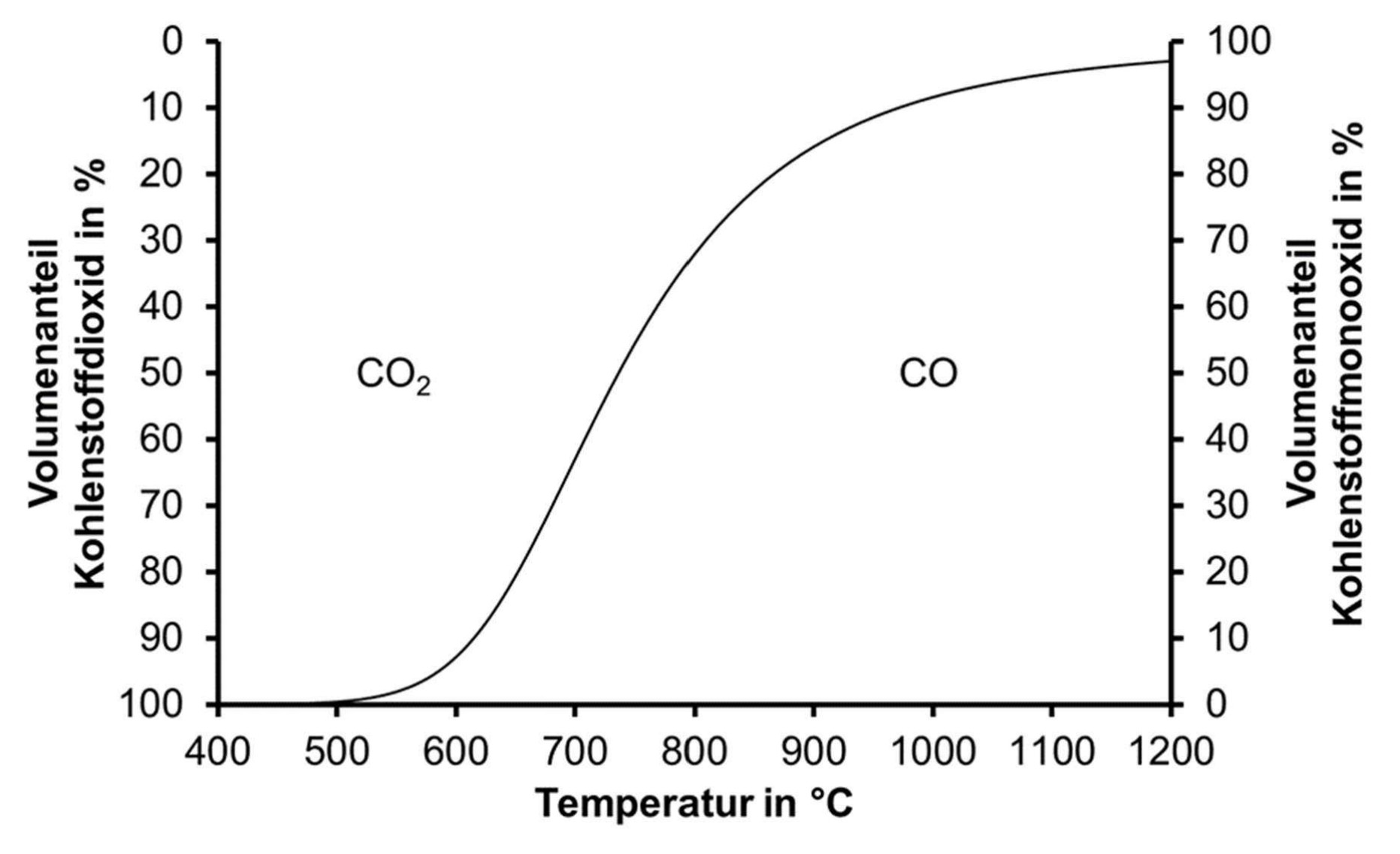
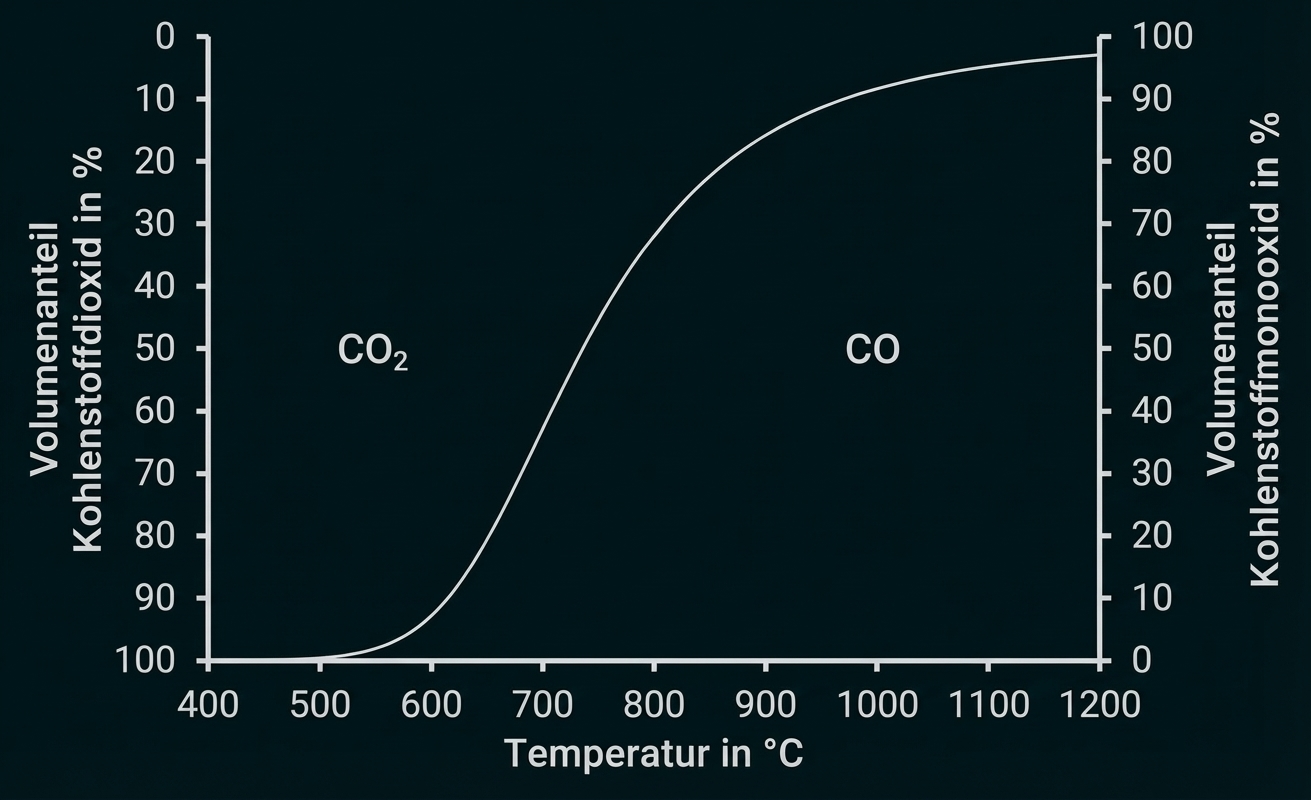
Abb. 5: Boudouard-Gleichgewicht bei (Werte aus [4])
Die im Hochofen bei ca. ablaufenden Prozesse können für Hämatit vereinfacht in einer Reaktionsgleichung zusammengefasst werden:
Dabei entstehen ca. Kohlenstoffdioxid pro Tonne Eisen.
Betrachtet man die Reduktion des Eisen(III)-oxids im Hochofen genauer, so stellt man fest, dass das Erz nicht in einem einzigen Schritt zu Eisen reduziert wird, sondern dass es in den verschiedenen Zonen des Hochofens zu unterschiedlichen Reaktionen kommt, z. B. der Reduktion von Eisen(III)-oxid mit Kohlenstoffmonooxid zu Eisen(II,III)-oxid und Kohlenstoffdioxid.
Weitere Reaktionen sind in Tabelle 3 dargestellt.
Tab. 3: Änderung der Enthalpien ausgewählter Reaktionen (bei
[4]
|
Reaktionsgleichung |
|
|---|---|
|
|
|
|
|
|
[3]
M 9: Eisen mithilfe von Wasserstoff (Direkt-Reduktionsverfahren)
Die Produktion von Eisen war im Jahr 2020 deutschlandweit für ca. sechs Prozent der Kohlenstoffdioxid-Gesamtemissionen verantwortlich. Um diese Emissionen zu senken, erproben verschiedene Firmen den Betrieb einer Eisenverhüttung mit Wasserstoff. Das Eisenerz (z. B. Eisen(III)-oxid) wird im Prozess zunächst durch Verbrennung von Erdgas (hauptsächlich Methan) auf ca. erhitzt. Dabei entstehen Kohlenstoffdioxid-Emissionen von etwa
pro Tonne Eisen. Bei der anschließenden Reaktion des Erzes mit dem Wasserstoff gemäß der folgenden Reaktionsgleichung entstehen elementares Eisen und Wasserdampf:
|
|
|
|
Die Industrie unterteilt den Wasserstoff je nach Herstellungsart wie in nachfolgender Übersicht dargestellt:
Grüner Wasserstoff
Herstellung durch Elektrolyse von Wasser, wobei die dafür notwendige Energie aus erneuerbaren Energien bereitgestellt wird.
Grauer Wasserstoff
Herstellung aus Erdgas unter Erzeugung von Kohlenstoffdioxid gemäß der Gleichung:
Blauer Wasserstoff
Herstellung aus Erdgas, anfallendes Kohlenstoffdioxid wird abgeschieden und gespeichert oder für Produkte weiterverwendet.
Türkiser Wasserstoff
Herstellung aus Erdgas mittels Methanpyrolyse (thermischer Zersetzung), anfallender fester Kohlenstoff wird abgeschieden und gespeichert
Tab. 4: Standardentropien ausgewählter Substanzen (bei
[5]
|
Aggregatzustand |
|
|
|---|---|---|
|
Eisen |
s |
|
|
Eisen(III)-oxid |
s |
|
|
Wasser |
g |
|
|
Wasserstoff |
g |
|
[5]–[7]
Quellen (ggf. verändert):
[3] Hochofen (2024, 25. Februar). Wikipedia. https://de.wikipedia.org/wiki/Hochofen (Zugriff am: 17.03.2024)
[4] Haynes, W., Lide, D. R. & Bruno, T. J. (2014). CRC Handbook of Chemistry and Physics (95. Aufl.). Taylor & Francis.
[5] Ingenieurbüro EMCEL GmbH (2022, 16. April). Wie reduziert Grüner Wasserstoff in der Stahlindustrie CO2-Emissionen? https://emcel.com/de/gruener-wasserstoff-in-der-stahlindustrie/ (Zugriff am: 17.03.2024)
[6] Hartbrich, I. (2022, 07. April). Direktreduktion: Diese Technik wird bei Thyssenkrupp und Co. den Hochofen beerben. VDI Nachrichten. https://www.vdi-nachrichten.com/technik/werkstoffe/direktreduktion-diese-technik-wird-den-hochofen-beerben/ (Zugriff am: 17.03.2024)
[7] Engagement für Stahl - Jahresbericht 2021 (2021). https://www.stahl-online.de/wp-content/uploads/WV-Stahl_Jahresbericht_2021_RZ_Web-1.pdf (Zugriff am: 17.03.2024)
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Formulieren der Reaktionsgleichung für die Umsetzung von Koks
Beschreibung der Abbildung
-
Das Diagramm zeigt die Volumenanteile von Kohlenstoffdioxid und Kohlenstoffmonooxid in Prozent in Abhängigkeit von der Temperatur in
-
Bei niedrigeren Temperaturen ist der Anteil an Kohlenstoffmonooxid gering und der Anteil an Kohlenstoffdioxid hoch.
-
Bei steigender Temperatur nimmt der Anteil an Kohlenstoffmonooxid zu und der Anteil an Kohlenstoffdioxid ab.
Angeben des Prinzips von Le Chatelier und Auswertung der Abbildung
Nach dem Prinzip von Le Chatelier weicht ein im Gleichgewicht befindliches System einem äußeren Zwang so aus, dass der Zwang minimiert wird.
-
Bei hohen Temperaturen läuft verstärkt die endotherme Reaktion ab (Ausweichen des Systems).
-
Die Bildung von Kohlenstoffmonooxid ist endotherm.
Die Reaktionsgleichung der zu betrachtenden Reaktion lautet:
Zugrunde liegende Reaktionsgleichungen:
Schlussfolgerung:
Somit gilt für
Berechnung der Temperatur
Zuerst muss berechnet werden:
Mithilfe der Gibbs-Helmholtz-Gleichung kann die Temperatur berechnet werden:
Die Reaktion läuft freiwillig ab, wenn gilt:
Erläutern der Abweichung
-
Rechnung mit Werten, die bei Standardbedingungen gelten (z. B. Temperatur von
-
Eine höhere Temperatur (Erhitzung des Eisenerzes auf bis zu
führt zu einer Erhöhung der Reaktionsgeschwindigkeit (und damit zu einer ökonomisch sinnvolleren Prozessführung)
Reaktionsgleichungen:
Verhältnisgleichungen:
Aus folgt:
Aus folgt:
Zuzüglich der Kohlenstoffdioxid-Emission für das Erhitzen des Eisenerzes von pro Tonne:
Kohlenstoffdioxid pro Tonne Eisen
Beurteilung der Varianten zur Herstellung von Wasserstoff
-
nachhaltig: Grüner Wasserstoff, da aus erneuerbaren Energien hergestellt und somit keinerlei Kohlenstoffdioxidemissionen
-
am wenigsten nachhaltig: Grauer Wasserstoff, da Erzeugung aus Erdgas, wobei Kohlenstoffdioxid freigesetzt wird
-
bedingt nachhaltig: Blauer Wasserstoff, da Erzeugung aus Erdgas, wobei Kohlenstoffdioxid entsteht, aber nicht freigesetzt wird
-
bedingt nachhaltig: Türkisfarbener Wasserstoff, wobei fester Kohlenstoff entsteht, aber Quelle der Energie für die Pyrolyse ist entscheidend
Beurteilung der Prozesse anhand der Kriterien Kohlenstoffdioxid-Vermeidung und Energieeinsparung
Herstellung mit Koks:
-
Es entsteht Kohlenstoffdioxid, das ein Treibhausgas ist.
-
Endotherme und exotherme Reaktionen laufen parallel ab, daher niedrigerer Energieaufwand.
Herstellung mit Wasserstoff:
-
Je nach Herstellungsart des Wasserstoffs entsteht auch Kohlenstoffdioxid.
-
Die Reaktion ist endotherm, daher hoher Energieaufwand.
Sachurteil fällen