Aufgabe 2 – Kupfer
Kupfer ist ein sehr wichtiger Rohstoff, der z. B. für die Elektronik und die Bauindustrie von großer Bedeutung ist. Die Veränderung des Preises von Kupfer an der Börse signalisiert den Zustand der ökonomischen Lage der Staaten und der Welt.
Nenne vier Eigenschaften von Kupfer.
Erkläre zwei dieser Eigenschaften mit seiner Struktur.
Formuliere die Elektronenkonfiguration von Kupfer.
Leite daraus die Stellung von Kupfer im Periodensystem der Elemente ab.
Kupfer reagiert nicht mit verdünnten Säuren. Konzentrierte Salpetersäure kann aber Kupfer lösen. Dabei entsteht neben einer blauen Lösung ein farbloses Gas, das sich an der Luft schnell rotbraun verfärbt.
Formuliere für beide Vorgänge eine Reaktionsgleichung.
Bestimme die Reaktionsart und begründe.
Für elektronische Leiter benötigt man sehr reines Kupfer. Dieses kann man durch Elektrolyse gewinnen.
Zeichne ein beschriftetes Schema der Kupferraffination.
Erkläre die ablaufenden Prozesse auch unter Einbeziehung von Reaktionsgleichungen.
Berechne die Masse an Kupfer, die man nach durch die Elektrolyse einer Kupfer(II)-sulfat-Lösung gewinnen kann, wenn die benutzte Stromstärke
beträgt.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Nennen von vier Eigenschaften von Kupfer
-
Chemische Widerstandsfähigkeit / kleine Reaktivität
-
Elektrische Leitfähigkeit
-
Thermische Leitfähigkeit
-
Glanz
-
Verformbarkeit
Hinweis: Auch andere Eigenschaften können genannt werden.
Erklären zweier Eigenschaften mithilfe der Struktur
-
Chemische Widerstandsfähigkeit / kleine Reaktivität: stabile Elektronenkonfiguration im Grundzustand
-
Elektrische Leitfähigkeit: Elektronengas mit frei beweglichen Elektronen
-
Thermische Leitfähigkeit: Schwingungen des Gitters aus Atomrümpfen
-
Glanz: leichte Energieaufnahme bzw. Absorption der Lichtenergie durch das Elektronengas und umgehende Freisetzung bzw. Emission führt zu nahezu vollständiger Reflexion
-
Verformbarkeit: Gitter aus Atomrümpfen und Elektronengas; das Elektronengas hebt die Anstoßung zwischen den positiv geladenen Atomrümpfen auf, wodurch Gleitbewegungen möglich sind
Hinweis: Auch andere Ansätze und Erklärungen anderer Eigenschaften sind hier zulässig.
Angeben der Elektronenkonfiguration
Ableiten der Stellung im PSE
-
vierte Periode
-
Übergangselemente,
-Elemente
-
Gruppe
bzw.
Formulieren der Reaktionsgleichungen
Bestimmung und Begründung der Reaktionsart
-
Reaktionsart: Redoxreaktion
-
Begründung: Änderung der Oxidationszahlen während der Reaktion
Hinweis: Auch eine Begründung mit Teilreaktionen ist zulässig.
Zeichnung eines beschrifteten Schemas der elektrolytische Kupferraffination
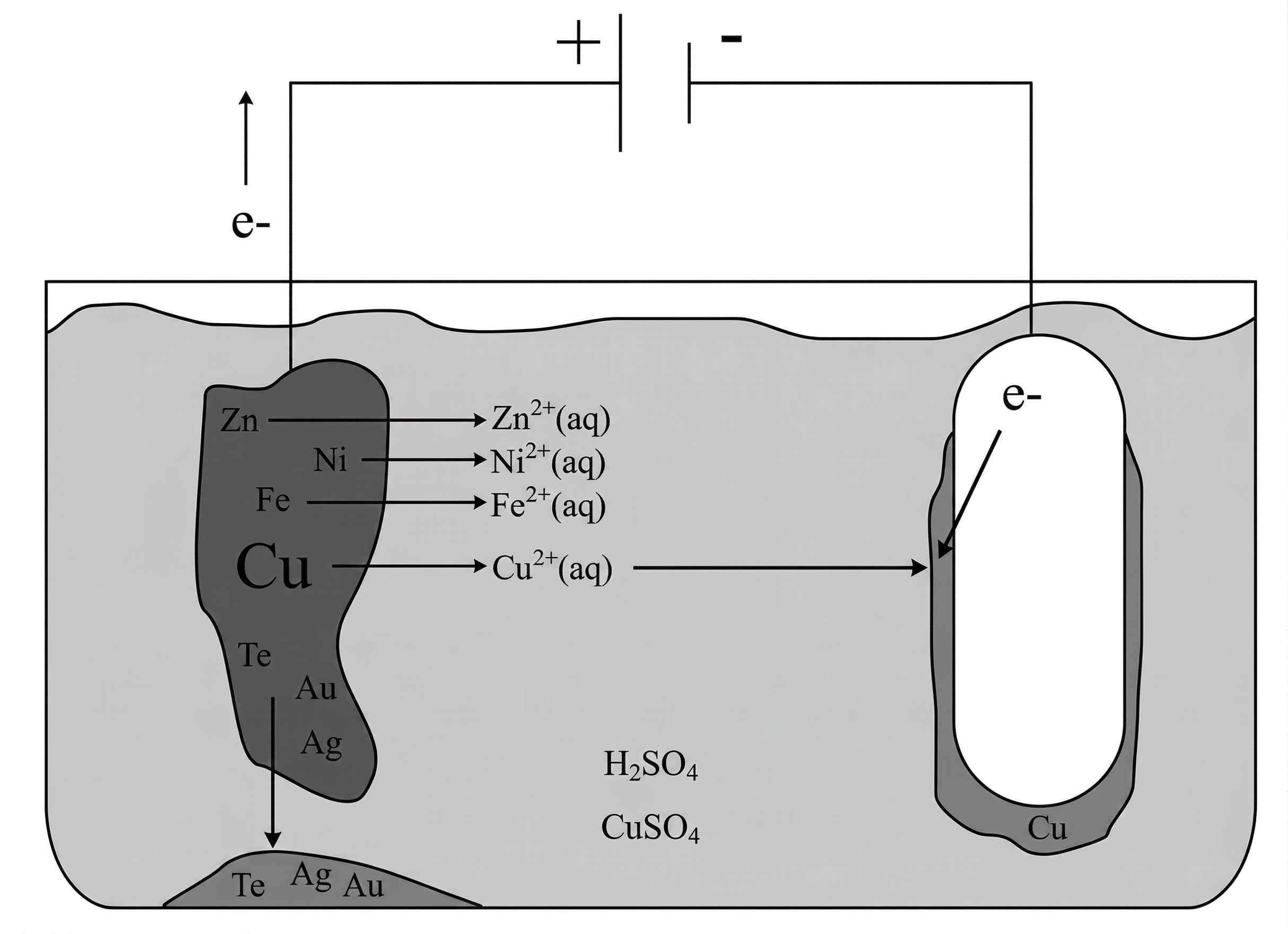
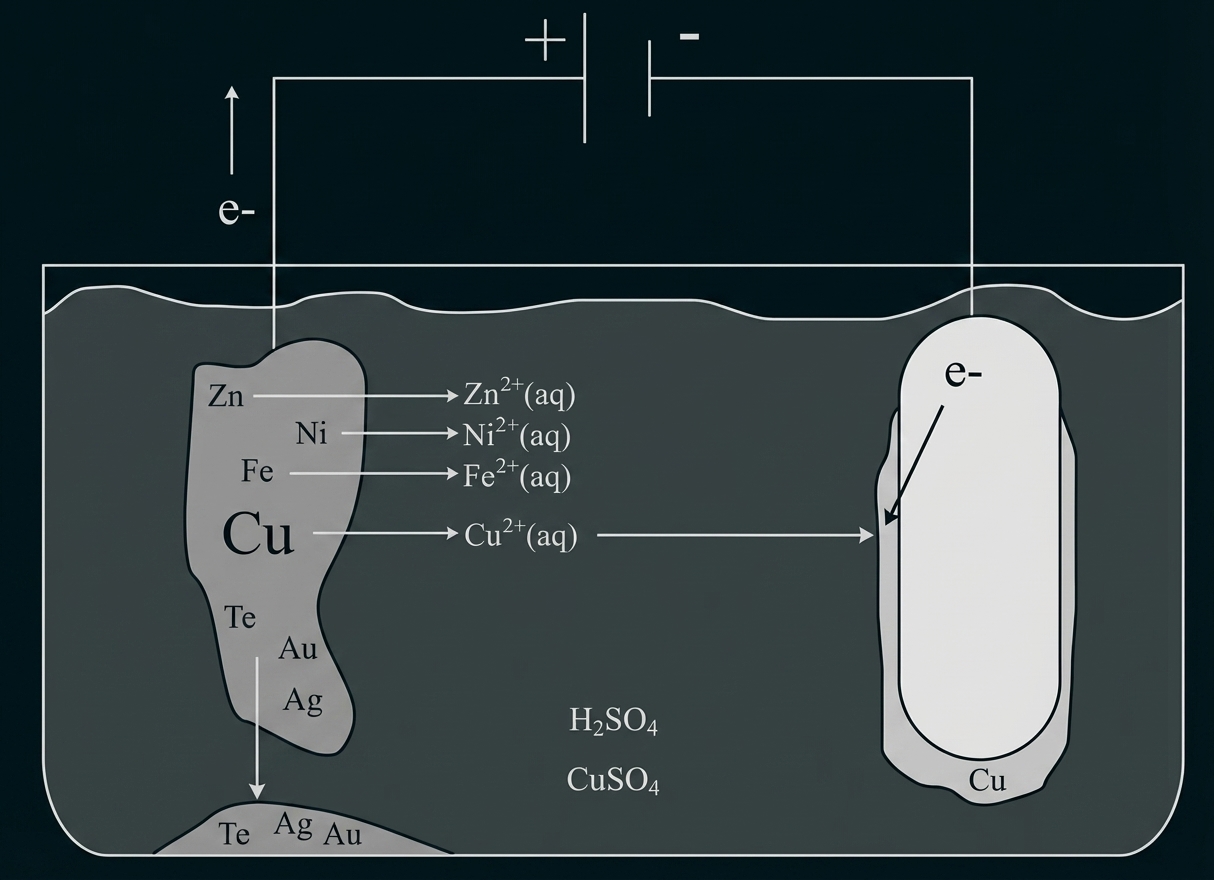
Beschriftungen:
-
Reinkupferelektrode – Kathode
-
Rohkupferelektrode – Anode
-
Spannungsquelle
-
Richtung des Stroms bzw. der Elektronen
-
Bewegung der Kupferionen
-
Anodenschlamm
Erklärung der ablaufenden Prozesse
|
Kathode: |
|
|
Anode: |
|
An der Anode findet die Oxidation statt, wobei Zink-, Nickel-, Eisen- und Kupferionen oxidiert werden und in Lösung gehen. Die Elektronen fließen hierbei von der Anode zum Pluspol. Die edleren Metalle Tellur, Silber und Gold werden nicht oxidiert und setzen sich als Anodenschlamm ab.
An der Kathode werden die Kupfer(II)-Ionen reduziert und elementares Kupfer scheidet sich ab.
Berechnung der gewinnbaren Masse an Kupfer bei einer Elektrolyse