HT 3
Der Franck-Hertz-Versuch mit Neon
Der Franck-Hertz-Versuch liefert wichtige Erkenntnisse über den Aufbau von Atomen. Teilaufgabe 1: Aufbau des Franck-Hertz-Versuchs Im Folgenden soll der Franck-Hertz-Versuch mit Neon durchgeführt werden. Abbildung 1 zeigt einen schematischen Aufbau für diesen Versuch. Darin ist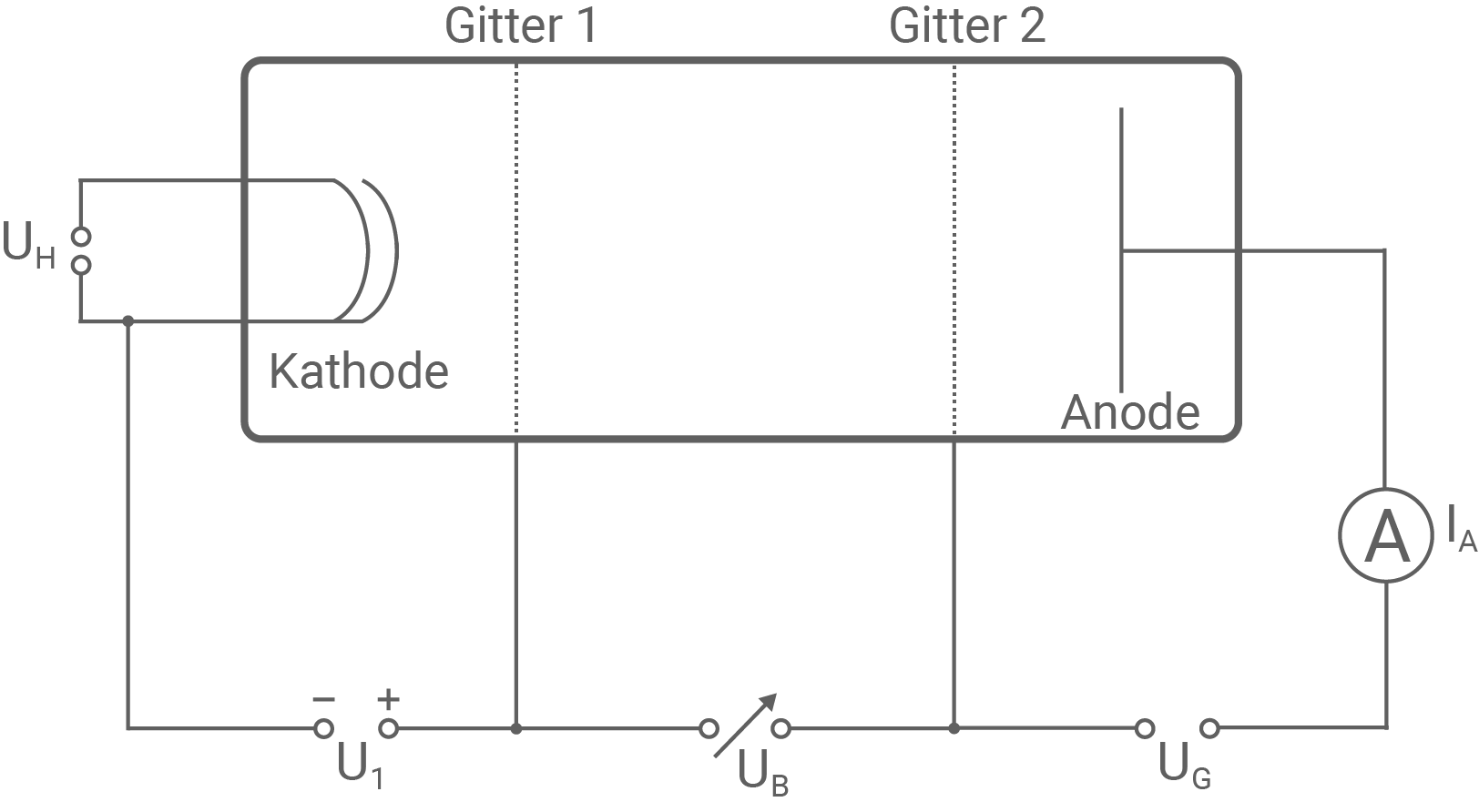
Abbildung 1: Schematischer Aufbau des Franck-Hertz-Versuchs mit Neongas
a)
- Beschreibe den Aufbau des Franck-Hertz-Versuchs aus Abbildung 1.
- Erläutere die Funktion der Bauelemente anhand Abbildung 1 und die Bedeutung
Größen
und
- Gib für eine übliche Durchführung des Franck-Hertz-Versuchs die Polung der Spannungen
und
in Abbildung 1 an.
(10 Punkte)

Abbildung 2:  -
- -Diagramm des Franck-Hertz-Versuchs mit Neon
-Diagramm des Franck-Hertz-Versuchs mit Neon
a)
- Beschreibe den Verlauf des Diagramms in Abbildung 2.
- Gib die Werte der Spannung
an, bei denen die Maxima der Stromstärke
im Diagramm in Abbildung 2 auftreten.
b)
Begründe, weshalb ein Anodenstrom der Stärke  größer als Null nur dann gemessen wird, wenn die Spannung
größer als Null nur dann gemessen wird, wenn die Spannung  größer ist als
größer ist als 
c)
- Erkläre das erstmalige Absinken der Stromstärke
im Diagramm in Abbildung 2.
- Erläutere, weshalb die Stromstärke
im weiteren Verlauf noch zwei weitere Male absinkt.
- Erläutere, weshalb die Minima der Stromstärke
im Diagramm in Abbildung 2 nicht immer bis auf Null absinken.
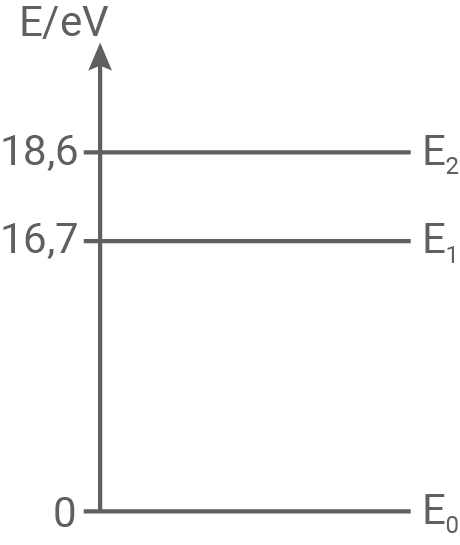
Abbildung 3: Energieniveauschema von Neon, vereinfacht
d)
Erläutere den Zusammenhang zwischen dem Energieniveauschema von Neon in Abbildung 3 und dem Diagramm des Franck-Hertz-Versuchs in Abbildung 2.
Teilaufgabe 3: Leuchterscheinungen beim Franck-Hertz-Versuch
Beim Franck-Hertz-Versuch mit Neon kann man das Auftreten eines roten Leuchtens beobachten. In Abbildung 4 sind zwei deutlich voneinander abgegrenzte rot leuchtende Zonen im Schwarzweißbild dargestellt und mit Pfeilen markiert.
(6 + 2 + 10 + 3 Punkte)

Abbildung 4: Rote Leuchterscheinungen beim Franck-Hertz-Versuch mit Neon
a)
- Bestimme, welcher der drei möglichen Übergänge im vereinfachten Energieniveauschema von Neon in Abbildung 3 zur roten Lichtemission führt.
- Bestimme, welchem Spektralbereich die anderen beiden Übergänge zuzuordnen sind.

Abbildung 5: Franck-Hertz-Röhre bei verschiedenen Spannungen 
b)
Gib zu den Bildern in Abbildung 5 begründet jeweils einen möglichen Spannungsbereich für  aus dem Diagramm in Abbildung 2 an, bei denen die jeweiligen Bilder in Abbildung 5 jeweils gemacht werden können.
aus dem Diagramm in Abbildung 2 an, bei denen die jeweiligen Bilder in Abbildung 5 jeweils gemacht werden können.
c)
Erläutere, inwiefern sich die Leuchterscheinungen in der Franck-Hertz-Röhre ändern, wenn man für die Spannung  einen Wert von etwa
einen Wert von etwa  bei der Versuchsdurchführung des Versuchs aus Abbildung 2 einstellt.
bei der Versuchsdurchführung des Versuchs aus Abbildung 2 einstellt.
Teilaufgabe 4: Atommodelle
Die Erklärung des Franck-Hertz-Versuchs gelingt nur mit geeigneten Atommodellen. In Abbildung 6 sind typische Darstellungen der Atommodelle von Dalton, Thomson, Rutherford und Bohr dargestellt.
(5 + 6 + 2 Punkte)
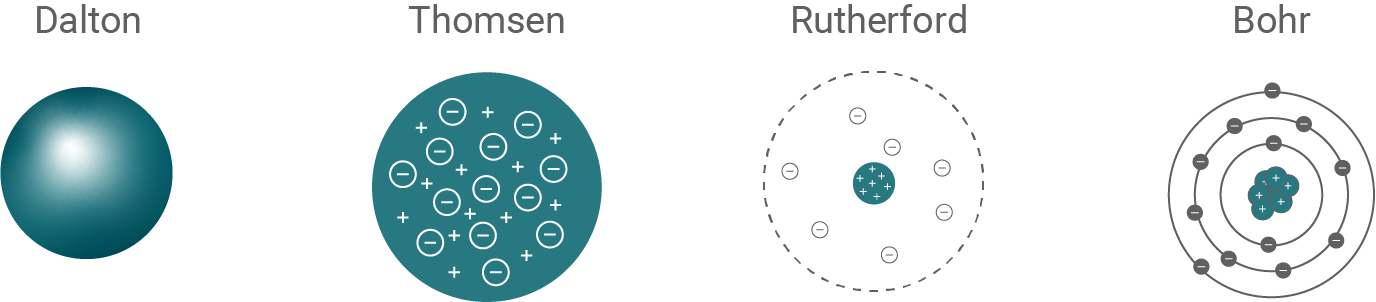
Abbildung 6: Typische Darstellungen der Atommodelle nach Dalton, Thomson, Rutherford und Bohr
a)
Beschreibe anhand von Abbildung 6 die Atommodelle von Dalton, Thomson, Rutherford und Bohr kurz in eigenen Worten.
b)
Erläutere zwei Kritikpunkte am Bohr'schen Atommodell.
c)
Erläutere, welche Eigenschaften ein Atommodell erfüllen muss, um die Ergebnisse des Franck-Hertz-Versuchs zu erklären.
d)
Unter Resonanzabsorption versteht man, dass Atome Photonen absorbieren können, welche die gleiche Energie besitzen wie Photonen, die die Atome emittieren.
- Beschreibe einen geeigneten Versuch, mit dem man die Resonanzabsorption deutlich machen kann.
- Erläutere den Unterschied bezüglich der Energieübertragung bei der Resonanzabsorption und dem Franck-Hertz-Versuch.
(8 + 4 + 2 + 7 Punkte)
Teillösung 1: Aufbau des Franck-Hertz-Versuchs
a)
Beschreibung des Aufbaus und der Funktion der Bauelemente
Der Franck-Hertz-Versuch besteht aus einem Glaskolben, der mit Neongas bei niedrigem Druck gefüllt ist. An der Kathode können durch Anlegen einer Heizspannung  Elektronen ausgelöst werden. Die Elektronen bilden eine Raumladungswolke um die Kathode. Zwischen Gitter 1 und Gitter 2 ist die variable Beschleunigungsspannung
Elektronen ausgelöst werden. Die Elektronen bilden eine Raumladungswolke um die Kathode. Zwischen Gitter 1 und Gitter 2 ist die variable Beschleunigungsspannung  angelegt, welche die Elektronen beschleunigt. Zwischen Gitter 2 und der Anode liegt die Gegenspannung
angelegt, welche die Elektronen beschleunigt. Zwischen Gitter 2 und der Anode liegt die Gegenspannung  an, welche ein Gegenfeld erzeugt. Nur Elektronen mit genügender kinetischer Energie, die das Gegenfeld überwinden, gelangen zur Anode und tragen zum Anodenstrom
an, welche ein Gegenfeld erzeugt. Nur Elektronen mit genügender kinetischer Energie, die das Gegenfeld überwinden, gelangen zur Anode und tragen zum Anodenstrom  bei, welcher mit einem geeigneten Amperemeter gemessen werden kann.
Angabe der Polung der Spannungen
bei, welcher mit einem geeigneten Amperemeter gemessen werden kann.
Angabe der Polung der Spannungen  und
und  Die Polungen der Spannungen gibt die folgende Darstellung wieder:
Die Polungen der Spannungen gibt die folgende Darstellung wieder:
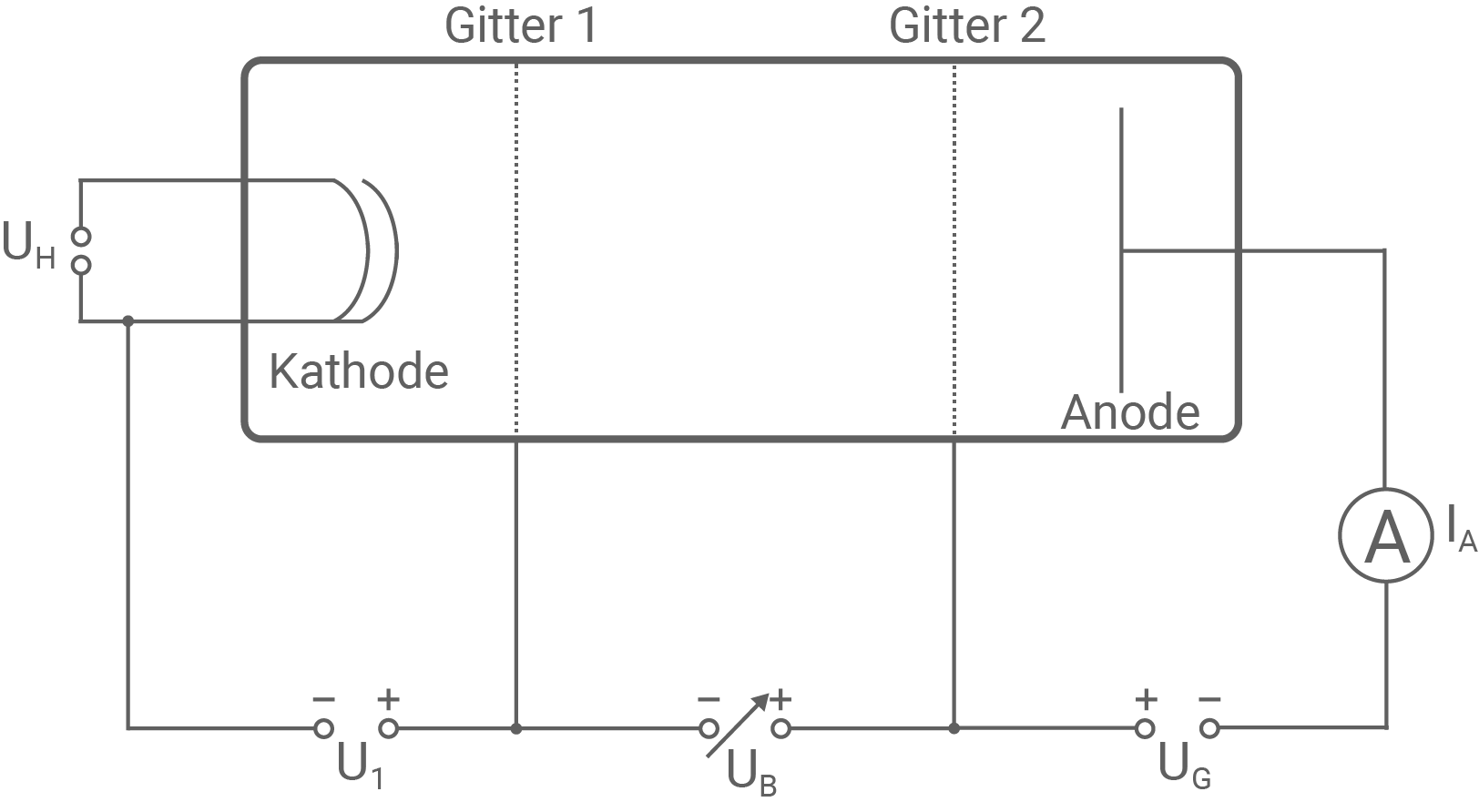
Teillösung 2: Auswertung des Versuchs

a)
Beschreibung des Verlaufs und Angabe der Werte der Spannung  Im
Im  -Diagramm in Abbildung 2 erkennt man zunächst, dass der Anodenstrom im Bereich der Beschleunigungsspannung von
-Diagramm in Abbildung 2 erkennt man zunächst, dass der Anodenstrom im Bereich der Beschleunigungsspannung von  bis etwa
bis etwa 
 beträgt. Danach steigt die Stromstärke an, bis sie bei etwa
beträgt. Danach steigt die Stromstärke an, bis sie bei etwa  ein erstes Maximum erreicht. Danach sinkt der Anodenstrom bis zur Beschleunigungsspannung von etwa
ein erstes Maximum erreicht. Danach sinkt der Anodenstrom bis zur Beschleunigungsspannung von etwa  auf fast
auf fast  ab. Anschließend steigt die Stromstärke wieder an, bis zum zweiten Maximum bei etwa
ab. Anschließend steigt die Stromstärke wieder an, bis zum zweiten Maximum bei etwa  Danach sinkt die Stromstärke wieder auf ein Minimum bei etwa
Danach sinkt die Stromstärke wieder auf ein Minimum bei etwa  ab und steigt anschließend wieder bis zu einem dritten Maximum bei etwa
ab und steigt anschließend wieder bis zu einem dritten Maximum bei etwa  an. Danach sinkt die Anodenstromstärke wieder auf ein Minimum bei etwa
an. Danach sinkt die Anodenstromstärke wieder auf ein Minimum bei etwa  ab und steigt anschließend wieder an. Maxima der Stromstärke
ab und steigt anschließend wieder an. Maxima der Stromstärke  bei
bei  gleich
gleich  und
und 
b)
Es ist erst ein Anodenstrom  ab
ab  messbar, da die kinetische Energie der Elektronen größer als
messbar, da die kinetische Energie der Elektronen größer als  sein muss, um gegen das Gegenfeld anzukommen, damit die Elektronen die Anode erreichen. Die Elektronen erhalten aus dem elektrischen Feld zwischen Kathode und Gitter 1 mit der Spannung
sein muss, um gegen das Gegenfeld anzukommen, damit die Elektronen die Anode erreichen. Die Elektronen erhalten aus dem elektrischen Feld zwischen Kathode und Gitter 1 mit der Spannung  die kinetische Energie von
die kinetische Energie von  Ab einer Beschleunigungsspannung von
Ab einer Beschleunigungsspannung von  erhalten die Elektronen zusätzlich aus dem elektrischen Feld zwischen Gitter 1 und Gitter 2 eine kinetische Energie von mindestens
erhalten die Elektronen zusätzlich aus dem elektrischen Feld zwischen Gitter 1 und Gitter 2 eine kinetische Energie von mindestens  und können somit zur Anode gelangen.
und können somit zur Anode gelangen.
c)
Erklärung des erstmaligen Absinkens der Stromstärke  Die Elektronen durchlaufen zwischen den Gittern eine Beschleunigungsspannung. Ist die Beschleunigungsspannung entsprechend groß, so können Neonatome durch Stöße mit Elektronen unmittelbar vor dem Gitter 2 angeregt werden. Dabei verlieren die Elektronen ihre kinetische Energie und können das Gegenfeld zwischen Gitter 2 und Anode nicht mehr überwinden. Der Strom
Die Elektronen durchlaufen zwischen den Gittern eine Beschleunigungsspannung. Ist die Beschleunigungsspannung entsprechend groß, so können Neonatome durch Stöße mit Elektronen unmittelbar vor dem Gitter 2 angeregt werden. Dabei verlieren die Elektronen ihre kinetische Energie und können das Gegenfeld zwischen Gitter 2 und Anode nicht mehr überwinden. Der Strom  beginnt zu sinken. Da dieses erstmalige Absinken bei
beginnt zu sinken. Da dieses erstmalige Absinken bei  stattfindet, deutet dies auf eine Anregungsenergie der Neonatome von etwa
stattfindet, deutet dies auf eine Anregungsenergie der Neonatome von etwa  hin
hin  Begründung der weiteren zwei Male, in denen die Stromstärke
Begründung der weiteren zwei Male, in denen die Stromstärke  absinkt
Dieses Absinken der Stromstärke tritt noch zwei weitere Male auf, da sich bei den ablesbaren Vielfachen der Spannung zwei bzw. drei solcher Stoßzonen zwischen den Gittern ausgebildet haben.
Erläuterung, weshalb die Minima nicht immer bis auf Null absinken.
Die Stromstärke
absinkt
Dieses Absinken der Stromstärke tritt noch zwei weitere Male auf, da sich bei den ablesbaren Vielfachen der Spannung zwei bzw. drei solcher Stoßzonen zwischen den Gittern ausgebildet haben.
Erläuterung, weshalb die Minima nicht immer bis auf Null absinken.
Die Stromstärke  sinkt nicht immer bis auf Null ab, da nicht alle Elektronen stoßen, wenn Sie die Energie von
sinkt nicht immer bis auf Null ab, da nicht alle Elektronen stoßen, wenn Sie die Energie von  bzw.
bzw.  angenommen haben.
angenommen haben.
d)
Im Diagramm aus Abbildung 2 erkennt man, dass die Maxima des Anodenstroms bei Spannungsdifferenzen von  bzw.
bzw.  auftreten. Das heißt, dass die Neonatome mit einer Energie von
auftreten. Das heißt, dass die Neonatome mit einer Energie von  angeregt werden. Diese Energie entspricht in etwa der Energiedifferenz
angeregt werden. Diese Energie entspricht in etwa der Energiedifferenz  des Neonatoms aus Abbildung 3.
des Neonatoms aus Abbildung 3.
Teillösung 3: Leuchterscheinungen beim Franck-Hertz-Versuch
a)
Bestimmung des Übergangs, der zur roten Lichtemission führt.
Der Übergang vom Energieniveau  auf das Energieniveau
auf das Energieniveau  entspricht dem Übergang, der zur Emission von rotem Licht führt:
entspricht dem Übergang, der zur Emission von rotem Licht führt:
![\(\begin{array}[t]{rll}
\Delta E&=& h \cdot \dfrac{\text{c}}{\lambda} &\quad \scriptsize \mid\; \cdot \dfrac{\lambda}{\Delta E} \\[5pt]
\lambda&=& h \cdot \dfrac{\text{c}}{\Delta E} &\quad \scriptsize \\[5pt]
\lambda&=& h \cdot \dfrac{\text{c}}{E_2-E_1} &\quad \scriptsize \\[5pt]
\end{array}\)](https://www.schullv.de/resources/formulas/57e7a470b81dcd9c0ded2da5f5a3a781553671c33f5aeb75dec77a9a91b5499c_light.svg) Einsetzen der Werte liefert:
Bestimmung des Spektralbereiches der anderen beiden Übergänge
Für den Übergang von
Einsetzen der Werte liefert:
Bestimmung des Spektralbereiches der anderen beiden Übergänge
Für den Übergang von  nach
nach  gilt:
Für den Übergang von
gilt:
Für den Übergang von  nach
nach  gilt:
Die anderen beiden Übergänge
gilt:
Die anderen beiden Übergänge  bzw.
bzw.  lassen sich dem UV-Bereich zuordnen.
lassen sich dem UV-Bereich zuordnen.
b)
In Bild 1 sind zwei Leuchtschichten zu erkennen. Diese treten ab dem zweiten Maximum im Diagramm aus Abbildung 2 auf. Deshalb kommen hier Beschleunigungsspannungen ab  bis
bis  in Betracht.
In Bild 2 sind drei Leuchtschichten zu erkennen. Diese treten ab dem dritten Maximum im Diagramm aus Abbildung 2 auf. Deshalb kommen hier Beschleunigungsspannungen ab
in Betracht.
In Bild 2 sind drei Leuchtschichten zu erkennen. Diese treten ab dem dritten Maximum im Diagramm aus Abbildung 2 auf. Deshalb kommen hier Beschleunigungsspannungen ab  bis
bis  in Betracht. In Bild 3 ist eine Leuchtschicht zu erkennen. Diese tritt ab dem ersten Maximum im Diagramm aus Abbildung 2 auf. Deshalb kommen hier Beschleunigungsspannungen ab
in Betracht. In Bild 3 ist eine Leuchtschicht zu erkennen. Diese tritt ab dem ersten Maximum im Diagramm aus Abbildung 2 auf. Deshalb kommen hier Beschleunigungsspannungen ab  bis
bis  in Betracht.
in Betracht.


c)
Ab etwa  erwartet man das Entstehen einer weiteren Leuchtschicht, da eine weitere Anregungszone des Neons hinzukommt:
erwartet man das Entstehen einer weiteren Leuchtschicht, da eine weitere Anregungszone des Neons hinzukommt:
![\(\begin{array}[t]{rll}
52,5 \;\text{V} + 18,5 \;\text{V}&=& 71 \;\text{V} &\quad \scriptsize \\[5pt]
\end{array}\)](https://www.schullv.de/resources/formulas/573691eb4e5e902a2666177612f1ab0a568303ff829d1c6afbdb3a023d926284_light.svg)
Teillösung 4: Atommodelle
a)
Dalton: Jeder Stoff besteht aus kleinsten, nicht weiter teilbaren, kugelförmigen Teilchen, den Atomen.
Thomson: Ein Atom besteht aus einer gleichmäßig positiv geladenen Materiekugel, in welche die Elektronen regelmäßig verteilt eingebettet sind (Rosinenkuchenmodell). Rutherford: Das Atom besteht aus einem positiv geladenen Kern, der fast die gesamte Masse des Atoms besitzt, aber sehr klein im Vergleich zum Atomdurchmesser (ca. 1/10.000) ist. Die gesamte negative Ladung tragen die Elektronen in der Atomhülle, die sich um den Kern bewegen.
Bohr: Das Bohr'sche Atommodell übernimmt den Aufbau des Rutherford'schen Atommodells. Jedoch bewegen sich die Elektronen in der Hülle nur auf bestimmten Kreisbahnen um den Kern strahlungsfrei.
b)
Mögliche Kritikpunkte am Bohr'schen Atommodell sind:
- Nach der Heisenberg'schen Unbestimmtheitsrelation sind Ort und Impuls eines Objekts nicht gleichzeitig beliebig genau bestimmbar. Im Bohr'schen Atommodell bewegen sich die Elektronen allerdings auf Kreisbahnen. Damit sind der Ort und der Impuls des Elektrons im Bohr'schen Atommodell exakt vorgegeben.
- Die Ausbreitung von Elektronen muss mit dem Wellenmodell beschrieben werden. Dies ist im Bohr'schen Atommodell nicht der Fall.
- Das Bohr'sche Atommodell beschreibt das Atom als „Scheibe“.
c)
Um den Franck-Hertz-Versuch zu erklären, muss das verwendete Atommodell die quantenhafte Absorption (bzw. Emission) von Energie beinhalten, um damit die quantenhaft absorbierte Energie der Elektronen zu erklären. (Die quantenhafte Emission erklärt dann die Leuchterscheinungen, z. B. beim Neon.)
d)
Beschreibung eines geeigneten Versuches
Ein Versuch, mit dem man die Resonanzabsorption deutlich machen kann, wäre beispielsweise, wenn man Kochsalz in der Flamme eines Bunsenbrenners verdampfen würde und über Kreuz mit dem Licht einer Quecksilberdampflampe und einer Natriumdampflampe beleuchtet. Durch die Resonanzabsorption ergebe sich nur ein Schatten der Flamme bei der Beleuchtung durch die Natriumdampflampe.
Erläuterung des Unterschiedes
Bei der Resonanzabsorption sind die Photonen die Wechselwirkungsobjekte mit den Atomen. Beim Franck-Hertz-Versuch wechselwirken die Elektronen mit den Atomen. Dabei können die Elektronen einen beliebigen Teil ihrer Bewegungsenergie an die Atome durch unelastische Stöße übertragen. Die kinetische Energie der Elektronen nimmt dann um den übertragenen charakteristischen Energiebetrag des Atoms ab. Die Photonen jedoch können nur bestimmte Energien übertragen, die durch ihre Wellenlänge bzw. Frequenz bestimmt sind. Bei der Resonanzabsorption übertragen die Photonen nur ihre Gesamtenergie, Teilenergien sind dabei nicht möglich. Demnach muss die Photonenenergie mit der charakteristischen Anregungsenergie des Atoms übereinstimmen.