Vorschlag B – Die Chemie der Brennnessel
Die Brennnessel ist als sogenanntes Wildkraut sehr bekannt. Sie wird seit Jahrtausenden als Heil- und Kulturpflanze genutzt. Die Große Brennnessel wurde deshalb zur Heilpflanze des Jahres 2022 gekürt. In der Küche finden die Blätter der Brennnessel Verwendung als Salat, Smoothie oder Pesto. Sie enthält unter anderem Vitamin C sowie zahlreiche Proteine mit essenziellen Aminosäuren (Material 1 und 2).
Außerdem können aus Brennnesseln auch Textilien hergestellt werden. Für die Herstellung von Naturfaser-Kleidung gelten die Fasern als gute Alternative zur Baumwolle.
In den Blättern der Brennnessel ist viel Nitrat enthalten. Deshalb wird die Brennnessel in ökologisch betriebenen Gärten unter anderem gerne zu Dünger verarbeitet.
Die Brennhaare der Brennnessel sitzen überall an der Pflanze und sollen diese vor Fressfeinden schützen. Die Brennhaare sind lange Röhren, deren Wände im oberen Bereich durch eingelagerte Kieselsäure hart und spröde wie Glas sind (Material 4). Bei der leichtesten Berührung dringen diese in die Haut ein. Die Brennflüssigkeit, in der unter anderem Methansäure (Material 3) enthalten ist, dringt dann in die Haut ein und kann juckende, schmerzende Schwellungen auf der Haut entstehen lassen.
 frische Brennnesselblätter enthalten eine Stoffmenge von
frische Brennnesselblätter enthalten eine Stoffmenge von  Vitamin C
Vitamin C  Der durchschnittliche Tagesbedarf einer erwachsenen Person an Vitamin C liegt bei etwa
Der durchschnittliche Tagesbedarf einer erwachsenen Person an Vitamin C liegt bei etwa  Berechne die Masse an Vitamin C, die in
Berechne die Masse an Vitamin C, die in  Brennnesselblättern enthalten ist.
Begründe, ob diese Portion den Tagesbedarf an Vitamin C decken kann.
Brennnesselblättern enthalten ist.
Begründe, ob diese Portion den Tagesbedarf an Vitamin C decken kann.
2.1
Die Textilfasern aus Brennnesseln enthalten zu einem hohen Anteil Cellulose.
Gib die Haworth- und die Fischer-Projektion des Monomers der Cellulose an.
Benenne dieses in der Haworth-Projektion dargestellte Monomer.
Zeichne einen Molekülausschnitt der Cellulose, in dem vier Monomer-Einheiten miteinander verknüpft sind.
Benenne die glykosidische Bindung.
(8 BE)
2.2
(5 BE)
2.3
Da Nitrat-Ionen  aus den Brennnesselblättern zu gesundheitsschädlichen Nitrit-Ionen
aus den Brennnesselblättern zu gesundheitsschädlichen Nitrit-Ionen  umwandelt werden, sollte ein Brennnesselgericht nicht zu lange gelagert werden.
Im Labor können Nitrat-Ionen in saurer Lösung mit elementarem Zink zu Nitrit-Ionen umgewandelt werden. Dabei entstehen auch
umwandelt werden, sollte ein Brennnesselgericht nicht zu lange gelagert werden.
Im Labor können Nitrat-Ionen in saurer Lösung mit elementarem Zink zu Nitrit-Ionen umgewandelt werden. Dabei entstehen auch  -Ionen.
Formuliere für diese im Labor stattfindende Reaktion die Reaktionsgleichung und zeige anhand der wesentlichen Oxidationszahlen und der Elektronenübergänge, dass es sich hierbei um eine Redoxreaktion handelt.
-Ionen.
Formuliere für diese im Labor stattfindende Reaktion die Reaktionsgleichung und zeige anhand der wesentlichen Oxidationszahlen und der Elektronenübergänge, dass es sich hierbei um eine Redoxreaktion handelt.
(6 BE)
2.4
Benenne die beiden Aminosäuren Lysin und Leucin (Material 1) nach der IUPAC-Nomenklatur.
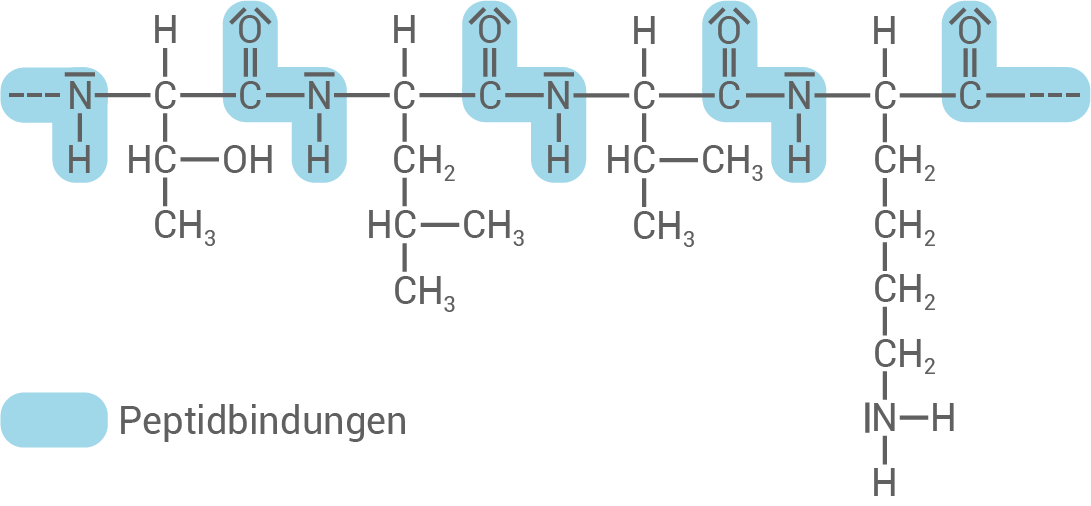
Zeichne einen Ausschnitt aus einem Protein, in dem die vier Aminosäuren Threonin, Leucin, Valin und Lysin (Material 1) in der angegebenen Reihenfolge miteinander verknüpft sind.
Ordne die vier Aminosäuren Threonin, Leucin, Valin und Lysin jeweils einer Gruppe (Material 2) zu und begründe auch anhand der Strukturformeln deine Entscheidung.
(13 BE)
2.5
Löst man Methansäure in Wasser und prüft den pH-Wert, so stellt man einen sauren pH-Wert fest. Hingegen ergibt Natriumformiat (enthält  - und
- und  -Ionen) in Wasser einen leicht alkalischen pH-Wert der Lösung.
Gib die Reaktionsgleichung der Reaktion von Methansäure mit Wasser an und beschrifte die korrespondierenden Säure-Base-Paare.
Berechne den
-Ionen) in Wasser einen leicht alkalischen pH-Wert der Lösung.
Gib die Reaktionsgleichung der Reaktion von Methansäure mit Wasser an und beschrifte die korrespondierenden Säure-Base-Paare.
Berechne den  - und den
- und den  -Wert von Methansäure mithilfe von Material 3.
Formuliere die Reaktionsgleichung der Reaktion von Natriumformiat mit Wasser und erkläre anhand dieser Reaktionsgleichung den alkalischen pH-Wert.
-Wert von Methansäure mithilfe von Material 3.
Formuliere die Reaktionsgleichung der Reaktion von Natriumformiat mit Wasser und erkläre anhand dieser Reaktionsgleichung den alkalischen pH-Wert.
(11 BE)
2.6
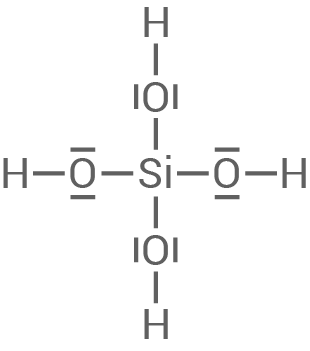
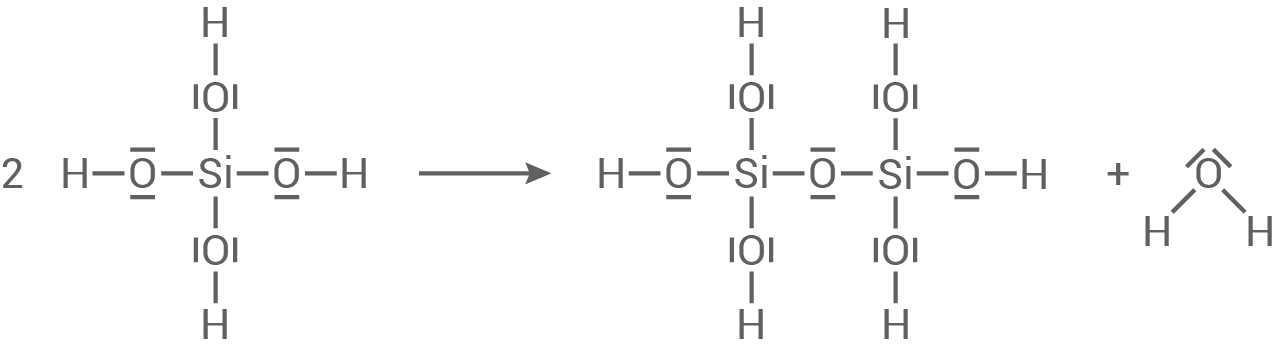
Entwickle die Reaktionsgleichungen der Reaktion von Mono-Kieselsäure zu Di-Kieselsäure sowie der Reaktion von Di-Kieselsäure mit Mono-Kieselsäure zu Tri-Kieselsäure unter Verwendung von Strukturformeln (Material 4).
Erkläre die Entstehung eines vernetzten Poly-Kieselsäure-Moleküls aus Mono-Kieselsäure durch weitere Kondensationsreaktionen (Material 4).
(7 BE)
Material 1
Natürlich vorkommende essenzielle Aminosäuren (nur die Reste sind angegeben)
| Name | Rest |
|---|---|
| Isoleucin | |
| Leucin | |
| Lysin | |
| Methionin | |
| Threonin | |
| Valin |
Material 2
Einteilung der Aminosäuren
Die Eigenschaften der Aminosäuren werden durch ihre Reste beeinflusst. Die Einteilung der Aminosäuren aufgrund ihrer Reste erfolgt in die folgenden vier Gruppen:- Neutrale Aminosäuren mit unpolarem Rest
- Neutrale Aminosäuren mit polarem Rest
- Saure Aminosäuren
- Basische Aminosäuren
Material 3
Gleichgewichtskonzentrationen in einer Methansäure-Lösung
| Verbindung | Konzentrationen im Gleichgewicht in |
|---|---|
| Methansäure | |
| Methansäure-Anion | |
Material 4
Kieselsäure
Als Kieselsäure bezeichnet man die Sauerstoffsäuren des Siliciums. Die einfachste Kieselsäure ist Mono-Kieselsäure, die zur (Poly-)Kondensation neigt. Zwei Mono-Kieselsäure-Moleküle reagieren in einer Kondensationsreaktion zu Di-Kieselsäure. Di-Kieselsäure-Moleküle können nun auf analoge Weise mit weiteren Kieselsäure-Molekülen reagieren, dabei können vernetzte Poly-Kieselsäure-Moleküle entstehen, die Bestandteile der Brennhaare der Brennnessel sind. Mono-Kieselsäure:
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?
2.1
Haworth-Projektion eines Cellulose-Monomers
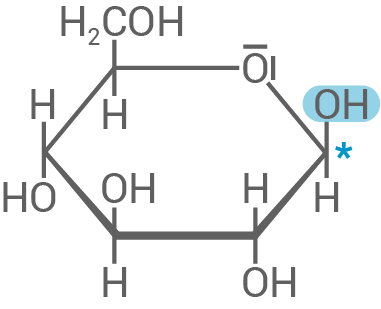 Fischer-Projektion eines Cellulose-Monomers
Fischer-Projektion eines Cellulose-Monomers
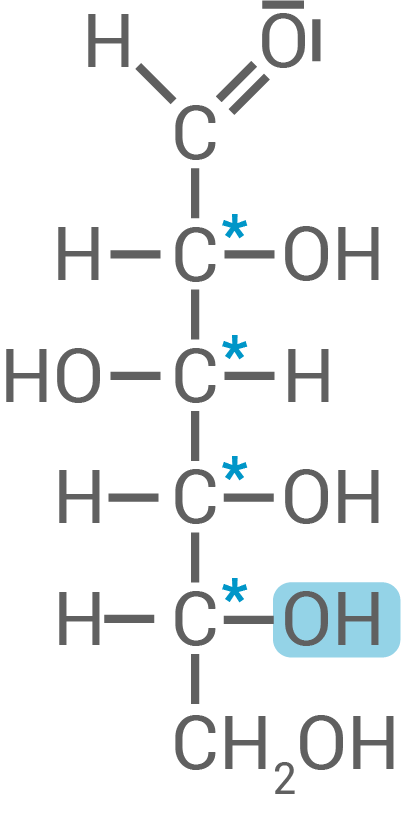 Bei dem Monomer handelt es sich um
Bei dem Monomer handelt es sich um  -D-Glucose.
Molekülausschnitt der Cellulose aus vier Monomer-Einheiten
-D-Glucose.
Molekülausschnitt der Cellulose aus vier Monomer-Einheiten
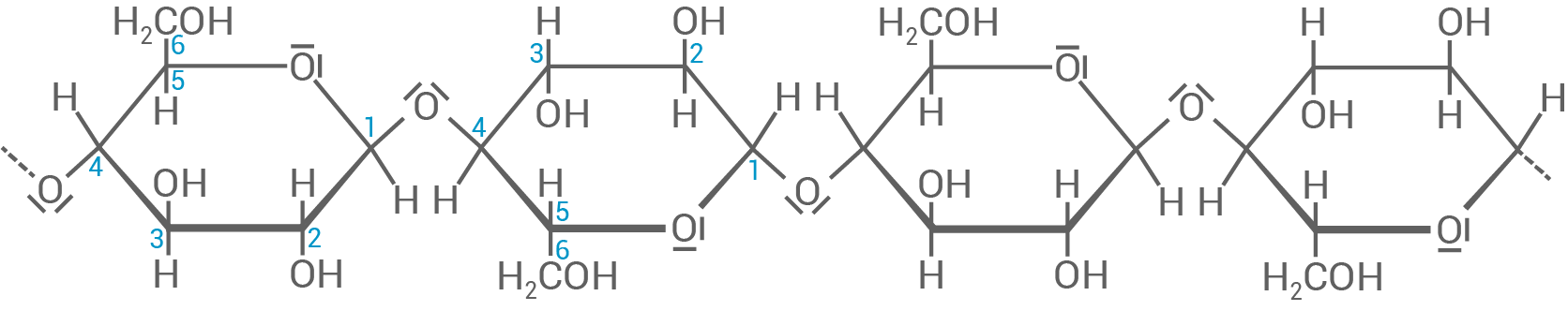 Die Monomere
Die Monomere  -D-Glucose-Einheiten
-D-Glucose-Einheiten sind über eine
sind über eine  -1,4-glycosidische Bindung miteinander verknüpft.
-1,4-glycosidische Bindung miteinander verknüpft.

* anomeres  -Atom
-Atom

* chirale  -Atome
-Atome

2.2
Berechnung der Masse an Vitamin C
Die molare Masse von Vitamin C ergibt sich aus der Summenformel:
Mit der gegebenen Stoffmenge von Vitamin C kann folglich die Masse berechnet werden:
In  frischen Brennnesselblättern sind
frischen Brennnesselblättern sind  Vitamin C enthalten.
Der Tagesbedarf an Vitamin C kann mit dieser Portion an Brennnesselblättern gedeckt werden, da diese mehr als
Vitamin C enthalten.
Der Tagesbedarf an Vitamin C kann mit dieser Portion an Brennnesselblättern gedeckt werden, da diese mehr als  enthalten.
enthalten.
2.3
Reaktionsgleichung der Nitratumwandlung
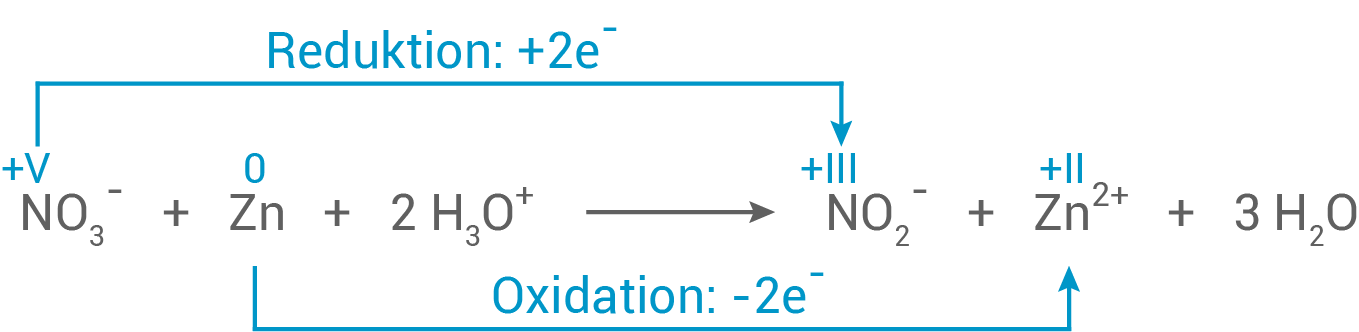 Oxidation: Das Zinkatom gibt zwei Elektronen ab und wird oxidiert.
Oxidation: Das Zinkatom gibt zwei Elektronen ab und wird oxidiert.
0 +II
Reduktion: Das Stickstoffatom im Nitrat-Ion nimmt zwei Elektronen auf und wird reduziert.
+II
Reduktion: Das Stickstoffatom im Nitrat-Ion nimmt zwei Elektronen auf und wird reduziert.
+V +III
+III

0
+V
2.4
Benennung der Aminosäuren nach der IUPAC-Nomenklatur
 Zuordnung der Aminosäuren
Zuordnung der Aminosäuren
- Lysin: 2,6-Diaminohexansäure
- Leucin: 2-Amino-4-methylpentansäure

| Threonin |
|
|---|---|
| Leucin |
|
| Valin |
|
| Lysin |
|
2.5
Reaktionsgleichung und Säure-Base-Paare



Berechnung des  - und des
- und des  -Werts von Methansäure
Für den
-Werts von Methansäure
Für den  -Wert gilt:
-Wert gilt:
![\(\begin{array}[t]{rll}
K_S&=& \dfrac{c(H_3O^+) \cdot c(HCOO^-)}{c(HCOOH)} & \\[5pt]
&=& \dfrac{0,00591 \cdot 0,00591}{0,194} & \\[5pt]
&=& 1,8 \cdot 10^{-4}
\end{array}\)](https://www.schullv.de/resources/formulas/63ade0866936b9d8b4728c032b246a2072c6b7fef7edb2c3d3941efeae378b35_light.svg) Daraus folgt der
Daraus folgt der  -Wert:
-Wert:
![\(\begin{array}[t]{rll}
pK_S&=& -\log (K_S)& \\[5pt]
&=& -\log (1,8 \cdot 10^{-4}) & \\[5pt]
&\approx& 3,75
\end{array}\)](https://www.schullv.de/resources/formulas/dbc6849bffedcb41bf3f35359433f58fff150373943cdc4f7feb1baf3c70cb21_light.svg) Reaktionsgleichung und alkalischer pH-Wert
Reaktionsgleichung und alkalischer pH-Wert


 Das Wasser fungiert hier als Protonendonator und die Format-Ionen als Protonenakzeptor. Es werden Hydroxid-Ionen
Das Wasser fungiert hier als Protonendonator und die Format-Ionen als Protonenakzeptor. Es werden Hydroxid-Ionen  gebildet und folglich wurde die Konzentration an Oxonium-Ionen
gebildet und folglich wurde die Konzentration an Oxonium-Ionen  verringert. Der pH-Wert wird demnach basischer
verringert. Der pH-Wert wird demnach basischer 
- Methansäure fungiert als Protonendonator (Säure) und gibt ein Proton ab.
- Wasser nimmt ein Proton auf, fungiert als Protonenakzeptor und stellt die Base dar.
2.6
Reaktionsgleichungen
Mono-Kieselsäure zu Di-Kieselsäure:
 Di-Kieselsäure mit Mono-Kieselsäure zu Tri-Kieselsäure
Di-Kieselsäure mit Mono-Kieselsäure zu Tri-Kieselsäure
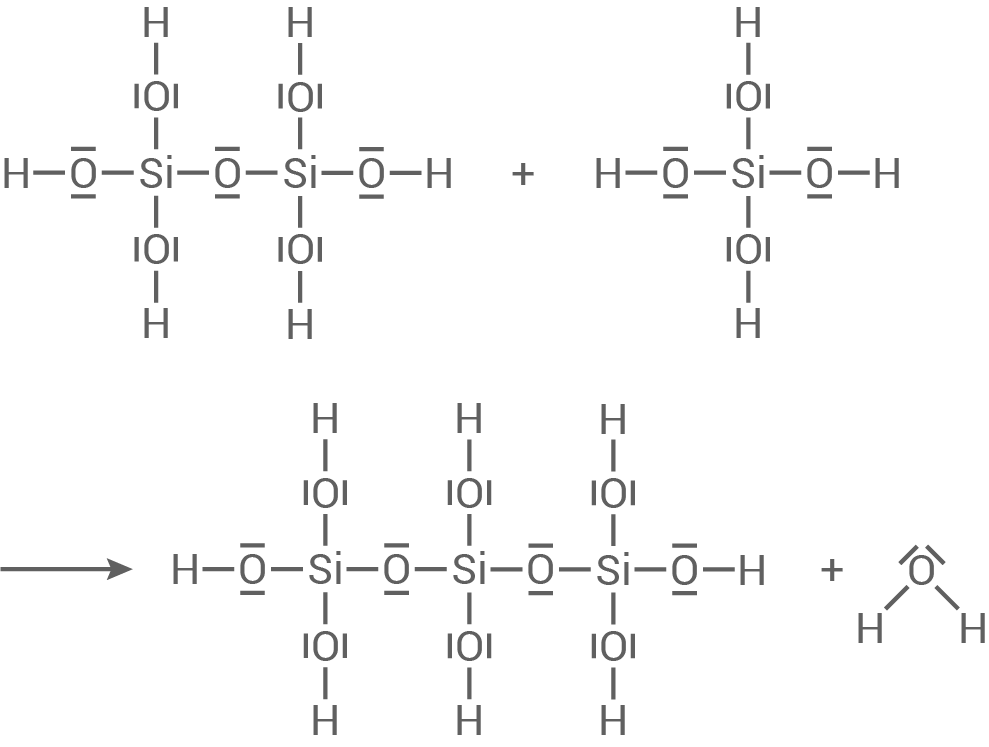 Entstehung eines vernetzten Poly-Kieselsäure-Moleküls
Entstehung eines vernetzten Poly-Kieselsäure-Moleküls


- Ein Kieselsäuremolekül verfügt über vier Hydroxygruppen, von denen zwei OH-Gruppen aus verschiedenen Molekülen durch eine Kondensationsreaktion miteinander verknüpft werden können.
- Dabei wird Wasser abgespalten und es entsteht eine sogenannte Sauerstoffbrücke.
- Aufgrund dieser Fähigkeit zur Reaktion aller vier Hydroxygruppen der Monokieselsäure mit weiteren Kieselsäuremolekülen kann die vernetzte Struktur der Polykieselsäure entstehen.