Vorschlag B – Kunststoffe
Ein häufig für Verpackungen verwendeter Kunststoff ist Polyethen (PE). Für dessen Herstellung wird Ethen benötigt, welches man u. a. aus Bio-Ethanol erzeugen kann. Unter Bio-Ethanol versteht man Ethanol, das man ausschließlich aus Biomasse oder den biologisch abbaubaren Anteilen von Abfällen herstellt.
Ein weiterer Kunststoff ist Polypropen (PP). Zur Herstellung dieses Kunststoffs wird Propen benötigt, welches man aus Ethen gewinnen kann (Material 1).
Aus Propan-1,2,3-triol kann man mit Citronensäure (Material 3) einen biobasierten Kunststoff gewinnen, das heißt einen Kunststoff, der auf der Basis nachwachsender Rohstoffe erzeugt wird. Im Labor kann man Propan-1,2,3-triol aus Propen herstellen (Material 2).
Kunststoffe werden in großen Mengen produziert (Material 4) und fallen dementsprechend als Müll an. Zur Lösung dieses sogenannten „Plastikmüllproblems“ werden verschiedene Ansätze diskutiert (Material 5).
1
Für die Herstellung von Polyethen wird häufig Bio-Ethanol als Ausgangsstoff verwendet.
Formuliere unter Verwendung von Strukturformeln für die organischen Verbindungen die Reaktionsgleichung der Reaktion von Ethanol zu Ethen und einem weiteren Produkt.
Formuliere den vollständigen Reaktionsmechanismus für die Synthese des Kunststoffs Polyethen ausgehend von Ethen mithilfe eines Peroxids  als Radikalstarter, wobei du zwei Monomere verknüpfst und zwei Reaktionen formulierst, die die Reaktion beenden.
Benenne den Reaktionsmechanismus und gib die Überschriften für die einzelnen Reaktionsschritte an.
als Radikalstarter, wobei du zwei Monomere verknüpfst und zwei Reaktionen formulierst, die die Reaktion beenden.
Benenne den Reaktionsmechanismus und gib die Überschriften für die einzelnen Reaktionsschritte an.
(10 BE)
2
Aus Ethen kann Propen hergestellt werden (Material 1), ein Ausgangsstoff zur Synthese des weiteren Kunststoffs Polypropen.
Formuliere für die drei Reaktionsschritte aus Material 1 jeweils eine Reaktionsgleichung in Strukturformeln.
Entwickle einen Strukturformelausschnitt aus einem Polypropen-Molekül, der drei Monomer-Einheiten umfasst.
(6 BE)
3
Propen ist ein Ausgangsstoff für die mehrstufige Synthese von Propan-1,2,3-triol (Material 2).
Formuliere die Strukturformeln für die in Material 2 genannten Verbindungen: Propen, 3-Chlorpropen, 1,2,3-Trichlorpropan und Propan-1,2,3-triol.
Ordne die in Material 2 angegebenen Syntheseschritte jeweils einem Reaktionsmechanismus zu und begründe deine Entscheidungen.
(8 BE)
4
Bei einer Veresterung handelt es sich um eine Gleichgewichtsreaktion, bei der sich die Ausbeute des Esters durch Änderungen der Konzentrationen, bei konstanter Temperatur, erhöhen lässt.
Propan-1,2,3-triol reagiert in einer Polykondensationsreaktion, deren Mechanismus dem einer säurekatalysierten Veresterung entspricht, mit Citronensäure (Material 3) zu einem biobasierten Kunststoff.
Erläutere die Grundlagen zur Erhöhung der Ausbeute des Esters unter den oben genannten Bedingungen.
Formuliere beispielhaft für jeweils eine funktionelle Gruppe den Reaktionsmechanismus der oben beschriebenen Reaktion von einem Molekül Propan-1,2,3-triol mit einem Molekül Citronensäure; nicht relevante Molekülteile können hierbei als „ “ und „
“ und „ “ definiert und abgekürzt werden.
“ definiert und abgekürzt werden.
(10 BE)
5
Der biobasierte Kunststoff aus Propan-1,2,3-triol und Citronensäure ist sehr gut in Wasser löslich, das Polyethen aus Aufgabe 1 nicht.
Entwickle einen Strukturformelausschnitt des biobasierten Kunststoffs aus Propan-1,2,3-triol und Citronensäure, indem du zwei Moleküle Propan-1,2,3-triol mit zwei Molekülen Citronensäure zu einem Polymer verknüpfst.
Hinweis
Bei der Entstehung des Kunststoffs reagieren nicht alle funktionellen Gruppen miteinander. Erkläre die unterschiedliche Wasserlöslichkeit von Polyethen und dem Kunststoff aus Propan-1,2,3-triol und Citronensäure.
Bei der Entstehung des Kunststoffs reagieren nicht alle funktionellen Gruppen miteinander. Erkläre die unterschiedliche Wasserlöslichkeit von Polyethen und dem Kunststoff aus Propan-1,2,3-triol und Citronensäure.
(9 BE)
6
Eine Grafik zur weltweiten Produktion von Kunststoffen im Jahr 2016 ist in Material 4 zu sehen. In Material 5 sind vier mögliche Verfahren beschrieben, Polyethen zu recyceln bzw. abzubauen.
Fasse die Hauptaussagen der Grafik in Material 4 zusammen.
Beurteile jede der vier in Material 5 aufgeführten Ansätze zur Lösung des Plastikmüllproblems.
(7 BE)
Material 1
Aus Ethen wird Propen
| Reaktionsschritt 1: | Zwei Moleküle Ethen reagieren unter Katalyse zu einem Molekül But-1-en. |
| Reaktionsschritt 2: | In einer Isomerisierung bildet sich But-2-en aus But-1-en. |
| Reaktionsschritt 3: | Ein Molekül But-2-en reagiert mit einem Molekül Ethen zu zwei Molekülen Propen. |
Material 2
Mehrstufige Synthese von Propan-1,2,3-triol aus Propen
- Zunächst wird Propen bei
oder unter Lichteinfluss mit elementarem Chlor zu 3-Chlorpropen und einem weiteren Produkt umgesetzt.
- Danach reagiert 3-Chlorpropen mit weiterem elementarem Chlor bei niedrigen Temperaturen und ohne Lichteinfluss zu 1,2,3-Trichlorpropan.
- Schließlich reagiert 1,2,3-Trichlorpropan mit Hydroxid-Ionen zu Propan-1,2,3-triol und Chlorid-Ionen.
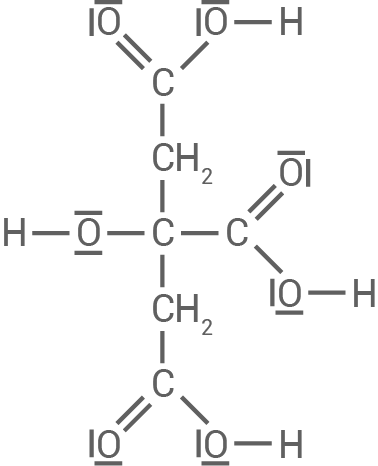
Material 3
Citronensäure

Material 4
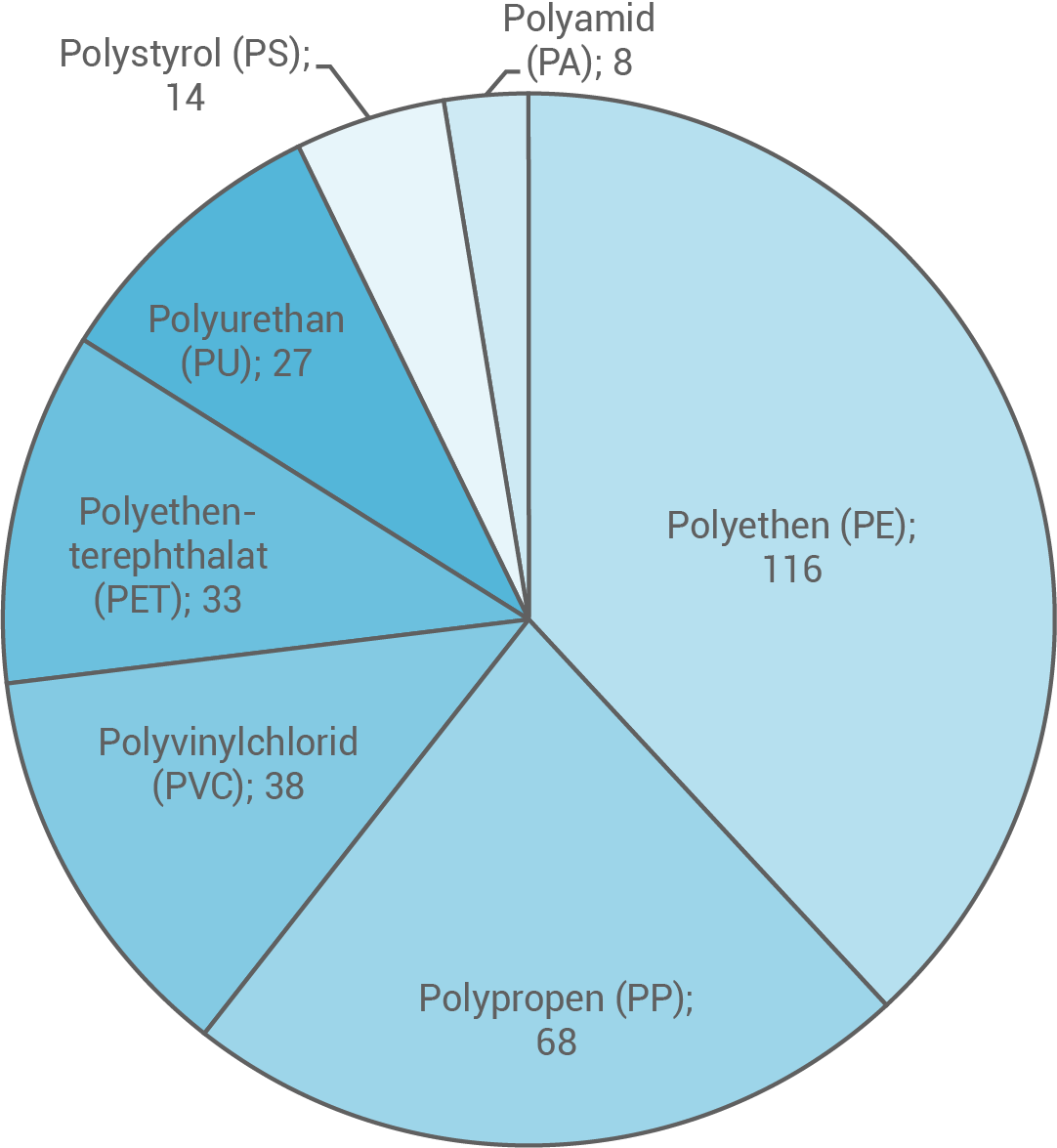
Weltweite Kunststoffproduktion im Jahr 2016
Jedes Jahr werden weltweit ca. 300 Millionen Tonnen Kunststoffe hergestellt. Die untenstehende Grafik zeigt die Anteile in Millionen Tonnen der im Jahr 2016 hauptsächlich produzierten Kunststoffe weltweit.
Material 5
Polyethen-Recycling – Kreislaufwirtschaft beim Plastik
Die Produktion, Verwendung und Entsorgung von Kunststoffen wird seit längerer Zeit auf verschiedenen Ebenen diskutiert. Ein Problem ist, dass Kunststoffe wie z. B. Polyethen häufig in die Umwelt gelangen und dort meist lange existieren, da sie sehr beständig sind und nur schwer abgebaut werden können. Dieser als „Plastikmüllproblem“ bezeichnete Fakt stellt eine Bedrohung für alle Lebewesen und deren Lebensräume dar. Neben bereits bekannten Recycling-Verfahren gibt es weltweit unterschiedliche Ansätze in der aktuellen Forschung, um das Plastikmüllproblem in den Griff zu bekommen bzw. im Idealfall zu vermeiden. Im Folgenden sind vier Möglichkeiten nur für Polyethen (PE) aufgeführt:- Werkstoffliches Recycling:
Wenn die Kunststoffe aus PE nicht verunreinigt oder mit Zusätzen versetzt sind, werden sie sortenrein sortiert, eingeschmolzen und danach zu neuen Produkten umgearbeitet. Dies geschieht mit etwades im Umlauf befindlichen PE.
- Rohstoffliches Recycling:
Die Rückgewinnung der Monomere Ethen durch rohstoffliches Recyceln erfolgt bei Temperaturen überDie Rückgewinnungsquote des Monomers bei diesem Verfahren liegt bei weniger als
- Umwandlung von Polyethen (PE) in Polypropen (PP):
In einem aktuell neu entwickelten Verfahren gelang es Forschern, aus PE den hochwertigeren Kunststoff PP herzustellen. PP ist ein Kunststoff, der vielseitiger als PE einsetzbar und besser durch Recycling-Verfahren wiederverwertbar ist. - Abbau von PE durch Pilze und Bakterien:
Indische Wissenschaftler haben herausgefunden, dass Organismen, wie z. B. bestimmte Pilze in der Lage sind, PE vollständig in Kohlenstoffdioxid und Wasser umzuwandeln. Chinesische Wissenschaftler untersuchten Bakterien, die die Fähigkeit besitzen, PE für den eigenen Stoffwechsel zu verwerten und damit abzubauen.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?
1
Reaktionsgleichung der Umwandlung von Ethanol zu Ethen
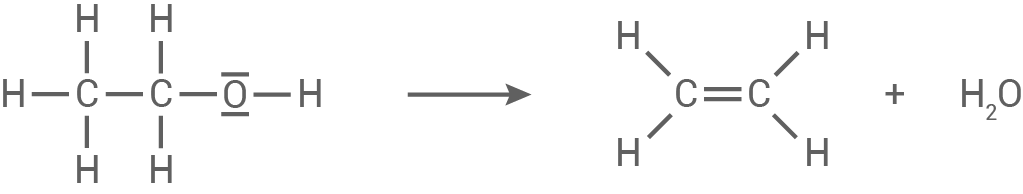 Reaktionsmechanismus für die Synthese von Polyethen aus Ethen
Ethen reagiert in einer radikalischen Polymerisation zu Polyethen.
Bildung des Startradikals:
Reaktionsmechanismus für die Synthese von Polyethen aus Ethen
Ethen reagiert in einer radikalischen Polymerisation zu Polyethen.
Bildung des Startradikals:
 Zunächst wird das Peroxid homolytisch gespalten.
Kettenstart:
Zunächst wird das Peroxid homolytisch gespalten.
Kettenstart:
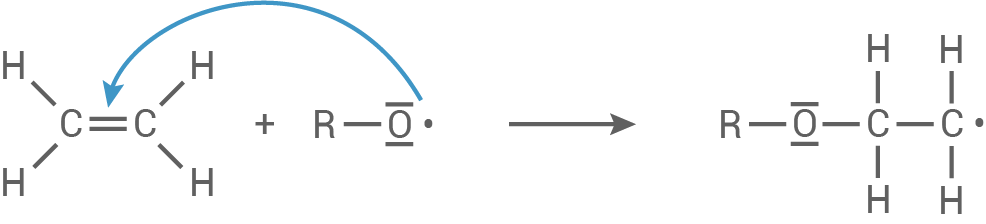 Das gebildete Radikal greift die Doppelbindung des 1,1,2,2-Tetrafluorethens an, wobei ein neues Radikal gebildet wird.
Kettenfortpflanzung:
Das gebildete Radikal greift die Doppelbindung des 1,1,2,2-Tetrafluorethens an, wobei ein neues Radikal gebildet wird.
Kettenfortpflanzung:
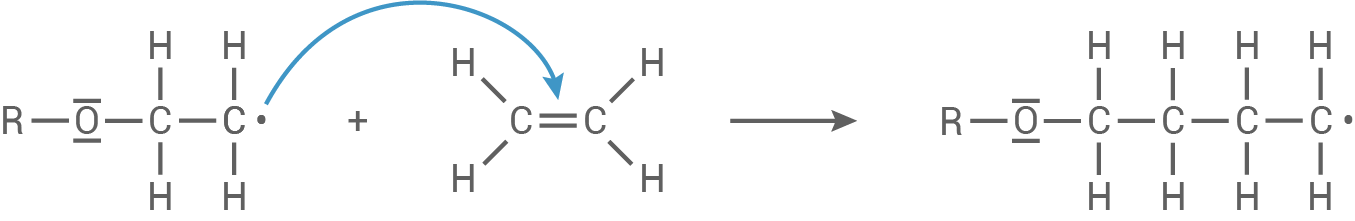 Das neue Radikal greift nun weitere Monomere an. Diese werden zum Makroradikal addiert.
Kettenabbruch:
Das neue Radikal greift nun weitere Monomere an. Diese werden zum Makroradikal addiert.
Kettenabbruch:
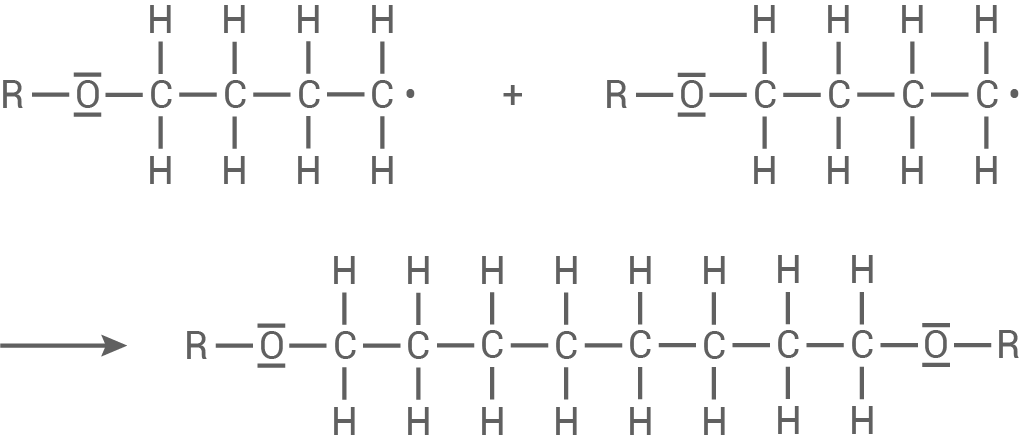 Es reagieren zwei Radikale zu einem stabilen Makromolekül.
Oder:
Es reagieren zwei Radikale zu einem stabilen Makromolekül.
Oder:
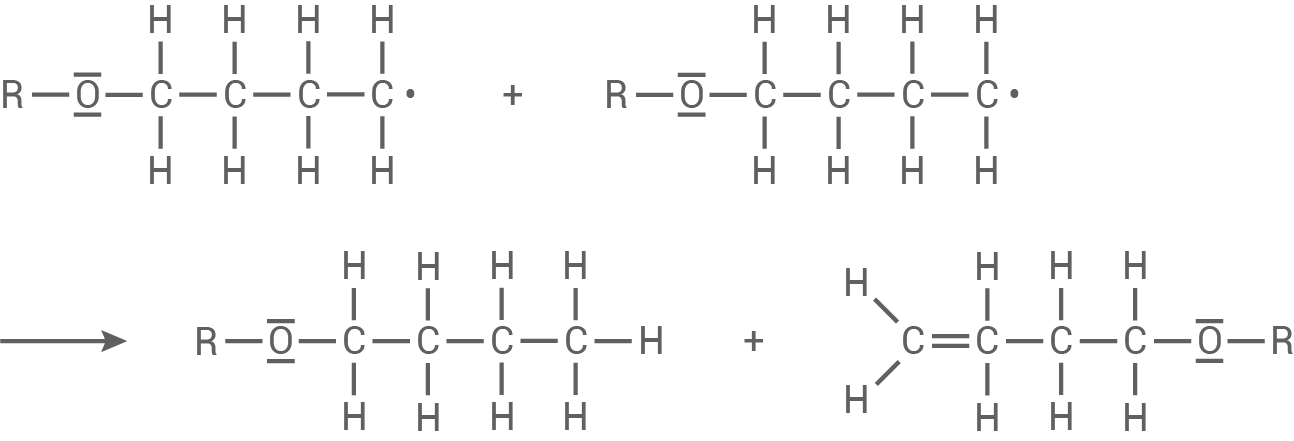 Es findet eine Disproportionierung statt.
Es findet eine Disproportionierung statt.


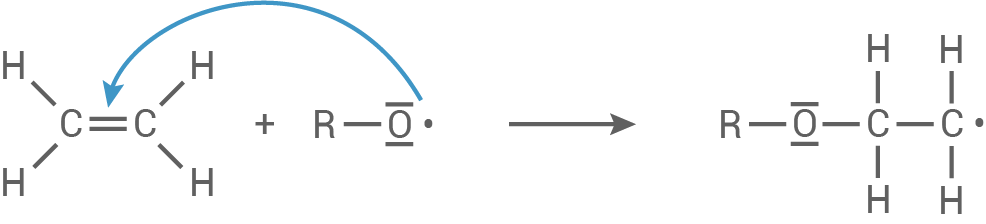



2
Reaktionsgleichungen in Strukturformeln
Reaktionsschritt 1: Dimerisierung von Ethen zu But-1-en
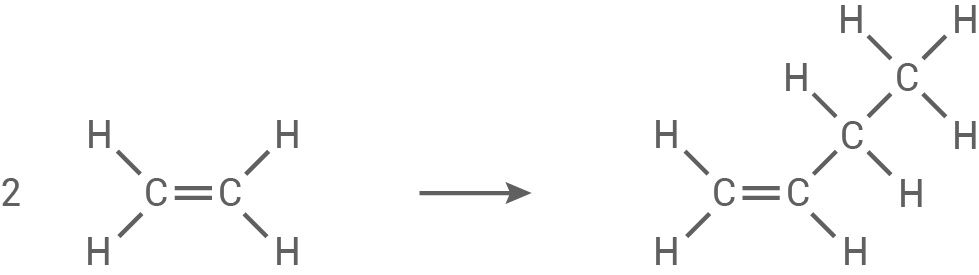 Reaktionsschritt 2: Isomerisierung von But-1-en zu But-2-en
Reaktionsschritt 2: Isomerisierung von But-1-en zu But-2-en
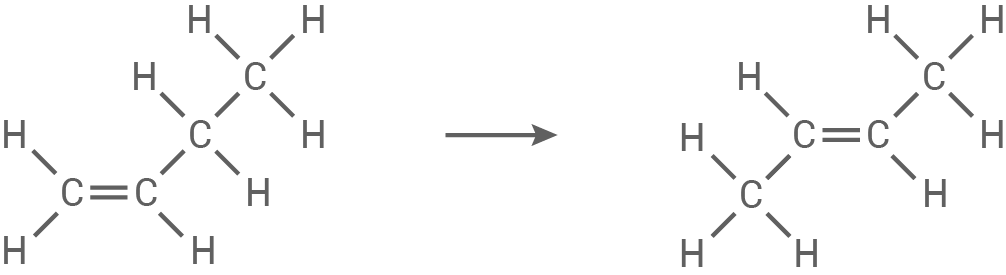 Reaktionsschritt 3: Bildung von Propen aus But-2-en und Ethen
Reaktionsschritt 3: Bildung von Propen aus But-2-en und Ethen
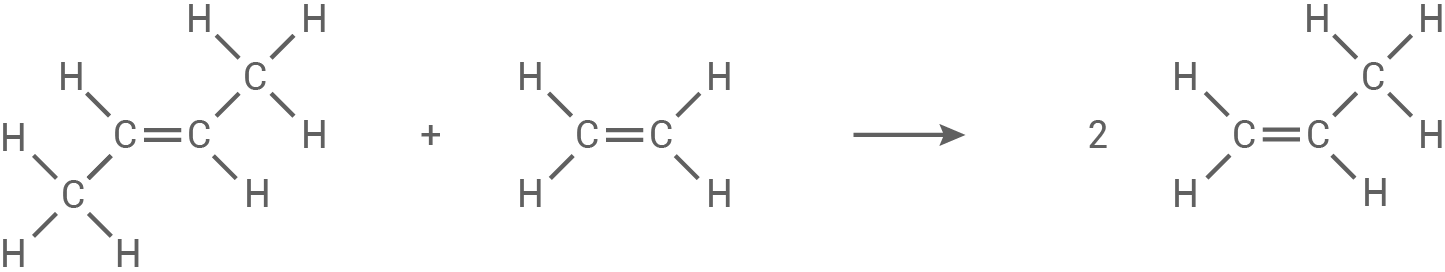 Strukturformelausschnitt von Polypropen
Strukturformelausschnitt von Polypropen
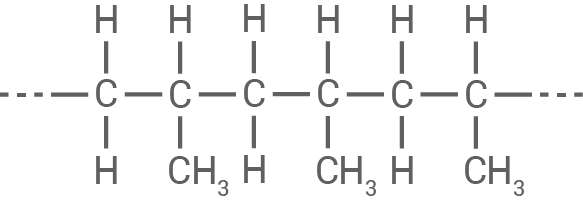




3
Strukturformeln
Zuordnung der Reaktionsmechanismen
| Propen |
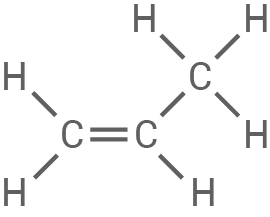
|
|---|---|
| 3-Chlorpropen |
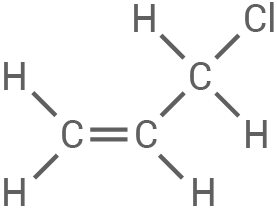
|
| 1,2,3-Trichlorpropan |
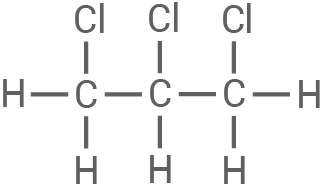
|
| Propan-1,2,3-triol |
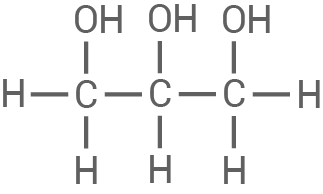
|
- Additionsreaktion (Propen zu 3-Chlorpropen):
Hier addiert sich ein Chlor-Radikal an die Doppelbindung von Propen. Das Chlor-Molekül wird durch Lichteinfluss in Radikale gespalten, wobei eines der Radikale die Doppelbindung angreift und 3-Chlorpropen bildet. - Substitutionsreaktion (3-Chlorpropen zu 1,2,3-Trichlorpropan):
Ohne Lichteinfluss erfolgt eine radikalische Substitution, bei der die Wasserstoffatome von 3-Chlorpropen durch Chloratome ersetzt werden. Dies führt zur Bildung von 1,2,3-Trichlorpropan, wobei Chlorid-Ionen als Nebenprodukte entstehen. - Hydrolyse (1,2,3-Trichlorpropan zu Propan-1,2,3-triol):
Hydroxid-Ionenersetzen in einer nukleophilen Substitution die Chloratome von 1,2,3-Trichlorpropan, was zur Bildung von Propan-1,2,3-triol (Glycerin) führt. Chlorid-Ionen werden als Nebenprodukt freigesetzt.
4
Ausbeutesteigerung bei der Veresterung
Die Veresterung ist eine Gleichgewichtsreaktion, bei der eine Carbonsäure mit einem Alkohol zu einem Ester und Wasser reagiert. Da es sich um eine Gleichgewichtsreaktion handelt gilt das Prinzip des kleinsten Zwangs von LE CHATELIER und BRAUN.
Die Ausbeute des Esters kann demnach zum einen erhöhrt werden, indem die Konzentration von Carbonsäure oder Alkohol erhöht wird und sich das Gleichgewicht auf die Produktseite verschiebt. Zum anderen kann das Nebenprodukt Wasser kontinuierlich entfernt werden, um die Rückreaktion zu verhindern und so die Esterbildung zu begünstigen.
Reaktionsmechanismus für die säurekatalysierte Veresterung
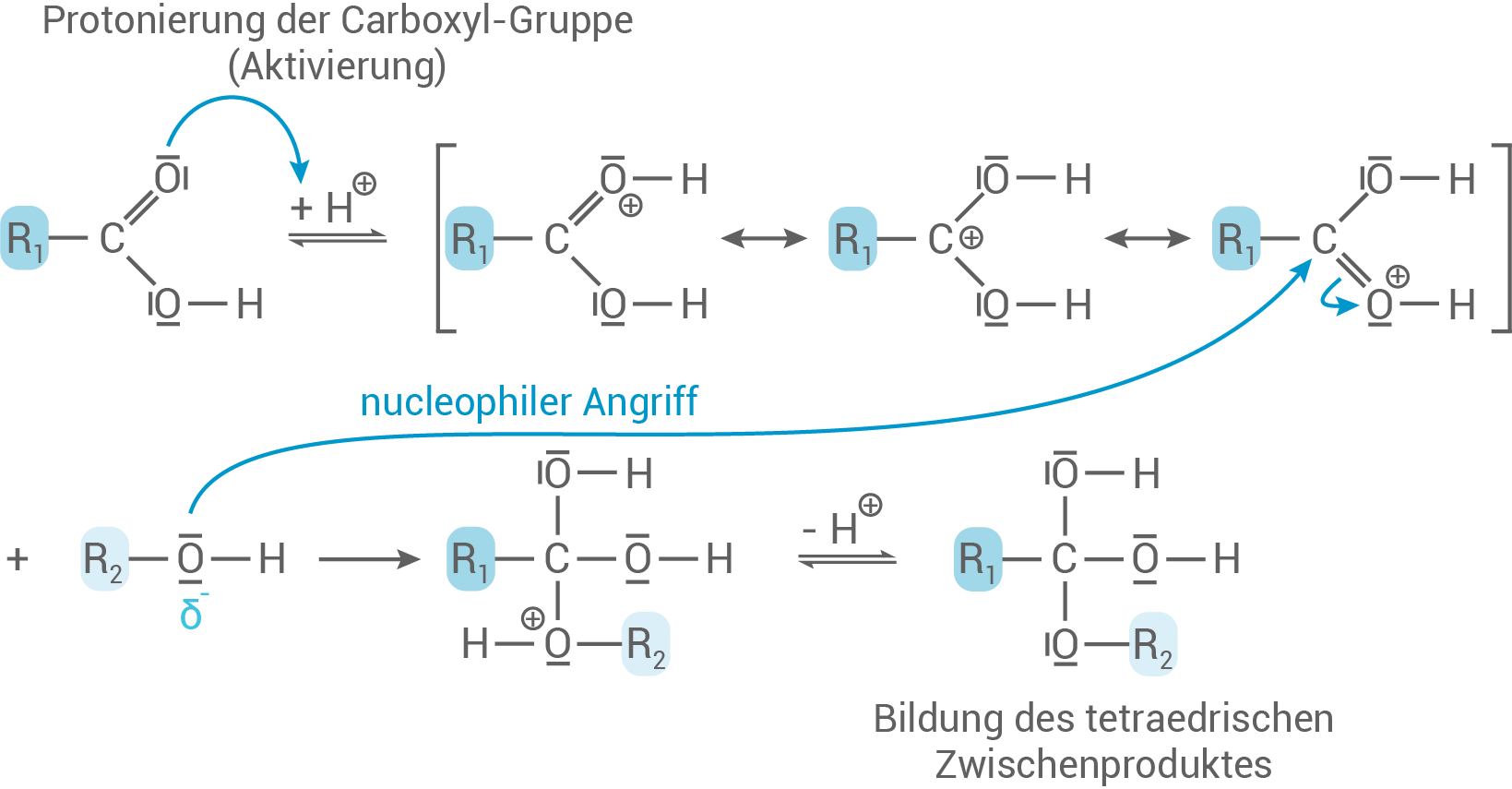 Zunächst wird die Carboxyl-Gruppe protoniert
Zunächst wird die Carboxyl-Gruppe protoniert  z.B. durch Zugabe von
z.B. durch Zugabe von  Hierbei greift das Carbonyl-Sauerstoffatom nucleophil
Hierbei greift das Carbonyl-Sauerstoffatom nucleophil  an. Es entsteht ein kationisches Zwischenprodukt, welches mesomeriestabilisiert ist. Diese erste katalytische Reaktion, durch Säurezugabe, ist wichtig, um die folgende Reaktion zu erleichtern. Der Alkohol besitzt eine Hydroxy-Gruppe, die das positiv polarisierte Carbonyl-Kohlenstoffatom nun nucleophil angreift. Es wird das tetraedrische Zwischenprodukt gebildet.
an. Es entsteht ein kationisches Zwischenprodukt, welches mesomeriestabilisiert ist. Diese erste katalytische Reaktion, durch Säurezugabe, ist wichtig, um die folgende Reaktion zu erleichtern. Der Alkohol besitzt eine Hydroxy-Gruppe, die das positiv polarisierte Carbonyl-Kohlenstoffatom nun nucleophil angreift. Es wird das tetraedrische Zwischenprodukt gebildet.
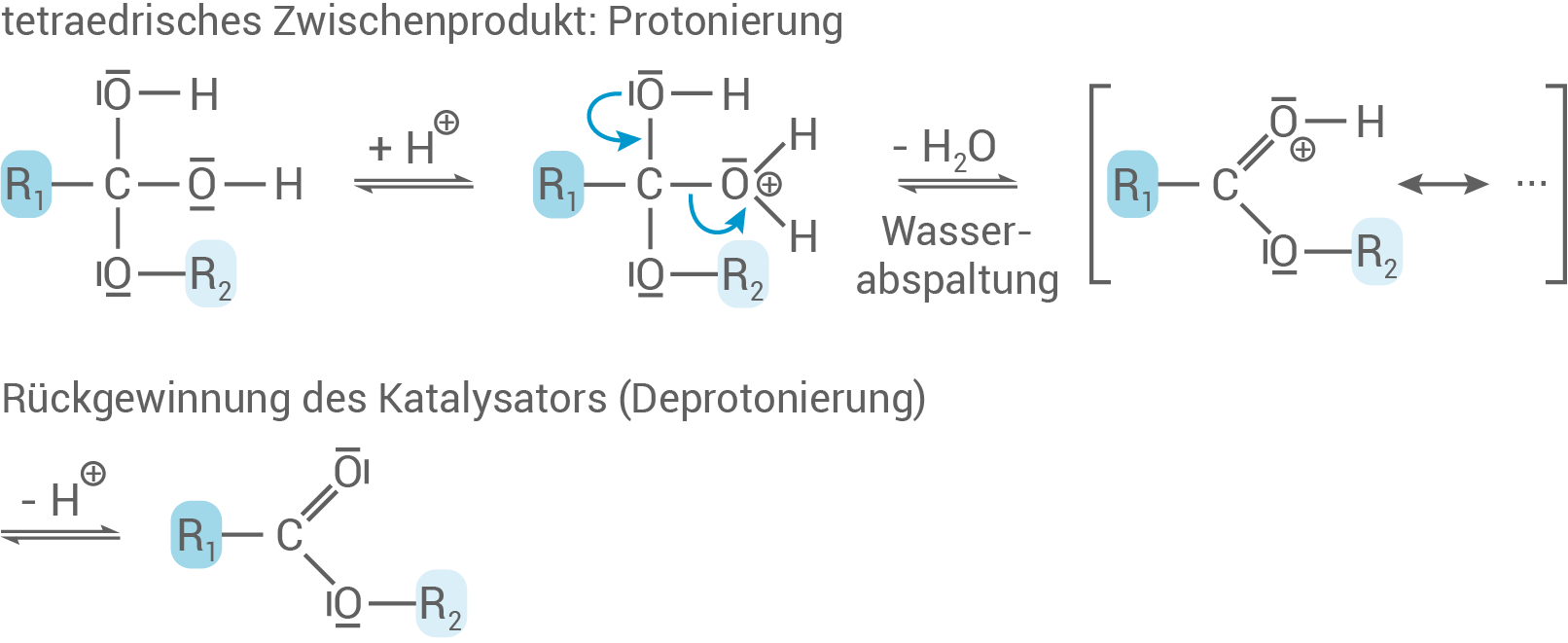 Durch erneute Protonierung bildet das tetraedrisches Zwischenprodukt eine gute Abgangsgruppe, nämlich
Durch erneute Protonierung bildet das tetraedrisches Zwischenprodukt eine gute Abgangsgruppe, nämlich  Wasser wird abgespalten und anschließend kommt es zur Deprotonierung des Kations. Der Katalysator wird zurückgewonnen und es bildet sich ein Ester.
Wasser wird abgespalten und anschließend kommt es zur Deprotonierung des Kations. Der Katalysator wird zurückgewonnen und es bildet sich ein Ester.


5
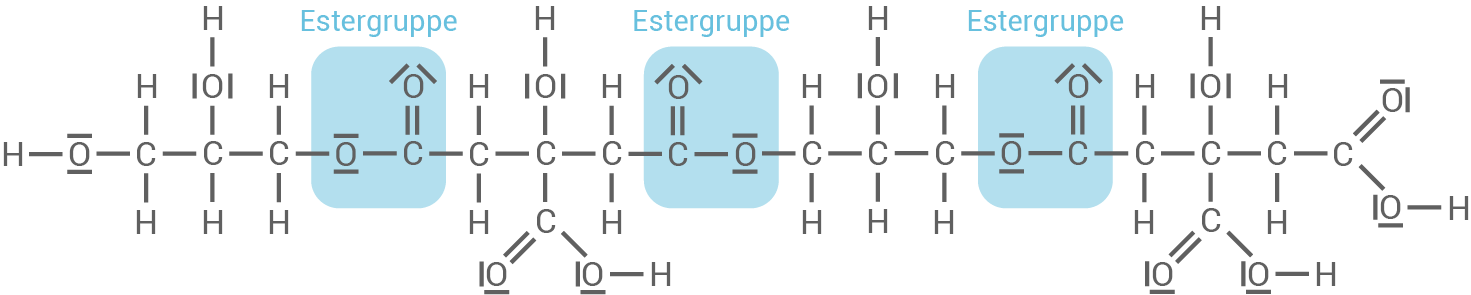
Strukturformelausschnitt des biobasierten Kunststoffs
 Wasserlöslichkeit von Polyethen vs. biobasierter Kunststoff
Polyethen (PE) ist wasserunlöslich, da es aus unpolaren Kohlenwasserstoffketten besteht, die keine funktionellen Gruppen enthalten, die mit Wasser interagieren können. Seine unpolare Struktur verhindert die Bildung von Wasserstoffbrückenbindungen mit Wassermolekülen, was es hydrophob macht.
Im Gegensatz dazu ist der biobasierte Kunststoff aus Propan-1,2,3-triol und Citronensäure wasserlöslich, da er viele polare funktionelle Gruppen wie Hydroxyl- und Carboxylgruppen enthält. Diese polaren Gruppen ermöglichen Wasserstoffbrückenbindungen mit Wassermolekülen, was zu einer guten Wasserlöslichkeit führt.
Diese Unterschiede in der Struktur machen Polyethen hydrophob und den biobasierten Kunststoff wasserlöslich.
Wasserlöslichkeit von Polyethen vs. biobasierter Kunststoff
Polyethen (PE) ist wasserunlöslich, da es aus unpolaren Kohlenwasserstoffketten besteht, die keine funktionellen Gruppen enthalten, die mit Wasser interagieren können. Seine unpolare Struktur verhindert die Bildung von Wasserstoffbrückenbindungen mit Wassermolekülen, was es hydrophob macht.
Im Gegensatz dazu ist der biobasierte Kunststoff aus Propan-1,2,3-triol und Citronensäure wasserlöslich, da er viele polare funktionelle Gruppen wie Hydroxyl- und Carboxylgruppen enthält. Diese polaren Gruppen ermöglichen Wasserstoffbrückenbindungen mit Wassermolekülen, was zu einer guten Wasserlöslichkeit führt.
Diese Unterschiede in der Struktur machen Polyethen hydrophob und den biobasierten Kunststoff wasserlöslich.

6
Zusammenfassung der Grafik zur weltweiten Kunststoffproduktion
Die Grafik zeigt, dass im Jahr 2016 weltweit rund 300 Millionen Tonnen Kunststoffe produziert wurden. Polyethen (PE) ist der am häufigsten hergestellte Kunststoff und wird in großen Mengen produziert, gefolgt von Polypropen (PP). Weitere wichtige Kunststoffe, die signifikante Anteile an der globalen Produktion haben, sind Polyvinylchlorid (PVC), Polystyrol (PS) und Polyethylenterephthalat (PET). Insgesamt zeigt die Grafik, dass die Kunststoffproduktion stark auf diese fünf Haupttypen konzentriert ist, was die zentrale Rolle dieser Kunststoffe in verschiedenen Industrien verdeutlicht.
Beurteilung der vier Ansätze zur Lösung des Plastikmüllproblems
- Werkstoffliches Recycling:
Bei diesem Verfahren wird Polyethen sortenrein eingeschmolzen und zu neuen Produkten verarbeitet. Es ist ein etabliertes Verfahren und relativ effizient, solange das Material sauber und frei von Verunreinigungen ist. Ein Nachteil besteht darin, dass die Qualität des recycelten Materials nach mehreren Recyclingzyklen abnimmt, was die Wiederverwendung einschränkt. - Rohstoffliches Recycling:
Beim rohstofflichen Recycling wird Polyethen bei hohen Temperaturen in seine Monomere, insbesondere Ethen, zerlegt. Dies ermöglicht die Herstellung von neuem Polyethen in hoher Qualität. Allerdings ist dieses Verfahren sehr energieintensiv, und die Rückgewinnungsrate ist oft gering, was seine Effizienz einschränkt. Es stellt jedoch eine Möglichkeit dar, die Abhängigkeit von neuem Kunststoff zu reduzieren. - Umwandlung von Polyethen (PE) in Polypropen (PP):
Diese neue Methode, Polyethen in Polypropen umzuwandeln, bietet großes Potenzial, da Polypropen vielseitiger einsetzbar und besser recycelbar ist. Da Polypropen höherwertiger ist als Polyethen, könnte diese Methode helfen, den Wert von Kunststoffabfällen zu erhöhen und sie in der Industrie häufiger wiederzuverwenden. Es handelt sich um einen vielversprechenden Ansatz, der die Menge an neu produziertem Kunststoff reduzieren könnte. - Abbau von PE durch Pilze und Bakterien:
Diese innovative Methode nutzt Mikroorganismen, um Polyethen in Kohlenstoffdioxid und Wasser zu zersetzen. Obwohl noch in der Entwicklungsphase, zeigt dieser Ansatz großes Potenzial für die langfristige Lösung des Plastikmüllproblems, da er eine biologische und umweltfreundliche Alternative zu herkömmlichen Recyclingmethoden darstellt. Allerdings ist noch viel Forschung notwendig, um diese Technologie im großen Maßstab anzuwenden.