Vorschlag B – Tenside
Stoffe, mit deren Hilfe sich beim Waschen Verschmutzungen entfernen lassen, werden zusammenfassend mit dem Oberbegriff „Tenside“ bezeichnet. Im Zusammenhang mit der jeweiligen Molekülstruktur lassen sich verschiedene Arten von Tensiden unterscheiden. Das älteste in der Menschheitsgeschichte bekannte Tensid ist Seife. Seifen lassen sich mithilfe von Lauge aus Fetten herstellen, wobei die Triglyceride, aus denen die Fette zusammengesetzt sind, durch eine alkalische Hydrolyse gespalten werden. Da das Waschen mit Seife auch Nachteile mit sich bringt, werden heute in vielen Fällen stattdessen sogenannte „synthetische Tenside“ verwendet, die künstlich hergestellt werden. Neben Wasch- und Spülmitteln enthalten auch Weichspüler Tenside, durch die sich beispielsweise aus Cellulose-Fasern bestehende Handtücher nach dem Waschen weicher anfühlen. Rohstoffe für die Herstellung synthetischer Tenside können aus Erdöl gewonnen werden, jedoch kommen auch tierische und pflanzliche Fette zum Einsatz.
Formuliere mithilfe von Material 1 die Strukturformel eines Triglycerid-Moleküls mit allen bindenden und nicht bindenden Elektronenpaaren, an das insgesamt genau zwei Moleküle Brom addiert werden können.
Formuliere den Reaktionsmechanismus der alkalischen Hydrolyse dieses Triglycerids mit Natronlauge beispielhaft an einer der funktionellen Gruppen, wobei du an der Reaktion nicht beteiligte Bereiche einmal an der Triglycerid-Molekülstruktur definieren und nachfolgend mit „R1“, „R2“ etc. abkürzen kannst.
Bei zwei Experimenten wird jeweils eine Base in Wasser gegeben. Im ersten Experiment wird ein Gramm festes Natriumhydroxid in so viel Wasser aufgelöst, dass 100 Milliliter Lösung entstehen. Im zweiten Experiment wird Natriumamid () in Wasser gegeben. Dabei kommt es zu einer Säure-Base-Reaktion, wobei das Protolysegleichgewicht weitgehend auf der Produktseite liegt.
Berechne den pH-Wert der im ersten Experiment entstehenden Natronlauge.
Formuliere zum zweiten Experiment die Reaktionsgleichung und prüfe am Beispiel dieser Reaktion im Zusammenhang mit dem Protolysegleichgewicht die Richtigkeit der folgenden Aussage: „Ist der pKB-Wert einer Brönsted-Base niedriger als der des Hydroxid-Ions, so liegt in einer wässrigen Lösung dieser Brönsted-Base die dazu korrespondierende Säure mit überwiegendem Anteil vor.“
Formuliere für jede der drei in Material 2 genannten nachteiligen Eigenschaften von Seife jeweils eine Reaktionsgleichung, wobei du nicht an der Reaktion beteiligte Bereiche der Molekülstruktur jeweils wie in Material 2 mit „R“ abkürzt.
Erkläre, wie sich die Verwendung von Wasser mit sehr hohem Gehalt an beim Waschen mit Seife auf den Seifenverbrauch und auf das Entfernen von Verschmutzungen aus Textilien auswirkt.
Beschreibe mithilfe von Material 3 Gemeinsamkeiten und Unterschiede in der Struktur der zu verschiedenen „Tensid-Klassen“ gehörenden Tensid-Teilchen auch unter Berücksichtigung der Polarität.
Benenne für den in Material 3 genannten Schritt 1 den Reaktionsmechanismus und für Reaktion 2 den Reaktionstyp.
Formuliere mithilfe von Material 3 für Schritt 3 der Herstellung eines anionischen Tensids den vollständigen Reaktionsmechanismus für die Reaktion von Benzol mit einem Alken nach der Balsohn-Alkylierung und erkläre, wie dazu beiträgt, dass diese Reaktion ablaufen kann.
Hinweis:
Mesomere Grenzstrukturen sollen beim Formulieren des Reaktionsmechanismus nicht berücksichtigt werden.
Formuliere mithilfe von Material 4 die mesomeren Grenzstrukturen für den Sigma-Komplex, der im Zuge der Entstehung von Struktur C auftritt.
Begründe, weshalb die Strukturen A und B im Produktgemisch mit höherem Anteil auftreten als die Struktur C.
Erkläre, weshalb die Sulfonierung eines Alkylbenzols schneller abläuft als die von Benzol.
Zeichne einen Strukturformelausschnitt eines Cellulose-Makromoleküls aus drei Monomer-Bausteinen.
Benenne die Verknüpfung der Monomer-Bausteine der Cellulose.
Erkläre mithilfe von Material 5 das Zustandekommen der Trockenstarre auf Teilchenebene und wie ein kationisches Tensid die Ausbildung der Trockenstarre verhindert.
Material 1
Namen verschiedener Fettsäuren
| Fettsäure (Trivialname) | Fettsäure (IUPAC-Nomenklatur) |
|---|---|
| Buttersäure | Butansäure |
| Caprylsäure | Octansäure |
| Laurinsäure ( |
Dodecansäure |
| Palmitinsäure ( |
Hexadecansäure |
| Stearinsäure ( |
Octadecansäure |
| Ölsäure ( |
(cis-)Octadec-9-ensäure |
| Linolsäure ( |
(cis-cis-)Octadeca-9,12-diensäure |
| Linolensäure ( |
(cis-cis-cis-)Octadeca-9,12,15-triensäure |
| Arachidonsäure ( |
(cis-cis-cis-cis-)Eicosa-5,8,11,14-tetraensäure |
Material 2
Aufbau und nachteilige Eigenschaften von Seifen
Seifen sind Natrium- oder Kaliumsalze langkettiger Carbonsäuren bzw. Fettsäuren oder
Bei der Anwendung der Seifen sind im Wesentlichen folgende Eigenschaften störend:
- Die Seifen-Anionen reagieren in wässriger Lösung als Brönsted-Basen. Die dadurch entstehende Lauge kann Textilien und auch die menschliche Haut angreifen.
- Starke Säuren setzen aus den Seifen-Anionen Carbonsäuren frei. Aus diesem Grund können Seifen für stark saure Verschmutzungen, wie sie zum Beispiel häufig in der Industrie auftreten, nicht verwendet werden.
- Die im Wasser unter anderem vorliegenden Calcium(II)-Ionen
bilden mit Seifen-Anionen schwer lösliche Salze, die sogenannten Kalkseifen. Die Kalkseifen lagern sich auf Textilien ab, wodurch diese grau und hart werden.
Material 3
Formeln von Tensiden
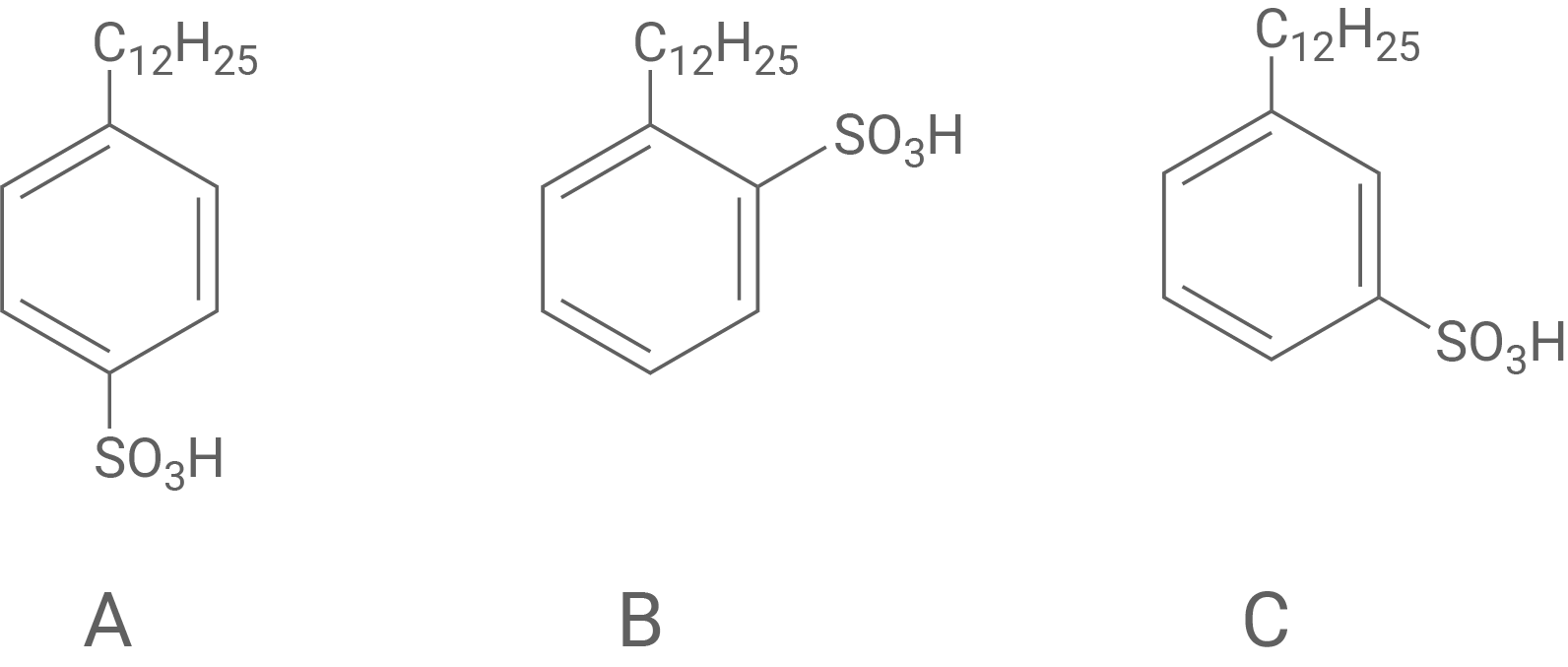
Die chemische Industrie hat in den letzten Jahrzehnten eine Vielzahl verschiedener Tenside mit jeweils charakteristischen Eigenschaften entwickelt. Die vier Strukturen A, B, C und D zeigen jeweils beispielhaft eine Struktur zu vier verschiedenen „Tensid-Klassen“.
A)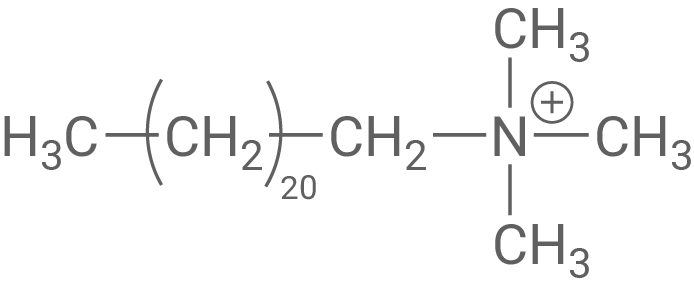
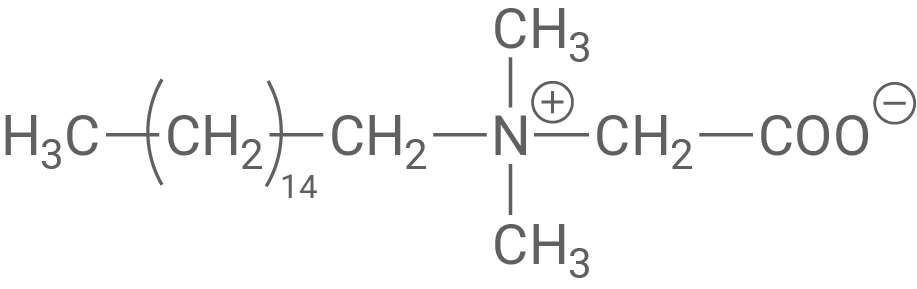
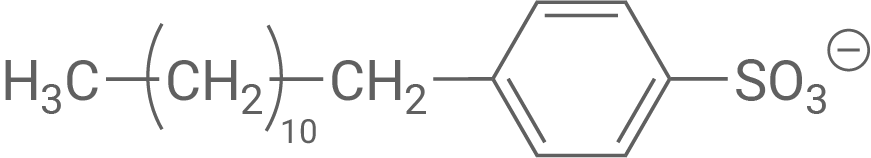
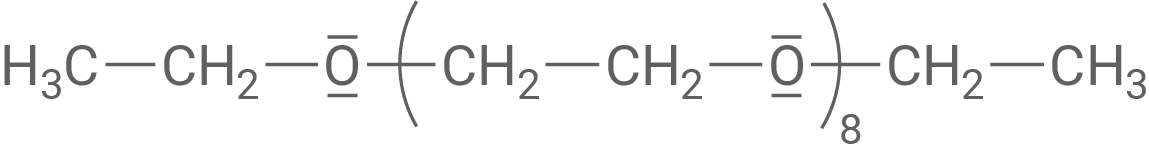
Herstellung eines anionischen Tensids
Alkylbenzolsulfonate sind häufig eingesetzte anionische Tenside. Sie können in großtechnischen Prozessen über verschiedene Reaktionsschritte hergestellt werden. Ein solcher Herstellungsweg ist folgender:
| Schritt 1: | Alkan + Chlor Chloralkan + Chlorwasserstoff |
| Schritt 2: | Chloralkan Alken + Chlorwasserstoff |
| Schritt 3: | Benzol + Alken |
| Schritt 4: | Alkylbenzol + Schwefeltrioxid |
| Schritt 5: | Alkylbenzolsulfonsäure + Natronlauge |
Balsohn-Alkylierung
Schritt 3 verläuft nach der sogenannten Balsohn-Alkylierung. Dabei wird Benzol (Benzen) in Anwesenheit von und
mit einem Alken zu einem sogenannten Alkylbenzol (Alkylbenzen) umgesetzt. Dies ist ein Stoff, bei dem ein Alkylrest an den Benzolring gebunden ist. Bei dieser Reaktion reagiert das Alken zunächst mit
und
Dabei wird ein Carbenium-Ion gebildet, das dann mit dem Benzol weiterreagiert. Im letzten Reaktionsschritt der Balsohn-Alkylierung werden
und
wieder freigesetzt.
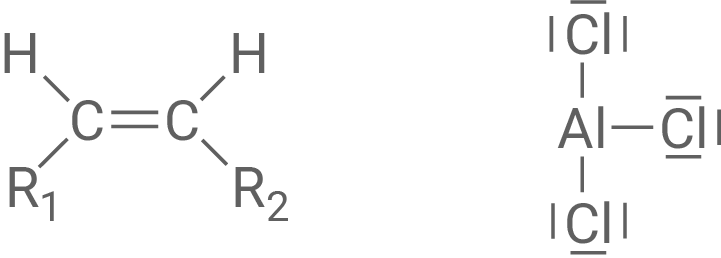
Material 4
Herstellung einer Alkylbenzolsulfonsäure
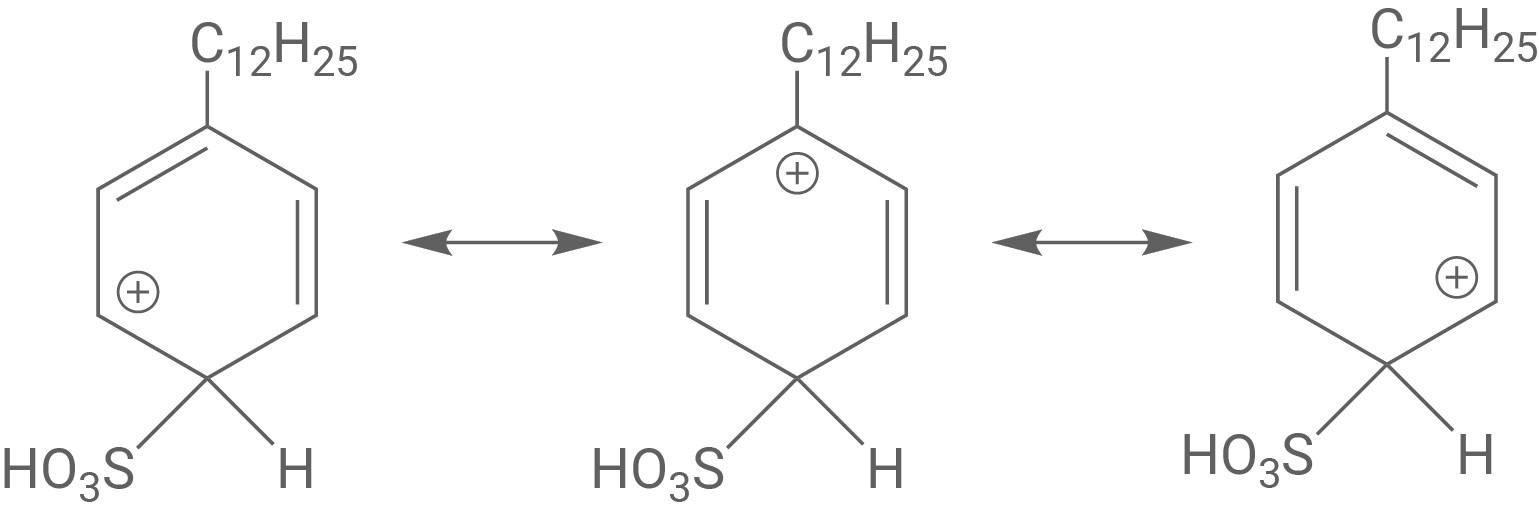
Lässt man ein Alkylbenzol mit Schwefeltrioxid reagieren, so können unter anderem die nachfolgend dargestellten Strukturen gebildet werden.
Sigma-Komplex, der bei der Bildung von Struktur A auftritt:
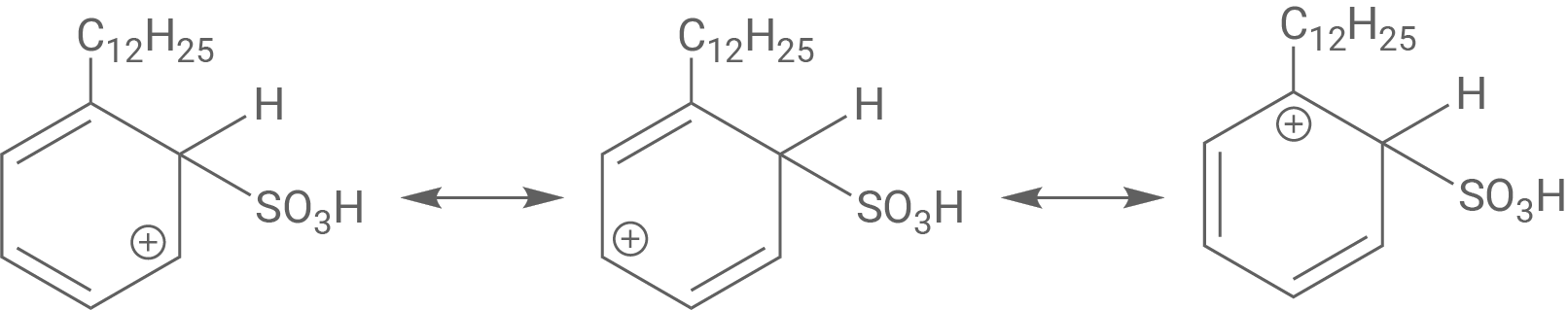
Sigma-Komplex, der bei der Bildung von Struktur B auftritt:
Material 5
Trockenstarre bei Baumwollhandtüchern
Baumwollhandtücher bestehen zu einem großen Teil aus Cellulose-Fasern. Lässt man gewaschene Baumwollhandtücher an der Luft trocknen, so können sich diese danach starr und hart anfühlen. Dieses Phänomen nennt man Trockenstarre.
Wissenschaftler haben herausgefunden, dass beim Lufttrocknen sehr geringe Mengen Wasser zwischen den Cellulose-Fasern in den Handtüchern zurückbleiben und am Zustandekommen der Trockenstarre beteiligt sind. Die Trockenstarre lässt sich vermeiden, indem man Handtücher entweder im Wäschetrockner trocknet oder beim Waschen Weichspüler verwendet, der kationische Tenside enthält.
Beispiel für ein kationisches Tensid:
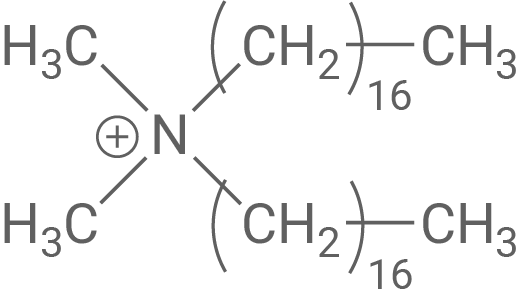
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Formulieren der Strukturformel eines Triglycerid-Moleküls
Alternative 1:
Ein Triglycerid-Molekül, das aus zwei Ölsäure-Bausteinen und einem Baustein einer gesättigten Fettsäure (Buttersäure, Caprylsäure, Laurinsäure, Palmitinsäure oder Stearinsäure) besteht.
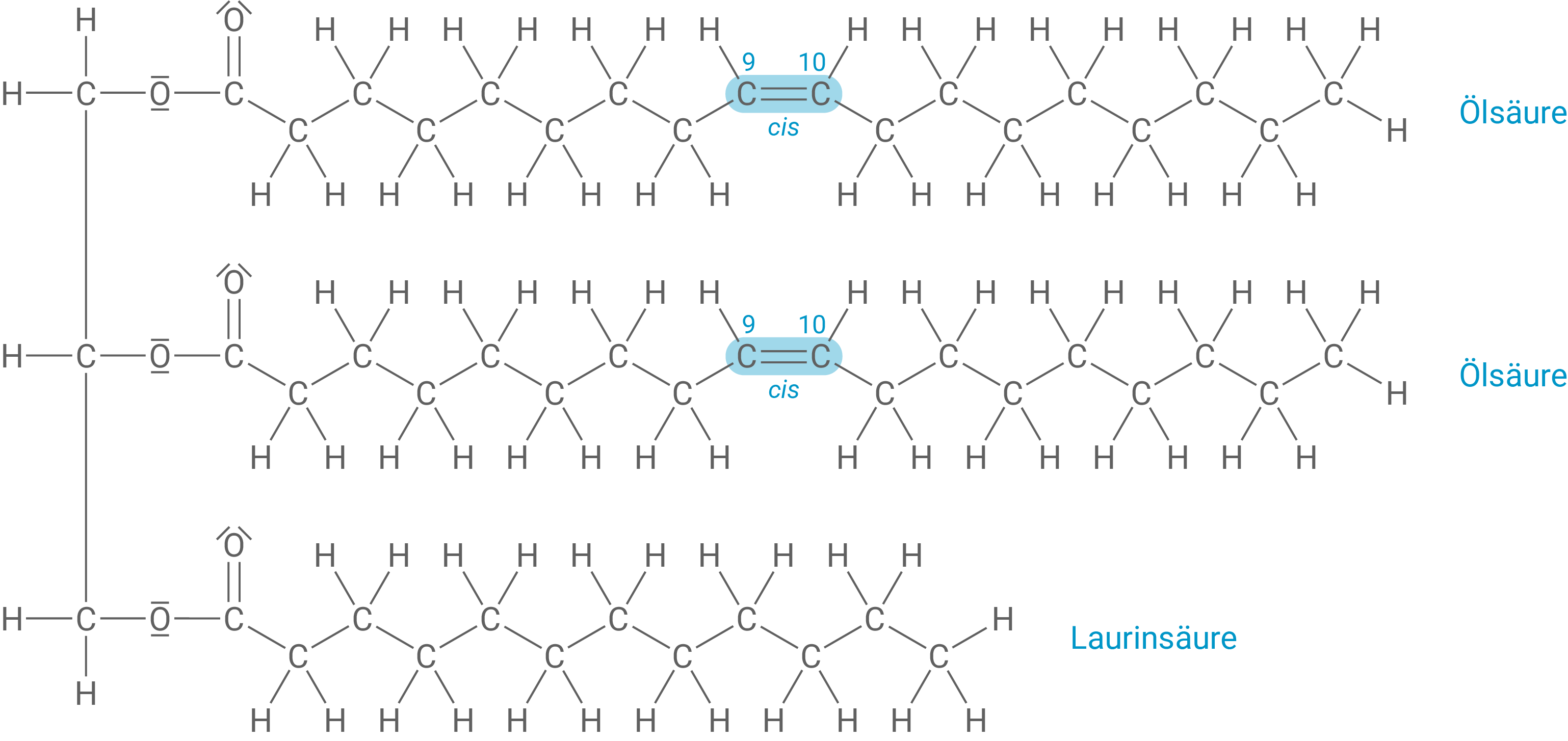
Alternative 2:
Ein Triglycerid-Molekül, das aus einem Linolsäure-Baustein und zwei Bausteinen einer gesättigten Fettsäure aufgebaut ist.
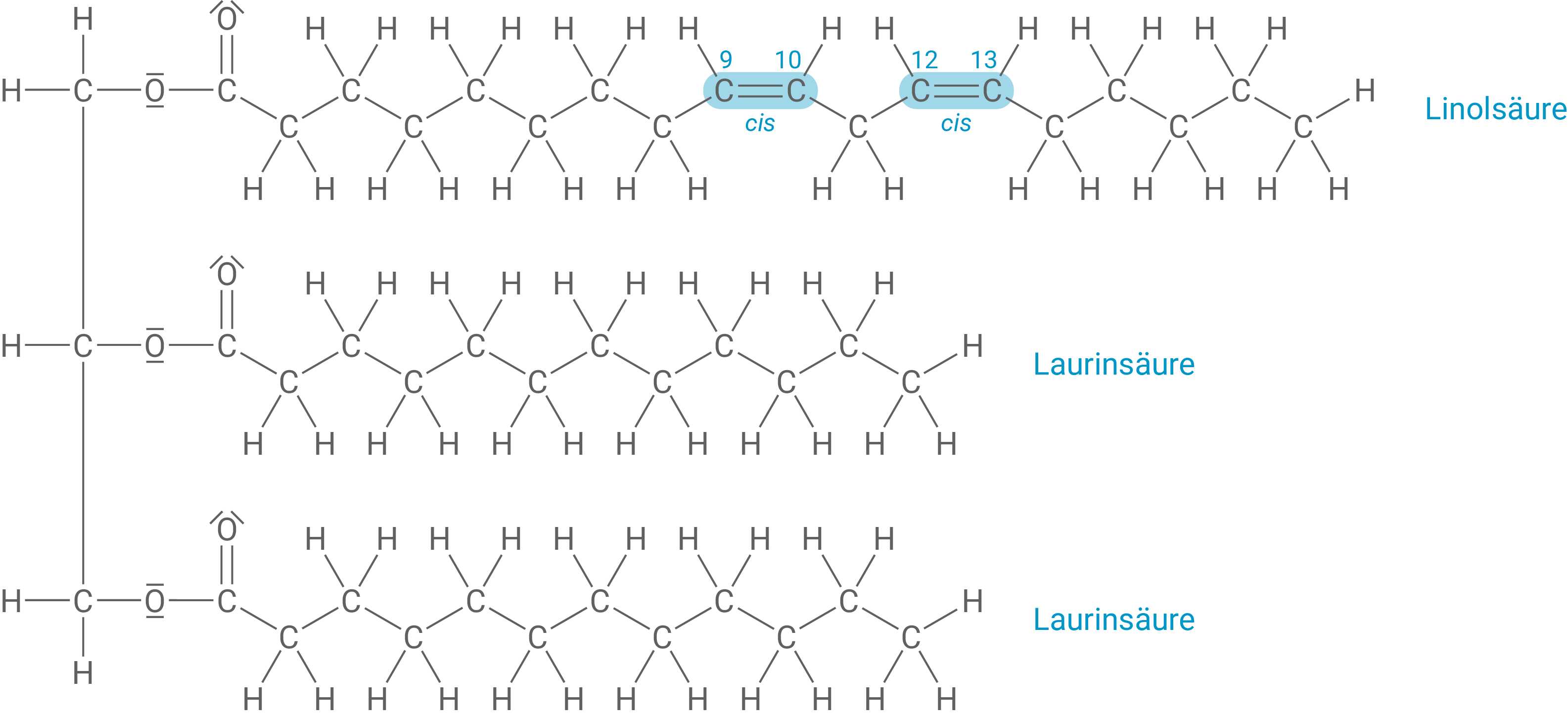
Formulieren des Reaktionsmechanismus
Der Reaktionsmechanismus der alkalischen Hydrolyse wird im Folgenden isoliert betrachtet nur an einer der Estergruppen dargestellt, dafür werden im Folgenden die an der Reaktion dieser Estergruppe nicht beteiligten Bereiche des Triglycerid-Moleküls mit „R1“ (Glycerin-Rest) und „R2“ (Fettsäure-Rest) gekennzeichnet. Bei den anderen beiden Estergruppen findet die alkalische Hydrolyse jedoch genauso statt.
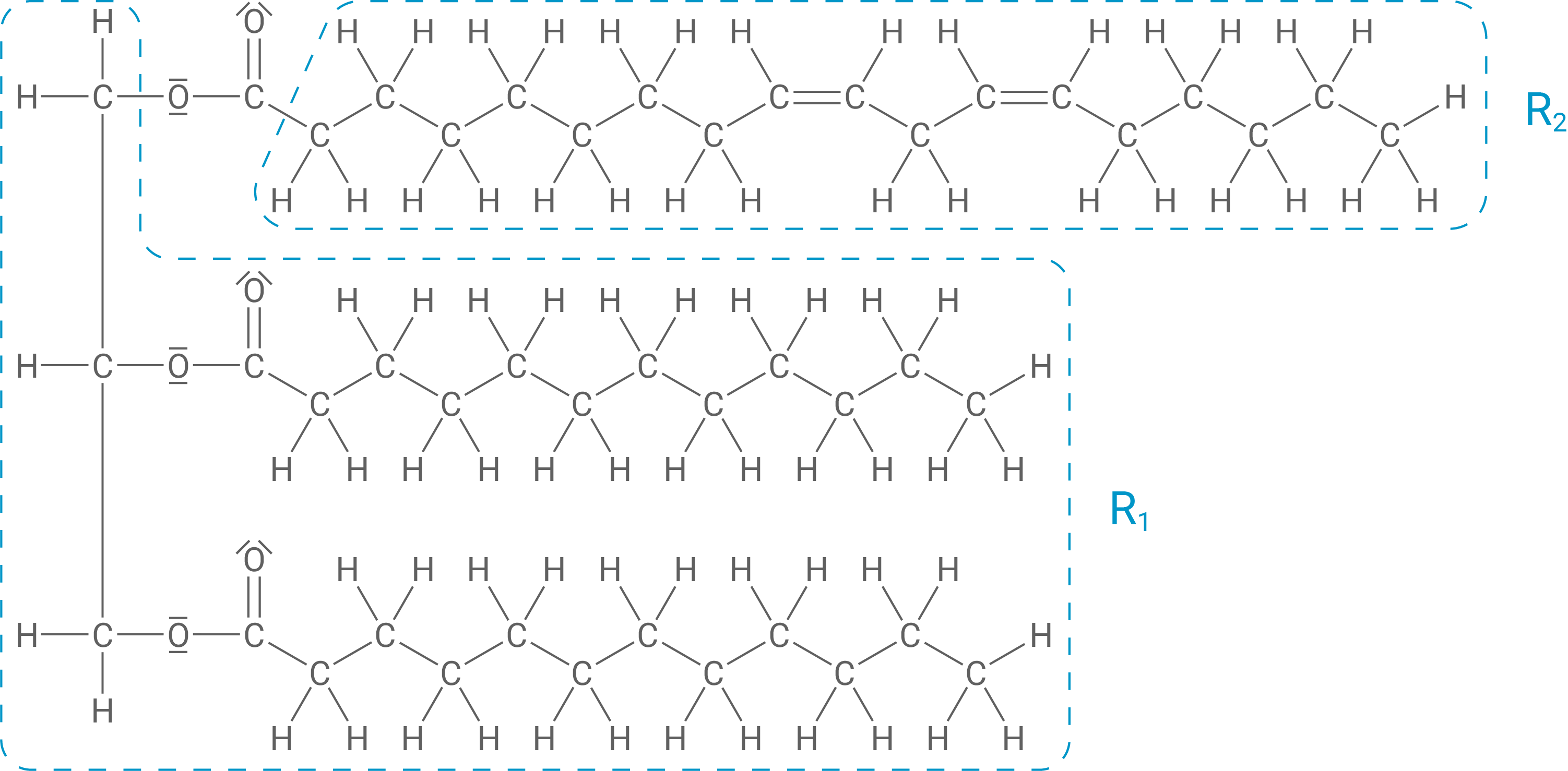
Schritt 1:
Das Kohlenstoff-Atom der Ester-Gruppe wird von einem freien Elektronenpaar des Sauerstoff-Atoms des Hydroxid-Ions nucleophil angegriffen, wodurch ein tetraedrisches Anion entsteht.
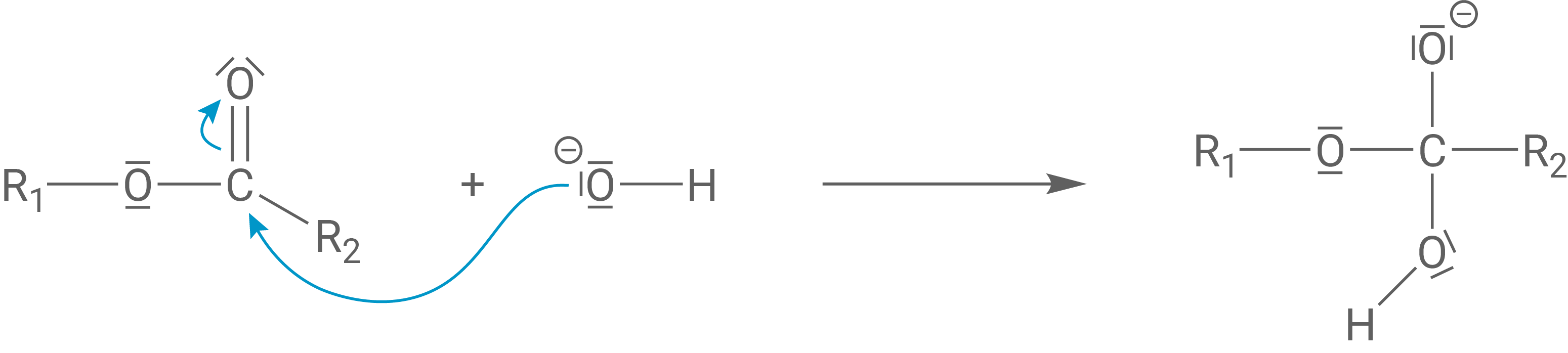
Schritt 2:
Durch erneute Ausbildung der Carbonyl-Doppelbindung wird Glycerin als Alkoholat-Ion eliminiert und die Fettsäure gebildet.
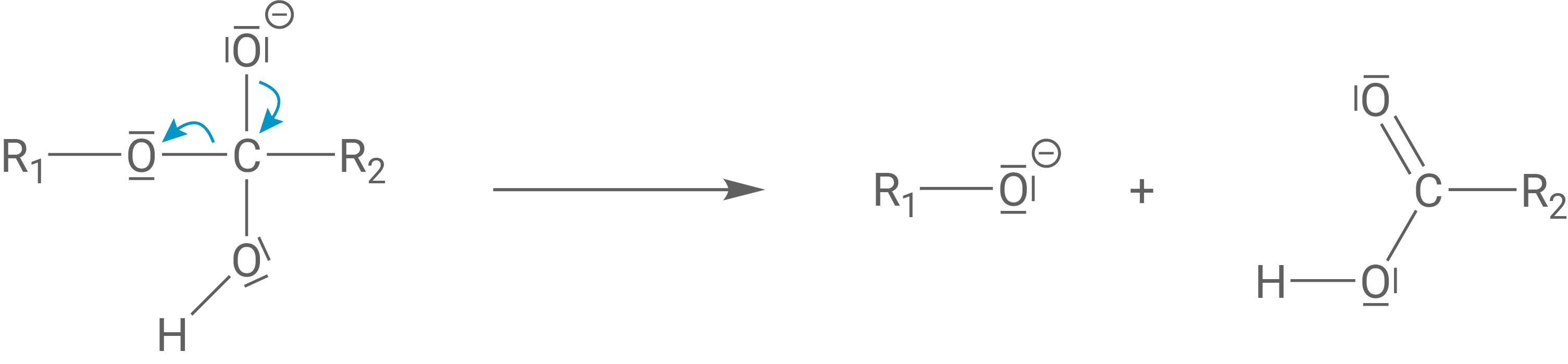
Schritt 3:
Durch eine Protonenübertragung von der Fettsäure zum Alkoholat-Ion entsteht die Hydroxy-Gruppe des Glycerins und das Fettsäure-Anion.
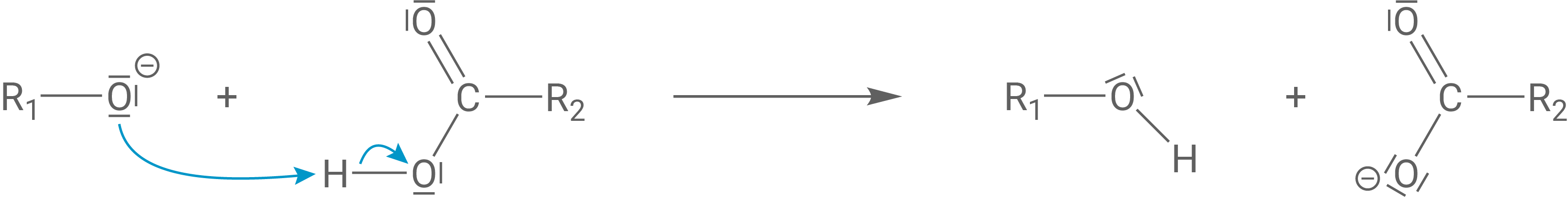
Berechnen des pH-Werts
Formulieren der Reaktionsgleichung
Hinweis: Die Berücksichtigung der Natrium-Ionen und die Verwendung eines Gleichgewichtspfeils sind jeweils optional.
Prüfen der Richtigkeit der Aussage im Zusammenhang mit dem Protolysegleichgewicht
Eine Base mit einem kleineren pKB-Wert als das Hydroxid-Ion besitzt eine höhere Basizität. Da das Amid-Ion mit Wasser reagiert, zeigt es eine stärkere Basenwirkung als das Hydroxid-Ion. Das Gleichgewicht der Protolyse liegt daher auf der Seite des Hydroxid-Ions und der konjugierten Säure der stärkeren Base, hier Ammoniak womit folglich die korrespondierende Säure überwiegend vorliegt. Die Aussage ist somit korrekt.
Formulieren der Reaktionsgleichungen
| 1. | |
| 2. | |
| 3. |
Erklärung der Auswirkung calciumhaltigen Wassers beim Waschen
Ein hoher Gehalt an Calcium-Ionen führt dazu, dass diese verstärkt ein schwer lösliches Salz mit den Seifen-Anionen bilden. Durch die Bildung dieser sogenannten Kalkseife stehen die am Aufbau des Salzes beteiligten Seifen-Anionen nicht mehr zur Entfernung von Verschmutzungen zur Verfügung. In der Folge erhöht sich der Verbrauch an Seife.
Gemeinsamkeiten und Unterschiede in der Struktur verschiedener Tensid-Teilchen
Gemeinsamkeiten:
Die Tensid-Teilchen besitzen einen vergleichsweise großen unpolaren Teil, der ausschließlich aus Kohlenstoff- und Wasserstoffatomen besteht. Daneben weisen sie einen deutlich kleineren, polaren Molekülbereich auf.
Unterschiede:
Die Struktur von Tensid A weist eine positive Ladung auf, wodurch es als Kation vorliegt.
Bei Tensid B sind sowohl eine positive als auch eine negative Ladung vorhanden, sodass es sich um ein Zwitterion handelt.
Tensid C trägt eine negative Ladung und liegt dementsprechend als Anion vor.
In der Struktur von Tensid D befinden sich mehrere Sauerstoffatome jeweils zwischen zwei Methylen-Gruppen wodurch sich polare und unpolare Bereiche im Molekül abwechseln.
Benennung des Reaktionsmechanismus und des Reaktionstyps
Schritt 1: Radikalische Substitution
Schritt 2: Eliminierung
Formulieren des Reaktionsmechanismus
Schritt 1:
Zunächst kommt es zu einer Wechselwirkung zwischen der Doppelbindung des Alkens und dem positiv polarisierten Wasserstoff-Atom des Chlorwasserstoff-Moleküls sowie zwischen dem negativ polarisierten Chlor-Atom von
und dem Aluminium-Atom von
. Die Bindung im HCl-Molekül wird heterolytisch gespalten und die Doppelbindung im Alken unter Ausbildung einer C-H-Bindung aufgebrochen. Neben dem Carbenium-Ion wird
gebildet.
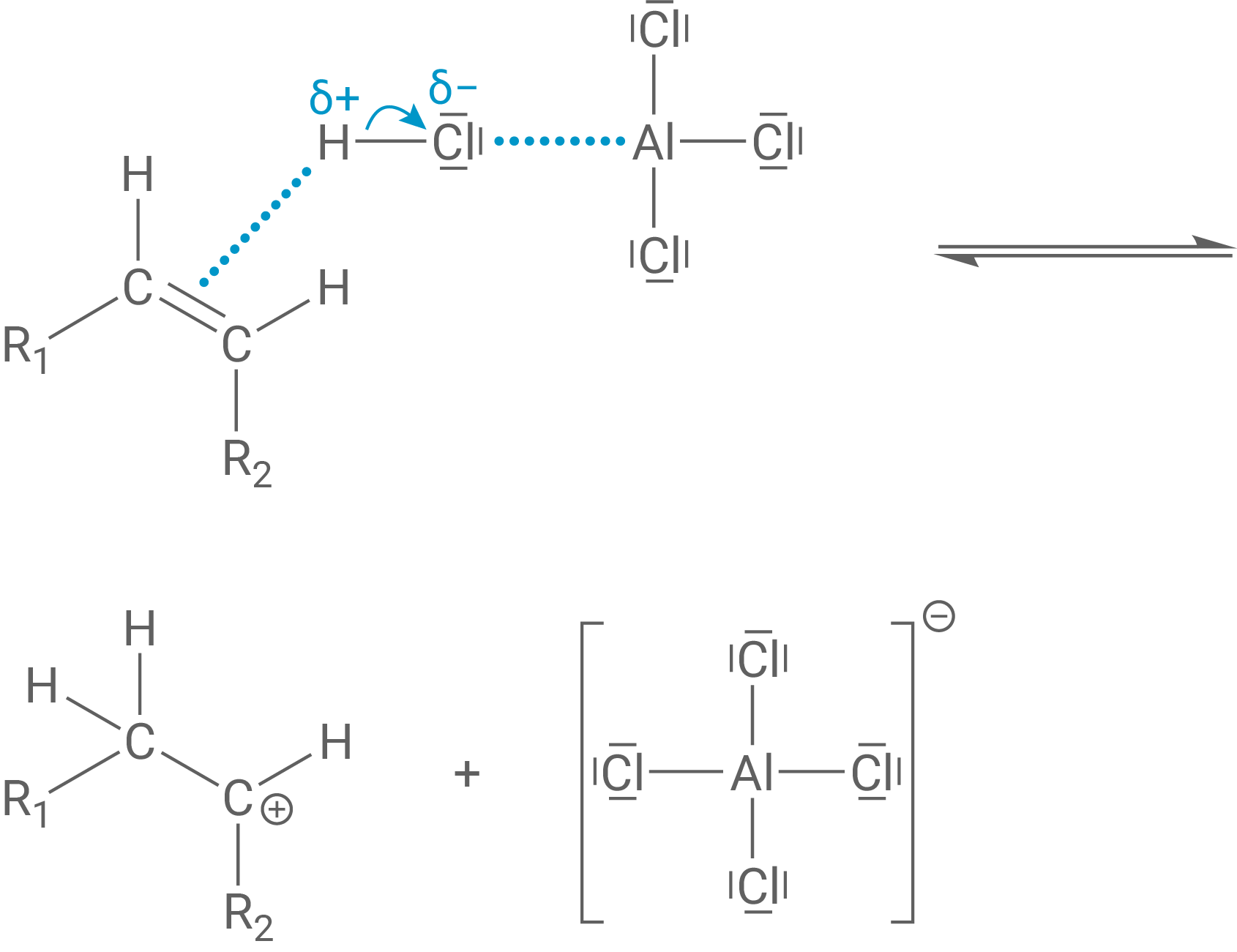
Schritt 2:
Das gebildete Carbenium-Ion kann aufgrund seiner positiven Ladung mit dem π-Elektronensystem des Benzols wechselwirken (π-Komplex). Das Elektrophil (Carbenium-Ion) wird durch eines der Kohlenstoff-Atome des Benzols unter Verlust der Aromatizität angegriffen. Der entstandene σ-Komplex ist durch Mesomerie stabilisiert, indem die positive Ladung über fünf Kohlenstoff-Atome im Benzol-Ring delokalisiert werden kann.
Hinweis: Die mesomeren Grenzstrukturen sind in dieser Aufgabe nicht für die volle Punktzahl notwendig.
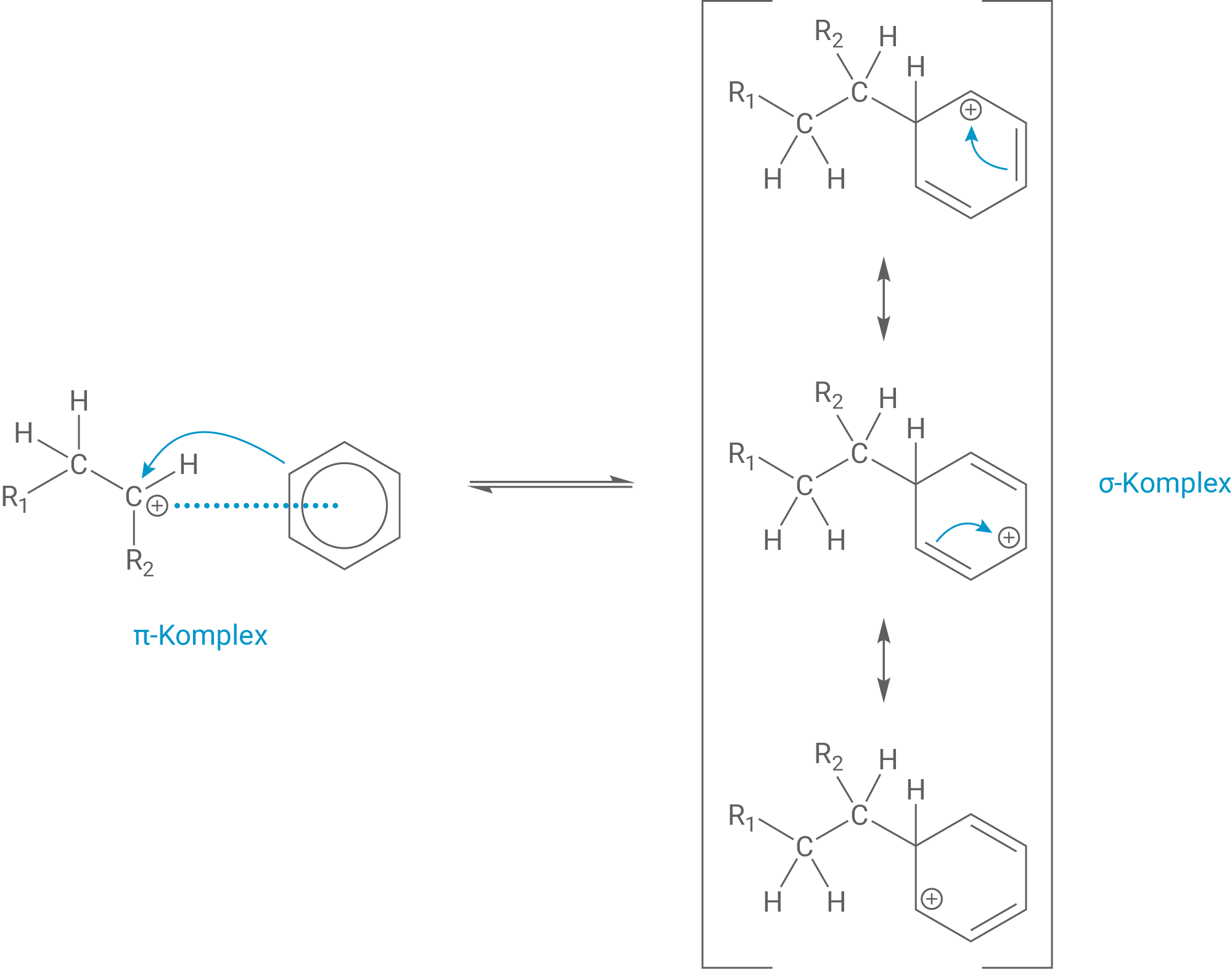
Schritt 3:
Zur Rearomatisierung des Rings wird das Proton am soeben substituierten Kohlenstoff-Atom abgespalten. Dieses kann mit einem der Chlor-Atome von reagieren, wodurch letztendlich neben dem Alkylbenzol
und
entstehen.
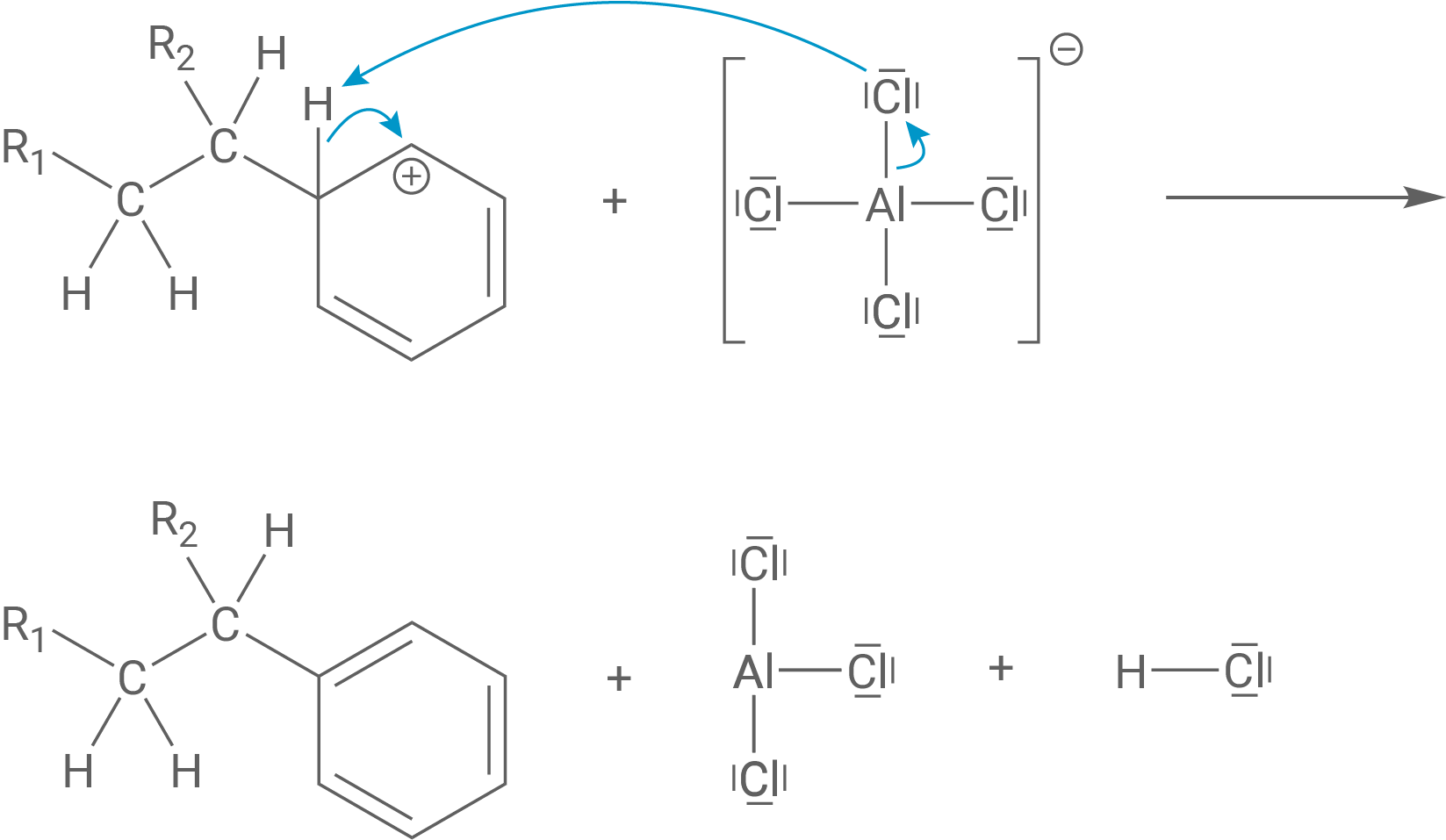
Erklärung des Beitrags von HCl
Durch Addition des von abgespaltenen Protons an die Doppelbindung des Alkens entsteht ein Carbenium-Ion. Aufgrund seiner positiven Ladung kann dieses mit den π-Elektronen des Benzolrings wechselwirken, wodurch eine Reaktion ermöglicht wird.
Formulierung der mesomeren Grenzstrukturen des σ-Komplexes von Struktur C
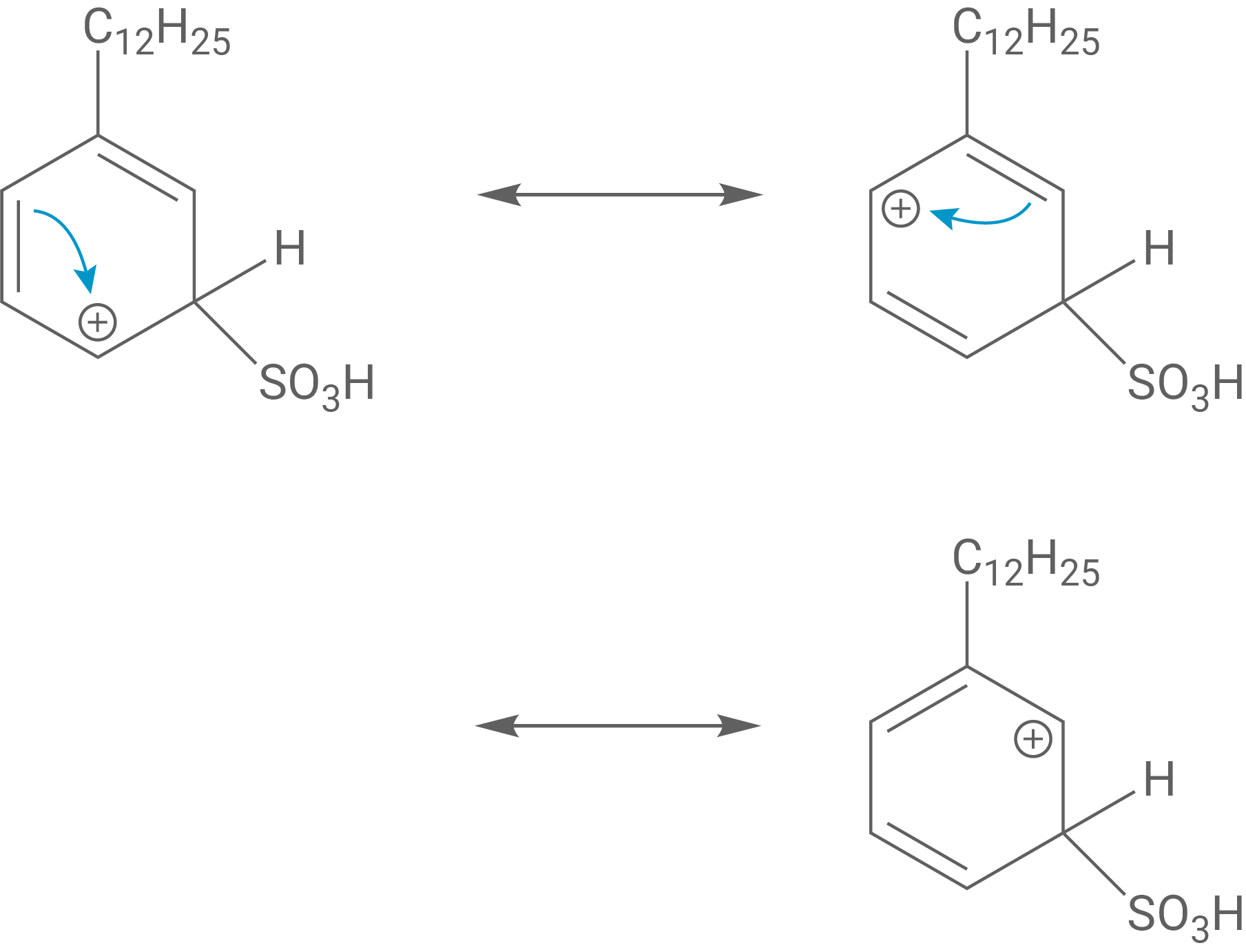
meta-Stellung der Substituenten
Begründung der Produktverhältnisse
Bei der Bildung der Strukturen A und B existiert jeweils eine mesomere Grenzstruktur des σ-Komplexes, in der die positive Ladung an dem Kohlenstoffatom sitzt, das die Alkylgruppe trägt. Der +I-Effekt dieser Alkylgruppe mindert die positive Ladung und stabilisiert dadurch die betreffende Grenzstruktur sowie den gesamten σ-Komplex. Für Struktur C lässt sich eine solche Grenzstruktur nicht formulieren, weshalb der entsprechende σ-Komplex insgesamt weniger stabil ist und mit geringerem Anteil gebildet wird. Daher entstehen die Strukturen A und B bevorzugt als Reaktionsprodukt, da sie aus den stabileren σ-Komplexen hervorgehen.
Geschwindigkeiten der Sulfonierung
Die Sulfonierung eines Alkylbenzols verläuft schneller als die von Benzol, da der +I-Effekt der Alkylgruppe die Elektronendichte im Benzolring erhöht. Dadurch wird die Reaktion mit dem Elektrophil erleichtert.
Strukturformelausschnitt eines Cellulose-Moleküls
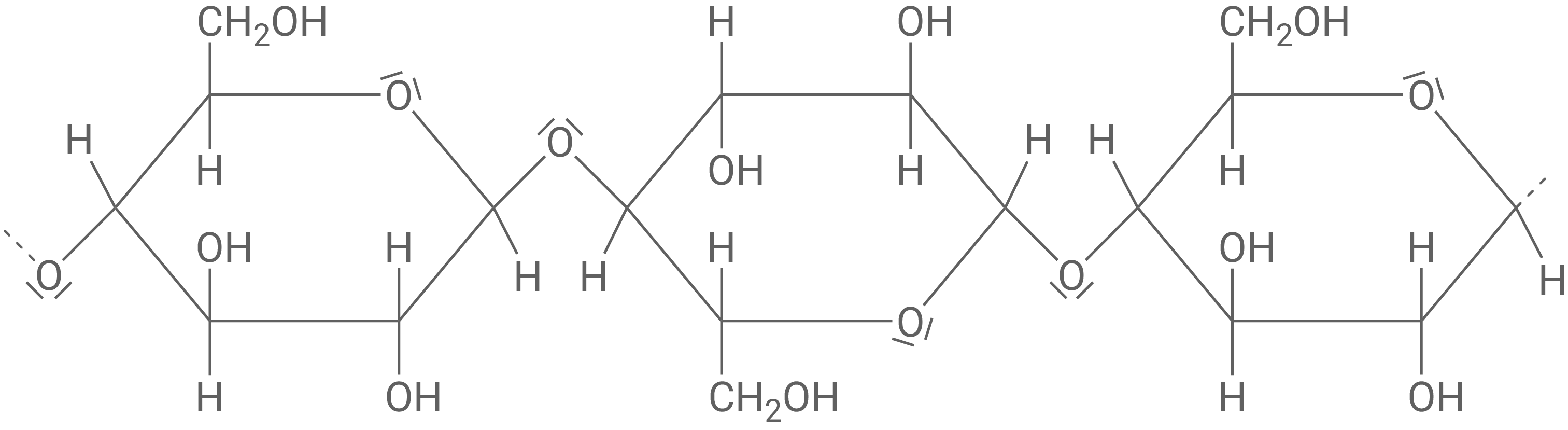
Benennung der Verknüpfung
β-1,4-glycosidische Bindung
Zustandekommen und Verhindern der Trockenstarre
Wenn die Hydroxy-Gruppen von Monomer-Bausteinen verschiedener Cellulose-Fasern Wasserstoffbrücken zu denselben in der Baumwolle vorhandenen Wassermolekülen ausbilden, können sich verschiedene Cellulose-Fasern miteinander verbinden. Dies erhöht die Stabilität des Materials, wodurch sich die Baumwolle hart anfühlt.
Aufgrund ihrer positiven Ladung können Moleküle der kationischen Tenside im Weichspüler ebenfalls mit den polaren Hydroxy-Gruppen der Cellulose wechselwirken und sich in die Struktur der Baumwolle zwischen die Cellulose-Moleküle einlagern. Ihre langen, unpolaren Alkyl-Reste können jedoch weder mit den Cellulose-Makromolekülen noch mit Wasser-Molekülen eine starke intermolekulare Wechselwirkung ausbilden. Dadurch wird die Bildung stabilerer bzw. härterer Strukturen unterbunden.