Vorschlag C – Silicium und Siliciumverbindungen
Silicium-Teilchen kommen mit einem Anteil von ungefähr 25,8 Prozent des Gewichts nach Sauerstoff-Teilchen am zweithäufigsten in der Erdkruste vor. Auch die Weltmeere sind ein sehr großer Speicher dafür, da beispielsweise die sogenannte Orthokieselsäure in allen Ozeanen in beträchtlicher Menge gelöst vorkommt. Orthokieselsäure ist eine schwache Säure, die sich auch in wässrigen Lösungen durch die Reaktion von Monosilan
mit Wasser bildet. Silane sind die Wasserstoffverbindungen des Siliciums und den Kohlenwasserstoffen entsprechend aufgebaut. Monosilan ist die erste und Pentasilan die fünfte Verbindung in der homologen Reihe der Silane, die grundlegend der homologen Reihe der Alkane entspricht. In Alkylsilanen ist mindestens ein Wasserstoff-Atom durch eine Alkyl-Gruppe ersetzt, in Halogensilanen zum Beispiel durch Chlor- oder Brom-Atome. Durch die Reaktion von Methylchlorsilanen mit Wasser bilden sich sogenannte Methylsilanole, zu denen auch die Edukte für die Herstellung von bestimmten Kunststoffen, den sogenannten Siliconen, zählen.
Bei einer Reaktion zur Gewinnung elementaren Siliciums im Labor reagiert Siliciumdioxid mit elementarem Kohlenstoff. Neben Silicium entsteht dabei Kohlenstoffmonooxid als zweites Reaktionsprodukt.
Formuliere die Reaktionsgleichung zur Gewinnung von elementarem Silicium durch die Reaktion von Siliciumdioxid mit elementarem Kohlenstoff.
Berechne mithilfe von Material 1 die molare Standardreaktionsenthalpie sowie die molare Standardreaktionsentropie für die oben beschriebene Reaktion.
Erläutere die Änderung der Entropie im Hinblick auf diese Reaktion.
Prüfe für jede der drei in Material 2 zum Methan-Molekül formulierten Aussagen, ob sie inhaltlich entsprechend auch für das Monosilan-Molekül zutrifft.
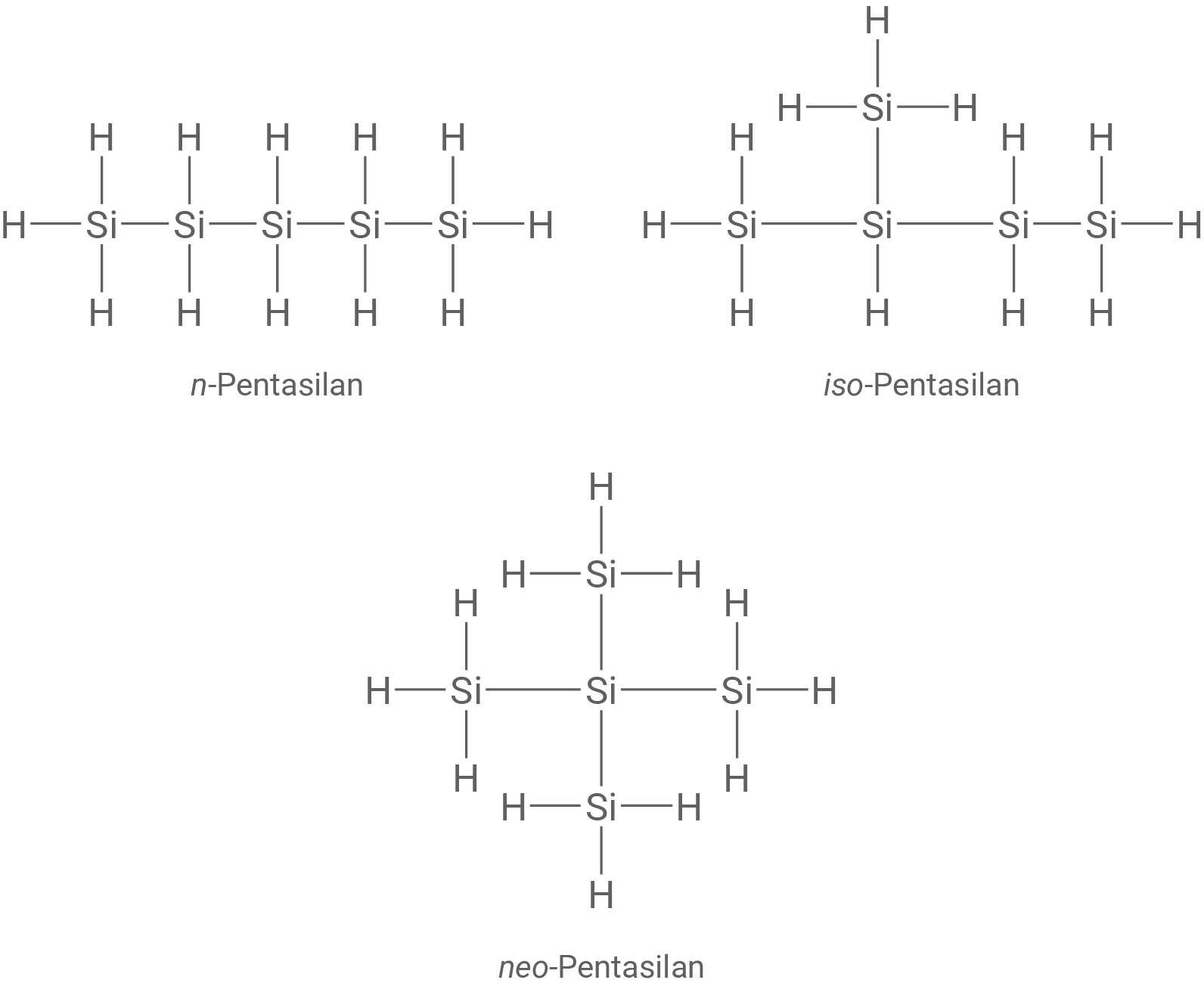
Formuliere für alle Konstitutionsisomere des Pentasilans die jeweilige Strukturformel.
Formuliere mithilfe von Material 3 für die Reaktion von Monosilan mit Wasser die Reaktionsgleichung und zeige anhand der wesentlichen Oxidationszahlen und der Elektronenübergänge, dass es sich bei dieser Reaktion um eine Redoxreaktion handelt.
Hinweis:
Im Monosilan-Molekül haben die Wasserstoff-Atome nicht die Oxidationszahl +I.
Formuliere mithilfe von Material 3 für die Protolysereaktion zwischen Orthokieselsäure und Wasser die Reaktionsgleichung und berechne den pKS-Wert für die erste Protolysestufe der Orthokieselsäure.
Formuliere mithilfe von Material 4 für die beiden Reaktionsschritte der Müller-Rochow-Synthese zur Herstellung von Chlortrimethylsilan die jeweilige Reaktionsgleichung.
Formuliere mithilfe von Material 4 den Reaktionsmechanismus für die Reaktion von Chlortrimethylsilan mit dem Methanolat-Anion
Begründe mithilfe von Material 4 anhand von zwei Aspekten, weshalb die Umsetzung von Chlortrimethylsilan mit dem Methanolat-Anion trotz des Vorliegens von drei Alkyl-Gruppen am Silicium-Atom nicht nach einem SN1-Mechanismus abläuft und weshalb ein SN2-Mechanismus möglich ist.
Benenne mithilfe von Material 5 für die Bildung des Kunststoffs Dimethylpolysiloxan den Polyreaktionstyp und formuliere für ein Makromolekül dieses Kunststoffs einen Strukturformelausschnitt aus drei Monomer-Bausteinen.
Formuliere für einen aus Methylsilantriol-Monomeren entstehenden Kunststoff einen Strukturformelausschnitt aus vier Monomer-Bausteinen, durch den der Unterschied zur Struktur des Dimethylpolysiloxans deutlich wird.
Auf der Erde konnten sich unter anderem basierend auf der Vielfalt der Kohlenstoff-Verbindungen Lebewesen entwickeln.
Beurteile mithilfe von Material 6 anhand von drei Aspekten, ob die Entwicklung von Lebewesen gleichermaßen auf der Basis von Silicium-Verbindungen möglich sein könnte, die für diesen Fall den Kohlenstoff-Verbindungen entsprechen und diese ersetzen sollen.
Material 1
Molare Standardbildungsenthalpien und molare Standardentropien
Berechnung von Standardreaktionsentropien
Um für eine chemische Reaktion die molare Standardreaktionsentropie zu berechnen, werden die Werte der molaren Standardentropien aller an der Reaktion beteiligten Stoffe unter Beachtung der Einheit grundlegend auf die gleiche Weise mathematisch zueinander in Beziehung gesetzt und miteinander verrechnet, wie es mit den Werten der molaren Standardbildungsenthalpien der einzelnen Stoffe im Zuge der Berechnung der molaren Standardreaktionsenthalpie der Fall ist.
Material 2
Methan
Für das Methan-Molekül gelten die folgenden Aussagen:
Die positive oder negative Teilladung der beiden an jeder der vier Bindungen beteiligten Atome ist jeweils nur vergleichsweise schwach ausgeprägt, da sich jede der vier Elektronenpaarbindungen als schwach polar (annähernd unpolar) einstufen lässt. Daher spricht man jede der vier Elektronenpaarbindungen betreffend auch von einem geringen „Dipolmoment“.
Jede der vier Elektronenpaarbindungen betreffend hat das Kohlenstoff-Atom die negative und das jeweilige Wasserstoff-Atom die positive Teilladung.
Im Zusammenhang mit der räumlichen Anordnung der Atome im Methan-Molekül heben sich die vier jeweils nur geringen Dipolmomente der einzelnen Elektronenpaarbindungen gegenseitig auf. Daher zeigt das Methan-Molekül keine Dipol-Eigenschaften.
Material 3
Bildung und Protolyse der Orthokieselsäure
Unter bestimmten Bedingungen reagiert Monosilan mit Wasser zu Orthokieselsäure und elementarem Wasserstoff.
Orthokieselsäure reagiert ihrerseits ebenfalls mit Wasser. Da es sich um eine schwache Säure handelt, kommt es in der ersten Protolysestufe durch die Abspaltung eines Protons zur Einstellung eines Gleichgewichts. Eine wässrige Lösung der Orthokieselsäure hat bei einer Ausgangskonzentration von einen
-Wert von
Material 4
Chlortrimethylsilan
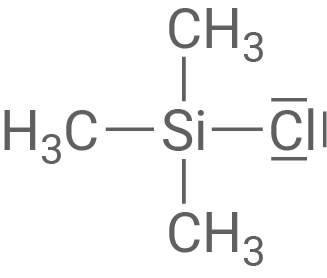
Chlortrimethylsilan lässt sich in einer nucleophilen Substitutionsreaktion mit Methanolat-Ionen umsetzen. Auch im Zusammenhang mit der Größe des Silicium-Atoms und seiner Elektronegativität läuft die Reaktion nach einem SN2-Mechanismus ab.
Dabei entsteht als organisches Reaktionsprodukt ein sogenannter Trimethylsilanether, in dessen Struktur eine der Methyl-Gruppen über ein Sauerstoff-Atom mit dem Silicium-Atom verbunden ist.
Material 5
Dimethylsilandiol und Methylsilantriol
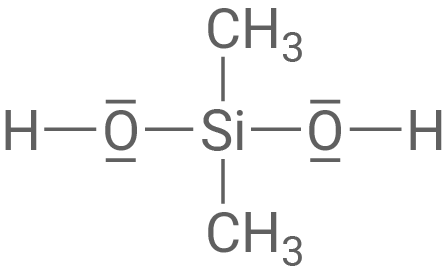
Methylsilantriol-Moleküle reagieren unter Wasserabspaltung miteinander zu einem weiteren Kunststoff, der eine andere Struktur aufweist als Dimethylpolysiloxan.
Material 6
Aufbau und Eigenschaften von Siliciumverbindungen
Es gibt deutlich weniger Silane als Kohlenwasserstoffe. So sind bisher lediglich unverzweigte und verzweigte Silane mit bis zu acht Silicium-Atomen bekannt. Dies ergibt sich auch im Zusammenhang mit der im Vergleich zu Alkanen geringeren Stabilität der Silane.
Je stärker eine Elektronenpaarbindung ist, desto mehr Energie ist für ihre Spaltung erforderlich.
Für die Spaltung von Si-H-Bindungen in Silanen muss im Vergleich mit den C-H-Bindungen der entsprechend aufgebauten Kohlenwasserstoffe ein geringerer Energiebetrag aufgebracht werden.
So sind Silane nur unter Luftabschluss herstellbar und einzig das Monosilan ist bei Raumtemperatur unbegrenzt haltbar. Die weiteren Silane zersetzen sich bereits bei Raumtemperatur. Im Unterschied zu Kohlenstoff-Atomen bilden Silicium-Atome in der Natur keine Doppel- oder Dreifachbindungen aus. Dies führt zum Beispiel dazu, dass Siliciumoxid im Unterschied zu Kohlenstoffdioxid und Kohlenstoffmonooxid ein Feststoff ist, in dem Silicium- und Sauerstoff-Atome dreidimensional über Einfachbindungen miteinander verbunden sind. Im Labor hergestellte Silicium-Verbindungen mit Doppelbindungen sind instabil.
Halogensilane lassen sich aus Silanen herstellen wie Halogenalkane aus Alkanen. Werden Halogensilane mit Wasser umgesetzt, so entstehen Silanole, die im Hinblick auf Kohlenstoff-Verbindungen den Alkoholen entsprechen. Silanole sind im Vergleich zu Alkoholen jedoch nicht sehr stabil und polymerisieren unter Wasserabspaltung zu Siloxanen. In den Molekülen von Siloxanen liegen Silicium- und Sauerstoff-Atome abwechselnd vor und sind wiederum ausschließlich über Einfachbindungen verknüpft. In Carbosilanen liegen Silicium-Atome und Kohlenstoff-Atome abwechselnd und jeweils über Einfachbindungen verknüpft vor und in Polysilazanen entsprechend Silicium-Atome und Stickstoff-Atome.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Reaktionsgleichung zur Silicium-Gewinnung
Berechnung der molaren Standardreaktionsenthalpie sowie der molaren Standardreaktionsentropie
Sowohl bei den Edukten als auch bei den Produkten liegt insgesamt eine Stoffmenge von je
Hinweis: Zum Erreichen der vollen Punktzahl gilt eine Erläuterung unter Einbezug der Berechnung als gleichwertig.
Prüfen der Aussagen
Die Teilladungen am Silicium- und am Wasserstoff-Atom sind in allen vier Bindungen nur schwach ausgeprägt, da die Elektronegativitätsdifferenz lediglich beträgt. Deshalb gelten die Elektronenpaarbindungen als schwach polar, nahezu unpolar, und weisen nur ein geringes Dipolmoment auf.
Die Aussage ist somit inhaltlich korrekt.
Da das Wasserstoff-Atom mit einem Elektronegativitätswert von elektronegativer ist als das Silicium-Atom mit
trägt im Monosilan-Molekül bei allen vier Bindungen das Silicium-Atom jeweils die positive Teilladung, während die negative Teilladung beim Wasserstoff-Atom liegt.
Die Aussage ist daher inhaltlich nicht korrekt.
Da vier Wasserstoffatome an das Siliciumatom gebunden sind, weist das Monosilan-Molekül eine tetraederartige Geometrie auf. Dadurch fallen die Schwerpunkte der positiven und negativen Teilladungen im Zentrum beim Siliciumatom zusammen. Die schwachen Dipolmomente der einzelnen Elektronenpaarbindungen heben sich somit gegenseitig auf, sodass das Monosilan-Molekül insgesamt keine Dipol-Eigenschaften besitzt.
Die Aussage ist daher inhaltlich korrekt.
Strukturformeln der Konstitutionsisomere des Pentasilans
Reaktionsgleichung der Redoxreaktion von Monosilan mit Wasser
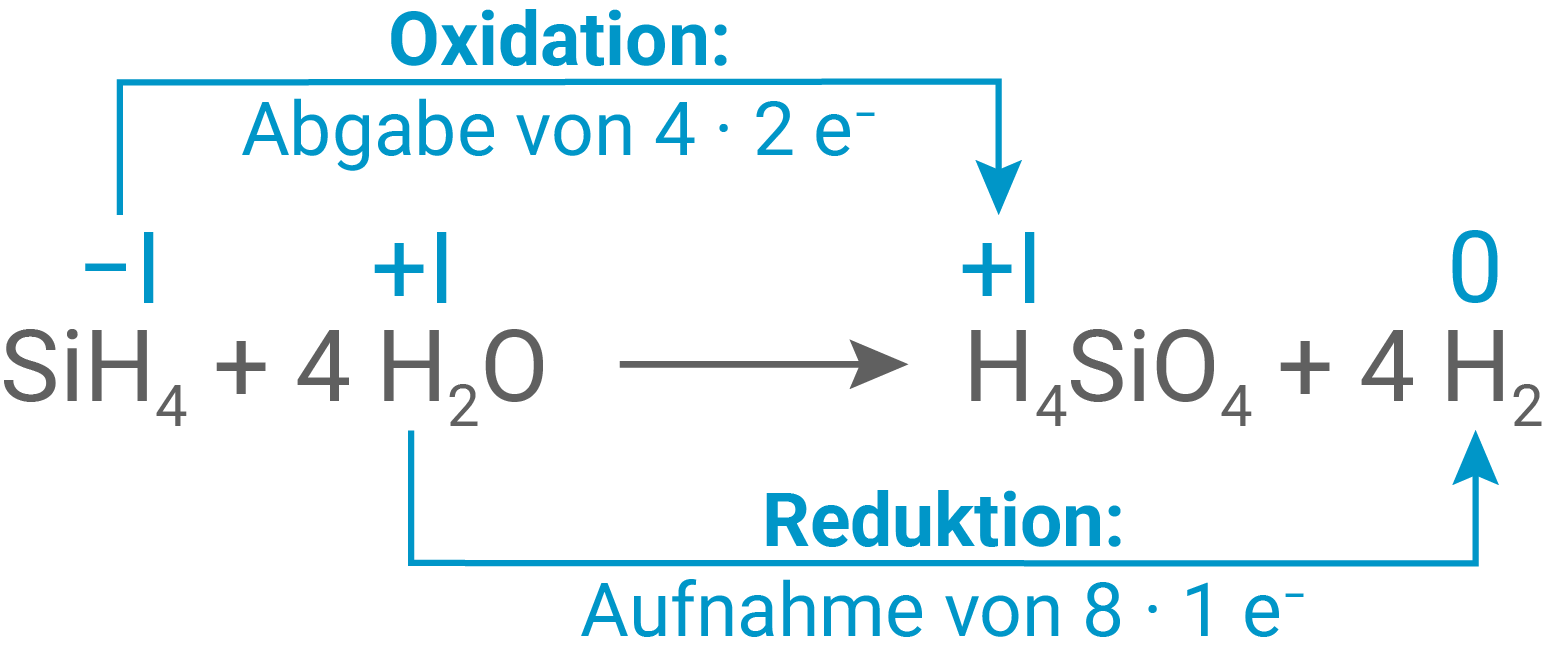
Reduktion: Verringerung der Oxidationszahl der H-Atome von +I im Wasser nach 0 im Wasserstoff-Molekül
Reaktionsgleichung der Protolysereaktion
Berechnung des pKS-Werts
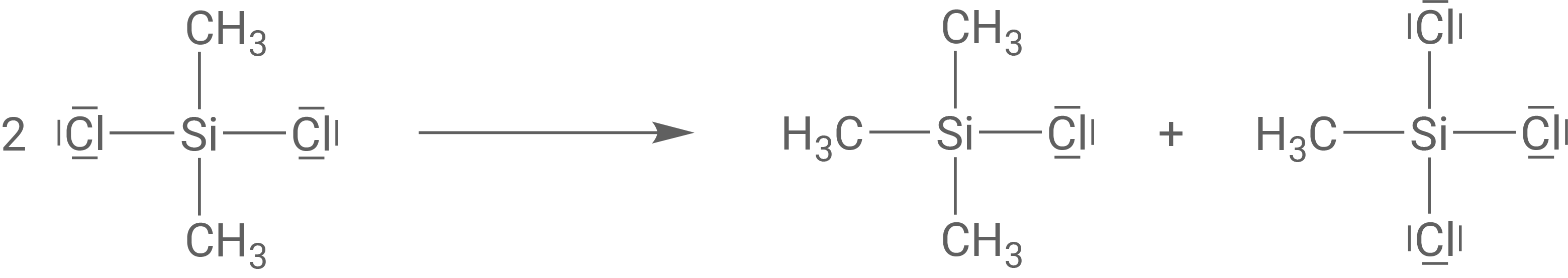
Reaktionsgleichungen zur Müller-Rochow-Synthese
Reaktionsschritt 1:

Reaktionsschritt 2:
Formulierung des SN2-Reaktionsmechanismus
Das Silicium-Atom des Chlortrimethylsilans wird von einem freien Elektronenpaar des Sauerstoff-Atoms des Methanolat-Anions nucleophil angegriffen, wodurch ein Übergangszustand mit fünf Substituenten am Silicium-Atom entsteht.

Im Übergangszustand kommt es zu einer Bindungs-Neubildung zwischen dem Silicium- und dem Sauerstoff-Atom, während das Chlor-Atom als Chlorid-Anion abgespalten wird. Somit entsteht der Trimethylsilanether.
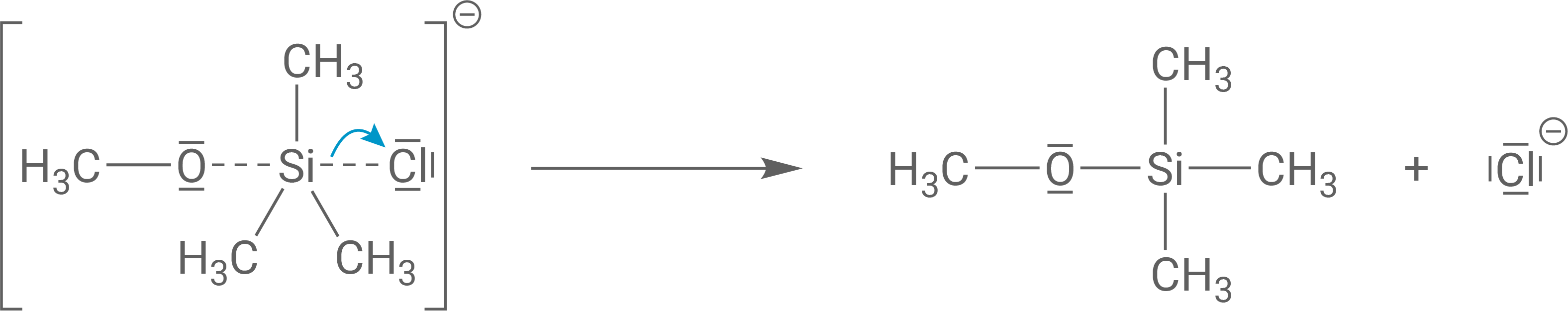
Begründung des SN2-Mechanismus im Vergleich zum SN1-Mechanismus
Die Kohlenstoff-Atome der drei Methylgruppen besitzen eine höhere Elektronegativität als das Silicium-Atom. Daher üben sie keinen +I-Effekt aus, was zur Folge hat, dass sich kein stabiles Kation als Zwischenprodukt bilden kann. Das Siliciumatom ist zudem relativ groß, da seine Elektronenhülle über drei Schalen verfügt. Im SN2-Mechanismus führt dies dazu, dass beim Übergangszustand mit fünf Substituenten nur eine geringe sterische Hinderung auftritt.
Benennung des Polyreaktionstyps
Es handelt sich um eine Polykondensation.
Strukturformelausschnitt des Kunststoffs Dimethylpolysiloxan
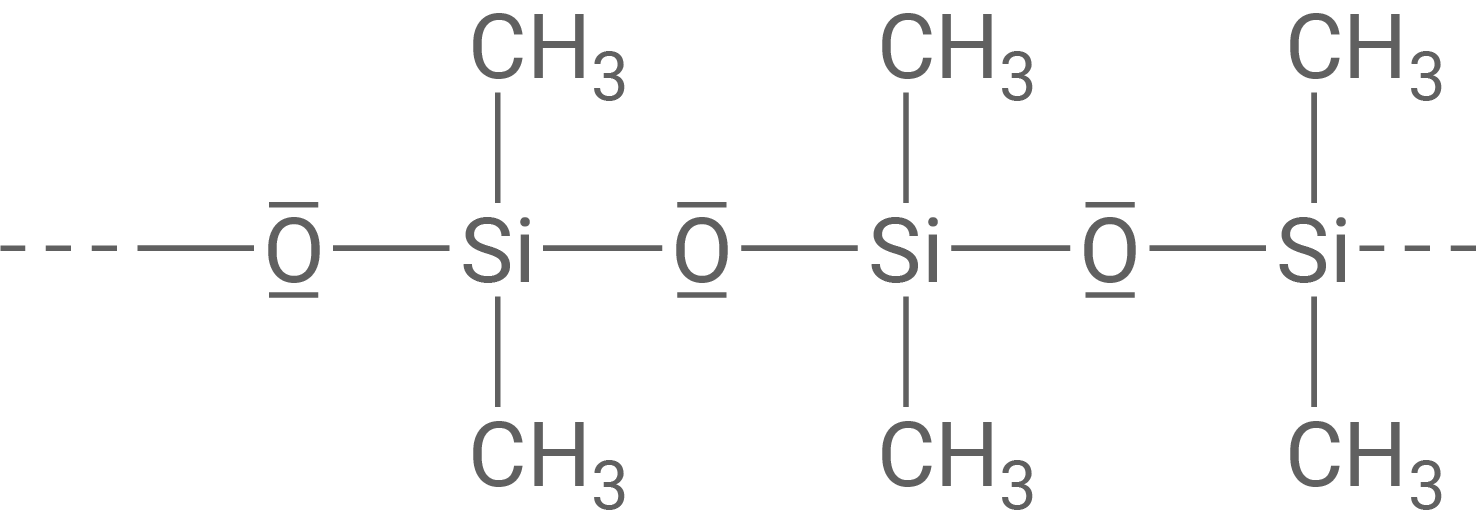
Strukturformelausschnitt eines aus Methylsilantriol-Monomeren bestehenden Kunststoffs
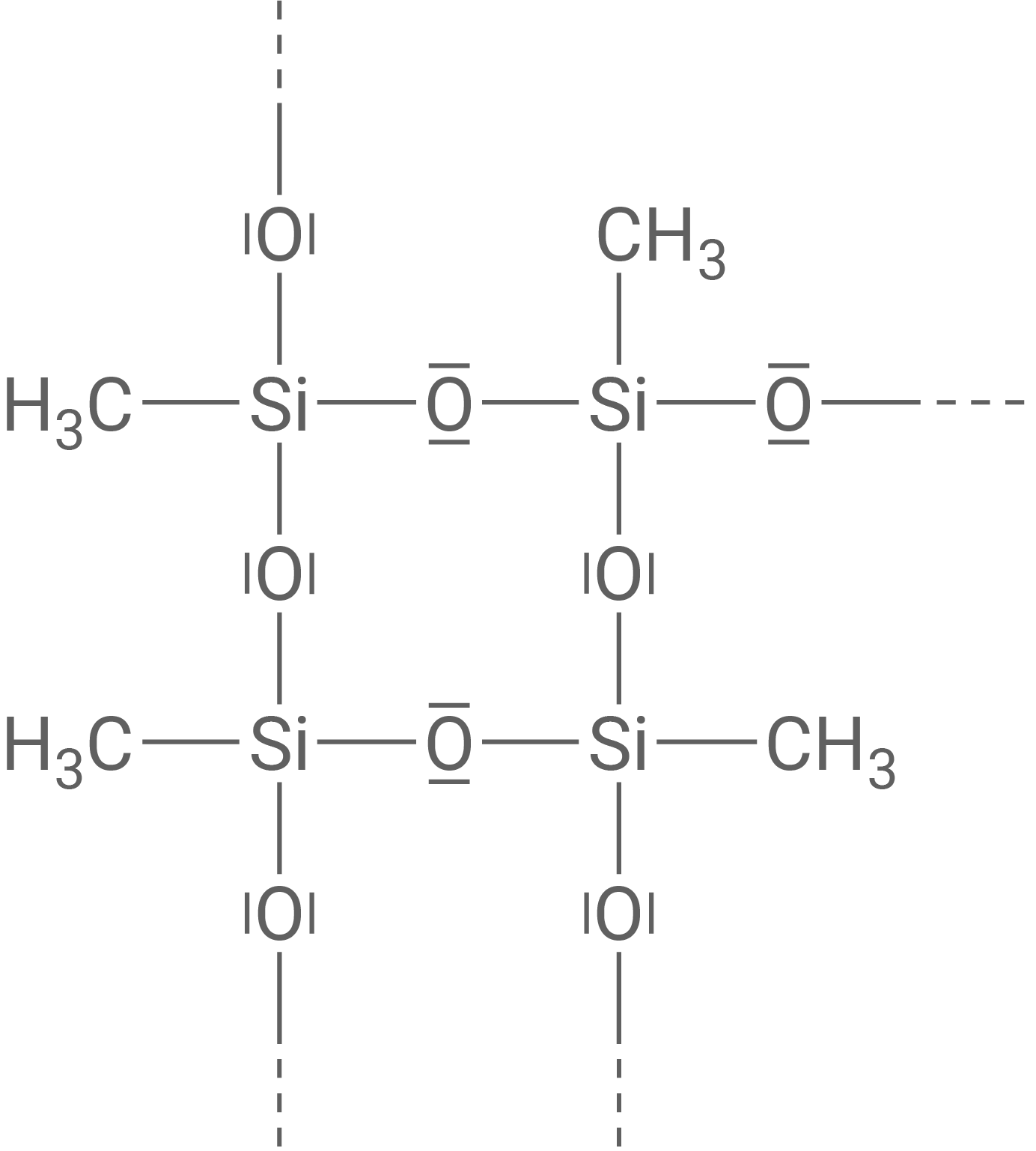
Beurteilung der Entwicklung von Leben auf Silicium-Basis
- Im Vergleich zu Kohlenwasserstoffen sind Silane unter den auf der Erde herrschenden Bedingungen wie Temperatur und Sauerstoffgehalt deutlich weniger stabil. Daher sind bisher nur Silane mit bis zu acht miteinander verknüpften Siliciumatomen bekannt. Viele für Lebewesen wichtige Verbindungen basieren hingegen auf Molekülstrukturen, in denen Kohlenstoffatome auch zu längeren Ketten verbunden sind.
- Die Si-H-Bindung ist weniger stabil als die C-H-Bindung. Letztere ist jedoch grundlegend für den Aufbau organischer Verbindungen und damit auch für Moleküle, auf denen Leben basiert. Das deutet darauf hin, dass Moleküle mit Si-H-Bindungen im Vergleich weniger stabil sind, sich möglicherweise nicht in ausreichender Menge bilden würden oder nur über einen kurzen Zeitraum hinweg beständig wären.
- Da Siliciumatome im Gegensatz zu Kohlenstoffatomen keine Doppel- oder Dreifachbindungen ausbilden, könnten viele für Lebewesen zentrale Stoffklassen nicht existieren, da die dafür erforderlichen funktionellen Gruppen fehlen würden. Dadurch wären sowohl der Aufbau lebender Organismen als auch die chemischen Reaktionen und Umwandlungsprozesse zwischen verschiedenen Molekülklassen, die für Lebensfähigkeit notwendig sind, möglicherweise nicht in ausreichendem Maße realisierbar.
Hinweis: Zum Erreichen der vollen Punktzahl sind inhaltlich äquivalente Alternativen gleichermaßen zulässig.