Aufgabe 4 — BOHR'sches Atommodell
Für das BOHR'sche Atommodell des Wasserstoff-Atoms gilt für die Energiewerte auf der -ten Bahn die Serienformel:
Berechne die Energiewerte für bis
Zeichne damit ein Energieniveauschema maßstabsgerecht.
Für diese Aufgabe wird angenommen, dass zunächst eine Anregung des Atoms aus dem Grundzustand bis in den angeregten Zustand
erfolgt ist.
Überprüfe, ob Stöße mit externen Elektronen, die über eine kinetische Energie von verfügen, als Ursache dafür möglich sind.
Beim Übergang in energieärmere Zustände kann sichtbares Licht emittiert werden, wenn der Übergang in den Zustand erfolgt.
Zeichne für jede dieser Möglichkeiten den Übergang im Energieniveauschema ein und berechne jeweils die Wellenlänge.
Sichtbares Licht einer Wasserstoffröhre wird mit einem optischen Gitter, das Linien je Millimeter aufweist, in einem Interferenzexperiment untersucht. Dabei beträgt der Abstand zwischen Gitter und Schirm
für den Abstand der beiden Maxima 1. Ordnung werden
abgelesen.
Ermittle aus den Messwerten die Wellenlänge des Lichts und gib den dazugehörenden Übergang im Energieniveauschema an.
Hinweis: Verwende die Näherung für kleine Winkel
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Energiewerte berechnen
|
|
|
|---|---|
|
|
|
|
|
|
|
|
|
|
|
|
Energieniveauschema zeichnen
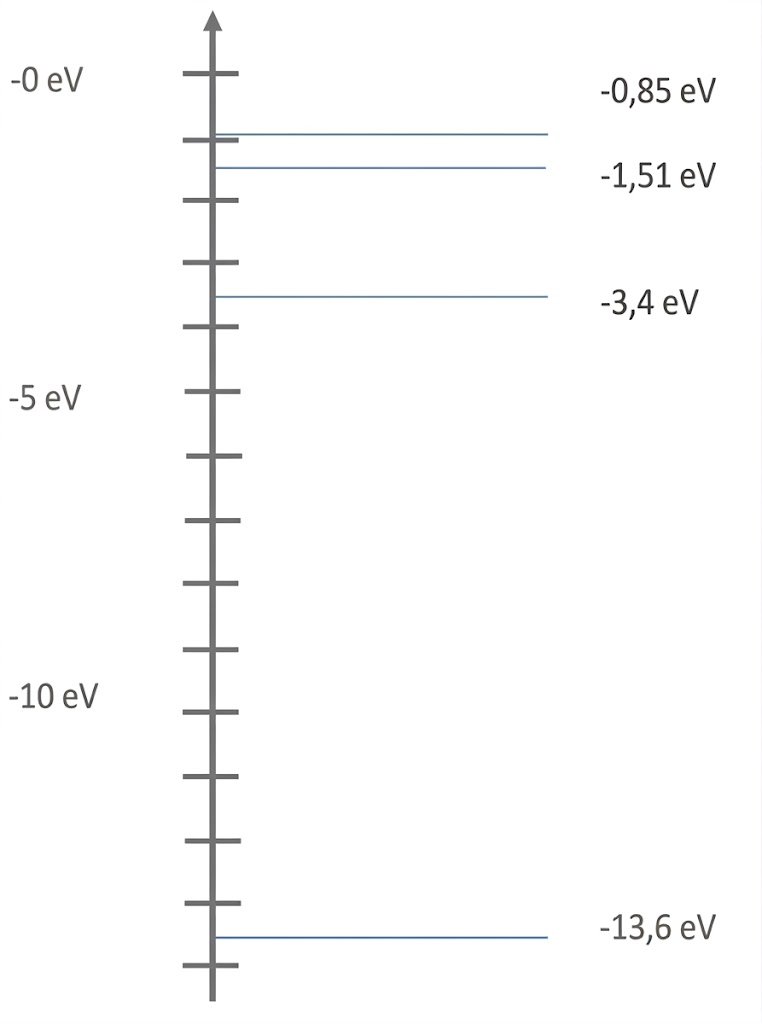
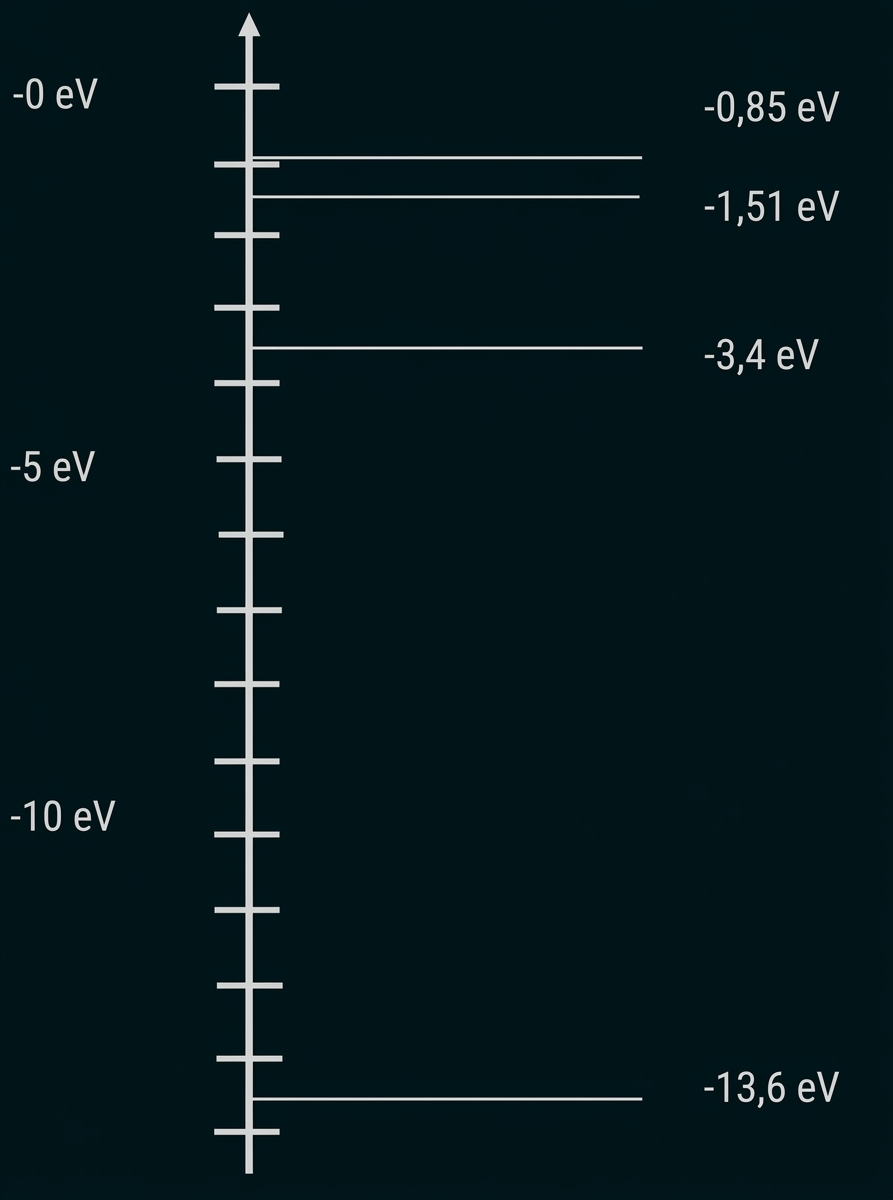
Ursache überprüfen
Für den Übergang von zu
wäre ein Energiebetrag von
notwendig. Daher sind Stöße mit externen Elektronen, die über eine kinetische Energie von
verfügen, dafür als Ursache nicht möglich.
Übergänge einzeichnen
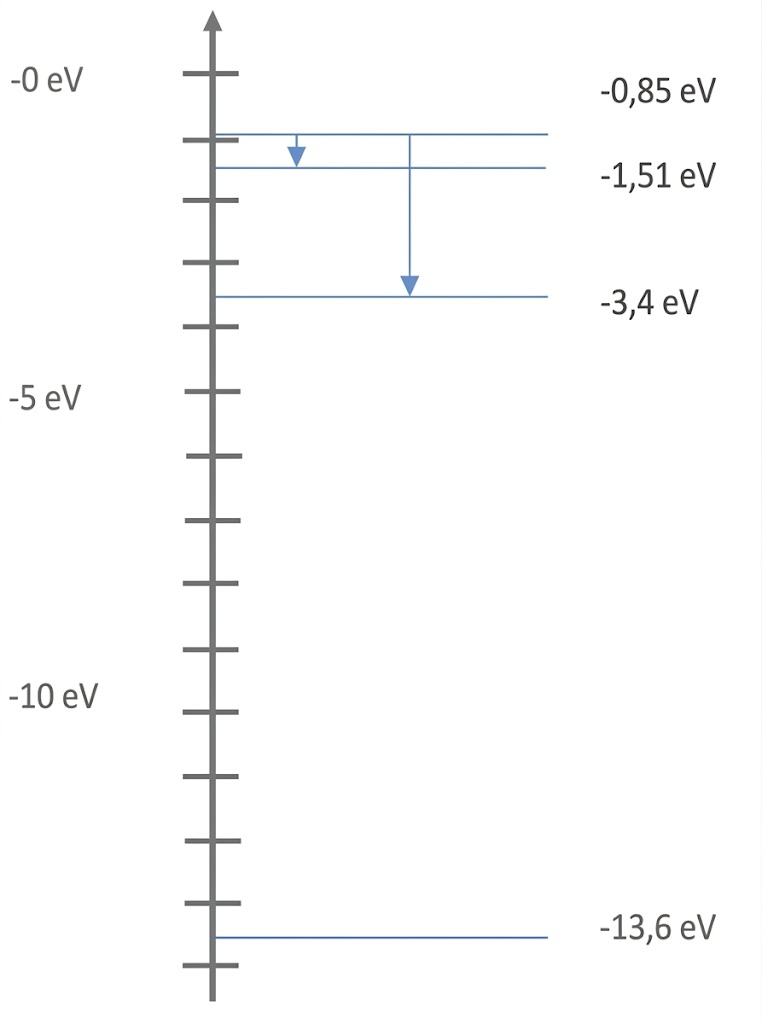
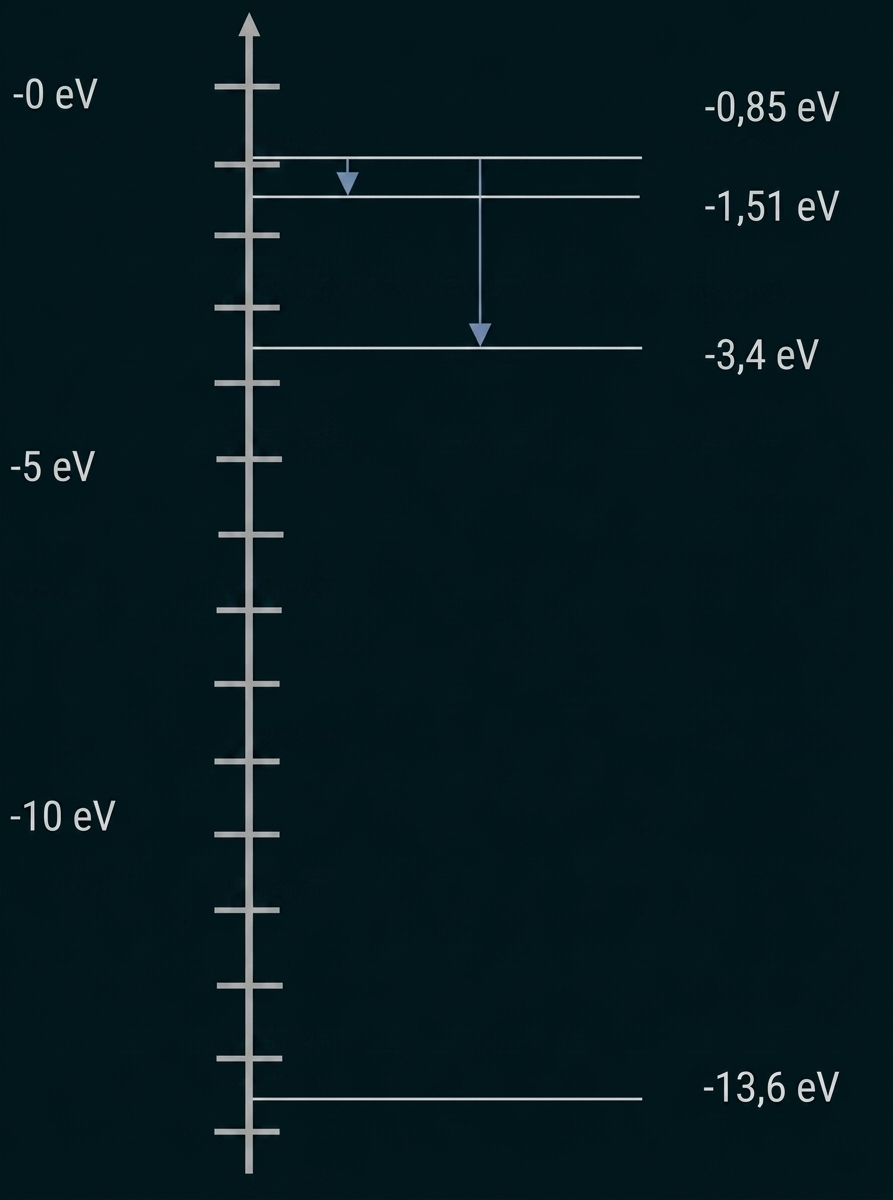
Wellenlängen berechnen
Für den Übergang gilt:
Für den Übergang gilt:
Die Näherung für kleine Winkel liefert und damit:
Somit handelt es sich um den Übergang