HT 1 — Doppelspaltversuch mit Heliumatomen
Teilaufgabe 1: Die Anfänge der Quantenphysik
Zu Beginn des 20. Jahrhunderts waren die klassischen Vorstellungen von Licht als Welle und dem Elektron als Teilchen fest etabliert. Experimente zum Verhalten von Licht am Doppelspalt und Experimente zum Verhalten von Elektronen in Feldern bestätigten diese Vorstellungen.
-
Beschreibe, wodurch die Welleneigenschaft von Licht bei einem Doppelspaltexperiment deutlich wird.
-
Beschreibe, wodurch die Teilcheneigenschaft von Elektronen in einem elektrischen Feld deutlich wird.
Die Teilcheneigenschaft des Lichts wurde im Jahr 1905 von Albert Einstein unter anderem durch die Gleichung beschrieben, wobei
die Photonenenergie,
das Planck’sche Wirkungsquantum und
die Frequenz des Lichts bezeichnen.
-
Erläutere die Gleichung
im Zusammenhang mit dem Fotoeffekt.
Fast zeitgleich stellte Albert Einstein die berühmte Gleichung auf, wobei
die Energie und
die Masse eines Objekts sowie
die Lichtgeschwindigkeit bezeichnen.
-
Erläutere die fundamentale Bedeutung, die der Gleichung
zugrunde liegt.
Der Physiker Louis de Broglie kombinierte im Jahr 1924 die beiden Gleichungen aus Aufgabenteil b) und erhielt den Zusammenhang für den Impuls eines Photons, wobei
die Wellenlänge des Lichts bezeichnet.
-
Leite diesen Zusammenhang ausgehend von den beiden Gleichungen aus Aufgabenteil b) her.
De Broglie stellte die Hypothese auf, dass dieser Zusammenhang auch für Objekte gelten müsse, die bisher klassisch als Teilchen betrachtet wurden.
-
Erläutere die Bedeutung der Gleichung
in Bezug auf das Elektron.
Teilaufgabe 2: Interferenz von Heliumatomen am Doppelspalt
Die De-Broglie-Hypothese aus Teilaufgabe 1 wurde bisher in vielen unterschiedlichen Experimenten bestätigt. Ein solches Experiment wurde im Jahr 1991 mit Heliumatomen (Atomen) durchgeführt. Abbildung 1 zeigt schematisch den entsprechenden Versuchsaufbau.
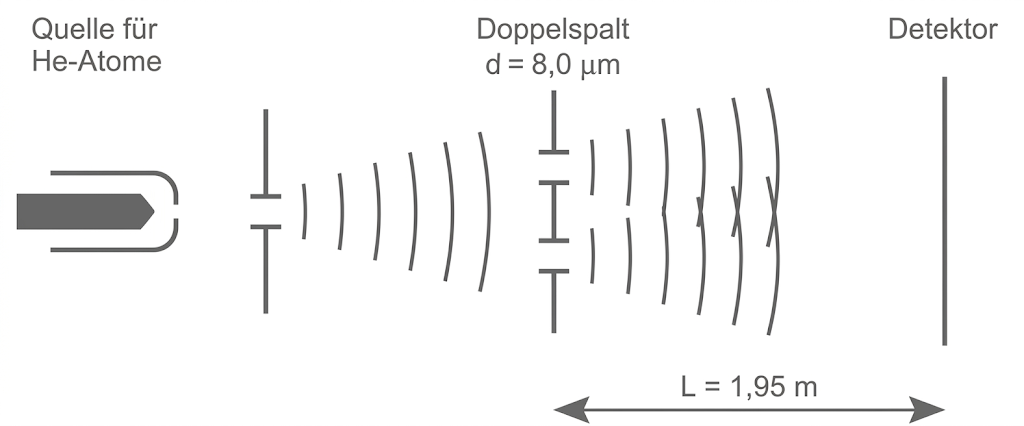
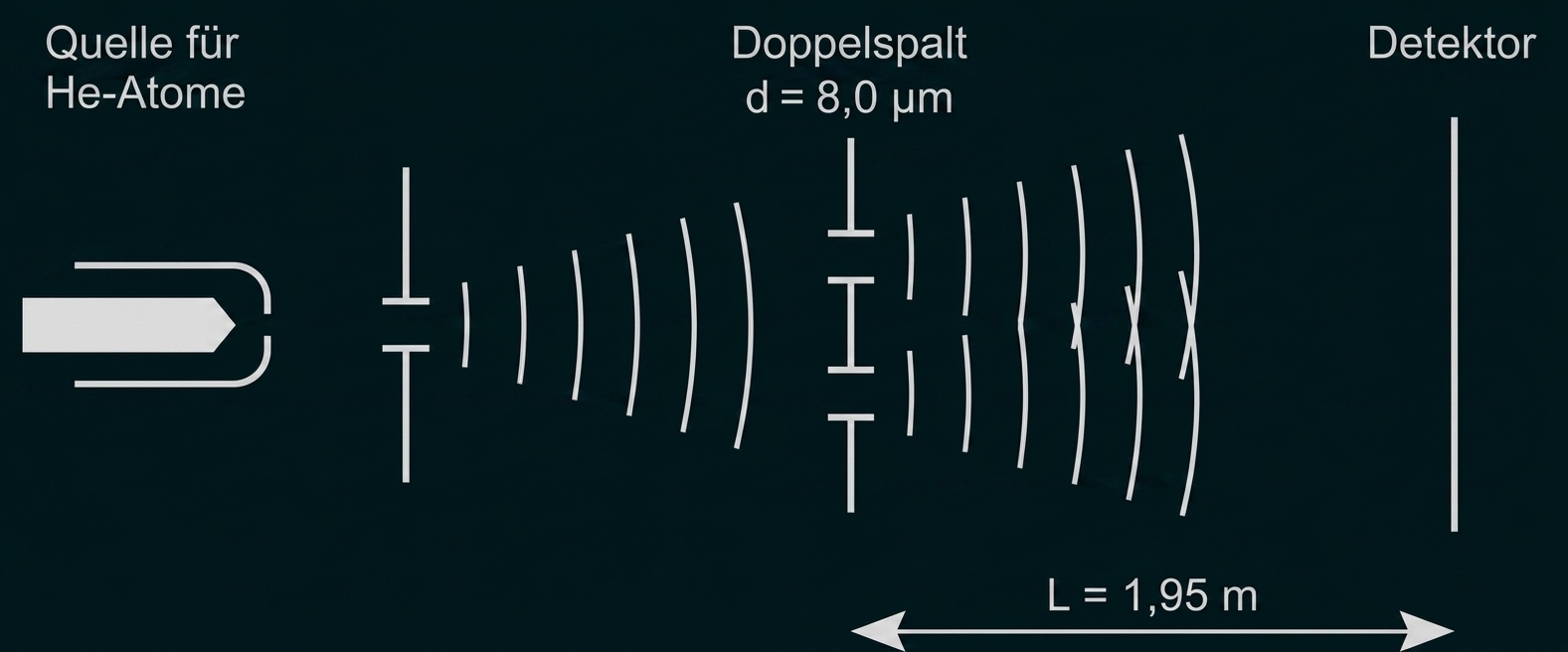
Abbildung 1: Schematische Darstellung des Versuchsaufbaus
(Quelle: Ludwig Bergmann / Clemens Schaefer: Lehrbuch der Experimentalphysik, Band 3 Optik, 2004, S. 1280; verändert)
Bei der Beugung der He-Atome mit der De-Broglie-Wellenlänge am Doppelspalt gilt für den Winkel
unter dem sich am Detektor das Interferenzmaximum
-ter Ordnung ausbildet, der folgende Zusammenhang:
-
Leite diesen Zusammenhang mithilfe einer geeigneten Skizze her.
Für die Herleitung muss der Abstand der Spaltmitten wesentlich kleiner sein als der Abstand
zwischen Doppelspalt und Detektor.
-
Begründe diese Notwendigkeit für die Herleitung.
Abbildung 2 zeigt zwei Verteilungen der am Detektor registrierten Atome bei unterschiedlichen De-Broglie-Wellenlängen.
Versuchsdurchführung (A)
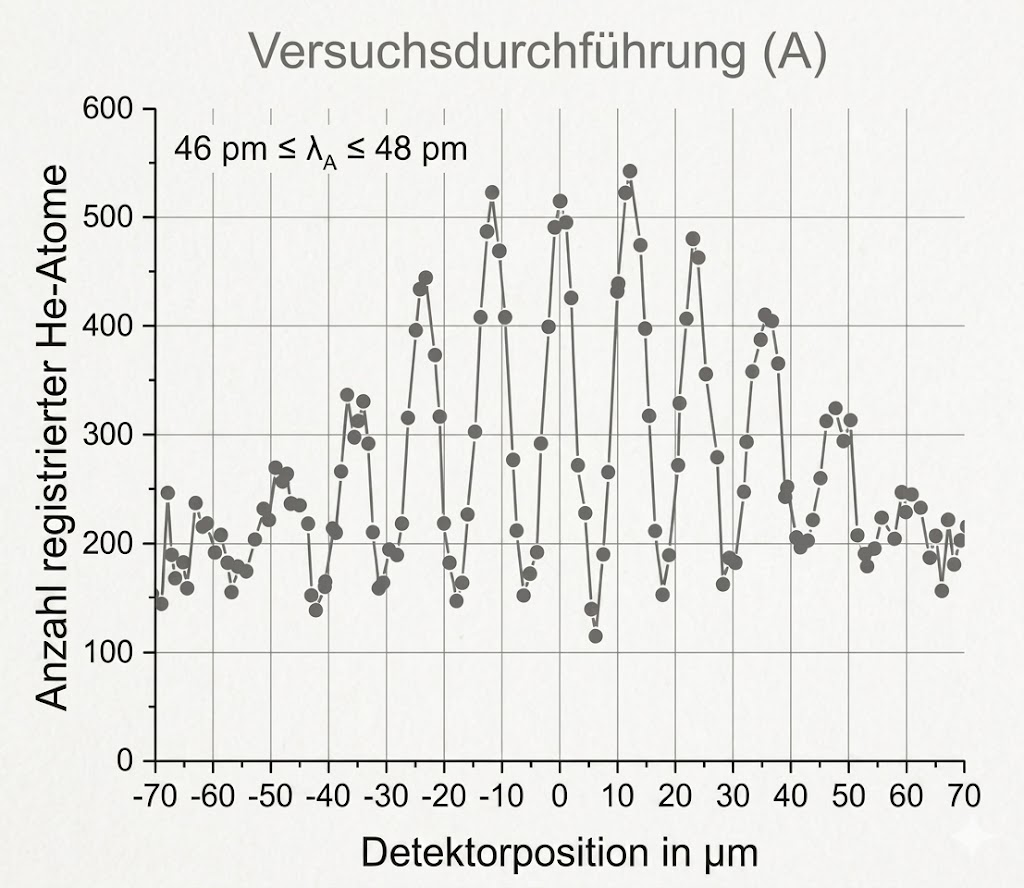
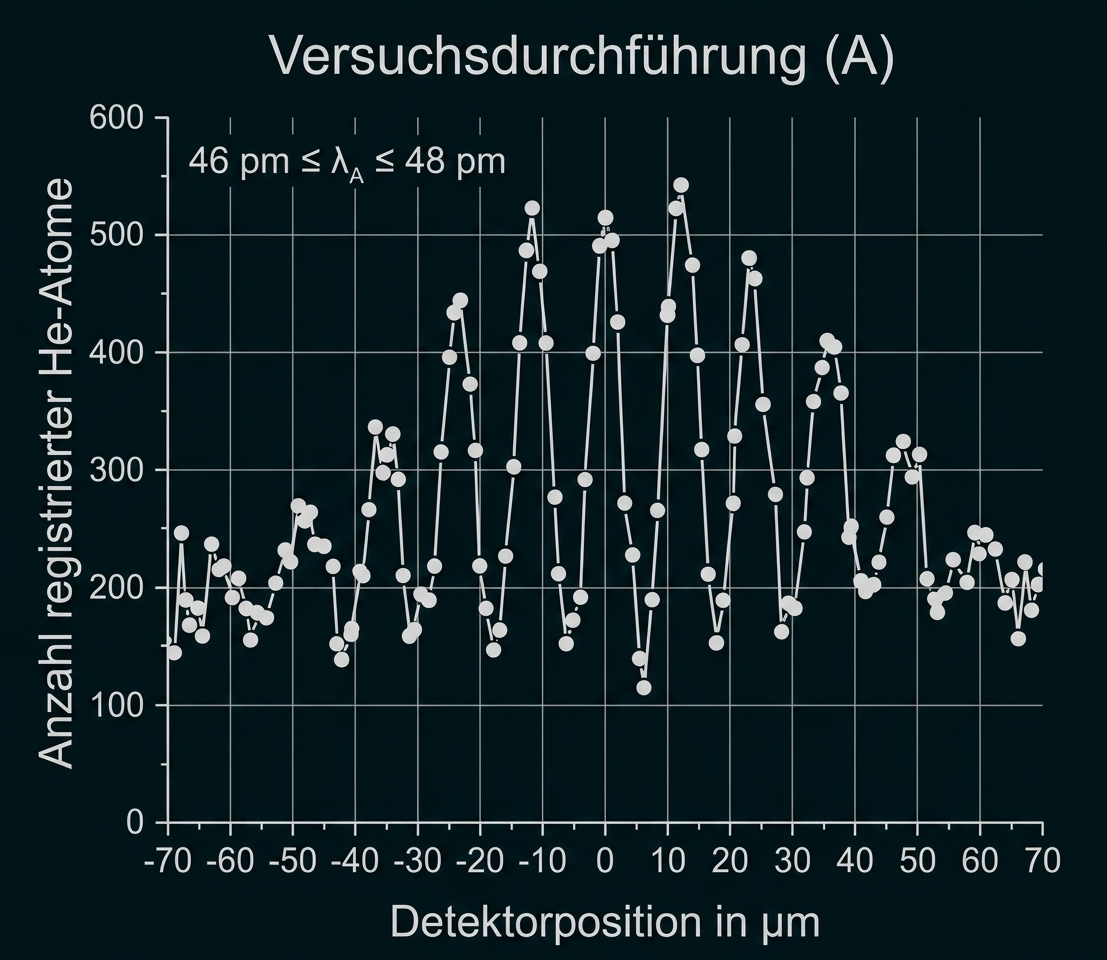
Versuchsdurchführung (B)
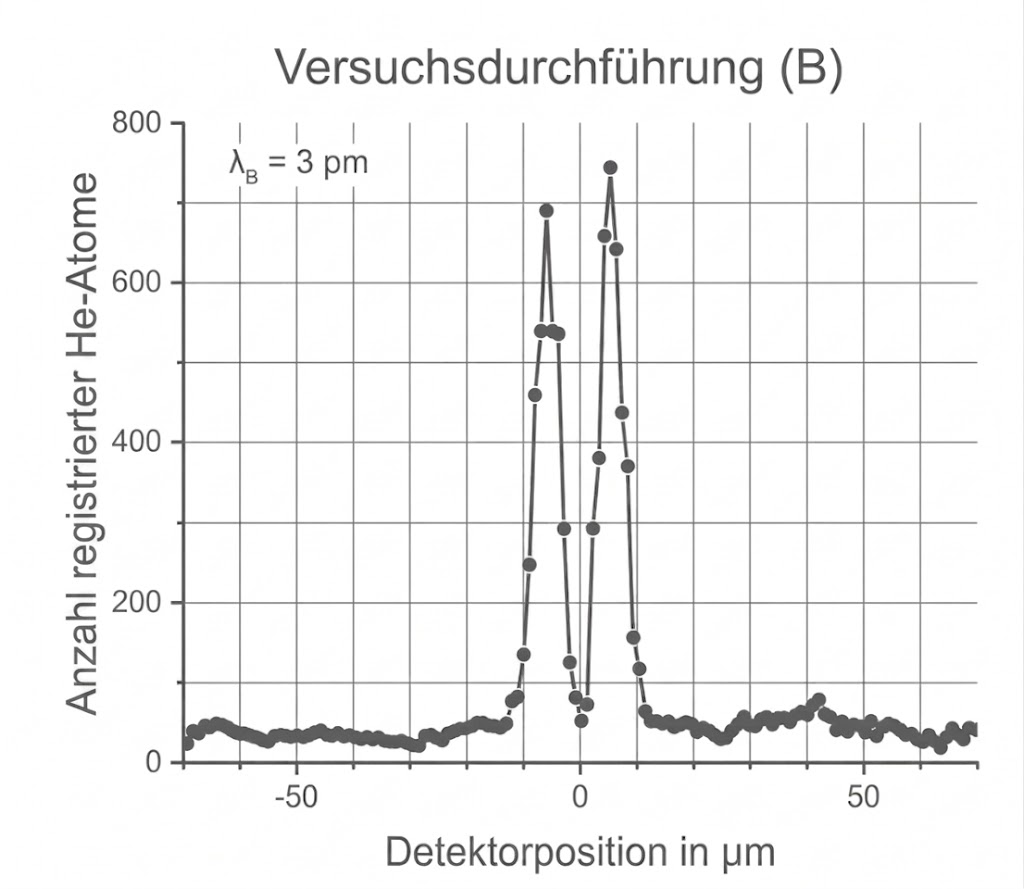
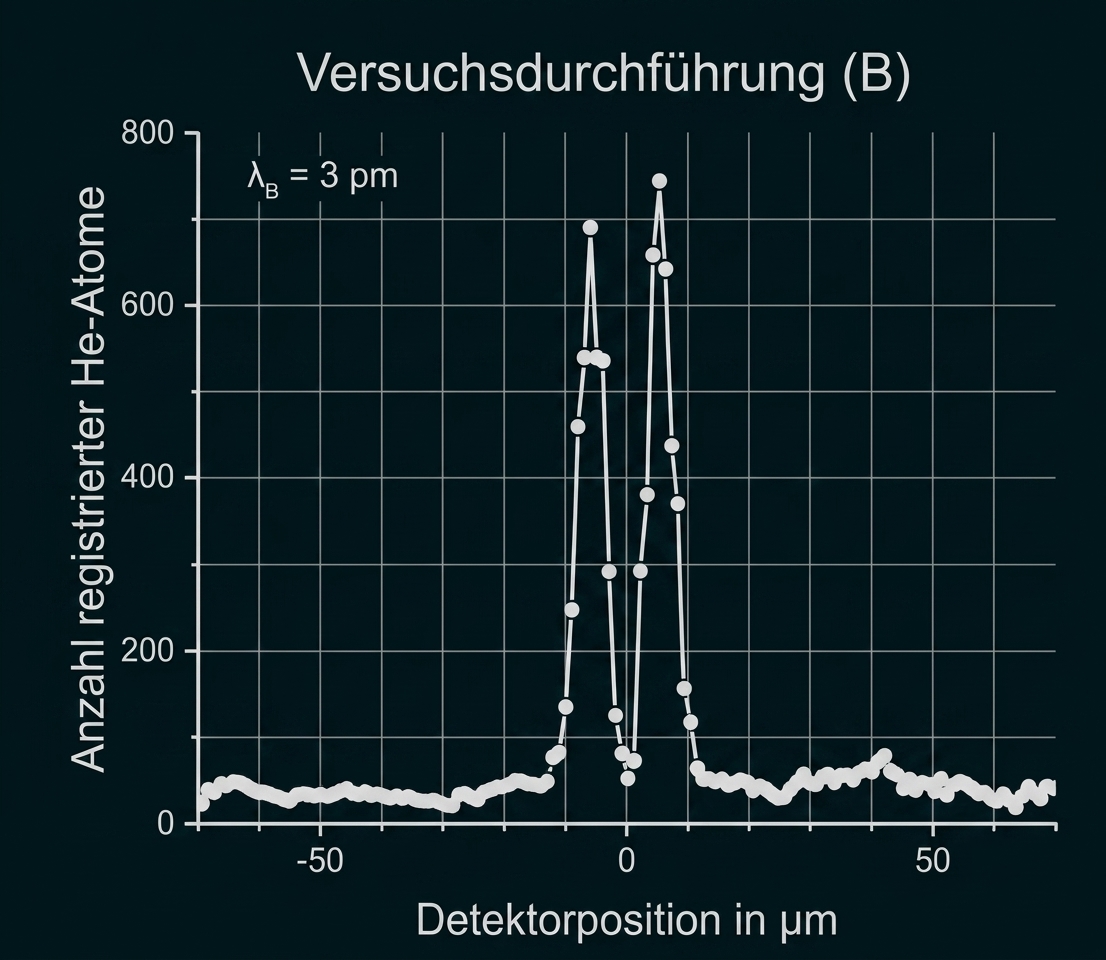
Abbildung 2: Verteilungen der Atome für zwei verschiedene Versuchsdurchführungen (A) und (B)
(Quelle: John S. Townsend: Quantum Physics – A Fundamental Approach to Modern Physics, 2010, S. 54; verändert)
-
Vergleiche die zu den Versuchsdurchführungen (A) und (B) gehörenden Verteilungen miteinander.
Die De-Broglie-Wellenlängen der verwendeten
Atome streuen bei Versuchsdurchführung (A) geringfügig im Intervall
Weitere Daten des Experiments: Abstand der Spaltmitten
Abstand Doppelspalt/Detektor
-
Weise nach, dass sowohl die untere als auch die obere Grenze des angegebenen Wellenlängenintervalls zur Lage des Maximums 4. Ordnung passen.
Die De-Broglie-Wellenlänge der verwendeten
Atome ist bei der Versuchsdurchführung (B) mit
angegeben.
-
Interpretiere die in Abbildung 2 dargestellte Verteilung für die Versuchsdurchführung (B).
Abbildung 3 zeigt die Verteilung der De-Broglie-Wellenlängen der von der Quelle für
Atome in Abbildung 1 emittierten
Atome.
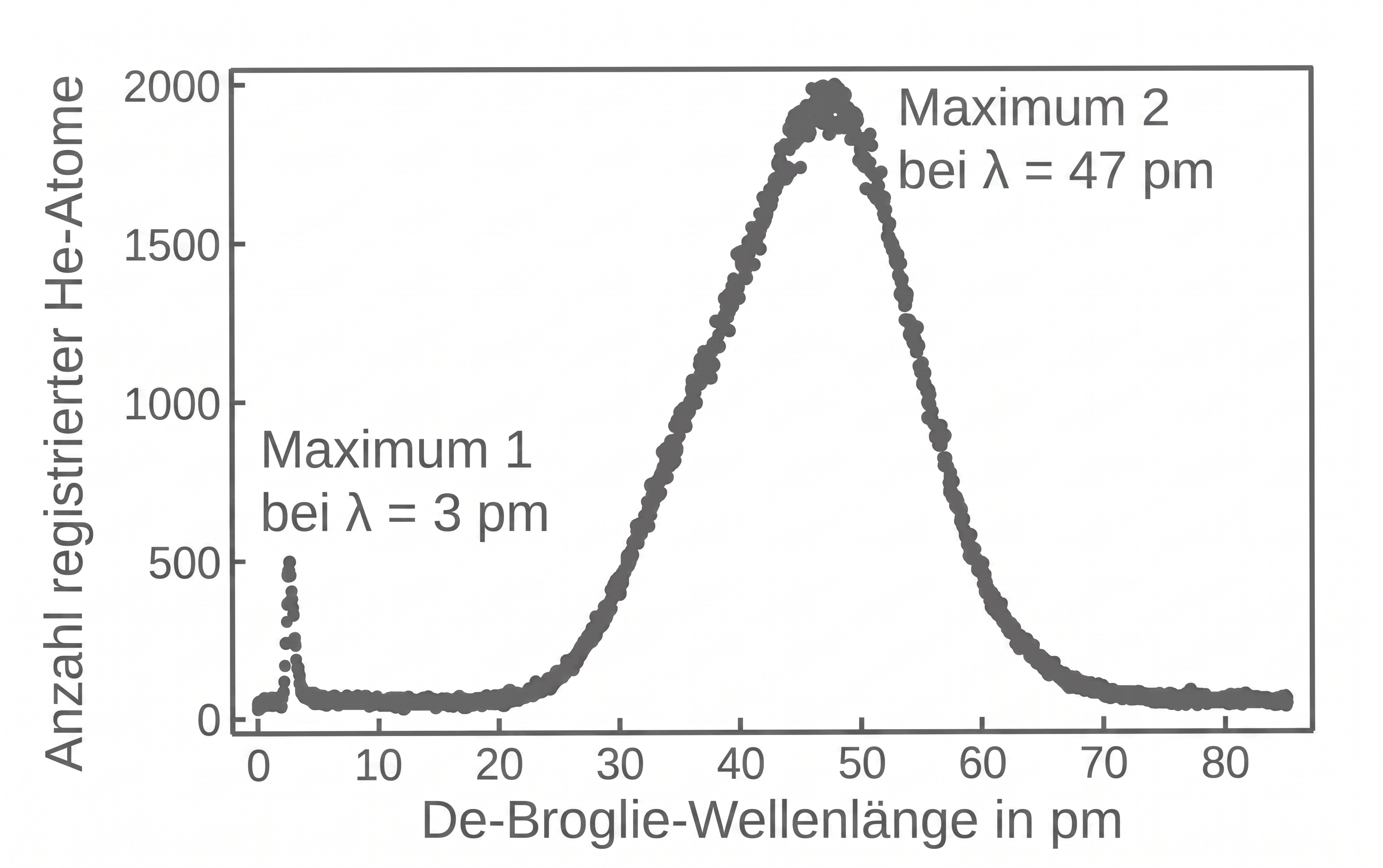
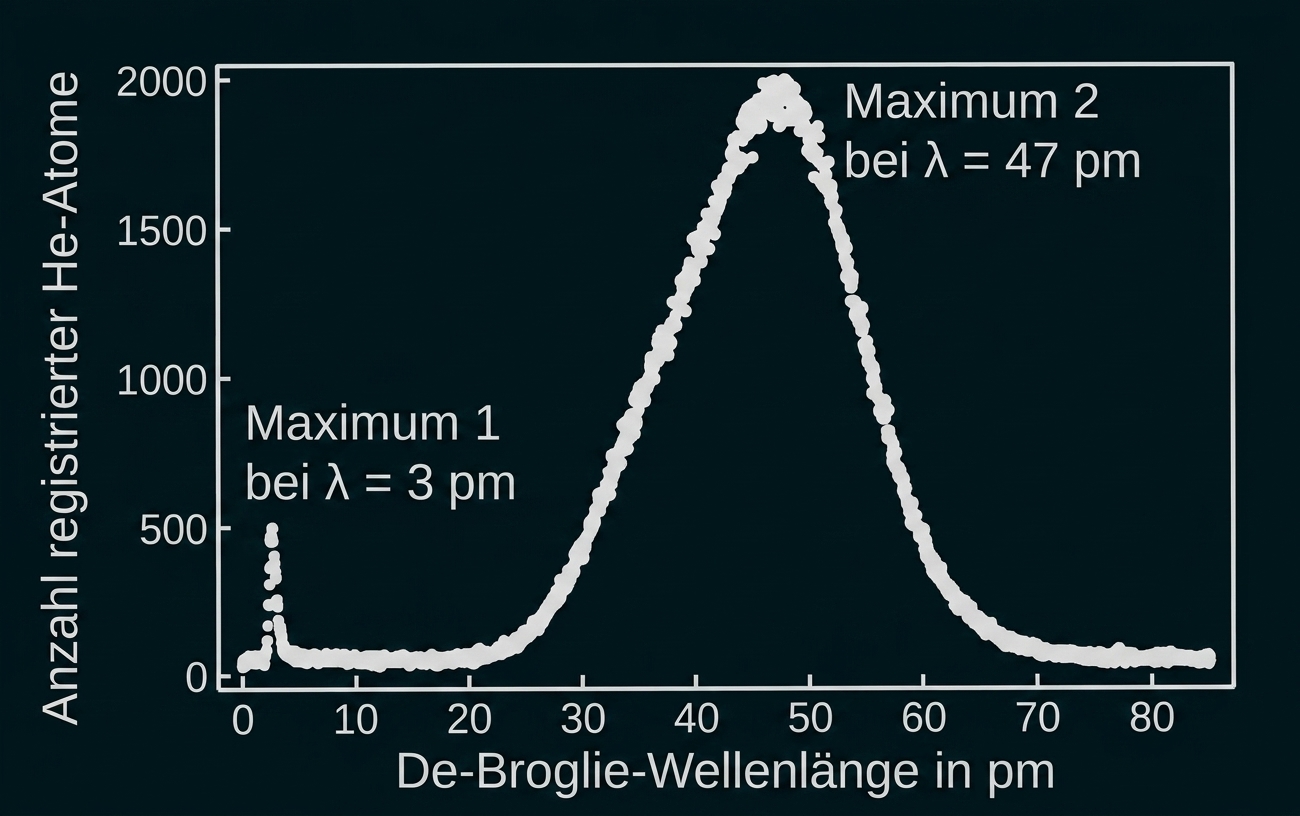
Abbildung 3: Verteilung der De-Broglie-Wellenlängen der Quelle
(Quelle: T. Pfau / C. Kurtsiefer: Partial reconstruction of the motional Wigner function of an ensemble of helium atoms, Journal of Modern Optics, 1997, 44:11 – 12, S. 2556; verändert)
Die Verteilung zeigt zwei deutliche Maxima, die zu Atomen mit unterschiedlichen Geschwindigkeiten
gehören.
-
Entscheide begründet, zu welchem der beiden Maxima diejenigen
Atome mit der größeren Geschwindigkeit gehören.
Die Masse eines Atoms beträgt
-
Bestimme nichtrelativistisch die Geschwindigkeit
der zu diesem Maximum gehörenden
Atome.
In einer Versuchsdurchführung (C) werden diejenigen Atome aus der Wellenlängenverteilung in Abbildung 3 verwendet, deren De-Broglie-Wellenlängen
in dem Intervall
liegen.
-
Erläutere die von dir erwartete Veränderung bei der Beurteilung der am Detektor registrierten Verteilung der
Atome im Vergleich zu der Verteilung aus Versuchsdurchführung (A) in Abbildung 2.
Um die Verteilung in Abbildung 2 für Versuchsdurchführung (A) zu ermitteln, wurde das in Abbildung 4 dargestellte Muster der Atome ausgewertet.
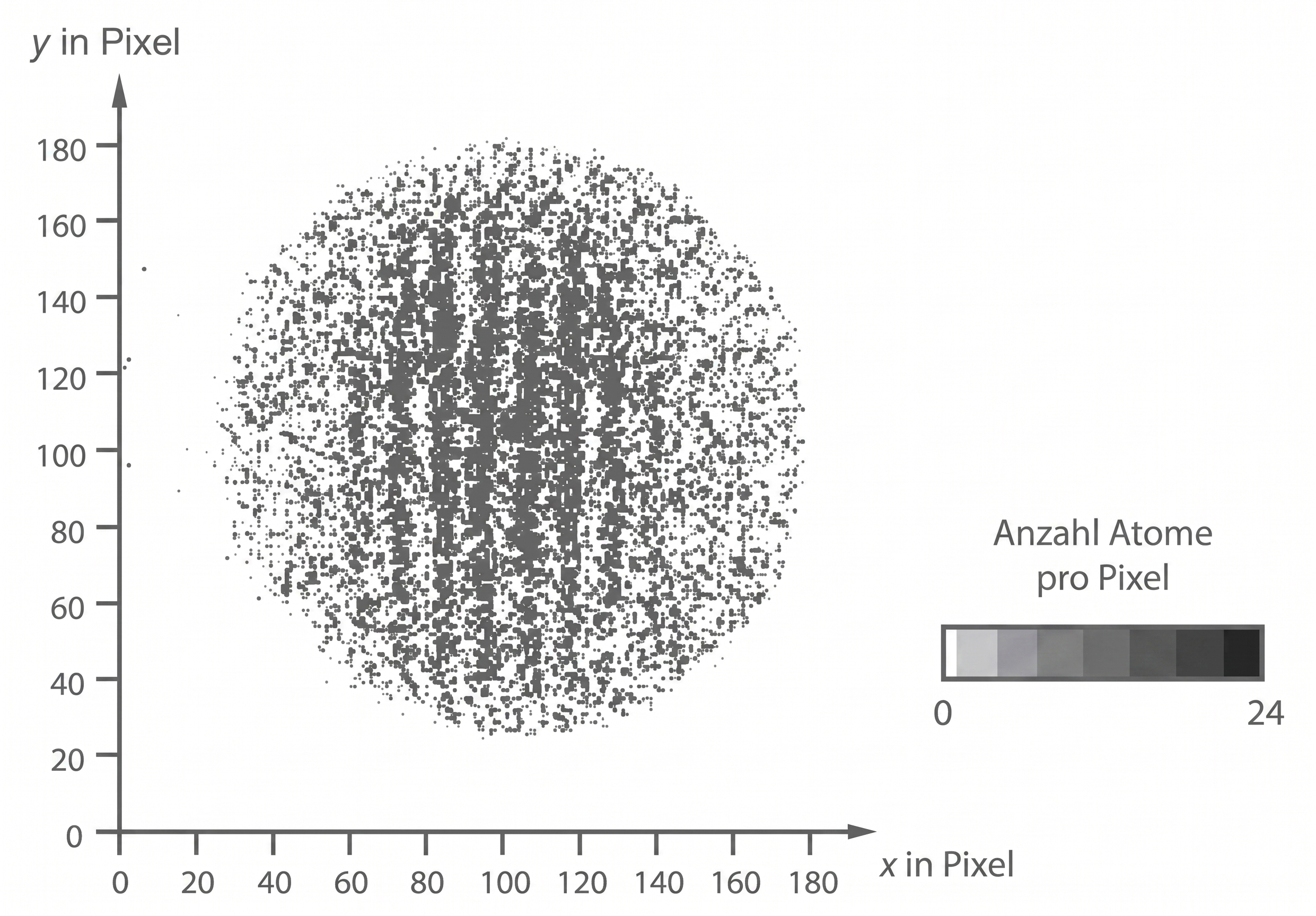
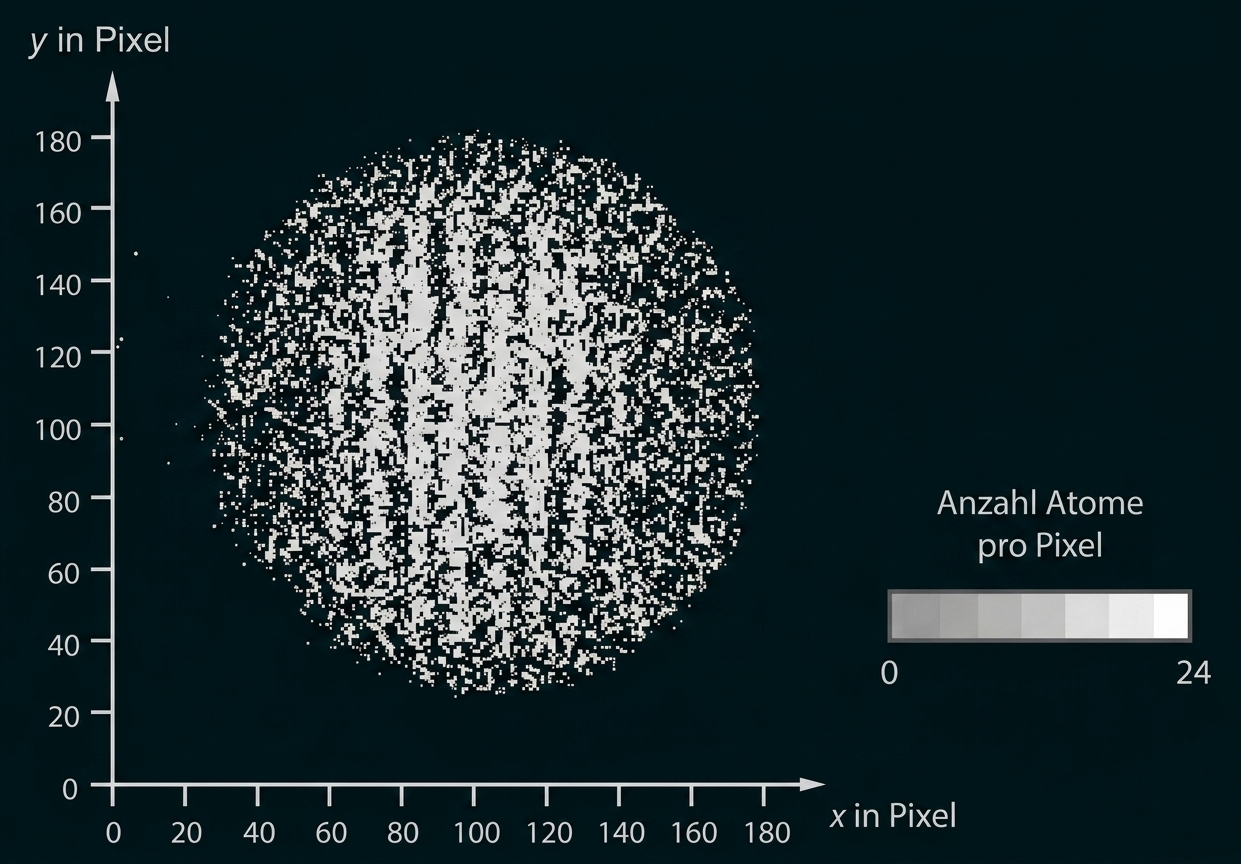
Abbildung 4: Muster der detektierten Atome
(Quelle: T. Pfau / C. Kurtsiefer: Partial reconstruction of the motional Wigner function of an ensemble of helium atoms, Journal of Modern Optics, 1997, 44:11 – 12, S. 2557; verändert)
-
Beschreibe das in Abbildung 4 dargestellte Muster der detektierten
Atome.
-
Erläutere anhand von Abbildung 4, dass das Verhalten der
Atome am Doppelspalt weder ausschließlich durch ein klassisches Wellenmodell noch ausschließlich durch ein klassisches Teilchenmodell beschrieben werden kann.
Teilaufgabe 3: Verändertes Doppelspaltexperiment mit Heliumatomen
In einem weiteren Versuch soll untersucht werden, wie sich die Verteilung der Atome am Detektor verändert, wenn diese vor dem Durchqueren des Doppelspalts angeregt werden und am Ort des Doppelspalts anschließend Photonen emittieren.
Abbildung 5 zeigt ein vereinfachtes Energieniveauschema von Helium.
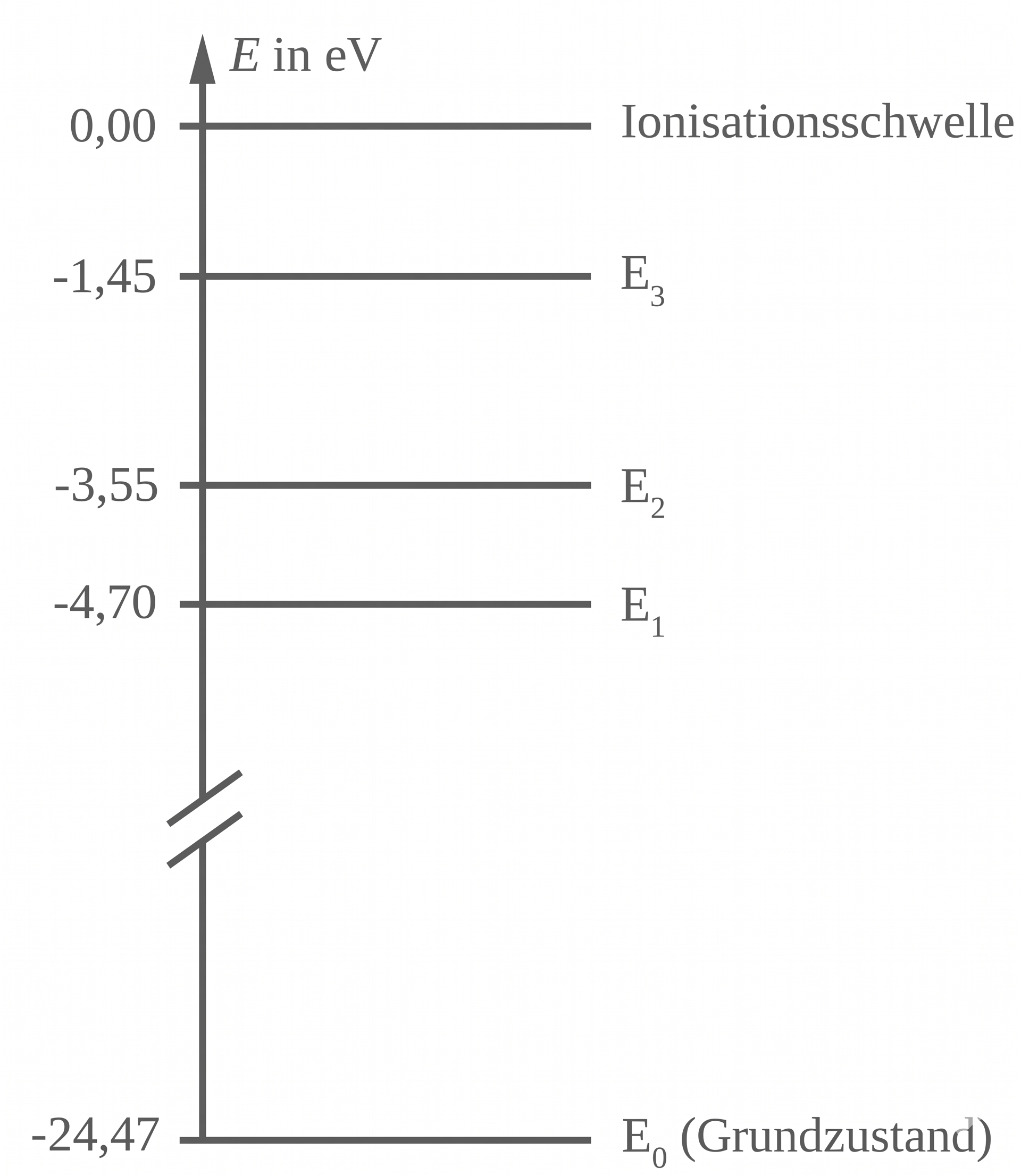

Abbildung 5: Vereinfachtes Energieniveauschema von Helium
Die aus der Quelle in Abbildung 1 entweichenden Atome werden unmittelbar nach dem Verlassen der Quelle angeregt.
-
Berechne die Energie
die einem
Atom im Grundzustand mindestens zugeführt werden muss, damit es sich in einem angeregten Zustand befindet.
Atome können auf unterschiedliche Weise angeregt werden.
-
Erläutere den Unterschied zwischen Anregung eines
Atoms durch Elektronenstoß und der Anregung durch ein Photon.
Der Aufbau aus Abbildung 1 wird so abgeändert, dass die in den Zustand angeregten
Atome unmittelbar vor dem Durchqueren des Doppelspalts mit den Photonen einer monochromatischen Lichtquelle der Wellenlänge
wechselwirken.
-
Zeige, dass diese Wechselwirkung die
Atome auf ein noch höheres Energieniveau anregen kann.
Jedes so angeregte Atom geht unmittelbar nach der weiteren Anregung noch am Ort des Doppelspaltes in den Grundzustand über. In den beiden Spalten befindet sich jeweils ein Messgerät für Photonen (siehe Abbildung 6).
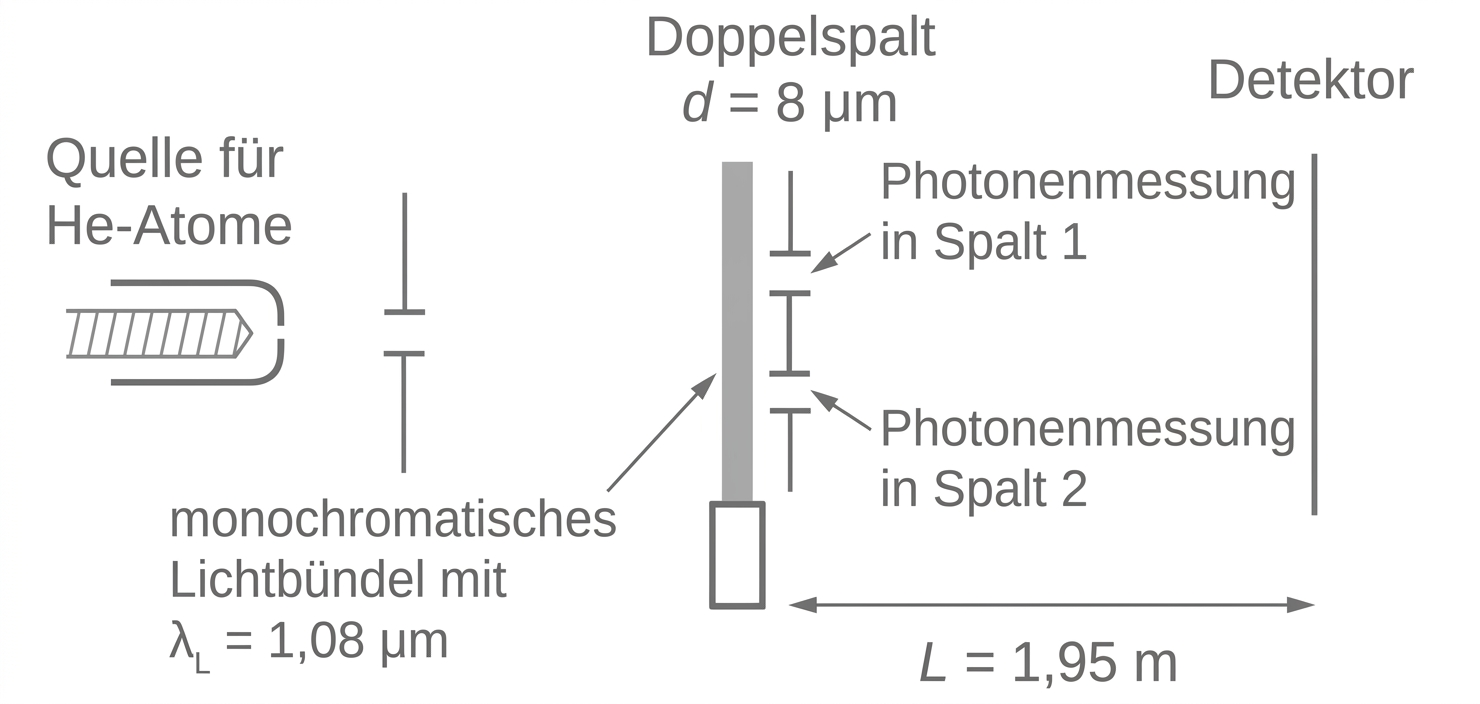
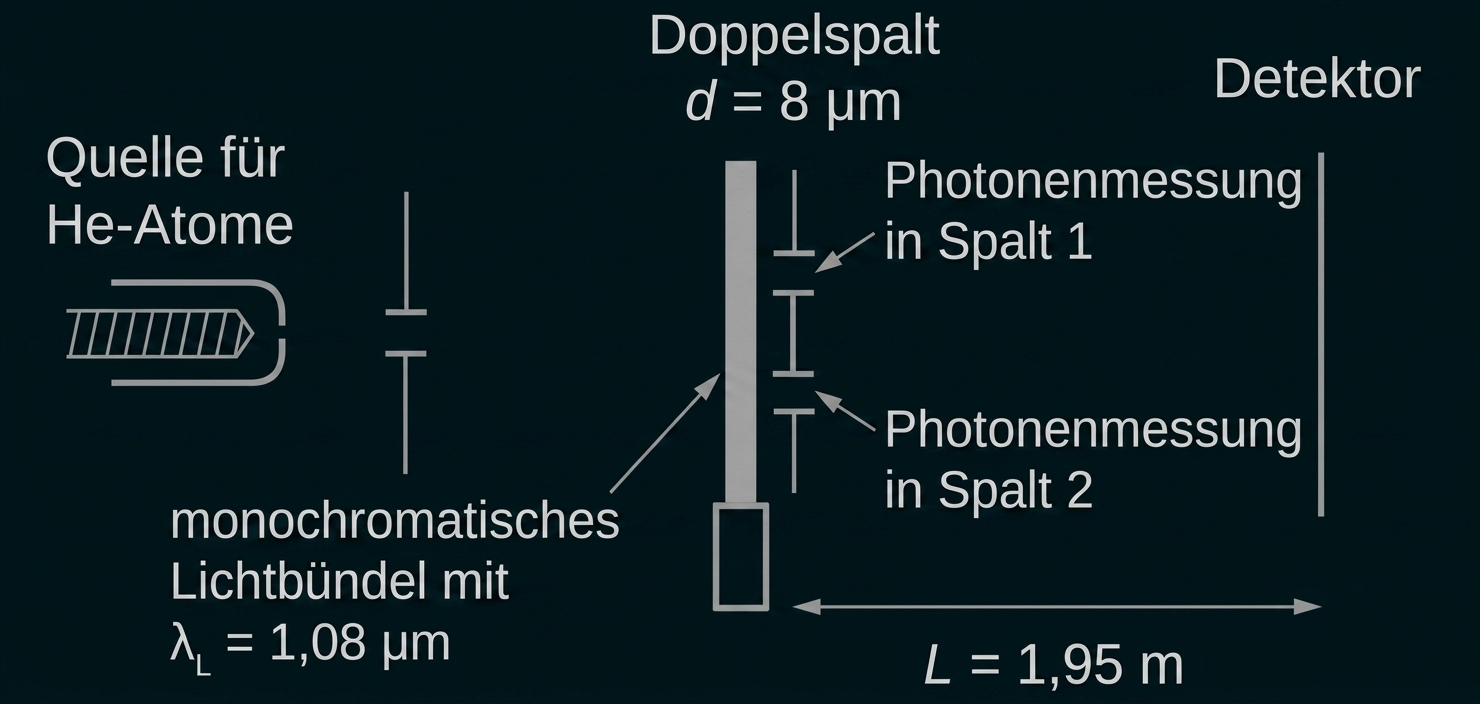
Abbildung 6: Schematische Darstellung des abgeänderten Versuchsaufbaus
(Quelle: Ludwig Bergmann / Clemens Schaefer: Lehrbuch der Experimentalphysik, Band 3 Optik, 2004, S. 1280; verändert)
Werden Atome im Wellenlängenbereich
verwendet, so ergibt sich im Gegensatz zu Abbildung 2 (A) die folgende Verteilung in Abbildung 7.
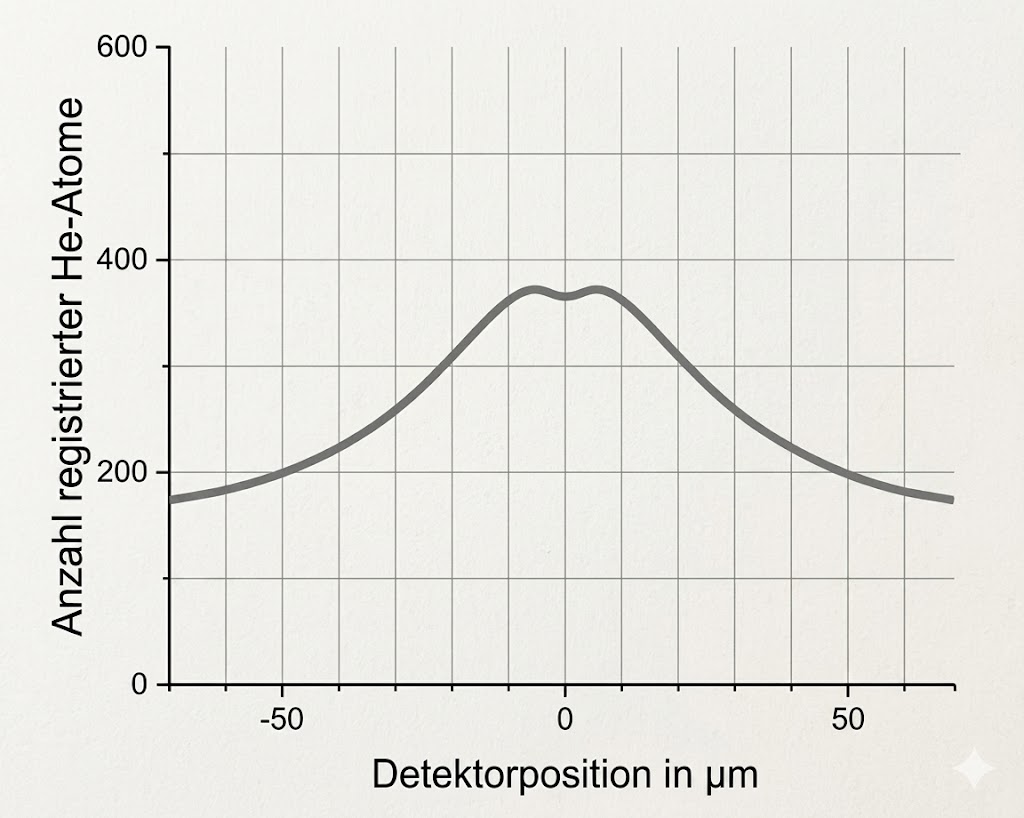
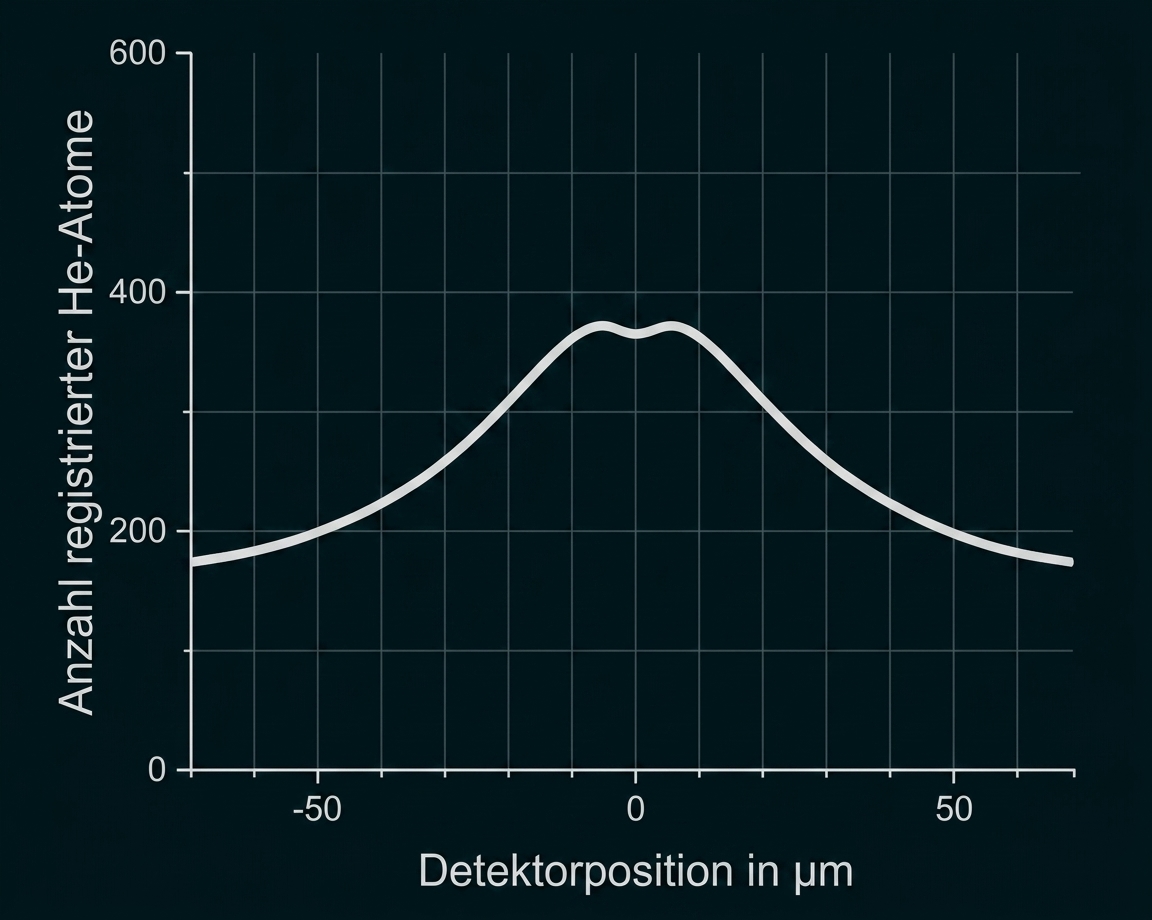
Abbildung 7: Verteilung der Atome
-
Begründe die Verteilung der am Detektor registrierten He-Atome.
Hinweis: Gehe davon aus, dass alle von der Quelle emittierten He-Atome durch das Licht der monochromatischen Lichtquelle angeregt werden.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Teilaufgabe 1: Die Anfänge der Quantenphysik
-
Welleneigenschaft von Licht: Beleuchtet eine monochromatische Lichtquelle einen Doppelspalt, entsteht auf einem Beobachtungsschirm ein zentraler heller Streifen. Symmetrisch zu diesem Zentrum bilden sich weitere, nach außen hin schwächer werdende helle Streifen ab. Es ist somit ein Interferenzmuster zu sehen, das aus der Interferenz der von den beiden Spalten ausgehenden Lichtwellen resultiert. Da die Fähigkeit zur Interferenz ein grundlegendes Merkmal von Wellen darstellt, verdeutlicht dieses Phänomen eindeutig die Welleneigenschaft von Licht.
-
Teilcheneigenschaft von Elektronen: Da Elektronen eine elektrische Ladung tragen, wirken auf sie beim Durchqueren eines elektrischen Feldes elektrische Kräfte. Diese Kräfte führen z.B. zu einer Beschleunigung in Bewegungsrichtung oder zu einer seitlichen Ablenkung der Elektronen. Daraus resultieren spezifische Flugbahnen, welche experimentell sichtbar gemacht werden können. Solche Bahnkurven weisen auf den Teilchencharakter der Elektronen hin.
Erläutern der Einstein-Gleichung des Fotoeffekts
Beim Fotoeffekt führt die Bestrahlung von Materie mit Licht zum Herauslösen von Elektronen aus Atomen. Dabei findet eine Umwandlung von Photonenenergie in die kinetische Energie der sogenannten Fotoelektronen statt. Dieser Energieaustausch ist quantisiert, da die Energie des Lichts durch einzelne Photonen ebenfalls quantisiert ist. Bei der Wechselwirkung mit Materie absorbiert ein einzelnes Elektron exakt ein Photon, wobei dieses seine gesamte Energie an das Elektron abgibt. Diese übertragene Energie wird demnach ausschließlich durch die Frequenz
des einfallenden Lichts bestimmt.
Erläutern der fundamentalen Bedeutung
Mit der Gleichung hob Albert Einstein die bis dahin getrennte Betrachtungsweise von Masse
und Energie
auf, stattdessen spricht er von einer Äquivalenz von Masse und Energie. Folglich besitzt jedes Objekt, das eine Masse
besitzt, auch eine Energie
Gleichermaßen weisen Objekte mit einer bestimmten Energie
auch eine Masse
auf. Das Quadrat der Lichtgeschwindigkeit
verknüpft dabei beide Größen.
Herleitung der De-Broglie-Gleichung
Die Photonenenergie entspricht der Energie des herausgelösten Elektrons:
Der Ausdruck entspricht dem klassischen Impuls
mit
Daraus folgt abschließend für den Impuls eines Photons:
Bedeutung der Gleichung für das Elektron
Durch Umstellen der zuvor hergeleiteten Gleichung nach der Wellenlänge ergibt sich die Beziehung Daraus folgt, dass auch jedem Elektron eine spezifische Wellenlänge
zugeordnet werden, welche einzig von seinem Impuls
abhängt. Dem Elektron, das zuvor klassisch rein als Teilchen galt, muss demzufolge auch ein Wellencharakter zugeschrieben werden. Diese theoretisch postulierte Welleneigenschaft lässt sich tatsächlich in Experimenten verifizieren.
Teilaufgabe 2: Interferenz von Heliumatomen am Doppelspalt
Herleitung der Beugungsbedingung und Begründung für den Spaltabstand
Gemäß dem Huygensschen Prinzip breiten sich von den beiden Spalten und
Elementarwellen aus. An der Position eines Maximums auf dem Detektor überlagern sich diese Wellen konstruktiv. Betrachtet wird ein Punkt
an dem ein solches Maximum
-ter Ordnung entsteht. In diesem Fall entspricht der Gangunterschied
der interferierenden Elementarwellen einem ganzzahligen Vielfachen der Wellenlänge
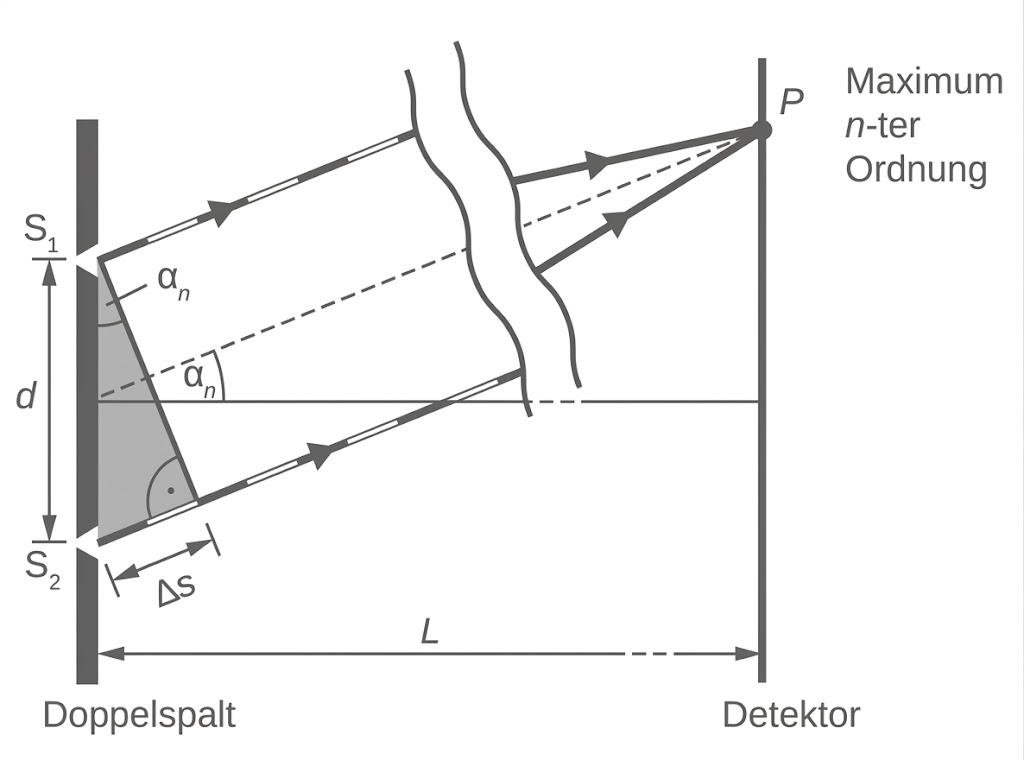
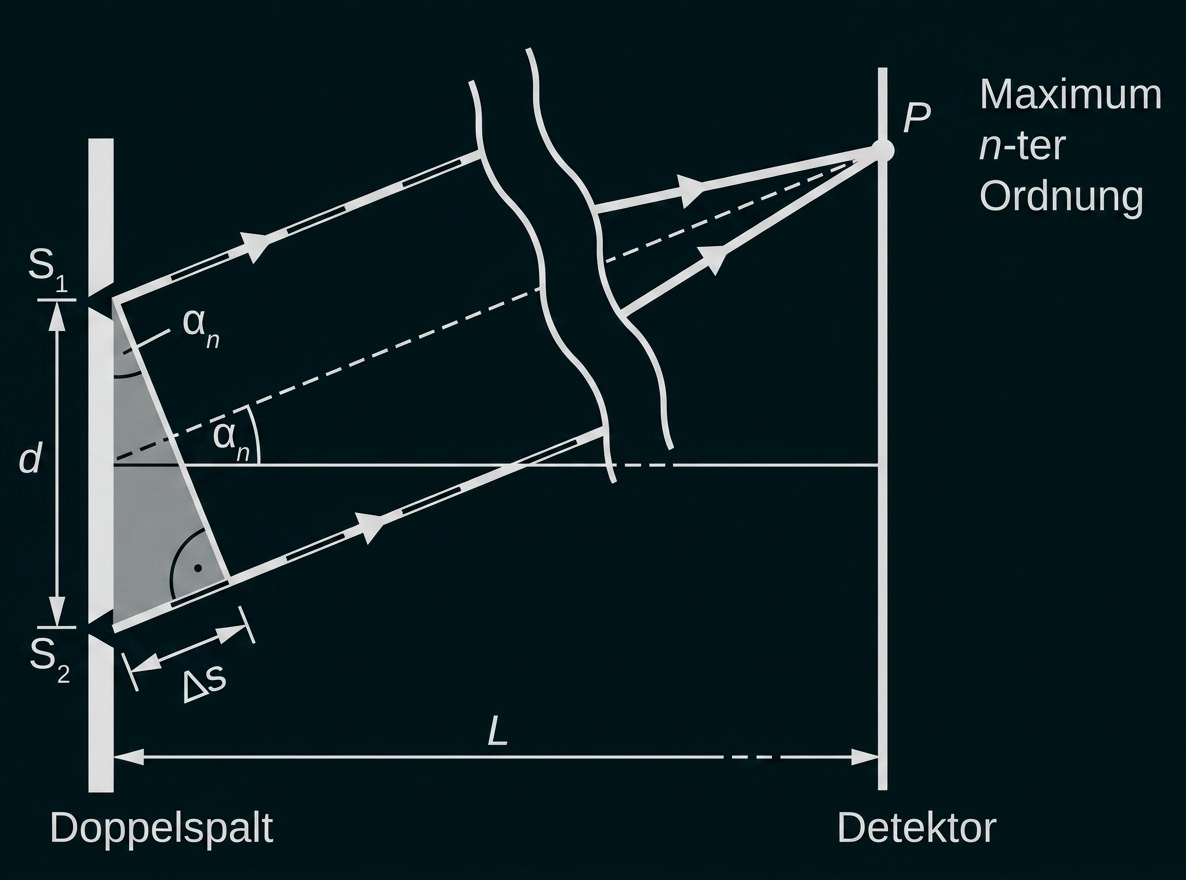
Die Strecken und
sind näherungsweise parallel. Somit ist das grau unterlegte Dreieck ein rechtwinkliges Dreieck, in dem auch der Winkel
auftaucht, unter dem das Maximum
-ter Ordnung beobachtet werden kann.
ist dabei die dem Beugungswinkel
gegenüberliegende Kathete. Daraus resultiert die trigonometrische Beziehung:
Durch Gleichsetzen der beiden Ausdrücke für den Gangunterschied ergibt sich die finale Beugungsbedingung:
Begründung für
Die vorangegangene Herleitung setzt zwingend ein rechtwinkliges Dreieck voraus. Dies ist nur gegeben, wenn die Strecken und
nahezu parallel verlaufen. Gleichzeitig müssen sich diese von den Spalten ausgehenden Strahlen jedoch im gemeinsamen Punkt
auf dem Detektor treffen. Beide Bedingungen lassen sich näherungsweise nur dann gleichzeitig erfüllen, wenn der Abstand
der beiden Spaltmitten um ein Vielfaches kleiner ist als die Entfernung
zwischen dem Doppelspalt und dem Detektor.
Vergleich der Verteilungen
Ein Vergleich der beiden Versuchsdurchführungen zeigt, dass beide Verteilungen deutlich erkennbare Maxima aufweisen. Bei Durchführung (A) sind jedoch mehrere Maxima und Minima zu erkennen, während bei Durchführung (B) lediglich zwei Maxima zu erkennen sind. Ein weiterer Unterschied liegt bei der Detektorposition dort zeigt Verteilung (A) ein Maximum, Verteilung (B) hingegen ein Minimum. Zudem weisen die beiden Peaks bei (B) eine größere Höhe auf als die Peaks bei (A).
Nachweis für das Maximum 4. Ordnung
Zur Überprüfung der Intervallgrenzen wird der Abstand des
-ten Maximums vom nullten Maximum betrachtet. Über die geometrische Beziehung
lässt sich der Abstand mit dem Beugungswinkel verknüpfen. Aus der Beugungsbedingung folgt für den Winkel:
Eingesetzt in die Gleichung für den Abstand ergibt dies:
Für das Maximum 4. Ordnung () werden die gegebenen Werte
und
sowie die beiden Grenzwellenlängen
und
verwendet. Für die untere Grenze ergibt sich somit:
Für die obere Grenze ergibt sich analog:
Das Diagramm zur Versuchsdurchführung (A) zeigt für das vierte Maximum einen Abstand der sich ungefähr zwischen
und
befindet. Somit passen beide Grenzen des Wellenlängenintervalls zur gemessenen Position dieses Maximums.
Interpretation der Versuchsdurchführung (B)
Bei der Versuchsdurchführung (B) weisen die beiden auftretenden Maxima einen Abstand von etwa zueinander auf. Da der Spaltmittenabstand mit
gegeben ist, befinden sich die Maxima nahezu exakt gegenüber den beiden Spalten. Dies lässt den Schluss zu, dass sich die Heliumatome in Versuchsdurchführung (B) ausschließlich wie klassische Teilchen verhalten haben und keinerlei Interferenz aufgetreten ist.
Zuordnung der Geschwindigkeit zu den Maxima
Gemäß der De-Broglie-Beziehung verhalten sich die De-Broglie-Wellenlänge
und die Geschwindigkeit
der
Atome antiproportional zueinander.
Da das Maximum 1 in Abbildung 3 zu der geringeren De-Broglie-Wellenlänge gehört, besitzen die zu diesem Maximum gehörenden Atome folglich die größere Geschwindigkeit.
Bestimmung der Geschwindigkeit
Aus dem Diagramm lässt sich für dieses Maximum die Wellenlänge ablesen. Die nichtrelativistische Geschwindigkeit
berechnet sich durch Umstellen der De-Broglie-Beziehung:
Erwartete Veränderung bei Versuchsdurchführung (C)
Das Intervall der verwendeten De-Broglie-Wellenlängen fällt in der Versuchsdurchführung (C) mit deutlich größer aus als in der Versuchsdurchführung (A). Da die exakte Lage der jeweiligen Maxima auf dem Detektor von der De-Broglie-Wellenlänge abhängt, werden sich die Maxima auf dem Schirm deutlich verbreitern und überlappen. Ein Interferenzmuster wird demnach insgesamt weniger stark ausgeprägt sein oder sogar gar nicht mehr erkennbar bleiben.
Beschreibung des Musters
Das abgebildete Muster zeigt für jeden Pixel die Anzahl der dort registrierten He-Atome. Es lassen sich deutlich Bereiche erkennen, in denen viele Atome auftreffen und wiederum andere Bereiche, in denen nur wenige
Atome registriert werden.
Erläuterung zur Unzulänglichkeit klassischer Modelle
-
Gegen ein reines Wellenmodell: Ließe sich das Verhalten der
Atome am Doppelspalt ausschließlich durch ein klassisches Wellenmodell beschreiben, wären keine isolierten Auftreffpunkte von einzelnen Atomen erkennbar. Es würde sich stattdessen ein kontinuierliches Interferenzmuster zeigen.
-
Gegen ein reines Teilchenmodell: Würde das Verhalten der Atome hingegen ausschließlich durch ein klassisches Teilchenmodell beschrieben werden, dann träten auf dem Detektor lediglich zwei Bereiche mit vielen registrierten
Atomen auf.
Teilaufgabe 3: Verändertes Doppelspaltexperiment mit Heliumatomen
Berechnung der minimalen Energie
Die mindestens zuzuführende Energie entspricht der Differenz der Energiewerte zwischen dem ersten angeregten Zustand
und dem Grundzustand
Daraus folgt:
Unterschied zwischen Elektronenstoß und Photonenabsorption
-
Elektronenstoß: Damit ein Atom durch einen Elektronenstoß angeregt wird, muss die kinetische Energie des stoßenden Elektrons mindestens so groß sein wie die Energiedifferenz
zwischen den beiden beteiligten Niveaus. Das Elektron gibt beim Stoß exakt den benötigten Energiebetrag
an das Atom ab und behält eine eventuell verbleibende Restenergie als kinetische Energie bei.
-
Photonenabsorption: Bei der Anregung durch ein Photon muss die Energie des Photons exakt der Energiedifferenz
zwischen den beiden beteiligten Energieniveaus entsprechen. Im Gegensatz zum Elektron wird das Photon bei diesem Prozess vollständig absorbiert und existiert nach der Anregung nicht mehr.
Nachweis der möglichen weiteren Anregung
Die Photonen aus der monochromatischen Lichtquelle besitzen folgende Energie:
Die Energiedifferenz zwischen den Zuständen und
beträgt:
Da die Photonenenergie exakt dieser Differenz entspricht, ist eine weitere Anregung der Atome vom Zustand
in den Zustand
möglich.
Beim Übergang in den Grundzustand emittiert jedes angeregte Atom ein einzelnes Photon. Da dieser Emissionsprozess unmittelbar am Ort des Doppelspaltes stattfindet, wird das Photon entweder im Messgerät von Spalt 1 oder von Spalt 2 registriert. Dadurch lässt sich eine Information über den Entstehungsort des Photons gewinnen und exakt nachweisen, durch welchen der beiden Spalte das jeweilige
Atom geflogen ist ("Welcher-Weg-Information"). Gemäß des quantenmechanischen Prinzips der Komplementarität schließen sich eine "Welcher-Weg-Information" und ein Interferenzmuster aus, folglich verschwindet das Interferenzmuster. Stattdessen ist nur noch die Überlagerung der jeweiligen durch Beugung an Spalt 1 oder an Spalt 2 hervorgerufenen Verteilungen sichtbar.