Aufgabe 5 — Wasserstoffatome
In einer Spektralröhre wird Wasserstoffgas durch Wechselwirkung mit Elektronen zum Leuchten gebracht. Es wird Licht in vier sichtbaren Spektralbereichen abgestrahlt.
|
Name der Linie |
|
|
|
|
|---|---|---|---|---|
|
Wellenlänge in |
|
|
|
|
Tabelle 3: Sichtbare Spektrallinien
Erläutere anhand eines geeigneten Atommodells die Entstehung dieser Spektrallinien.
Berechne die kinetische Energie, die die Elektronen mindestens haben müssen, damit Strahlung im sichtbaren Bereich entsteht.
In einem weiteren Versuch treffen Elektronen mit der kinetischen Energie von auf ein Gas aus Wasserstoffatomen, die sich zum größeren Teil im Grundzustand, zum kleineren Teil im ersten angeregten Zustand (
) befinden. Die Energiewerte der möglichen Elektronenbahnen lassen sich mit der Gleichung
bestimmen.
Bestimme die Energiezustände für das 1. bis 5. Energieniveau in
Zeichne das entsprechende Energieniveauschema.
Weise nach, dass die Wasserstoffatome im Grundzustand von den Elektronen nicht angeregt werden können.
Zeige, dass die Wasserstoffatome im ersten angeregten Zustand von den Elektronen in jeden beliebigen höheren Zustand angeregt und auch ionisiert werden können.
Erläutere, wie die drei Werte
und
im Energiespektrum dieser Elektronen nach der Wechselwirkung mit dem Wasserstoffgas zustande kommen.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Die Entstehung der Spektrallinien lässt sich z.B. mit dem Bohrschen Atommodell erklären:
-
Stabile Bahnen: Im Wasserstoffatom bewegen sich die Elektronen auf bestimmten, stabilen Bahnen (Energieniveaus) um den Atomkern, ohne dabei elektromagnetische Strahlung abzugeben.
-
Energieaufnahme und -abgabe: Durch die Wechselwirkung mit den auftreffenden Elektronen nehmen die Atome Energie auf und die Hüllenelektronen werden auf höhere Energieniveaus angeregt. Beim Zurückfallen auf ein niedrigeres Energieniveau geben sie die Energiedifferenz in Form eines Lichtquants (Photons) ab.
-
Frequenz und Wellenlänge: Die Frequenz (und damit die Farbe bzw. Wellenlänge) der emittierten Photonen entspricht genau der Energiedifferenz der beiden beteiligten Energieniveaus.
-
Sichtbarer Bereich: Aus der Vielzahl aller möglichen Elektronenübergänge im Wasserstoffatom erzeugen nur vier Übergänge Strahlung im sichtbaren Bereich. Diese vier sichtbaren Linien gehören zur sogenannten Balmer-Serie.
Damit überhaupt Strahlung im sichtbaren Bereich entsteht, müssen die anregenden Elektronen mindestens die Energie besitzen, die dem energieärmsten (langwelligsten) sichtbaren Photon entspricht.
Laut der gegebenen Tabelle besitzt die -Linie die größte Wellenlänge mit
Die Energie dieses Photons beträgt:
Durch Einsetzen ergibt sich die Energie:
Die kinetische Energie der Elektronen muss also mindestens betragen, um sichtbare Strahlung zu erzeugen.
Mit Hilfe der in der Aufgabenstellung gegebenen Gleichung können die Energieniveaus berechnet werden:
|
Quantenzahl |
|
|
|
|
|
|---|---|---|---|---|---|
|
Energie |
|
|
|
|
|
Damit kann das entsprechende Energieniveauschema gezeichnet werden:
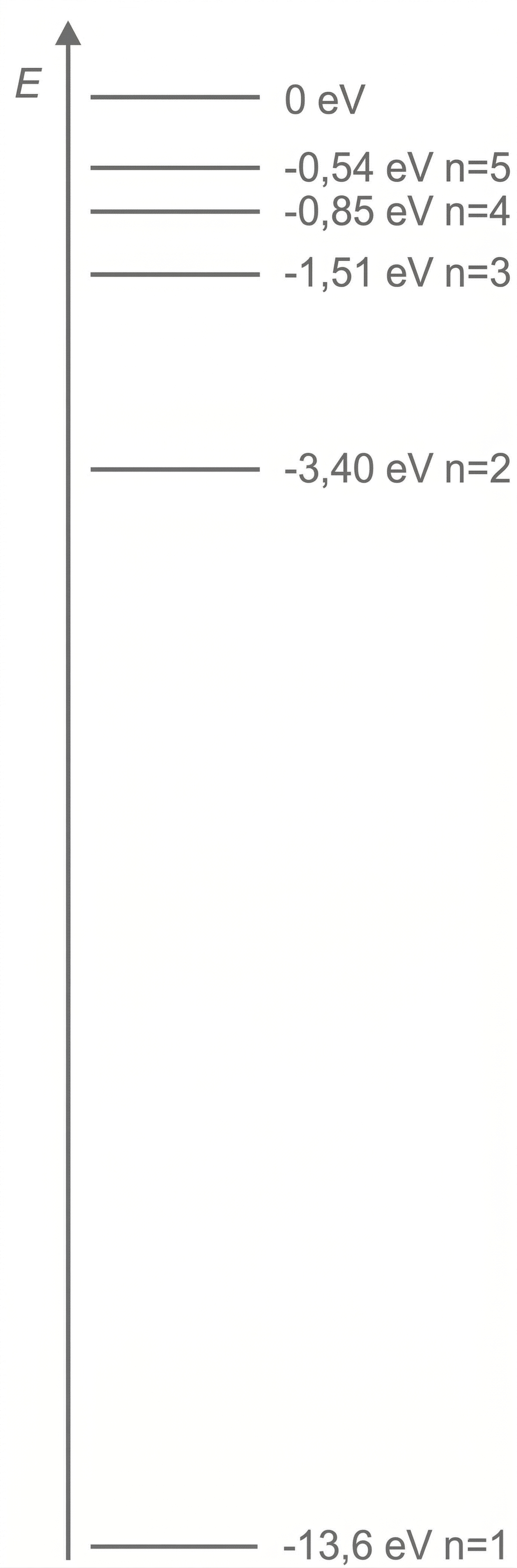

Um ein Wasserstoffatom aus dem Grundzustand () anzuregen, muss das Atom mindestens auf das nächsthöhere Energieniveau (
) gehoben werden. Die Mindestenergie zur Anregung aus dem Grundzustand entspricht der Differenz dieser beiden Niveaus:
Die eintreffenden Elektronen besitzen jedoch nur eine kinetische Energie von Da diese Energie kleiner ist als die geforderten
reicht sie nicht aus, um die Atome aus dem Grundzustand anzuregen.
Die maximale Energie, die vom ersten angeregten Zustand () aus aufgewendet werden muss, ist die Ionisationsenergie (Übergang von
nach
). Diese Ionisationsenergie entspricht der Differenz dieser beiden Energieniveaus:
Da die eintreffenden Elektronen mit deutlich mehr Energie besitzen als die für die Ionisation benötigten
können sie diese Energie mühelos aufbringen. Folglich können die Wasserstoffatome im ersten angeregten Zustand auch in jeden anderen höheren Zustand angeregt werden.
-
Einige Elektronen passieren das Gas, ohne Energie abzugeben. Sie behalten ihre ursprüngliche kinetische Energie.
-
Diese Elektronen haben ein Wasserstoffatom vom Zustand
in den Zustand
angeregt. Die dafür abgegebene Energie beträgt:
Folglich besitzt das Elektron danach eine Energie von
-
Diese Elektronen haben ein Wasserstoffatom vom Zustand
in den Zustand
angeregt. Die dafür abgegebene Energie beträgt:
Folglich besitzt das Elektron danach eine Energie von