Struktur und Eigenschaft
Wenn du dich ausruhen willst, dann wirst du höchstwahrscheinlich auf eine angenehme Matratze zurückgreifen und nicht auf einen Haufen Ziegelsteine. Der Unterschied scheint zunächst trivial, ist aber zentral für dieses Skript: Die Ziegelsteine sind „hart“ und durch deinen Körper nicht deformierbar, ganz im Gegensatz zur Matratze. Dieser Unterschied liegt in den Eigenschaften der beiden Objekte begründet und diese lassen sich auf die Baueinheiten und deren Charakteristika zurückführen. Wir werden uns in diesem Skript mit den Eigenschaften von Polymeren beschäftigen. Diese lassen sich aus der Struktur des Polymers und den Wechselwirkungen innerhalb von Polymeren ableiten. Im Rahmen dieses Skripts werden wir drei zentrale Gruppen von Kunststoffen kennen lernen: Elastomere, Duroplaste und Thermoplaste. Wir werden uns die molekulare Struktur dieser Kunststoffe anschauen und die spezifischen Eigenschaften auf dieser Basis verstehen lernen. Auf dieser Grundlage können wir dann den Einsatz verschiedener Kunststoffe als Werkstoffe verstehen und die Verfahren bewerten, die für das Recycling angewendet werden.
Struktur
Anmerkung:
Ein zentraler Begriff ist hier die Struktur. Bevor wir dazu übergehen, die verschiedenen Kunststofftypen kennen zu lernen und die Struktur-Eigenschafts-Beziehungen zu verstehen, wollen wir kurz einen Blick auf den Begriff der Struktur werfen. Dieser wird vielleicht nicht so eingängig in der Schule behandelt, deshalb darfst du dieses Kapitel als Blick über den Tellerrand ansehen mit dem Ziel, dass du dir etwas unter dem Begriff der Struktur vorstellen kannst.
Am Anfang dieses Skripts steht ein zentraler Begriff, den wir im Zusammenhang mit Materialien verwenden: die Struktur-Eigenschafts-Beziehungen. Prinzipiell können wir diesem Begriff die Information entnehmen, dass es eine Beziehung oder auch einen Zusammenhang zwischen der Struktur und den Eigenschaften eines Stoffes gibt. Im Speziellen wollen wir uns hier um die Feststoffe kümmern, da die Kunststoffe hierzu zählen. Das scheint banal zu sein, ist es aber nicht, wenn wir weiterfragen. Über welche Art von Strukturen reden wir hier? Was sind diese Strukturen genau?
Im Speziellen reden wir hier von der chemischen Struktur von Feststoffen. Diese beschreibt den Aufbau verschiedener Stoffe auf molekularer Ebene. Wir wollen hier mit einem Beispiel einsteigen. Von Diamanten hast du sicher schon etwas gehört oder du hattest schon das Glück, welche zu sehen. Bleistifte verwendest du möglicherweise jeden Tag und nur von den sogenannten „Buckyballs“ hast du möglicherweise noch nicht gehört. Bevor wir aufklären, was sich hinter diesen verbirgt, wollen wir uns anschauen, aus welchen Elementen diese drei Stoffe aufgebaut sind: Kohlenstoff. Das scheint zunächst verwirrend, ist aber die Realität. Es handelt sich hierbei um drei Modifikationen von Kohlenstoff, die sich alle in ihrer Struktur unterscheiden.

Diamant weist ein ausgeprägtes Kohlenstoffgerüst auf, in welchem jedes C-Atom mit vier weiteren verknüpft ist. Die „Buckyballs“ sind auch unter dem Namen Fullerene bekannt und sehen aus wie Fußbälle. Im Speziellen verdankt das Molekül seinen Namen dem US-amerikanischen Architekten Richard Buckminster Fuller und dessen geodätischen Kuppeln. Graphit finden wir beispielsweise in unseren Bleistiften und ist aus planare Kohlenstoffgittern aufgebaut, die übereinander geschichtet sind.
Nun aber zurück zum Begriff der chemischen Struktur. Diese beschreibt uns die räumliche Anordnung von molekularen Bausteinen. In diesem Fall haben wir unterschiedliche Strukturen und erhalten bei gleichen elementaren Bestandteilen unterschiedliche Stoffe. Das bedeutet, dass wir uns im Fall der Polymere insbesondere für den räumlichen Aufbau interessieren, also wie die einzelnen Monomere miteinander vernetzt sind. Anhand dieses räumlichen Aufbaus können wir dann im nächsten Schritt auch die Eigenschaften der Kunststoffe s verstehen.
Strukturen und Eigenschaften
Wir haben gerade am Beispiel des Kohlenstoffs gesehen, dass bereits mit einem einzigen Element verschiedene Strukturen realisiert werden können. Im nächsten Schritt wollen wir uns fragen, wie die Begriffe der Struktur und der Eigenschaft zusammenpassen. Die Eigenschaft eines Körpers könnte sich beispielsweise auf seine Stabilität beziehen. Aus dem Alltag weißt du, dass Graphit in Form von Bleistiften zum Schreiben oder Zeichnen verwendet werden kann. Diamant findet hingegen keine Anwendung als Schreibwerkzeug, sondern beispielsweise als sehr widerstandsfähiges Schneidewerkzeug. Dieser Unterschied liegt einzig und allein in der Anordnung der Kohlenstoffatome in den beiden Stoffen, der Struktur, begründet. Die Anordnung der Bausteine und der Aufbau von Festkörpern bestimmt deren Eigenschaften.

Diese Graphik soll das bisher Erarbeitete zusammenfassen. Bedenke: Es kommt auch immer darauf an wie einzelne Atome oder Bausteine zusammengesetzt werden, sollten mehrere Möglichkeiten bestehen. Das Beispiel des Kohlenstoffs verdeutlicht, wie „extrem“ sich diese Tatsache auswirkt. Nun können wir dazu übergehen, die Struktur-Eigenschafts-Beziehungen von Polymeren kennen zu lernen.
Die Glasübergangstemperatur
Wir wollen nun einen Blick auf eine der wichtigsten Kenngrößen von Kunststoffen werfen, die Glasübergangstemperatur. Dazu ziehen wir die allgemeine Struktur von Polymeren heran. Diese sind teilkristalline Stoffe. Sie weisen sowohl kristalline, als auch amorphe Bereiche auf.
Wenn ein Stoff kristallin ist, dann besitzt er eine Fernordnung, das bedeutet, dass es eine gewisse Anordnung der Bausteine gibt, die sich so kontinuierlich durch den gesamten Festkörper zieht. Das Gegenteil sind amorphe Stoffe, welche im Bezug auf die Anordnung der Atome ein unregelmäßiges Muster aufweisen. Das wird dann auch Nahordnung genannt. Teilkristalline Stoff besitzen Bereiche, in welchen die Atome regelmäßig angeordnet sind, also solche, die kristallin (hier mit türkisen Atomen) sind und auch solche, die amorph sind (hier orange).
Die Glasübergangstemperatur hat nun etwas mit diesen amorphen und kristallinen Bereichen zu tun. Wenn Kristalle schmelzen, dann verläuft dieser Prozess bei konstanter Temperatur. Die ganze Wärmeenergie, die wir zuführen, wird dafür aufgewendet das Kristallgitter, also die Struktur des Kristalls, zu zerstören. Bei amorphen Festkörpern ist dies nicht der Fall. Wenn wir diese erhitzen, dann steigt die Temperatur an, ohne dass Energie für die Zerstörung des Kristallgitters verloren gehen würde.
Fassen wir nochmal kurz zusammen:
- Amorphe Festkörper erwärmen sich bei der Zufuhr von Wärmeenergie, ohne dass diese für einen Schmelzvorgang verloren gehen würde.
- Kristalline Körper schmelzen bei einer bestimmten Temperatur. Hier wird die gesamte Wärmeenergie darauf verwendet das Kristallgitter zu zerstören.
Da Kunststoffe teilkristallin sind, besitzen sie quasi beide Eigenschaften und je nach Anteil kristalliner oder amorpher Bereiche dominiert eine der beiden. Unterhalb der Glasübergangstemperatur sind Kunststoffe spröde und brüchig, darüber elastisch und verformbar. Je nachdem, wo diese Temperatur liegt, bekommen wir unterschiedliche Eigenschaften der Kunststoffe bei Raumtemperatur. Beispielsweise haben Elastomere, welche wir im nächsten Abschnitt besprechen, eine Glasübergangstemperatur, die deutlich geringer ist als die normale Raumtemperatur. Dadurch sind dies hochflexible Materialien.
Anmerkung:
Wenn du dich fragst, woher man weis, dass manche Bereiche von Polymeren kristallin sind und manche amorph, dann hat das mit Röntgenstrahlung zu tun. Stell dir vor, du schießt diese Strahlung, deren Eigenschaften du haargenau kennst, auf so ein Polymer. Die Röntgenstrahlung, die eine elektromagnetische Welle darstellt, wird an diesem Polymer gebeugt. Das Gute ist, dass diese Beugungsprozesse eng an die Struktur des Materials gekoppelt sind. Das heißt, dass man sich die gebeugte Strahlung anschaut und aufgrund deren Eigenschaften feststellen kann, wie das Polymer aussieht. Diese Methode ist sehr effektiv, wenn es um die Strukturaufklärung von Festkörpern geht, also wenn man wissen will, wie diese aufgebaut sind.
Polymere und ihre physikalischen Eigenschaften
Polymere lassen sich anhand ihrer physikalischen Eigenschaften in drei Gruppen einteilen: Elastomere, Duroplaste und Thermoplaste. Hierbei spielen Eigenschaften wie die Verformbarkeit, die Härte, die Dehnbarkeit und der Einfluss von Wärme eine zentrale Rolle. Diese Eigenschaften bestimmten das Einsatzgebiet als Werkstoff. Wir werfen nun einen Blick auf die einzelnen Gruppen und schauen uns insbesondere die Strukturen und die damit verbundenen Eigenschaften an.
Elastomere
Eines der bekanntesten Beispiele für Elastomere ist Naturkautschuk. Das daraus hergestellte Material Gummi kennst du aus dem Alltag. Eine Eigenschaft dieses Stoffes ist seine hohe Dehnbarkeit.
Wir wollen nun einen Blick auf die Struktur von Elastomeren im Allgemeinen werfen:

Elastomere sind weitmaschige Makromoleküle, die dichte „Knäuel“ ausbilden. Bei Raumtemperatur sind diese Moleküle elastisch und durch äußere Kräfte verformbar. Wirkt eine solche Kraft auf ein Elastomer, indem wir bspw. daran ziehen, dann wird sich dieses bezüglich dieser Kraft verformen.
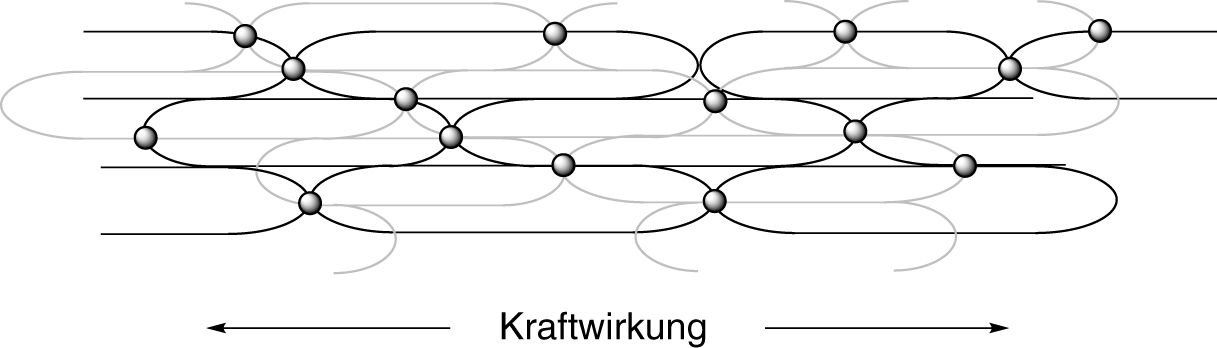
Die einzelnen Molekülketten können aneinander vorbei gleiten. Sobald die äußere Kraft verschwindet, wird sich das Elastomer wieder in seinen ursprünglichen Zustand zurückbegeben. Dieses Verhalten hat eine interessante Grundlage. Wenn wir das Elastomer ohne äußere Krafteinwirkung betrachten, dann hat es auf molekularer Ebene genau die Form, in der es sich „am wohlsten“ fühlt: Die Struktur ist ungeordnet und verknäuelt. Dehnen wir das Elastomer durch eine äußere Kraft, dann ändern wir diese Struktur und sozusagen das „Wohlempfinden“ des Kunststoffs. Die neue Situation war nur durch das Aufwenden einer Kraft möglich, sobald diese nicht mehr vorhanden ist, kehrt das Molekül in seine ursprüngliche Form zurück.
Anmerkung:
Elastomere liegen in ungeordneten Strukturen vor, was bedeutet, dass die Entropie hier sehr groß ist (bedenke Entropie Unordnung). Ändern wir diese Struktur, dann ändern wir die Entropie des Systems.
Wichtig ist, dass Elastomere ihre Eigenschaften unter der Glasübergangstemperatur verlieren. Gummi wird hart und spröde, wenn die Temperatur stark abnimmt. Bei zu hohen Temperaturen wird die Molekülstruktur geschädigt und das Material zersetzt sich. Ein Beispiel für ein Elastomer ist Polyurethan (PE), welches wir im Rahmen der Polyaddition (vgl. ChemieLV - Skript Polymersynthese III: Polyaddition) kennen lernen.
Duroplaste
An nächster Stelle stehen die Duroplaste, die sich in ihren Eigenschaften insbesondere durch hohe Stabilität, Härte und Inelastizität auszeichnen. Duroplaste sind dreidimensional vernetzte Makromoleküle, welche durch Atombindungen (kovalente Bindungen) zusammengehalten werden. Das macht sie auch sehr stabil.
Sind Duroplaste einmal ausgehärtet, dann werden sie durch hohe Temperaturen nicht zum Schmelzen gebracht, sondern zersetzen sich. Wenn wir die Temperatur erhöhen, dann fangen die einzelnen Atome und Moleküle an zu schwingen. Dadurch, dass diese hier aber fest über kovalente Bindungen in einem dreidimensionalen Gitter gebunden sind, kann es nicht zur Verschiebung der Ketten gegeneinander kommen. Stattdessen brechen die Bindungen ab einer gewissen Temperatur, also wenn die Atome einfach zu stark schwingen. Zusammengefasst bedeutet das, dass Duroplaste einerseits über gewisse Temperaturbereiche stabil sind, andererseits ab einer gewissen Grenztemperatur aber zerstört werden.
Ganz ähnlich verhält es sich mit der Verformbarkeit auf Grundlage von Krafteinwirkungen. Wirkt eine Kraft auf einen Duroplasten, dann wird sich dieser nicht verformen: Die Moleküle sind in einer stabilen, unflexiblen Struktur gebunden. Um einen Duroplasten durch äußere Krafteinwirkung zu verformen, müssten wir die Bindungskräfte überwinden. Dies führt zu einer hohen Stabilität.
Duroplaste zeichnen sich durch einige Eigenschaften aus, die ihnen ein weites Anwendungsfeld bescheren. Wichtig sind hierbei insbesondere eine hohe Formbeständigkeit gegenüber Wärme, wie wir gerade gesehen haben sowie ein allgemein resistenteres Verhalten gegenüber hohen Temperaturen. In Verbindung mit ihrer Stabilitüt finden diese Kunststoffe bspw. im Fahrzeugbau oder der Elektroindustrie große Anwendung. Ein Beispiel für einen Duroplast ist bspw. ein Polyester (PES).
Thermoplaste
Der dritte Kunststofftyp wird Thermoplast genannt. Das Wort sagt uns bereits, dass diese irgendetwas mit Temperatur (gr. thermos = warm) zu tun haben. Thermoplaste bestehen aus langkettigen linearen oder wenig verzweigten Molekülen, die gut gegeneinander verschoben werden können. Bei erhöhten Temperaturen werden diese weich und formbar.
Beim Erhitzen von Thermoplasten geraten die kettenförmigen Moleküle in Bewegung und können gegeneinander verrutschen: Es findet ein Schmelzvorgang statt. Beim Erkalten bleiben diese Moleküle dann in ihrer neuen Form erhalten. Werden zu hohe Temperaturen erreicht, dann zersetzen sich die Makromoleküle selbst, die kovalenten Bindungen werden zerstört. Dieser Prozess wird als Pyrolyse bezeichnet. Hier wirken insbesondere van-der-Waals Kräfte und Dipol-Dipol Kräfte. Dies macht erst die thermische Bewegung möglich.



