Aminosäuren
Definition
Aminosäuren sind im Allgemeinen Carbonsäuren (R-COOH), die eine Aminogruppe () im Molekül enthalten. Sie spielen eine zentrale Rolle beim Aufbau von Proteinen und der Mensch benötigt einige davon, um zu überleben. Nahrungsmittel mit hohen Anteilen an Aminosäuren sind bspw. Spargel, Lachs und Eier.



Wir wollen in diesem Skript die Aminosäuren sowie deren Eigenschafften kennen lernen, damit wir sie im ChemieLV-Skript Peptide und Proteine zu Makromolekülen verknüpfen können.
Wir beginnen ganz allgemein mit dem Begriff der Aminosäure und einer geeigneten Darstellungsform der Moleküle: der Fischer-Projektion. Anschließend gehen wir auf die proteinogenen Aminosäuren und die Benennung der Moleküle ein. Daraufhin besprechen wir ausführlich die Säure-Base-Chemie von Aminosäuren. Nach eine kurzen Wiederholung wichtiger Konzepte der Säure-Base-Theorie nach Broensted diskutieren wir die Begriffe des Zwitterions und des isoelektrischen Punkts. Abschließend betrachten wir die experimentelle Trennung von Aminosäuren mittels Dünnschichtchromatographie und Elektrophorese.
Aminosäuren
Darstellung von Aminosäuren: Die Fischer-Projektion
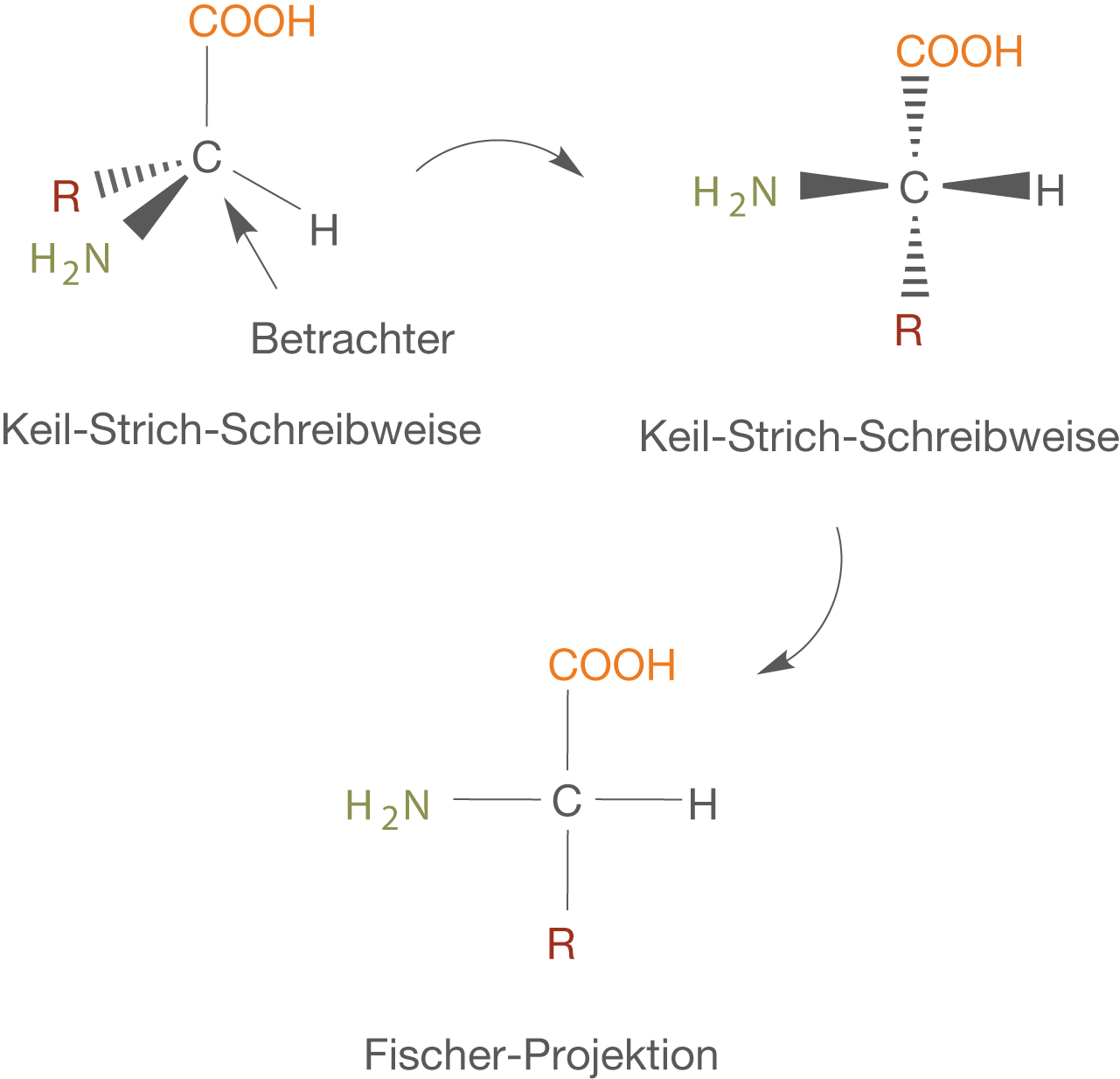
Die Darstellungsprobleme von Aminosäuren gehen auf die dreidimensionale Struktur organischer Moleküle zurück. Drei Dimensionen sind in aller Regel nicht einfach zu zeichnen, wenn man bedenkt, dass die Zeichenebene (das Blatt Papier vor dir bspw.) nur zweidimensional ist. Eine Möglichkeit dieses Problem zu lösen ist die Keil-Strich-Schreibweise (vgl. Abb. 2). Diese erweist sich insbesondere bei kleineren Molekülen als sehr effektiv, bei größeren kann es jedoch schnell kompliziert werden. Abhilfe schafft die von Emil Fischer (Nobelpreis für Chemie, 1902) eingeführte Fischer-Projektion. Wir wollen uns an einem konkreten Beispiel den Nutzen und die Darstellung dieser Projektion anschauen (vgl. Abb. 2).
Gehe beim Überführen der Keil-Strich-Schreibweise in die Fischer-Projektion folgendermaßen vor:
- Schaue von schräg unten auf das C-Atom, sodass die Aminogruppe (
) links und das H-Atom rechts von dir steht.
- Die zweite Ansicht ergibt sich direkt aus Schritt 1: Die Aminogruppe und das H-Atom zeigen aus der Zeichenebene heraus, während die Carboxygruppe (R-COOH) und der Rest (R) hinter die Zeichenebene zeigen. Die Stellung der Substituenten in diesem Schritt ist zentral, da wir nur auf diese Weise die Fischer-Projektion erhalten können.
- Wir „drücken“ das Molekül nun gedanklich „platt“. Damit liegen alle Bindungen in einer Ebene und wir erhalten die Fischer-Projektion.
Diese Darstellung werden wir nun im weiteren Verlauf dieses Skripts für die Darstellung der Aminosäuren verwenden. Ausführlichere Informationen zur Fischer-Projektion, die über das hier benötigte Wissen hinausgehen, findest du im ChemieLV-Skript Monosaccharide.
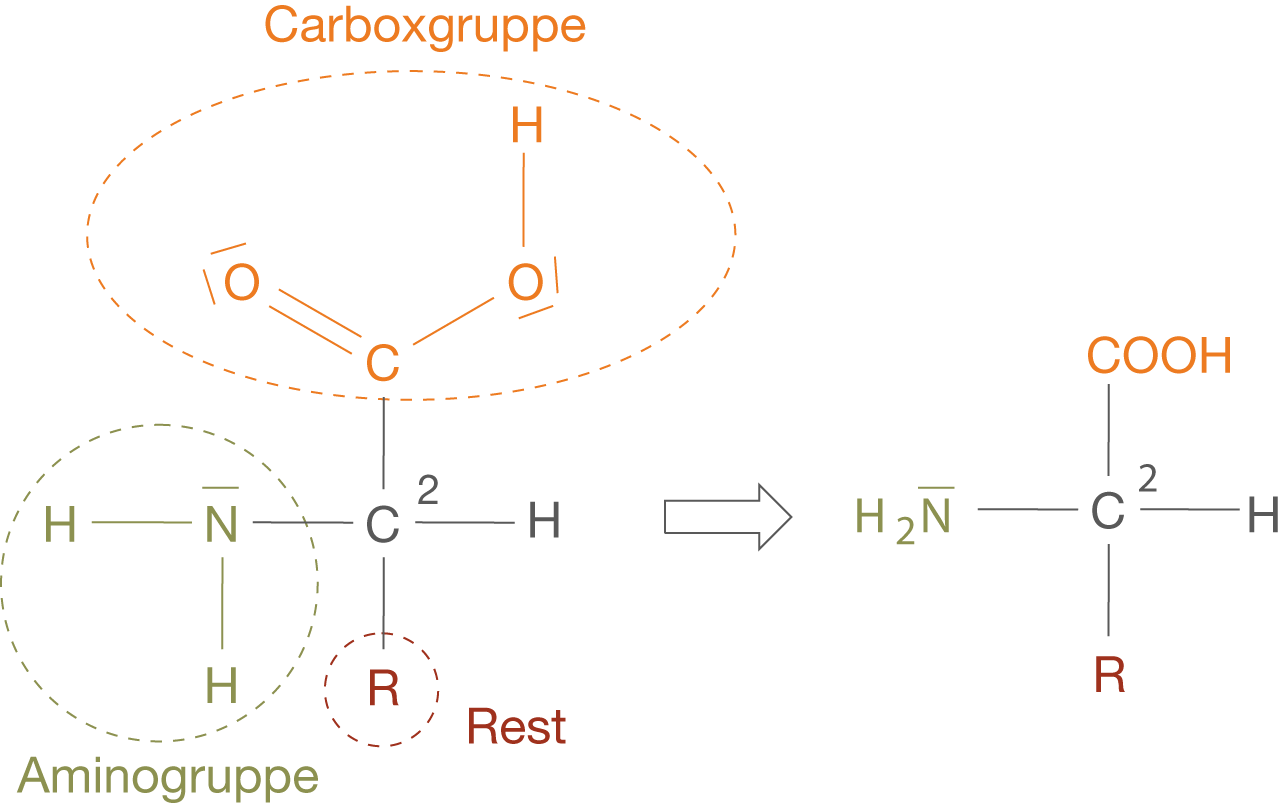
Aminosäuren zeichnen sich dadurch aus, dass sie mindestens zwei funktionelle Gruppen aufweisen: eine Carboxygruppe und eine Aminogruppe (vgl. Abb. 3). Eine Unterscheidung verschiedener Aminosäuren ist auf Grundlage des Rests (R) möglich.
Wir werden im Verlauf dieses Skripts vor allem die rechte Darstellung in Abbildung 3 verwenden, da wir nahezu alle wichtigen chemischen Eigenschaften daran erklären können. Die hier gewählte Stellung der Substituenten entspricht der, die auch bei den zwanzig häufigsten natürlich vorkommenden Aminosäuren zu finden ist. Dabei befindet sich die Aminogruppe (
Proteinogene Aminosäuren und Nomenklatur
In der Natur kommen einige hundert verschiedene Aminosäuren vor, doch nur zwanzig davon werden für den Aufbau von Proteinen verwendet (vgl. ChemieLV-Skript Peptide und Proteine). Wir wollen uns in diesem Skript auf eine Auswahl dieser proteinogenen Aminosäuren beschränken.
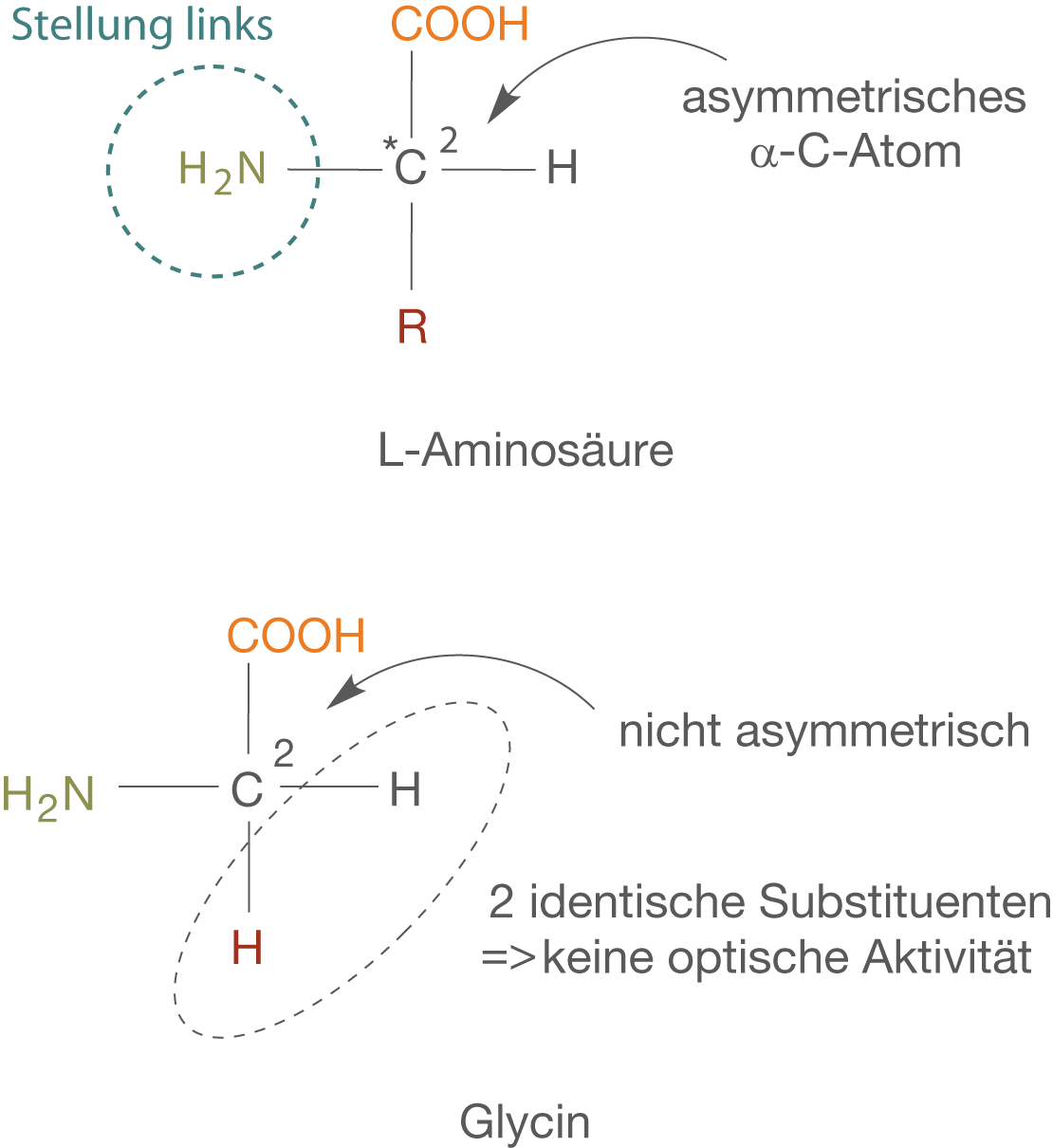
Auf Grundlage der Stellung der Amino-Gruppe (
Beachte: Glycin ist zwar die einfachste Aminosäure, hat aber kein asymmetrisches C-Atom und ist folglich nicht optisch aktiv.
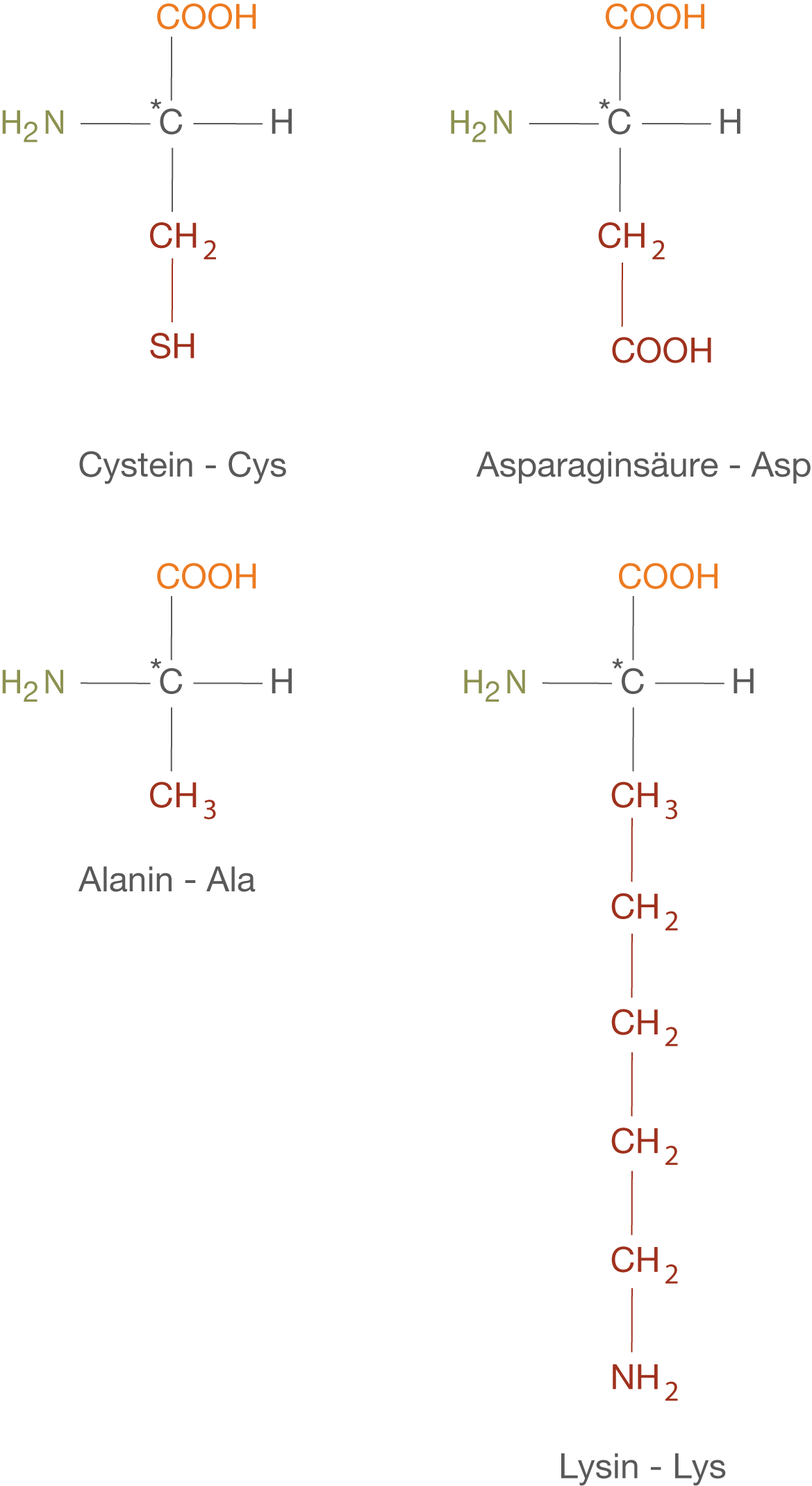
Die Benennung (Nomenklatur) von Aminosäuren ist vergleichbar mit der Benennung von Zuckern: Weil die systematische Benennung unhandliche Bezeichnungen ergeben würde, finden viele Trivialnamen Verwendung. Um die Benennung noch weiter zu vereinfachen, was insbesondere im Zusammenhang mit dem Aufbau von Proteinen wichtig wird, verwendet man einen Drei-Buchstaben-Code. Dieser umfasst die ersten drei Buchstaben des Trivialnamens der jeweiligen Aminosäure (vgl. Abb. 5).
In Abbildung 5 siehst du beispielhaft vier Aminosäuren aufgeführt. Die Carboxygruppe ist wie bisher orange eingefärbt und die Aminogruppe blau. Die jeweiligen Reste sind rot hervorgehoben. Beachte, dass wir hier zusätzliche funktionelle Gruppen vorliegen haben:
- Lysin mit einer endständigen Aminogruppe (
)
- Cystein einer endständigen Thiolgruppe (
)
- Asparaginsäure mit einer endständigen Carboxygruppe (
)
Diese haben eine entscheidenden Einfluss auf die Chemie der Aminosäuren, wie wir im Abschnitt Der isoelektrische Punkt sehen werden.
Die Säure-Base-Chemie von Aminosäuren
Aminosäuren weisen mit der Carboxygruppe eine Säuregruppe (Protonendonator) auf, die relativ leicht deprotoniert (Abgabe des H-Atoms) werden kann. Gleichzeitig befindet sich jedoch im selben Molekül auch noch eine basische funktionelle Gruppe in Form der Aminogruppe, welchen ihren basischen Charakter (Protonenakzeptor) durch das freie Elektronenpaar am Stickstoff erhält. Da die wässrige Säure-Base-Chemie der Aminosäuren sehr wichtig für ihre Eigenschaften ist, wollen wir an dieser Stelle mit einer kurzen Wiederholung der wichtigsten Konzepte beginnen und anschließend damit die Eigenschaften der Aminosäuren erklären. Eine ausführliche Darstellung der Säure-Base-Chemie in wässrigen Lösungen findest du im ChemieLV-Themengebiet Säure-Base-Gleichgewichte.
Wiederholung: Protolysegleichgewicht und  -Werte
-Werte
Wir nehmen beispielhaft die Carboxygruppe
Wir erhalten hier folgende Säure-Base-Paare:
Bedenke: Die Konzentration des Lösungsmittels Wasser wird
Durch die Lage des Protolysegleichgewichts können wir eine Aussage über die Säurestärke treffen:
: hoher Anteil der deprotonierten Form im Gleichgewicht auf der Produktseite
je größer
desto stärker die Säure.
: geringer Anteil der deprotonierten Form im Gleichgewicht auf der Produktseite
je kleiner
desto schwächer die Säure.
Gewöhnlich wird jedoch nicht die Säurekonstante
Achtung: Der
- Je kleiner der
-Wert, desto stärker die Säure und desto schwächer die korrespondierende Base. Achtung: Der
-Wert kann im Fall starker Säuren negativ sein (
).
- Je größer der
-Wert, desto schwächer die Säure und desto stärker die korrespondierende Base.
Im Fall der Aminosäuren haben wir wie bereits angemerkt mindestens zwei funktionelle Gruppen, die für die Säure-Base-Chemie relevant sind: die Carboxygruppe und die Aminogruppe.
Von Carboxygruppen, Aminogruppen und Zwitterionen
Das Zwitterion
Wir wollen nun die eben wiederholten Konzepte verwenden, um Aussagen über die Säure- bzw. Basenstärke der Carboxy- bzw. der Aminogruppe zu treffen und anschließend die Folgen zu besprechen.
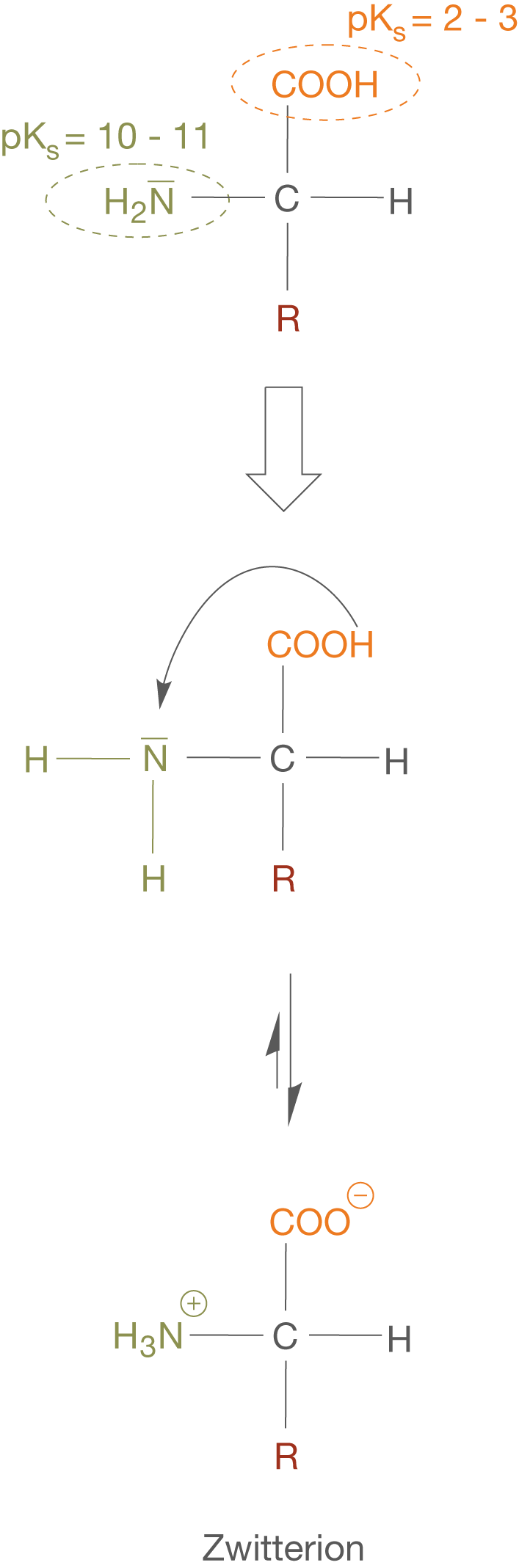
Um genau zu sein, handelt es sich bei Aminosäuren um amphotere Verbindungen, also solche die sowohl als Säure als auch als Base fungieren können. Schauen wir uns die -Werte der beiden funktionellen Gruppen an, dann fällt ein interessanter Aspekt auf, den du in Abbildung 6 nachvollziehen kannst.
Die Carboxygruppe ist mit einem -Wert von
zwar eher eine mäßig starke Säure, aber im Vergleich zur Aminogruppe (
) mit ihren Säureeigenschaften in jedem Fall dominant. Das Resultat ist ein Protolysegleichgewicht innerhalb der Aminosäure, wobei die Aminogruppe die Rolle der Base einnimmt. Hierbei entsteht ein so genanntes Zwitterion, das zwei gegensätzliche Ladungen trägt, die sich im Mittel wieder ausgleichen. Korrekt lautet die Bezeichnung des Zwitterions allgemein Ammoniumcarboxylat.
Auswirkungen auf Struktur und Eigenschaften
Im Falle des zwitterionischen Ammoniumcarboxylats handelt es sich um eine stark polare Verbindung, was direkt Auswirkungen auf die Eigenschaften von Aminosäuren hat.
- Aminosäuren bilden kristalline Feststoffe aus, die aufgrund der stark polaren Struktur besonders stabil sind.
- Die Stabilität der Kristallgitter von Aminosäuren führt dazu, das sie schlecht wasserlöslich sind und sich beim Erhitzen thermisch zersetzen und nicht schmelzen.
Der isoelektrische Punkt
Eine weitere wichtige Eigenschaft von Aminosäuren bezieht sich auf deren Zusammensetzung in wässrigen Lösungen und die pH-Abhängigkeit dieser Zusammensetzung.
Der pH-Wert ist für wässrige Lösungen über die Stoffmengenkonzentration der Oxoniumionen (
Achtung: Der pH-Wert wird über die Autoprotolyse des Wassers definiert; es macht demnach keinen Sinn pH-Werte für anderer Lösungsmittel als Wasser anzugeben. Des Weiteren hat der pH-Wert keine Einheit, was mit dem Logarithmus zusammenhängt: Wir können keinen Logarithmus aus Einheiten ziehen!
Es werden grob drei Bereiche für den pH-Wert unterschieden:
: saures Milieu
hohe Stoffmengenkonzentrationen der Oxoniumionen.
: neutrales Milieu
: alkalisches (basisches) Milieu
niedrige Stoffmengen-konzentrationen der Oxoniumionen.
Achtung: Oft werden pH-Bereich von 0 bis 14 angegeben. Das bedeutet nicht, dass der pH-Wert im Fall besonderes hoher Stoffmengenkonzentrationen von Oxoniumionen nicht auch kleiner als null (
Die Zusammensetzung von Aminosäuren in wässrigen Lösungen ist pH-abhängig. Das hängt mit den vorhandenen funktionellen Gruppen zusammen. Wir betrachten an dieser Stelle die einfachste Aminosäure in Form von Glycin mit
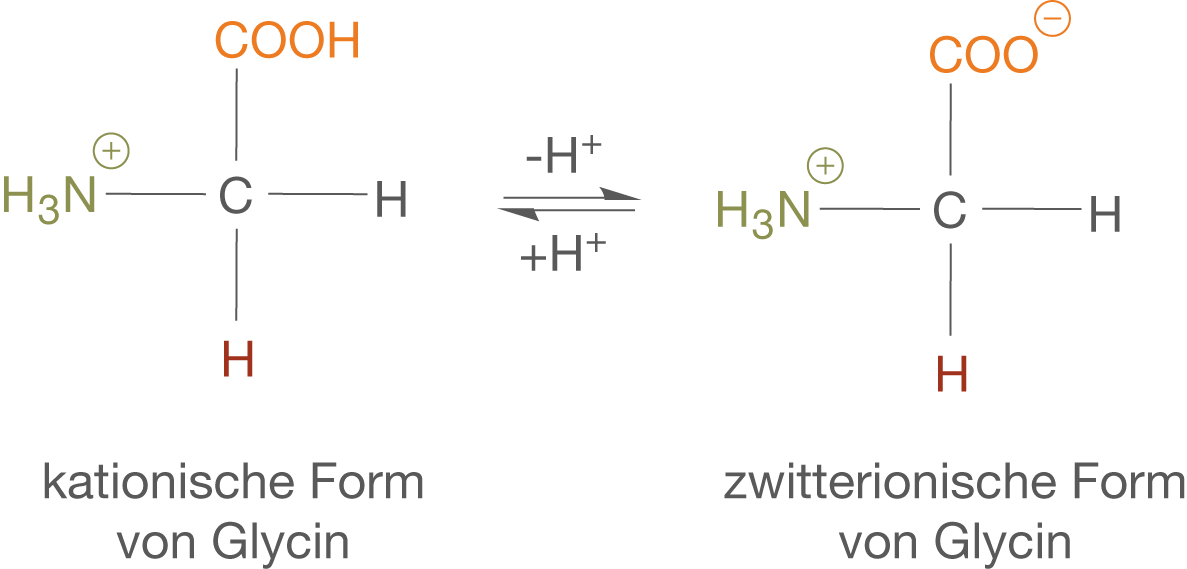
(a) stark saure Lösungen
Ist der pH-Wert kleiner als 1, dann liegen sehr viele
In stark sauren Lösungen liegt die Aminosäure folglich überwiegend als Kation vor, sie trägt also eine positive Ladung.
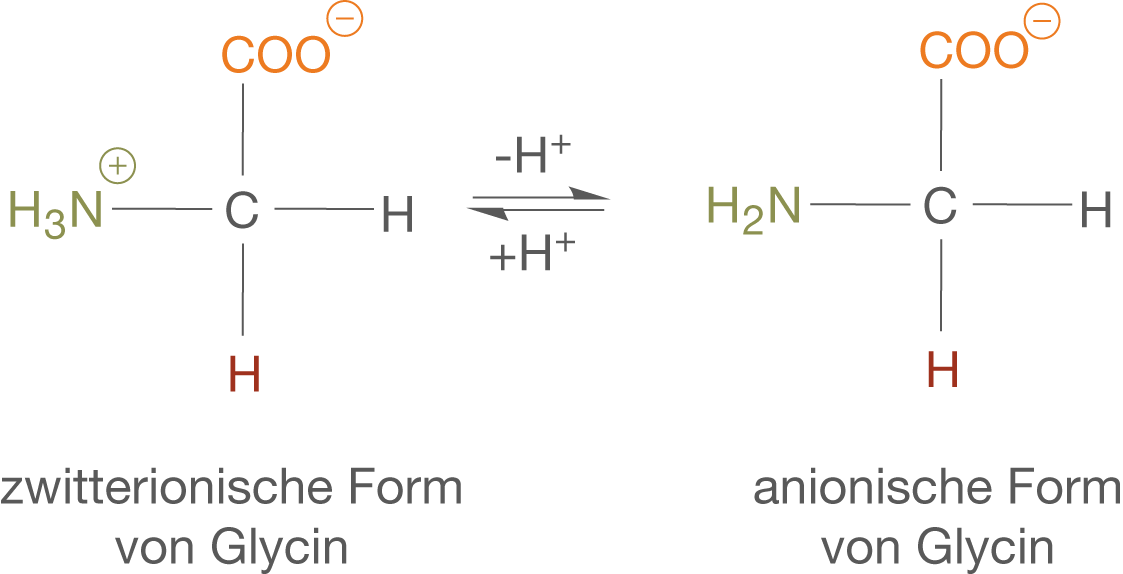
(b) stark alkalische Lösungen
In stark alkalischen Lösungen mit
In stark alkalischen Lösungen liegt die Aminosäure folglich als Anion vor; sie trägt eine negative Ladung.
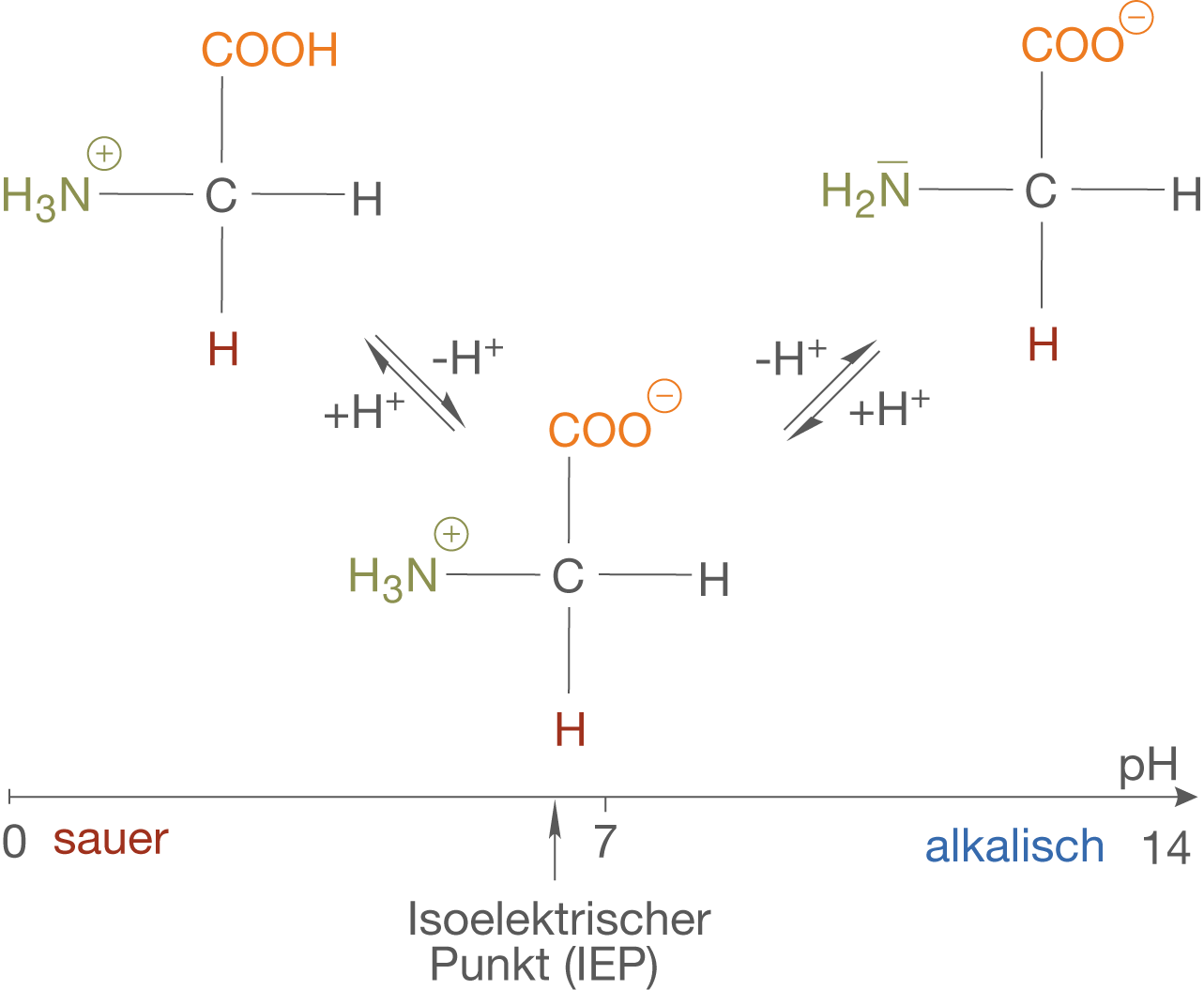
Eine Frage, die wir noch nicht beantwortet haben, bezieht sich auf die zwitterionische Form von Glycin und den zugehörigen pH-Wert. Wie wir bereits gesehen haben, handelt es sich bei dem Zwitterion um ein Molekül, das sowohl eine positive als auch eine negative Ladung trägt. Im Mittel gleichen sich beide Ladungen aus und das Molekül ist nach außen hin neutral. In wässrigen Lösungen bedeutet das, dass das Zwitterion nicht zur elektrischen Leitfähigkeit der Lösung beiträgt. Der pH-Wert, bei welchem überwiegend das Zwitterion in wässriger Lösung vorliegt, wird isoelektrischer Punkt (kurz: IEP) genannt (vgl. Abb. 9).
Die Lage des isoelektrischen Punkts ist in jedem Fall auch von weiteren sauren oder basischen funktionellen Gruppen abhängig, die als Rest der Aminosäure auftreten können. Je mehr saure Gruppen vorhanden sind, desto niedriger liegt der IEP und je mehr basische Gruppen vorhanden sind, desto höher fällt der IEP aus.
Vergleiche hierzu Abbildung 5. Lysin weist eine zusätzliche Aminogruppe auf, was ihren basischen Charakter deutlich erhöht. Im Vergleich dazu weist die Asparaginsäure eine zusätzliche Carboxygruppe auf, was ihren Säurecharakter insgesamt deutlich verstärkt. Durch Vergleich des isoelektrischen Punkts der beiden Verbindungen mit dem von Glycin können wir den Einfluss der neuen Substituenten erkennen:
Experimentelle Trennung von Aminosäuren
Die Dünnschichtchromatographie
Ein sehr wichtiges Verfahren, um Gemische von Aminosäuren effektiv zu trennen, ist die Dünnschichtchromatographie.
Grundlagen der Chromatographie
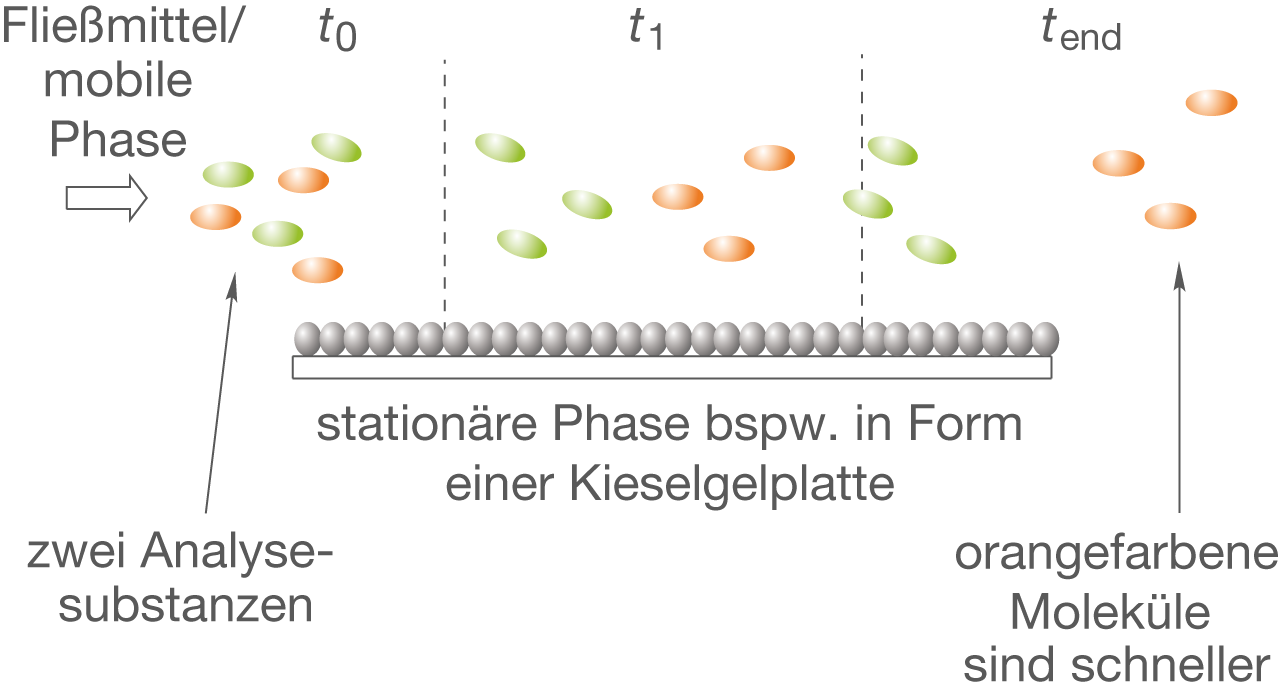
Die Chromatographie stellt ein physikalisch-chemisches Trennverfahren dar, bei welchem das Trennungsprinzip auf unterschiedlichen Verweilzeiten der Analysesubstanzen auf einer stationären Phase beruht. Diese Verweilzeiten kommen auf Grund unterschiedlicher Wechselwirkungen zwischen den Molekülen der Analysesubstanz und der stationären bzw. mobilen Phase zu Stande. In Abbildung 10 betrachten wir das Prinzip graphisch:
Du kannst dir das Trennprinzip so vorstellen, dass die grünen Moleküle stärker mit den Molekülen der stationären Phase wechselwirken, somit werden sie länger „festgehalten“ als die orangen. Folglich bekommst du eine effektive Trennung deines Gemischs über den Zeitraum bis
Experimentelle Durchführung
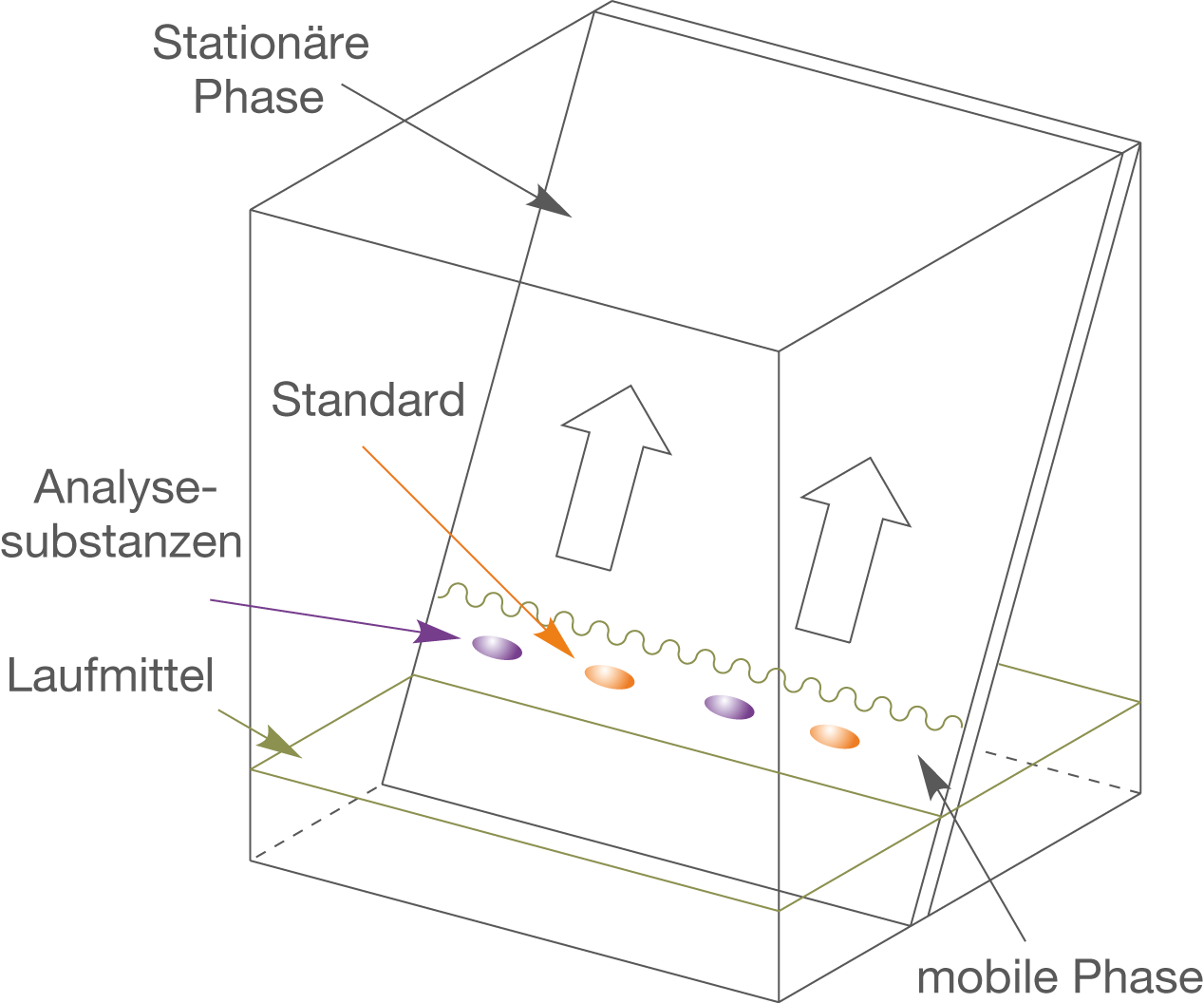
In Abbildung 11 siehst du den experimentellen Aufbau eines Dünnschichtchromatographen.
- Die Analysesubstanz und eine Vergleichssubstanz (Standard) werden auf der stationären Phase aufgebracht.
- Die stationäre Phase wird in ein geeignetes Fließmittel gestellt.
- Durch Kapillarkräfte wandert das Fließmittel an der stationären Phase nach oben.
- Die unterschiedlichen Wechselwirkungen der enthaltenen Aminosäuren führen zu einer zeitlichen Auftrennung des Gemischs.
- Die Trennleistung der Dünnschichtchromatographie hängt stark von der gewählten stationären und mobilen Phase ab, sowie von deren chemischer Zusammensetzung bzw. Aufbau.
Die Elektrophorese
Neben der Dünnschichtchromatographie existiert noch die Elektrophorese, die zur Trennung von Aminosäuregemischen herangezogen wird. Diese spielt insbesondere in der Biochemie eine wichtige Rolle.
Experimenteller Aufbau
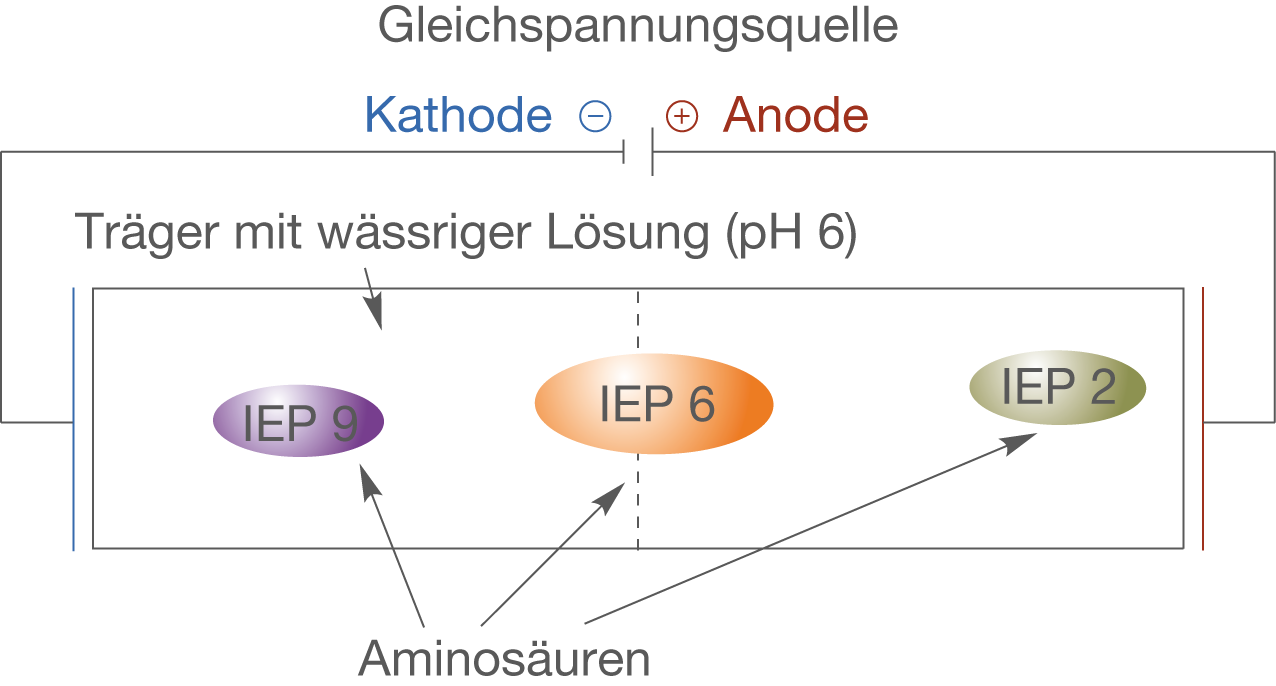
Das Prinzip der Elektrophorese beruht auf der pH-Wert-Abhängigkeit der Ladung von Aminosäuren (vgl. Abschnitt Der isoelektrische Punkt). Der experimentelle Aufbau gestaltet sich hierbei vom Prinzip her relativ einfach (vgl. Abb. 12):
Folgende Komponenten sind wichtig:
- Der Probenträger enthält eine wässrige Lösung, deren pH-Wert mit einem Puffer kontrolliert wird.
- Eine Gleichspannungsquelle ist an den Träger angeschlossen und baut dort ein elektrisches Feld auf.
- Die Analysesubstanz wird auf die Mitte des Trägers gegeben. In Abbildung 12 sind beispielhaft Aminosäuren mit unterschiedlichen
angegeben.
Ladungen im elektrischen Feld
Die Gleichspannung führt zu einem elektrischen Feld . In Abbildung 12 befindet sich die Anode (Pluspol) rechts und die Kathode (Minuspol) links. Wie wir im Abschnitt Der isoelektrische Punkt gesehen haben, weisen Aminosäuren je nach pH-Wert unterschiedliche Ladungen auf:
: Im sauren Milieu dominiert die kationische Form der Aminosäure.
: Am isoelektrischen Punkt dominiert das Zwitterion, das nach außen hin neutral ist.
: Im alkalischen Milieu dominiert die anionische Form der Aminosäure.
In einem elektrischen Feld wirkt eine Kraft auf ein geladenes Molekül, was bedeutet, dass das Molekül in Bewegung versetzt wird. Die kationische Form bewegt sich aufgrund ihrer positiven Ladung in Richtung der Anode und die anionische Form aufgrund ihrer negativen Ladung in Richtung der Kathode. Die Ladungen innerhalb des Zwitterions gleichen sich aus, sodass diese nach außen hin neutral sind und hier nicht durch das elektrische Feld beeinflusst werden. In Abbildung 12 sehen wir beispielhaft einen Träger mit einer Lösung mit pH 6. Die „blaue Aminosäure“ hat bei eine negative Ladung und wandert in Richtung der Anode, während die „violette Aminosäure“ bei
positiv geladen ist und zur Kathode wandert. Da die „orangenfarbene Aminosäure“ bei pH 6 als Zwitterion vorliegt, wandert sie gar nicht und wir erhalten eine Trennung unseres Aminosäuregemischs.
Zusammenfassung
- Die zweidimensionale Darstellung von Aminosäuren erfolgt in der Fischer-Projektion.
- Aminosäuren weisen charakteristisch eine Carboxygruppe und eine Aminogruppe auf, sowie einen organischen Rest, der die Unterscheidung ermöglicht.
- Die Stellung der Aminogruppe am C-2-Atom (
-C-Atom) bestimmt die Zugehörigkeit zur D- oder L-Reihe.
- Aminosäuren mit asymmetrischen C-Atomen sind optisch aktiv.
- Proteinogene Aminosäuren dienen dem Aufbau von Proteinen und gehören fast ausschließlich der L-Reihe an.
- Die Trivialnamen von Aminosäuren werden mittels des Drei-Buchstaben-Codes abgekürzt.
- Durch die Anwesenheit einer sauren Carboxygruppe und einer basischen Aminogruppe kommt es zur intramolekularen Protolyse: das nach außen neutrale Zwitterion entsteht.
- Die Ladung von Aminosäuren in wässrigen Lösungen ist vom pH-Wert abhängig: im sauren Milieu (
) dominiert die kationische Form, im alkalischen Milieu (
) die anionische.
- Der pH-Wert an welchem das Zwitterion dominiert, wird isoelektrischer Punkt (IEP) genannt.
- Der IEP hängt von den Säure-Base-Eigenschaften der Reste der Aminosäuren ab.
- Gemische von Aminosäuren können mittels Dünnschichtchromatographie effektiv getrennt werden.
- Die Elektrophorese nutzt die pH-Abhängigkeit der Ladung von Aminosäuren aus, um Aminosäuregemische effektiv zu trennen.