Vorschlag A1 — Das Bohr’sche Atommodell und Welleneigenschaften von Elektronen
Zum Ende des 19. Jahrhunderts wurden die Emissionsspektren von verschiedenen Gasen vermessen. Niels Bohr postulierte 1913 ein Modell zur Erklärung des Spektrums von Wasserstoff. Nach dem Bohr'schen Atommodell bewegt sich das Elektron im Wasserstoff nur auf Bahnen, deren Energien mit der folgenden Gleichung berechnet werden können:
Bestätige durch eine Einheitenrechnung, dass es sich bei der Größe in Gleichung
um eine Energie handelt, und zeige, dass eine Umrechnung in die Einheit
die Gleichung
ergibt.
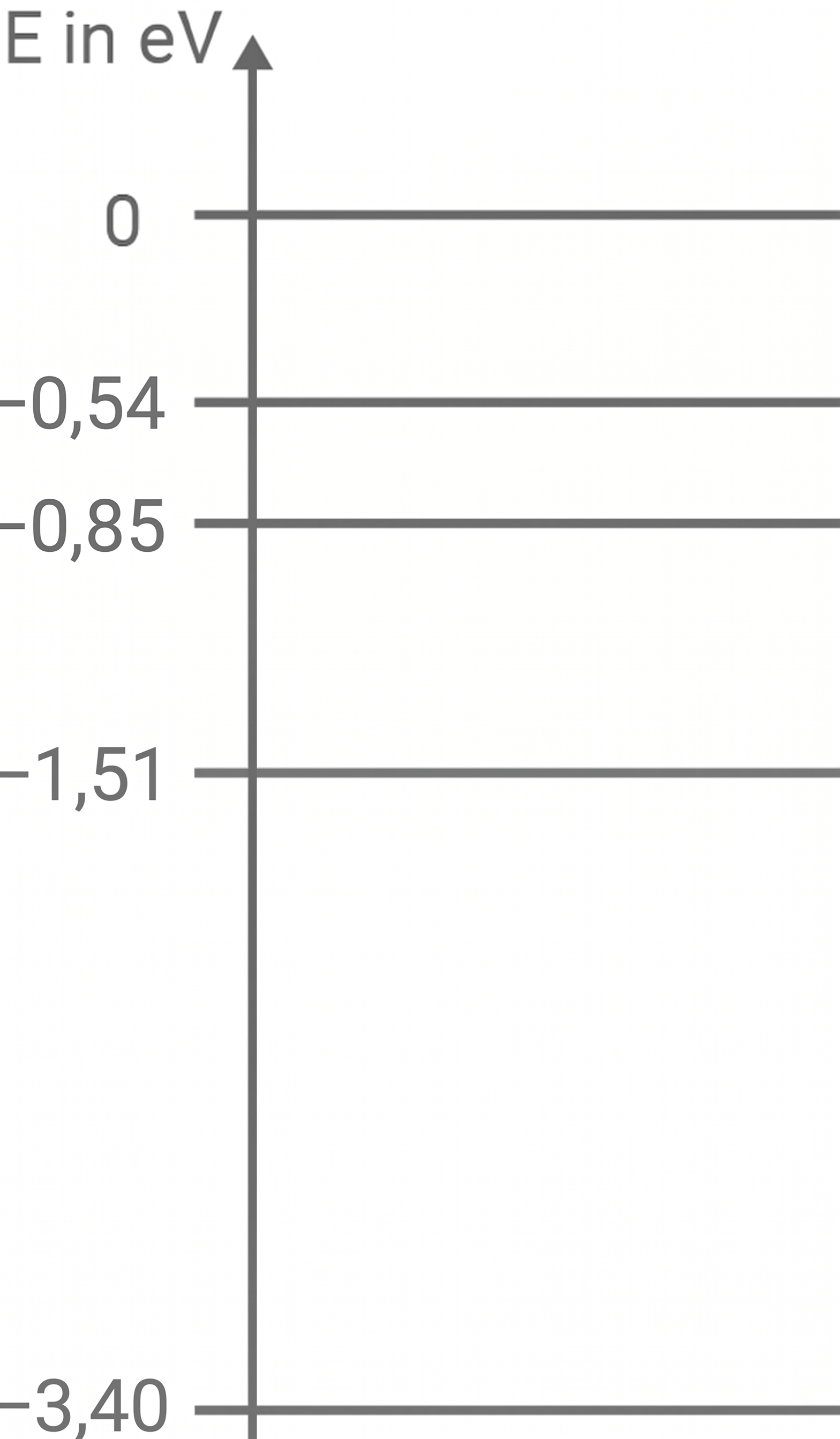
In Material 1 werden drei der niedrigsten fünf Energieniveaus von Wasserstoff in einem Ausschnitt eines Termschemas gezeigt.
Ordne durch geeignete Rechnungen jedem der drei eingezeichneten Energieniveaus die entsprechende Quantenzahl zu.
Zeichne im Ausschnitt von Material 1 das noch zwischen den Energieniveaus und
fehlende Energieniveau maßstabsgetreu ein.
Berechne die Wellenlängen der Strahlung, die bei den Übergängen von diesem Niveau auf die beiden tiefer liegenden Energieniveaus des Wasserstoffs emittiert wird.
Gib an, welcher dieser Übergänge Strahlung im sichtbaren Bereich erzeugt.
Erkläre im Rahmen des Bohr'schen Atommodells, dass das Wasserstoffspektrum aus einzelnen Linien besteht.
Im Bohr'schen Atommodell umläuft das Elektron den Kern auf einer Kreisbahn. Aus dem Bohr'schen Postulat zur Quantisierung des Bahndrehimpulses folgen für die Geschwindigkeiten
auf den Elektronenbahnen und deren Radien
die Bedingungen:
und
Berechne mit den Gleichungen und
die fehlenden Werte für den Bahnradius und die Bahngeschwindigkeit in Material 2.
Louis de Broglie postulierte für klassische Teilchen Welleneigenschaften. Wird das Elektron durch eine Materiewelle beschrieben, so muss der Umfang der Elektronenbahnen im Bohr'schen Atommodell ein ganzzahliges Vielfaches der De-Broglie-Wellenlänge sein.
Berechne für die in Material 2 vorgegebenen Quantenzahlen die entsprechende De-Broglie-Wellenlänge des Elektrons und untersuche, ob die Forderung erfüllt wird.
Leite aus der Bedingung die Quantisierung des Bahndrehimpulses
her.
Nenne einen klassischen und einen quantenmechanischen Aspekt des Bohr'schen Atommodells und nenne darüber hinaus zwei Grenzen des Bohr'schen Atommodells.
Ungefähr 35 Jahre nachdem de Broglie die Welleneigenschaften von Teilchen postuliert hatte, gelang es Claus Jönsson, durch Beugung eines Elektronenstrahls an einem Doppelspalt ein Interferenzmuster zu erzeugen. Eine stark vergrößerte Abbildung des Interferenzmusters findet sich in Material 3. Es kann davon ausgegangen werden, dass in dem beobachteten Bereich alle Streifen im gleichen Abstand von einem Mikrometer zueinander liegen. Der Abstand des Schirms zum Doppelspalt beträgt die Beschleunigungsspannung
der Abstand der beiden Spalte
Für die weitere Rechnung kann die Kleinwinkelnäherung verwendet werden. Relativistische Effekte sollen vernachlässigt werden.
Zeige, dass die De-Broglie-Wellenlänge der beschleunigten Elektronen beträgt und dass die Flugzeit vom Doppelspalt bis zum Schirm in der Größenordnung von wenigen Nanosekunden liegt.
Der Abstand von nur einem Mikrometer zwischen den Interferenzstreifen erfordert eine technisch aufwändige Beobachtung. Wesentlich einfacher wäre es, lägen die Streifen zumindest einen Zehntel Millimeter auseinander, was aber aus anderen Gründen nicht zu realisieren ist.
Berechne die theoretisch dafür benötigte Beschleunigungsspannung bei sonst gleichem Versuchsaufbau.
Über eine Versuchsdauer von werden in gleichen Zeitabständen insgesamt
Elektronen emittiert und tragen dazu bei, ein Interferenzmuster zu erzeugen. Jemand behauptet, zur Erzeugung des Musters müssten jeweils mindestens zwei Elektronen miteinander interferieren.
Beurteile diese Behauptung mithilfe einer geeigneten Rechnung, wie viele Elektronen sich bei einer Beschleunigungsspannung von gleichzeitig in der Versuchsapparatur mit einer Gesamtlänge von etwa einem halben Meter befinden.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Material 1: Maßstabsgetreuer Ausschnitt aus dem Termschema des Wasserstoffatoms
.png)
-dark.png)
Material 2: Tabelle mit Quantenzahl, Bahnradius, Bahngeschwindigkeit und De-Broglie-Wellenlänge
|
Quantenzahl |
|
|
|---|---|---|
|
Bahnradius |
|
|
|
Bahngeschwindigkeit |
|
|
|
De-Broglie-Wellenlänge |
Material 3: Interferenzmuster im Experiment von Jönsson


Quelle (abgerufen am 17.04.2026)
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Bestätigen durch Einheitenrechnung
Zeigen der Gleichung
In Gleichung können die Literaturwerte der Naturkonstanten eingesetzt werden:
Durch Umstellen der zuvor hergeleiteten Gleichung nach der Quantenzahl lassen sich die Niveaus aus dem Termschema berechnen:
Hier können nun die in Material 1 abgelesenen Energieniveaus eingesetzt werden:
-
Für
-
Für
-
Für
Einzeichnen des fehlenden Energieniveaus
Zwischen den Energieniveaus (
) und
(
) fehlt das Energieniveau für
Dessen Energie berechnet sich wie folgt:
Das kann nun maßstabsgetreu in Material 1 eingezeichnet werden:

Berechnen der Wellenlängen
Für den Übergang von auf die beiden tiefer liegenden Energieniveaus wird die jeweilige Wellenlänge mit der Formel
berechnet.
-
Übergang auf
:
-
Übergang auf
(Grundzustand bei
):
Angeben des sichtbaren Bereichs
Die Strahlung, die beim Übergang auf das Niveau emittiert wird (
), liegt im sichtbaren Bereich.
Nach dem Bohr'schen Atommodell kann sich das Elektron im Wasserstoffatom nur auf bestimmten Bahnen bewegen und hat dabei jeweils bestimmte Energien. Das Wasserstoffatom emittiert Strahlung, wenn das Elektron von einer energetisch höheren Bahn auf eine energetisch niedrigere Bahn übergeht.
Die Energie des emittierten Photons ist exakt gleich der Differenz der Energien des Elektrons auf diesen beiden Bahnen. Da die Energieniveaus und damit auch die Energiedifferenzen nur bestimmte Werte annehmen können, hat auch die Energie und damit auch die Wellenlänge der entstehenden Photonen jeweils einen bestimmten Wert. Im optischen Spektrum ergeben sich somit einzelne, scharf voneinander abgegrenzte Linien.
Mithilfe der gegebenen Gleichungen lassen sich die fehlenden Werte für Material 2 berechnen.
Für den Bahnradius bei der Quantenzahl wird die Gleichung
verwendet:
Für die Bahngeschwindigkeit bei der Quantenzahl wird die Gleichung
verwendet:
Die De-Broglie-Wellenlänge berechnet sich über den Impuls der Elektronen.
Für ergibt sich:
Für ergibt sich analog:
Um zu untersuchen, ob der Umfang der Elektronenbahnen ein ganzzahliges Vielfaches der Wellenlänge ist, wird der Umfang jeweils durch die berechnete Wellenlänge dividiert:
-
Überprüfung für
-
Überprüfung für
Die Forderung wird erfüllt, da das Ergebnis in beiden Fällen annähernd ganzzahlig ist.
Die Quantisierung des Bahndrehimpulses lässt sich durch Einsetzen der De-Broglie-Wellenlänge in die gegebene Bedingung
herleiten:
Das entspricht der geforderten Gleichung.
Nennen eines klassischen und quantenmechanischen Aspekts:
-
Klassischer Aspekt: Das Bohr'sche Atommodell beschreibt eine klassische Bewegung eines Elektrons im elektrischen Feld des Kerns.
-
Quantenmechanischer Aspekt: Dass sich das Elektron ausschließlich auf bestimmten Bahnen aufhalten kann, stellt einen quantenmechanischen Aspekt dar.
Nennen zweier Grenzen des Modells:
-
Atome mit mehr als einem Elektron lassen sich mit diesem Modell nur ansatzweise beschreiben.
-
Im Bohr'schen Atommodell wird lediglich postuliert, jedoch nicht erklärt, warum das Elektron den Atomkern umkreisen kann, ohne dabei elektromagnetische Strahlung zu emittieren.
-
Nach Bohr bewegt sich das Elektron auf einer Kreisbahn, also in einer Ebene. Damit müsste ein Wasserstoffatom die Form einer Scheibe mit sehr geringem Volumen haben.
Zunächst wird die Geschwindigkeit der Elektronen über den Energieerhaltungssatz (
) ermittelt:
Durch Einsetzen der Beschleunigungsspannung ergibt sich:
Mit dieser Geschwindigkeit lässt sich die De-Broglie-Wellenlänge berechnen:
Außerdem kann mit der Geschwindigkeit die Flugzeit über die Distanz
berechnet werden:
Damit ist gezeigt, dass die Flugzeit in der Größenordnung von wenigen Nanosekunden liegt.
Für einen gewünschten Abstand der Interferenzstreifen von wird zunächst die benötigte Wellenlänge
unter Anwendung der Kleinwinkelnäherung ermittelt:
Über die De-Broglie-Beziehung wird die zugehörige Elektronengeschwindigkeit berechnet:
Die theoretisch dafür benötigte Beschleunigungsspannung ergibt sich anschließend wieder durch den Energieerhaltungssatz (
):
Durch Einsetzen ergibt sich somit:
Zunächst wird der zeitliche Abstand zwischen zwei emittierten Elektronen berechnet. Da insgesamt Elektronen in
emittiert werden, wird alle
ein neues Elektron in die Apparatur entlassen.
Ein einzelnes Elektron hält sich bei einer Gesamtlänge von etwa und der in Aufgabe 3.1 berechneten Geschwindigkeit von
nur für eine sehr kurze Zeit
in der Anordnung auf:
Da die Aufenthaltsdauer eines Elektrons () extrem viel kürzer ist als der zeitliche Abstand zweier aufeinanderfolgender Emissionen (
), ist es unmöglich, dass sich zwei Elektronen gleichzeitig in der Versuchsapparatur befinden.
Die Behauptung ist folglich falsch. Für die Erzeugung des Interferenzmusters kann nicht die Interferenz mindestens zweier Elektronen miteinander verantwortlich sein; stattdessen interferiert jedes Elektron mit sich selbst.