Vorschlag B2 — Bohr’sches Atommodell und Fluoreszenz in QD-LEDs
Auf dem Markt der Fernseher ist QD-LED eine relativ neue Technik. QD-LED ist dabei die Abkürzung für „Quantum Dot-LED“. Ausgehend von einer allgemeinen Betrachtung des Bohr’schen Atommodells wird hier am Beispiel der QD-LED-Technik das Phänomen der Fluoreszenz betrachtet.
Niels Bohr erweiterte das Atommodell von Rutherford ausgehend von zwei Postulaten. Nach einem Bohr’schen Postulat kann das Elektron des Wasserstoffatoms nur bestimmte Energiezustände besetzten, die durch die Gleichung
gegeben sind. Dabei ist die Quantenzahl, die die Bahn angibt, auf der sich das Elektron strahlungsfrei bewegt.
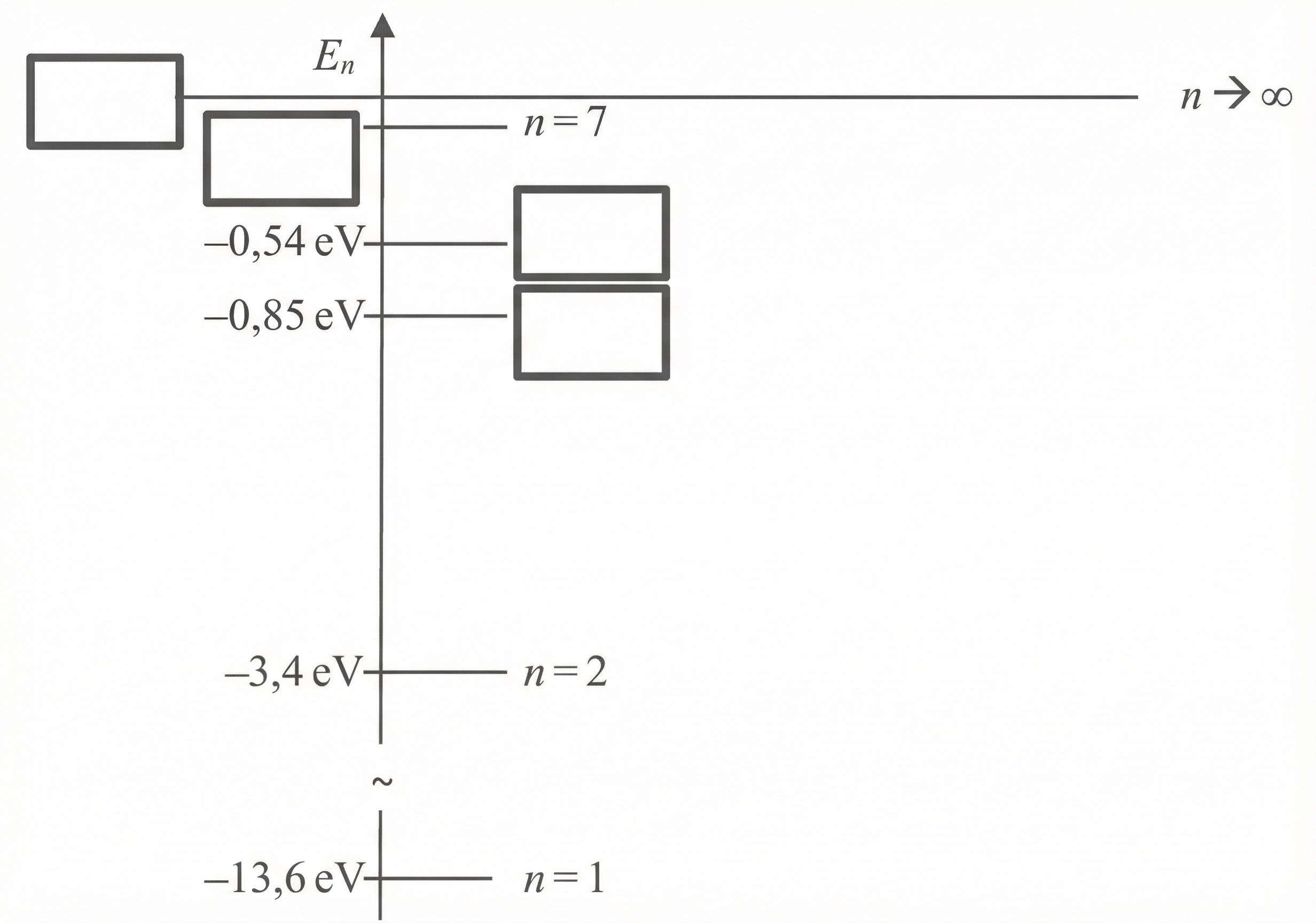
In Material 1 ist das Termschema des Wasserstoffatoms dargestellt.
Berechne die beiden fehlenden Energien in der Einheit Elektronenvolt und bestimme die beiden fehlenden Quantenzahlen im Material.
Beschrifte die durch Kästen vorbereiteten Stellen.
Die oben genannte Formel für ergibt sich unter anderem aus der Quantenbedingung der n-ten Bahn
und der Coulomb-Kraft zwischen dem Proton im Kern und dem Elektron.
Gib die Bedeutung der Größen und
im Atommodell nach Bohr an.
Das andere Bohr’sche Postulat bezieht sich auf den Übergang des Elektrons von einem Energiezustand in einen anderen Energiezustand.
Nenne das Postulat.
Berechne die Wellenlänge eines Photons, welches beim Übergang zwischen den beiden Energiezuständen und
emittiert wird.
Bestimme mithilfe von Material 2 den Spektralbereich des emittierten Photons.
Begründe mithilfe von Material 1, dass ein Wasserstoffatom im Grundzustand von einem Photon mit einer Energie von nicht angeregt werden kann.
Erläutere zwei verschiedene Vorgänge, die möglich sind, wenn ein Photon mit einer Energie von auf ein angeregtes Wasserstoffatom trifft.
Die Vorteile von QD-LED-Bildschirmen sind ein besonders helles Bild mit kräftigen Farben und eine längere Lebensdauer der Pixel. QD-LEDs arbeiten mit sogenannten Quantenpunkten. Ein Quantenpunkt ist, stark vereinfacht ausgedrückt, ein räumlich begrenzter Bereich in einem Halbleiter, in dem Elektronen gebunden sind und diskrete Energieniveaus besetzen.
Die Funktionsweise vieler QD-LEDs beruht auf Fluoreszenz.
Erkläre allgemein auf atomarer Ebene, was unter Fluoreszenz verstanden wird.
Die Quantenpunkte einer QD-LED haben die besondere Eigenschaft, dass ihr Termschema vom Durchmesser des Quantenpunkts abhängt. Beispielhaft sind drei Termschemata für verschiedene Durchmesser von Cadmiumselenid-Quantenpunkten () in Material 3 dargestellt.
Beschreibe die Gemeinsamkeiten und Unterschiede der drei Termschemata.
Zunächst wird das in den Zustand mit der Energie
angeregt. Nach einem ersten Übergang des beteiligten Elektrons befindet sich das
in dem Energiezustand
Nach einem weiteren Übergang des beteiligten Elektrons befindet sich das
wieder im jeweiligen Grundzustand.
Zeige, dass beim ersten Übergang nach der Anregung kein Photon entsteht, das im sichtbaren Bereich des elektromagnetischen Spektrums (Material 3) liegt.
Die dargestellten Quantenpunkte emittierten jeweils Photonen einer bestimmten Wellenlänge. Berechne die Wellenlängen und bestimme mithilfe von Material 2 die drei zugehörigen Farben.
[zur Kontrolle:
]
Bestimme für den größten der drei Quantenpunkte den prozentualen Anteil der Energie des im sichtbaren Bereich emittierten Lichts an der absorbierten Energie.
Die Anregung der Quantenpunkte im Bildschirm erfolgt durch das sogenannte Backlight in der Ebene hinter den Quantenpunkten. Als Voraussetzung muss die Energie des anregenden Lichtquants mindestens der Energiedifferenz zwischen dem Grundzustand und dem obersten Energiezustand entsprechen.
Entwickle einen rechnerisch begründeten Vorschlag, welche Farbe (nach Material 2) das Backlight haben sollte, um alle drei in Material 3 gezeigten Quantenpunkte anregen zu können.
Erkläre, warum die genannte Voraussetzung einem Bohr’schen Postulat widerspricht.
Es soll für einen Quantenpunkt mit dem Durchmesser eine Abschätzung der Wellenlänge der erzeugten Photonen vorgenommen werden. Zeichne dafür ein Diagramm, in dem die Wellenlänge
der erzeugten Photonen in Abhängigkeit vom Durchmesser des Quantenpunkts
aufgetragen wird. Schätze damit die Wellenlänge ab, die bei einem Quantenpunkt mit dem Durchmesser
erwartet werden kann.
Es wird vorgeschlagen, dass die Energie des Grundzustands eines Quantenpunkts durch
berechnet werden kann, wobei der Durchmesser des Quantenpunkts in Nanometer ist.
Prüfe diese Formel mit einem Quantenpunkt aus Material 3.
Ohne Berücksichtigung des Backlights fehlt zur Wiedergabe eines farbechten Bildes die Farbe Blau.
Untersuche, wie groß der Durchmesser eines mit leuchtenden Quantenpunkts sein muss.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Material 1: Unvollständiges Termschema des Wasserstoffatoms

Material 2: Spektralbereiche, Farben und Wellenlängen
|
Spektralbereiche |
|
|---|---|
|
IR |
|
|
Rot |
|
|
Orange |
|
|
Gelb |
|
|
Grün |
|
|
Blau |
|
|
Violett |
|
|
UV |
|
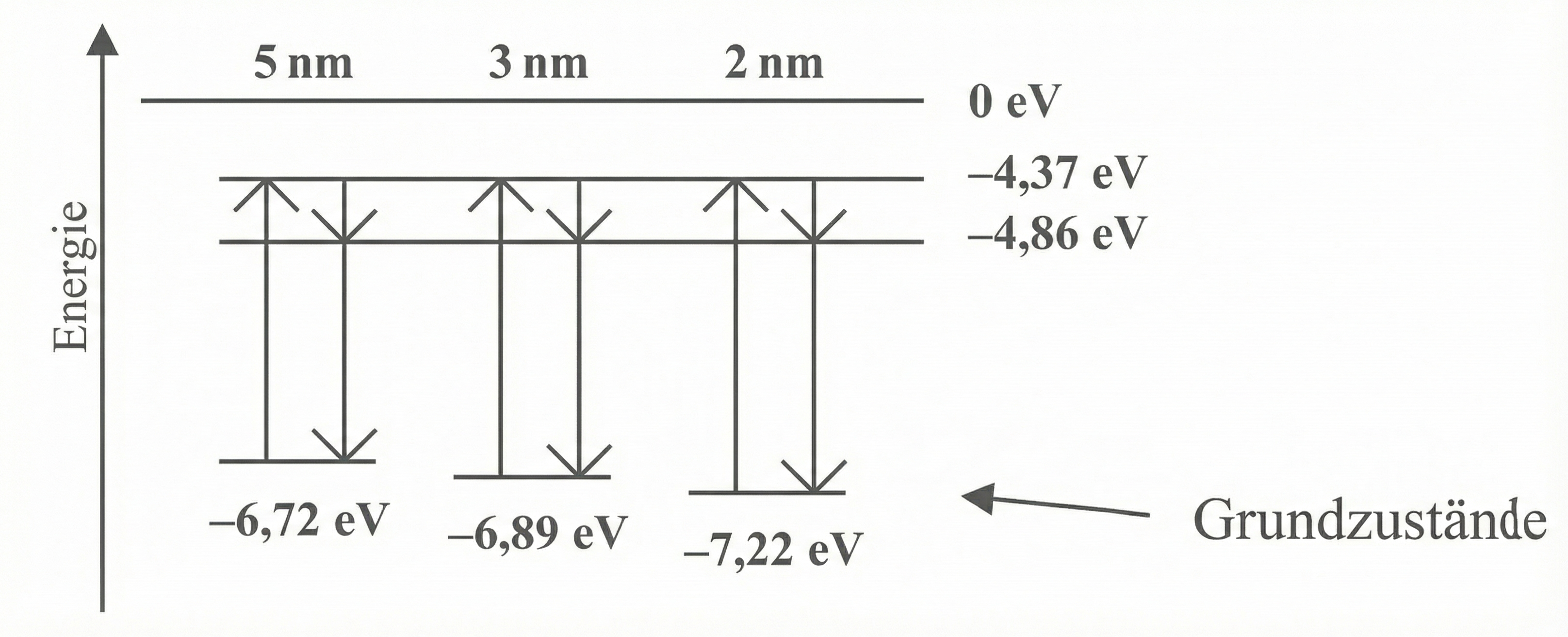
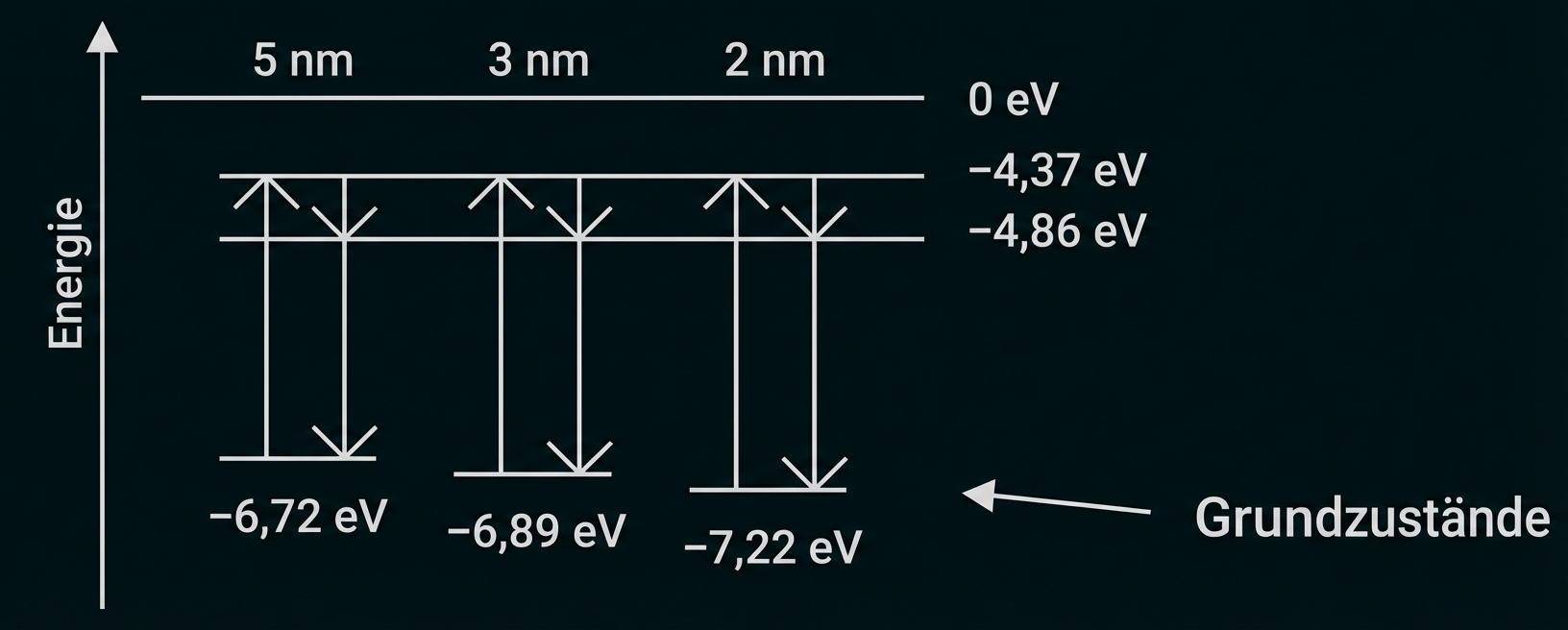
Material 3: Vereinfachte Termschemata von drei unterschiedlich großen CdSe-Quantenpunkten
(Durchmesser
und
)
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?In der Aufgabenstellung ist die Formel gegeben. Damit lassen sich die im Termschema noch fehlenden Werte durch Einsetzen bestimmen.
|
|
|
|---|---|
|
|
|
|
|
|
|
|
|
|
|
|
Somit gehört der Energiewert zur Quantenzahl
Die beiden gegebenen Energiewerte lassen sich damit auch einer Quantenzahl zuordnen. Die Quantenzahl
gehört zum Energiewert
und die Quantenzahl
zum Energiewert
Für
gilt
somit lässt sich der Quantenzahl
der Energiewert
zuordnen.
Somit ergibt sich als ausgefülltes Termschema:


-
ist die Bahngeschwindigkeit des Elektrons auf der
-ten stationären Kreisbahn um den Kern.
-
ist der Radius der
-ten stationären Kreisbahn des Elektrons um den Kern.
Nach dem zweiten Bohrschen Postulat emittiert oder absorbiert ein Atom Strahlung nur dann, wenn ein Elektron aus der Elektronenhülle sprunghaft von einem stationären Zustand in einen anderen stationären Zustand
übergeht. Die dabei emittierte bzw. absorbierte Energie in Form eines Photons ist dabei genau gleich der Energiedifferenz der beiden Niveaus. Solange sich das Elektron in einem stationären Zustand befindet, gibt das Elektron keine Strahlung ab.
Berechnung der Wellenlänge des Photons
Fällt das Elektron vom Energieniveau mit herab auf das Energieniveau mit
wird nach dem zweiten Bohr'schen Postulat die fehlende Energie als Photon abgegeben. Daraus folgt:
Hier lassen sich die gegebenen Werte einsetzen:
Zuordnung zum Spektralbereich
Mit Hilfe von Material lässt sich der Wellenlängenbereich bestimmen. Da
werden die beim Übergang vom Energieniveau mit
auf das Energieniveau mit
freigegeben Photonen dem infraroten Bereich des elektromagnetischen Spektrums zugeordnet.
Begründung der ausbleibenden Anregung
Ein Photon kann von einem Atom nur dann absorbiert werden, wenn die Photonenenergie exakt einer Energiedifferenz zwischen zwei stationären Energieniveaus entspricht. Alternativ kann das Photon das Atom ionisieren, wenn seine Energie mindestens so groß wie dessen Ionisationsenergie ist, was jedoch mehr Energie benötigt als die erste Möglichkeit.
Somit ist die kleinstmögliche Energie, die das Photon haben muss, um das Wasserstoffatom anregen zu können, die Energiedifferenz beim Übergang von nach
Die Werte aus Material
ergeben hierfür
Das ist deutlich größer als die Photonenenergie mit somit kann das Photon das Wasserstoffatom im Grundzustand nicht anregen.
Beschreibung möglicher Vorgänge
Trifft ein Photon mit der Energie auf ein angeregtes Wasserstoffatom, sind folgende Vorgänge möglich:
-
Resonante Absorption: Die Energiedifferenz zwischen dem zweiten und dem vierten angeregten Zustand eines Wasserstoffatoms beträgt
was der angegebenen Photonenenergie entspricht. Trifft also ein Photon mit der Energie
auf ein Wasserstoffatom im Zustand
kann dieses Wasserstoffatom das Photon absorbieren, wodurch das Wasserstoffatom auf das Energieniveau
angehoben wird.
-
Stimulierte Emission: Da
kann das ankommende Photon mit der Energie
das Elektron im Niveau
stimulieren, ein identisches zweites Photon abzustrahlen, wobei das Elektron auf das Niveau
zurückfällt.
-
Ionisieren: Befindet sich das Elektron auf einem Niveau mit
dann reicht die Photonenenergie von
wegen
aus, um das Elektron aus dem Atom zu lösen und das Atom somit zu ionisieren.
Anmerkung:
Zwei dieser Vorgänge zu erläutern genügt laut Aufgabenstellung.
Fluoreszenz beschreibt eine Lichtemission, die unmittelbar an eine Anregung gekoppelt ist. Ein quantisiertes System (z. B. ein Atom, ein Molekül oder ein Quantenpunkt) nimmt zunächst ein Photon auf. Dadurch wird ein Elektron in einen energetisch höheren Zustand gehoben. Dieser angeregte Zustand ist typischerweise sehr kurzlebig (Größenordnung Nanosekunden). Anschließend fällt das Elektron auf einen energetisch tieferen Zustand zurück und gibt dabei ein Photon ab (ein Photon wird emittiert). Charakteristisch ist: Sobald die Anregung endet, verschwindet auch die Emission nahezu sofort. Fluoreszenz beschreibt hierbei dieses kurze Aufleuchten während der Anregung.
Gemeinsamkeiten:
-
Alle drei dargestellten Termschemata besitzen diskrete Energieniveaus.
-
In jedem Termschema sind außerdem zwei angeregte Zustände auf denselben Energiestufen eingezeichnet: Der energetisch höchste Zustand bei
und ein darunter liegender bei
-
Der für die Fluoreszenz relevante Emissionsübergang verläuft jeweils vom Niveau
in den jeweiligen Grundzustand des Quantenpunkts.
Unterschiede:
-
Die verschiedenen Quantenpunkte unterscheiden sich in den Energieniveaus der jeweiligen Grundzustände. Sie liegen einmal bei
einmal bei
und einmal bei
-
Dadurch unterscheiden sie sich auch in ihrer jeweiligen Energiedifferenz zwischen dem Niveau
und dem jeweiligen Grundzustand. Dabei gilt: Umso kleiner der Durchmesser eines Quantenpunkts, desto größer die Energiedifferenz.
Bestimmung der Wellenlänge beim ersten Übergang
Die Energie eines Photons kann mit berechnet werden. Die Energie des emittierten Photons entspricht außerdem der Energiedifferenz der beteiligten Niveaus. Daraus folgt für die Wellenlänge:
Um die Wellenlänge eines Photons beim ersten Übergang zu berechnen, wird für die Differenz der beiden obersten Energieniveaus eingesetzt:
Mit Hilfe von Material lässt sich erkennen, dass diese Wellenlänge im infraroten Bereich und somit nicht im sichtbaren Bereich des elektromagnetischen Spektrums liegt.
Berechnung weiterer Wellenlängen und deren Farben
Um die Wellenlängen zu berechnen, kann wieder die Formel verwendet werden. Für die Energiedifferenz
wird nun die Differenz des mittleren Niveaus mit
und des jeweiligen Grundzustandes genommen. Daraus folgt für die unterschiedlichen Quantenpunkte:
-
Durchmesser
mit dem Grundzustand bei
Das entspricht rot.
-
Durchmesser
mit dem Grundzustand bei
Das entspricht orange.
-
Durchmesser
mit dem Grundzustand bei
Das entspricht grün.
Für den Quantenpunkt mit Durchmesser muss zur Anregung vom Grundzustand (
) auf das oberste Niveau (
) ein Photon mit der Energie dieser Energiedifferenz absorbiert werden:
Bei der anschließenden Emission von rotem Licht fällt der Quantenpunkt vom mittleren Niveau () zurück auf das Energieniveau des Grundzustands (
). Somit besitzt das emittierte Photon folgende Energie:
Der prozentuale Anteil der Energie des im sichtbaren Bereich emittierten Lichts an der anfangs absorbierten Energie beträgt somit:
Vorschlag zur Backlightfarbe
Damit alle drei Quantenpunkte angeregt werden können, muss die Energie eines Backlight—Photons mindestens der größten möglichen Energiedifferenz entsprechen. Diese findet sich zwischen dem Grundzustand des Quantenpunkts mit Durchmesser und dem höchsten Niveau (
). Damit lässt sich die maximal erlaubte Wellenlänge des Photons berechnen:
Somit muss das Backlight kurzwelliger als etwa sein. Das liegt am kurzwelligen Rand des blauen Lichtspektrums. Um sicherzugehen, dass alle Quantenpunkte angeregt werden, ist somit ein violettes Backlight zu wählen.
Widerspruch zum Bohr'schen Postulat
Die Annahme, dass eine Energie "mindestens" so groß wie die Energiedifferenz sein muss, steht im Widerspruch zum zweiten Bohr'schen Postulat. Nach Bohr können Photonen nur dann eine Anregung bewirken, wenn ihre Energie exakt der Differenz zweier Energieniveaus entspricht. Das ist mit violettem Backlight nicht der Fall, da die Energie des violetten Backlights größer ist als alle möglichen Energiedifferenzen. Somit wird violettes Backlight nicht funktionieren.
Die Wellenlänge des emittierten Lichts im sichtbaren Bereich hängt vom Durchmesser
des jeweiligen Quantenpunkts ab. Aus Teilaufgabe 2.3 sind folgende Werte gegeben:
Mit Hilfe dieser Werte, kann ein —Diagramm erstellt werden:


Für die gegebenen Werte kann eine Ausgleichsgerade gezeichnet werden. Dafür wird davon ausgegangen, dass zwischen der Wellenlänge und dem Durchmesser
ein linearer Zusammenhang besteht. Ausgehend von dieser Annahme, ergibt sich mit Hilfe der Ausgleichsgerade für einen Quantenpunkt mit dem Durchmesser
eine ungefähre Wellenlänge von
Rechnerische Überprüfung der angegebenen Formel
Zur Überprüfung der angegebenen Formel wird ein bekannter Wert aus Material (z. B.
) in die vorgegebene Näherungsformel für die Grundzustandsenergie
eingesetzt und der daraus berechnete Energiewert mit dem aus dem Termschema verglichen. Für
liefert die Formel folgenden Wert:
Dieser Wert liegt sehr nahe am Wert aus Material
Größe des Durchmessers eines blau leuchtenden Quantenpunkts
Die angegebene Formel kann nach dem gesuchten Durchmesser des Quantenpunkts aufgelöst werden, dabei ergibt sich:
Um den Durchmesser berechnen zu können, muss somit zuerst die Energie
beim Grundzustand bestimmt werden. Beim Übergang vom mittleren Niveau (
) in den Grundzustand wird das Photon mit der Wellenlänge
emittiert. Die Energie dieses Photons entspricht der Differenz der Energieniveaus:
Das lässt sich in die Gleichung einsetzen:
Somit muss der Durchmesser eines Quantenpunkts
betragen, wenn er mit
leuchten soll.